新藥審查
|
|
|
- 椅荃 耿
- 9 years ago
- Views:
Transcription
1 新藥審查 衛生福利部食品藥物管理署 藥品組 鄒玫君組長 1
2 內容大綱 新藥研發與上市流程法規科學藥品上市前審查要項 IND 藥品臨床試驗管理與相關法規 NDA 新藥查驗登記與相關法規 TFDA 對藥品審查改革之努力 2
3 發現活性新成分 ( 建立智財保護措施 ) IND 試驗用新藥 新藥研究開發與上市流程 NDA 新藥 Approval 許可證核准 建議事先與主管機關討論 生合成及純化 Phase I Phase II 監視藥物不良反應蒐集產品缺陷報告 動物藥 / 毒理 藥動試驗 製程確效 安定性試驗 短期毒性試驗 ( 急性 亞急性 ) 其他必要之毒性試驗 長期毒性試驗 (3-6 個月 ) Phase III 孤兒藥及臨床特殊用藥申請 Phase IV 產品抽樣調查 上市後追蹤調查 處方藥市場及廣告監視 生殖及發育毒性試驗 ( 第一 二 三期 ) 免疫 基因 致癌性 長期毒性試驗 非臨床試驗臨床試驗新藥審核新藥監視期 3
4 Drug Discovery 5,000-10,000 compounds 2-3 years 藥品從研發至上市的特性 IND NDA Approval Phase IV Phase I 人 1 Approved Drug 3-6 years Phase II 人 6-7 years Phase III 人 years Drug Development 開發時程長 高風險 高附加價值 跨領域團隊合作 法規要求嚴格 智慧財產權議題 非臨床試驗臨床試驗新藥審核新藥監視期 ( 上市 ) 4
5 藥品生命週期之管理 產品開發 臨床前試驗臨床試驗上市申請量產上市 一般 / 專案諮詢輔導 優良實驗室操作規範 / 人體細胞組織優良操作規範 (GLP/GTP) 臨床試驗查核 (GCP) 臨床試驗計畫審查 (TFDA/IRB) 上市前把關 查驗登記 (Approval) 上市後監控 生產源頭管理 產品風險管理 製造廠品質系統稽查 (GMP) 風險管理計畫 (REMS/RMP) 不良品 / 不良事件通報 (ADR) GLP :Good Laboratory Practice ( 優良實驗室操作規範 ) GTP :Good Tissue Practice( 人體細胞組織優良操作規範 ) 安全監視及警訊蒐集 (GPvP) GCP:Good Clinical Practice ( 優良臨床試驗規範 ) IRB: Institutional Review Board ( 人體試驗委員會 ) 藥物流通 (GDP) GMP:Good Manufacturing Practice ( 優良製造規範 ) 藥事服務 (GPP) ADR:Adverse Drug/Device Reactions ( 藥物不良反應 ) GPvP:Good Pharmacovigilance Practices ( 優良上市後安全監控 ) GDP:Good Distribution Practice ( 藥品優良運銷規範 ) GPP:Good Pharmacy Practice ( 優良藥事作業規範 ) REMS/RMP: Risk evaluation and mitigation strategy/risk management plan( 風險管理計畫 ) 5
6 法規科學 6
7 The Science of Pharmaceutical Regulation ( 法規科學 ) Science and Risk-based regulation 藥品核准是基於有力的科學原則 (Sound scientific principle), 並應以風險評估 (Risk evaluation) 確認其具備合理的安全及療效 Risk/Benefit assesshe ment Safety (risk) is always relative to efficacy (benefit) R B 當正確使用及適當警示下, 用在某一適應症 (intended use), 對大多數人 (significant portion of the target population) 具有臨床效益 且其效益 (benefit) 超過其危害 (risk) 7
8 The Science of Pharmaceutical Regulation ( 法規科學 ) Regulatory Science Pure science 與 Practical Science (limited by reality) 之平衡 適時的審查程序, 避免不必要的延遲上市 (undue delay) 適當的審查要求, 確保管理的負荷 (regulatory burden) 是適當與負責的 (appropriate and responsible) No perfect answers (evidence-based) Consensus building, common opinion of experts (advisory committee) Update of Regulation 科技不斷進步, 法規亦應不斷更新 審查要求應與科技發展同步 8
9 藥品上市前審查要項 9
10 藥品上市前審查 審查要項新藥學名藥 安全性有效性 藥理 / 毒理試驗 藥動 (PK/PD/BA/BE) 臨床試驗 以生體相等性試驗 (bioequivalence, BE) 取代非臨床及臨床試驗 品質 化學製造管制 (Chemistry, Manufacturing and Controls, CMC) GLP, GCP, PIC/S GMP 仿單 Labeling(direction of use) 10
11 技術審查 Requirements for Drug Approval (1) 療效與安全性相關資料 (Safety, Efficacy) 藥 / 毒理 (Pharm/Tox): Drug substance, excipients 藥物動力學 (PK/PD/BA): Drug substance, pilot formulations 臨床試驗 Phase I & II clinical trials: Drug substance, pilot formulations Phase III clinical trials: Pivotal clinical formulation (exhibition batch) 銜接性試驗評估生體相等性試驗 (BE): Drug products Marketed formulation Generic drug products Post-approval changes for both brand and generic drug products 11
12 技術審查 Requirements for Drug Approval (2) 品質相關資料 (Quality) Chemistry, Manufacturing and Controls (CMC) Quality-Raw materials, drug substance, excipients, drug product, container/closure, equipment, process, specifications, release, stability Demostrate manufacturing capacity Validation, specifications, controls, scale up, PAI Direction of use (Labeling) Data integrity and honest communication PAI-cGMP, GLP, GCP audit *PAI (Pre-approval Inspection) 批准前檢查 Continue to commit to product quality and performance Post-approval commitments and post-marketing monitoring 12
13 臨床試驗 臨床試驗資料是證明藥物安全性 有效性的最關鍵依據 Phase I study Phase II study Phase III study Phase IV study First Human Dose 建立 PK/PD profile (ADME 交互作用等 ) 確認人體安全使用劑量範圍 少數受試者 ( 人, 通常為健康人 ) First Efficacy Dose 建立藥品有效性, 並持續監測藥品安全性 確認藥品療效, 並作為 ˋ 是否進入 Phase III 之參考 少數病患 ( 人 ) 可能由多國多中心 收集特定療效及安全性資料 通常以新藥查驗登記為目的進行 針對特定的病患族群, 大規模收納受試者 ( 數百至數千人 ) 由多國多中心聯合執行 經由藥物上市後的監視, 針對藥物不良反應事件, 進行長期的追蹤, 為消費者安全把關 執行 樞紐性試驗 (Pivatol Trial): 作為新藥查驗登記用的驗證性試驗, 以支持藥品之適應症 給藥劑量 使用途徑 安全性 等資料 13
14 銜接性試驗 根據國際醫藥法規協和會 (ICH) E5 Guidance- Ethic factor in the acceptability of foreign clinical data 銜接性試驗定義 銜接性試驗 (Bridging study) 為可提供與國人相關之藥動 / 藥效學或療效 安全 用法用量等臨床試驗數據, 使國外臨床試驗數據能外推至本國相關族群之試驗 銜接性試驗目的 訂定可以顯示族群因素對安全 療效 用法用量之影響的藥品研發策略 提供不同疾病 族群有意義之臨床試驗資料, 以調整適用於國人的劑量 14
15 生體相等性試驗 Bioequivalence Study, BE 學名藥查驗登記時 用以銜接學名藥與對照藥品 ( 通常為原開發廠藥品 ) 間之療效及安全性 新藥研發過程中或藥品核准上市後 隨著對藥品特性的了解, 為進一步改良或因應臨床上使用需求等目的, 會改變藥品劑型 配方 製程或製造新單位含量藥品, 為連結之前所獲得的臨床安全性與療效性資料, 必要時亦會進行生體相等性試驗 證明變更前後, 或同廠牌同成分同劑型不同單位含量的藥品, 具有相似的吸收速率及吸收程度, 進而推論兩藥品間距有相似的臨床療效與安全性 15
16 IND 藥品臨床試驗管理與相關法規 16
17 發現活性新成分 ( 建立智財保護措施 ) IND 試驗用新藥 新藥研究開發與上市流程 NDA 新藥 Approval 許可證核准 建議事先與主管機關討論 生合成及純化 Phase I Phase II 監視藥物不良反應蒐集產品缺陷報告 動物藥 / 毒理 藥動試驗 製程確效 安定性試驗 短期毒性試驗 ( 急性 亞急性 ) 其他必要之毒性試驗 長期毒性試驗 (3-6 個月 ) Phase III 孤兒藥及臨床特殊用藥申請 Phase IV 產品抽樣調查 上市後追蹤調查 處方藥市場及廣告監視 生殖及發育毒性試驗 ( 第一 二 三期 ) 免疫 基因 致癌性 長期毒性試驗 非臨床試驗臨床試驗新藥審核新藥監視期 17
18 醫療法 藥品臨床試驗管理之法源依據 (I) 第 8 條 : 本法所稱人體試驗, 係指醫療機構依醫學理論於人體施行新醫療技術 新藥品 新醫療器材及學名藥生體可用率 生體相等性之試驗研究 人體試驗之施行應尊重接受試驗者之自主意願, 並保障其健康權益與隱私權 第 78 條 : 為提高國內醫療技術水準或預防疾病上之需要, 教學醫院經擬定計畫, 報請中央主管機關核准, 或經中央主管機關委託者, 得施行人體試驗 但學名藥生體可用率 生體相等性之人體試驗研究得免經中央主管機關之核准 非教學醫院不得施行人體試驗 但醫療機構有特殊專長, 經中央主管機關同意者, 得準用前項規定 人體試驗管理辦法 發布施行 依據醫療法 79-1 規定訂定之 ( 有關人體試驗之申請程序 審查作業基準及利益迴避原則 資訊揭露 監督管理 查核 其他告知內容等事項 ) 18
19 藥品臨床試驗管理之法源依據 (II) 藥事法 第 5 條 : 本法所稱試驗用藥物, 係指醫療效能及安全尚未經證實, 專供動物毒性藥理評估或臨床試驗用之藥物 第 44 條 : 試驗用藥物, 應經中央衛生主管機關核准始得供經核可之教學醫院臨床試驗, 以確認其安全與醫療效能 藥品優良臨床試驗準則 (GCP) 第 3 條 : 臨床試驗定義 : 以發現或證明藥品在臨床 藥理或其他藥學上之作用為目的, 而於人體執行之研究 依藥事法第 42 條第 2 項規定訂定之 目的 : 保障受試者的權利 安全及福祉 ( 倫理 ) 確保臨床試驗數據的可信度 ( 科學 ) 19
20 赫爾辛基宣言 1964, Declaration of Helsinki 芬蘭赫爾辛基召開之世界醫學大會 (World Medical Association, WMA) 1975, 1983, 1989, 1996, 2000, 2008 經 WMA 陸續修訂 作為醫師及醫學研究人員進行人體醫學試驗的倫理指導原則 The health of my patient will be my first consideration 要求所有以人為對象之研究計畫都必須通過倫理審查委員會 (Ethic Review Committee) 的審查與核准 人體試驗倫理審查委員會之最早設立依據 重視受試者保護 受試者同意書的簽署 ( Inform Consent) GCP 建立的重要參考依據之一 20
21 GCP 架構 人體試驗委員會試驗主持人試驗委託者 倫理安全科學 監測 (monitor) 稽核 (audit) 及查核 (inspection) 受試者同意書試驗計畫書試驗藥品試驗執行數據處理 21
22 藥品臨床試驗相關規範 醫療法 人體試驗管理辦法 藥事法 藥品優良臨床試驗準則 試驗計畫書 Protocol 計畫執行 Conduction 結案或終止 Results or Termination 藥品臨床試驗申請須知 ( ) 藥品臨床試驗受試者 各類藥品臨床試驗基準招募原則 (96.6.6) (88.3.6~90.8.7) 藥物樣品贈品管理辦 各類藥動學試驗基準法 ( ) ( ~ ) 研究用人體檢體採集 植物藥新藥臨床試驗基準與使用注意事項 ( ) ( ) 銜接性試驗基準 (98.7.9) 生物檢體輸入輸出作 藥品臨床試驗計劃書主要審查事業要點 ( ) [ 含項 ( ) 人體生物資料庫管理 藥品臨床試驗受試者同意書範本條例 人體器官組織 ( ) 細胞輸入輸出管理辦 藥物基因體學研究者之受檢者同法 ] 意書內容參考指引 ( ) 臨床試驗報告之格式及內容基準 (92.2.8) 臨床試驗用藥品銷毀規定 ( ) 22
23 藥品臨床試驗計畫書標準審查程序 醫院 試驗委託者 CRO TFDA 收件 First-inhuman 種族倫理考量 細胞 / 基因療法 等 整合藥品審查辦公室 Integrated Medicinal Products Review Office (impro) 行政部門 技術部門 CMC Pharm/Tox PK/PD Clinical Statistics 審查報告 必要時諮詢專家 IRB/ JIRB 藥品諮議小組 TFDA 呈判 醫院 試驗委託者 CRO 23
24 申請藥品臨床試驗計畫案應檢附資料 (Ⅰ) 藥品臨床試驗申請須知 藥商執照影本 人體試驗委員會同意臨床試驗證明書 有國外上市證明或國外衛生主管機關或國外人體試驗委員會同意進行臨床試驗證明 藥品臨床試驗計畫內容摘要表 計畫中 / 英文摘要 臨床試驗計畫書 (Clinical Trial Protocol) 加註版本與日期, 且須由計畫主持人簽章 受試者同意書 (Informed Consent Form) 加註版本與日期, 須由試驗主持人簽章 個案報告表 (Case Report Form) 藥物不良反應通報表 藥品特性資料或主持人手冊 (Investigator Brochure) 24
25 申請藥品臨床試驗計畫案應檢附資料 ( II ) 計畫主持人與協同研究人員之資歷及著作 ( 含訓練時數證明 ) 臨床試驗可能之傷害賠償及相關文件 主成分 成品檢驗規格成績書及成品安定性試驗 ( 必要時得要求檢送製造管制標準書 批次製造紀錄 ) 供查驗登記用藥品臨床試驗計畫案應繳交繳費證明 視個案而定之其他相關資料 25
26 試驗執行應注意重點 I. 試驗執行 招募受試者 知情同意與退出試驗 檢體採集與使用 偏離或變更計畫書 SAE 通報 試驗中止 終止 II. 藥品管理 III. 詳實記錄與文件的保存管理 26
27 試驗執行期間嚴重不良事件通報 藥品優良臨床試驗準則第 106 條 受試者發生任何嚴重不良事件, 試驗主持人應立即通知試驗委託者, 並儘快提供書面報告 發生未預期嚴重藥品不良反應, 試驗主持人應立即通知人體試驗委員會 但若試驗計畫書或其他文件明確排除者, 不在此限 試驗委託者獲知未預期之死亡或危及生命之嚴重藥品不良反應, 應於獲知日 7 日內通報主管機關或其委託機構, 並在獲知日起 15 日內提供詳細書面資料 試驗委託者獲知未預期之死亡或危及生命以外之嚴重藥品不良反應, 應於獲知日 15 日內通報主管機關或其委託機構, 並提供詳細書面資料 嚴重不良事件與嚴重藥品不良反應之項目由中央主管機關公告之 27
28 嚴重藥物不良反應 通報者 因藥物所引起之嚴重藥物不良反應發生時, 醫療機構 藥局 藥商應依本辦法填具通報書, 連同相關資料, 向中央衛生主管機關或其委託機構通報 嚴重藥物不良反應, 係指 : 死亡 危及生命 造成永久性疾病 胎嬰兒先天性畸形 導致病人住院或延長病人住院時間 其他可能導致永久性傷害需作處置者 28
29 藥品臨床試驗結案報告標準辦理流程 試驗委託者 CRO TFDA 收件 GCP 查核小組 試驗委託者 CRO 查核委員 試驗中心及執行人員 GCP 實地查核 藥品諮議小組 TFDA 呈判 TFDA 首頁 > 業務專區 > 藥品 > 查驗登記專區 > 藥品諮詢委員會會議結果 試驗委託者 CRO 29
30 台灣臨床試驗研究中心 林口長庚紀念醫院 * # 彰化基督教醫院 + 國家衛生研究院 # 中國醫藥大學附設醫院 * # 台中榮民總醫院 + 中山醫學大學附設醫院 + 台灣大學醫學院附設醫院 * # 台北市立萬芳醫院 * 台北榮民總醫院 # 台北醫學大學附設醫院 #+ 馬偕紀念醫院 + 和信治癌中心醫院 + 署立八里療養院 + 署立嘉南療養院 + i 署立玉里醫院 + 成功大學醫學院附設醫院 * # 奇美醫療財團法人奇美醫院 + 高雄醫學大學附設中和紀念醫院 #+ 高雄市立凱旋醫院 + 臨床試驗研究中心種類 數量 卓越臨床試驗研究中心 * 5 癌症卓越研究中心 # 8 新藥臨床試驗研究中心
31 台灣臨床試驗合作聯盟 醫院與學術單位之臨床試驗研究資訊交流平台 肺癌臨床試驗聯盟 (9 家 ) 台灣肝炎及肝癌臨床試驗聯盟 (14 家 ) 癌症早期臨床試驗聯盟 (5 家 ) 婦科癌症研究聯盟 (18 家 ) 血脂和動脈粥樣硬化聯盟 (18 家 ) 慢性阻塞性肺病聯盟 (10 家 ) 小兒感染症聯盟 (10 家 ) 台灣胃腸疾病及幽門桿菌臨床試驗聯盟 (14 家 ) 乳癌臨床試驗聯盟 (17 家 ) 高血壓相關疾病試驗聯盟 (6 家 ) 法布瑞氏試驗聯盟 (6 家 ) 精神疾病臨床試驗聯盟 19 家 ) 31
32 NDA 新藥查驗登記與相關法規 32
33 發現活性新成分 ( 建立智財保護措施 ) IND 試驗用新藥 新藥研究開發與上市流程 NDA 新藥 Approval 許可證核准 建議事先與主管機關討論 生合成及純化 Phase I Phase II 監視藥物不良反應蒐集產品缺陷報告 動物藥 / 毒理 藥動試驗 製程確效 安定性試驗 短期毒性試驗 ( 急性 亞急性 ) 其他必要之毒性試驗 長期毒性試驗 (3-6 個月 ) Phase III 孤兒藥及臨床特殊用藥申請 Phase IV 產品抽樣調查 上市後追蹤調查 處方藥市場及廣告監視 生殖及發育毒性試驗 ( 第一 二 三期 ) 免疫 基因 致癌性 長期毒性試驗 非臨床試驗臨床試驗新藥審核新藥監視期 33
34 藥品之定義 藥事法第 7 條本法所稱新藥, 係指經中央衛生主管機關審查認定屬新成分 新療效複方或新使用途徑製劑之藥品 藥事法施行細則第 2 條本法第七條, 用詞定義如下 : 一. 新成分 : 係指新發明之成分可供藥用者 二. 新療效複方 : 指已核准藥品具有新適應症 降低副作用 改善療效強度 改善療效時間或改變使用劑量之新醫療效能, 或二種以上已核准成分之複方製劑具有優於各該單一成分藥品之醫療效能者 三. 新使用途徑 : 指已核准藥品改變其使用途徑者 藥品查驗登記審查準則第 4 條學名藥 : 指與國內已核准之藥品具同成分 同劑型 同劑量 同療效之製劑 34
35 NDA Classifications (US FDA 的新藥定義 ) CDER(Center for Drug Evaluation and Research) 1. New molecular entity 2. New Salt (not a new molecular entity) 3. New Formulation (not a new salt or a new molecular entity) 4. New combination of two or more drugs 5. New manufacturer (Duplication) 6. New indication (claim) Including switching marketing status from prescription to OTC 7. Already marketed drug products with no previously approved NDA CBER (Center of Biologics Evaluation and Research) Biological products (vaccines, serum & blood products) Human cells, tissues, and cellular- and tissue-based products US FDA- Drug Development and Review Definitions alapplications/investigationalnewdrugindapplication/ucm htm 35
36 Definition of a new active substance (EMA 的新藥定義 ) A chemical, biological or radiopharmaceutical substance not previously authorised as a medicinal product in the European Union; An isomer, mixture of isomers, a complex or derivative or salt of a chemical substance previously authorised as a medicinal product in the European Union but differing in properties with regard to safety and efficacy from that chemical substance previously authorised; A biological substance previously authorised as a medicinal product in the European Union, bur differing in molecular structure, nature of the source material or manufacturing process; A radiopharmaceutical substance which is a radionuclide, or a ligand not previously authorised as a medicinal product in the European Union, or the coupling mechanism to link the molecule and the radionuclide has not been authorised previously in the EuropeanUnion 36
37 Introduction General issues Review Checklist for NDAs (US FDA 的 NDA 審查要項 ) Organizing the main folder Organizing the electronic submission A. Item 1: table of contents (Index) B. Item 2: labeling C. Item 3: summary D. Item 4: chemistry, manufacturing, and control (CMC) E. Item 5: nonclinical pharmacology and toxicology F. Item 6: human pharmacology and bioavailability/bioequivalence G. Item 7: clinical microbiology H. Item 8: clinical I. Item 9: safety update J. Item 10: statistical K. Item 11: case report tabulations (crts) L. Item 12: case report forms M. Item 13: patent information N. Item 14: patent certification O. Item 15: establishment description (CBER only) P. Item 16: debarment certification Q. Item 17: field copy certification R. Item 18: user fee cover sheet S. Item 19: other 37
38 Guidance documents for NDA (US FDA) Bioavalibility and Bioequivalence Studies for Orally Administered Drug Products- General Considerations Changes to an Approved NDA or ANDA Container Closure Systems for Packaging Human Drugs and Biologics Format and Content of the Microbiology Section of an Application Format and Content of the Clinical and Statistical Sections of an Application Format and Content of the Summary for New Drug and Antibiotic Applications Formatting, Assembling and Submitting New Drug and Antibiotic Applications Submitting Supporting Documentation in Drug Applications for the Manufacture of Drug Substances Submitting Samples and Analytical Data for Methods Validation Submitting Supporting Documentation in Drug Applications for the Manufacture of Drug Products NDAs: Impurities in Drug Substances Format and Content of the Human Pharmacokinetis and Bioavaliability Section of an Application Format and Content of the Nonclinical Pharmacology/Toxicology Section of an Application Providing Clinical Evidence of Effectiveness for Human Drug and Biological Products Drug Master Files Required Specifications for FDA's IND, NDA, and ANDA Drug Master File Binders Qualifying for Pediatric Exclusivity PET Drug Applications-Content 38
39 ICH 國際醫藥協和組織訂定的 NDA 審查資料要求 International Conference on Harmonization (ICH) of Technical Requirements for Registration of Pharmaceuticals for Human Use ICH-M4: Common Technical Document (CTD) ICH-M4 之重點 制定多國共通的 CTD 格式 清楚列明必要之文件以及非必要之試驗資料 申請者必須依照格式填報 資訊必須清楚 透明化, 以利審查人員判定, 使審查流程順暢 文件格式包含文字 表格 紙張 排版都必須一致 39
40 ICH M4: Common Technical Document Module 2 Module 單元 內容 Module 1 地域性之行政管理資料 Module 2 摘要 ( 產品簡介 ) Module 3 品質 Module 4 非臨床試驗報告 ( 安全性 ) Module 5 臨床試驗報告 ( 有效性 ) Module 3 Module 4 Module 5 Quality Nonclinical Clinical Study Reports Study Reports 40
41 ICH M4: Common Technical Document Module 1. Administrative Information and Prescribing Information This module contain documents specific for each region specified by the relevant regulatory authorities Application forms Proposed label for use in this region Module 2. Common Technical Document Summaries CTD Table of Contents CTD Introduction Quality Overall Summary Nonclinical Overview Clinical Overview Nonclinical Written and Tabulated Summaries Clinical Summary Module 3. Quality Module 4. Nonclinical Study Reports Module 5. Clinical Study Reports 41
42 我國新藥查驗登記應檢送資料 採用證明 / 處方依據技術性資料 安全性 有效性 品質 動物藥理 / 毒理試驗藥物動力學 生體可用率臨床試驗資料 化學 製造 管制 (CMC) 國內臨床試驗報告 ( 民國 82 年起需檢附 ) 轉型為銜接性試驗 ( 民國 年起 ) 42
43 公告 銜接性試驗 新藥查驗登記應執行國內臨床試驗 中美智慧財產權協議結果 引進臨床試驗, 帶動新藥發展 為鼓勵藥品之研究發展 保障醫藥品之創新, 並提升國內臨床試驗之水準, 修訂新藥安全監視制度 申請新藥查驗登記, 應另檢附國內臨床試驗報告, 國內臨床試驗為新藥查驗登記之必要條件 新藥核准後五年內, 申請學名藥查驗登記需檢附相同標準之國內臨床試驗 公告 國內臨床試驗轉型為銜接性試驗 新藥研發臨床試驗與國際接軌 43
44 銜接性試驗 背景 特點 衝擊 轉型前 - 七七公告 (1993) 中美智慧財權協議 - 過渡期之智財權保護 執行確認性試驗 (confirmatory trial) 引進國內臨床試驗, 促進新藥研發 轉型後 - 銜接性臨床試驗 (2000) 國際醫藥法規協會化 (ICH E5) 根據疾病 種族等的不同, 執行差異性試驗, 可依試驗結果調整適用於國人之使用劑量 - 避免重覆進行臨床試驗 臨床試驗與國際接軌, 引進早期臨床試驗 44
45 銜接性試驗評估 Bridging Study Evaluation, BSE 98 年 02 月 13 日衛署藥字第 號令 新成分新藥須於其查驗登記申請案前或與查驗登記申請案同時申請銜接性試驗評估 98 年 9 月 3 日衛署藥字第 號公告 基因工程藥品 疫苗類藥品 生物相似性藥品 屬新成分藥品之血漿製劑及過敏原製劑為應申請銜接性試驗評估之藥品品項 同意免除銜接性試驗之意義 認定該藥品不具內因性 ( 如遺傳 生理 ) 及外因性 ( 如文化 環境 ) 族群差異 或其差異在臨床上是可接受的 同意免除銜接性試驗並不代表認可此藥之臨床試驗數據之療效及安全性已完備 申請銜接性試驗評估, 應檢附藥品之完整臨床試驗數據資料 (complete clinical data package), 且宜含亞洲人種資料 45
46 我國新成分新藥 NDA 審查資料 一. 藥理 1. 體外藥理試驗 2. 活體內藥理試驗 3. 安全性藥理試驗 二. 毒理 1. 單一劑量毒性試驗 2. 重複劑量毒性試驗 3. 生殖毒性試驗 4. 致突變性試驗 5. 致癌性試驗 6. 局部容忍性試驗 7. 毒理動力學 8. 其他 46
47 我國新成分新藥 NDA 審查資料 三. 動物之藥動資料 1. 藥物之吸收試驗 2. 藥物之分布試驗 3. 藥物之代謝試驗 4. 藥物之排泄試驗 5. 性別之影響 6. 其他 四. 人體之藥動資料 1. 藥物之吸收試驗 2. 藥物之分布試驗 3. 藥物之代謝試驗 4. 藥物之排泄試驗 5. 藥物交互作用試驗 6. 藥物在特殊族群之試驗 47
48 我國新成分新藥 NDA 審查資料 五. 臨床試驗 1. 仿單 原產國 / 其他以上市國家 原產國仿單之中譯本 2. 綜合臨床報告 (Clinical Summary) 整合性療效摘要 (Integrated Summary of Efficacy) 整合性安全摘要 (Integrated Summary of Safety) 危險效益評估 (Risk/Benefit Assessment) 3. 臨床樞紐試驗報告 (Reports of Pivotal Studies) 48
49 我國新成分新藥 NDA 審查資料 五. 臨床試驗 ( 續 ) 4. 其他 劑量 反應試驗報告 (Report of Dose-Response Study) 其他臨床試驗資料 (Other Supportive Studies and Information) 5. 銜接性試驗之考量 (Consideration of Bridging Studies) 亞洲人種資料 (Clinical Data of Asian Population) 國內臨床試驗 (Local Clinical Trials) 自我評估 (Self-Evaluation) 49
50 我國新成分新藥 NDA 審查資料 五. 臨床試驗 ( 續 ) 6. 各國上市後安全報告 (Post-Marketing Safety Update) 7. 參考資料 (References) 8. ICH 所屬國家之審查報告 (Review Report of Regulatory Agency in ICH Regions) 美國 歐盟 / 會員國 日本 50
51 我國新成分新藥 NDA 審查資料 六. 化學 製造 管制 (CMC) 原料藥 1. 化學名稱與結構 (Chemical Name and Chemical Structure) 2. 化學式 (Chemical Formula) 3. 物化性質 (Physical and Chemical Properties) 4. 結構鑑定 (Characterization) 5. 不純物與分解產物資料 6. 製造 (Manufacture) 製造廠 合成 / 製造方法 製程管制 / 確效 7. 原料藥 ( 主成分 ) 分析方法與規格 (Control of Drug Substance) 8. 標準品之檢驗報告 (Reference Standard) 9. 容器及包裝 (Container/Closure System) 10. 安定性 (Stability) 51
52 我國新成分新藥 NDA 審查資料 六. 化學 製造 管制 (CMC) 成品 1. 成分 / 組成 (Component/Composition) 2. Pharmaceutical Development 3. 製造 (Manufacture) 製造廠 製造方法與包裝過程 (Methods of Manufacture and Packaging) 製程管制 / 確效 4. 主成分 賦形劑之規格與分析方法 (Specification and Analytical Method) 主成分, 不純物與分解產物資料 分析方法確效 5. 標準品之檢驗報告 (Reference Standard) 6. 容器封裝系統 (Container/Closure System) 7. 安定性 長期儲存與加速安定性試驗 ) (Stability: Long-Term Storage and Accelerated Stability Studies) 8. 溶離率曲線比對或生體相等性試驗 (Dissolution Profile or Bioequivalence) 52
53 新藥查驗登記應檢附之技術性資料表 (1) 新藥類別 技術性資料 CMC 安全性試驗 藥理作用 PK 臨床試驗 (ADME) 新成分 BA+CT* 新使用途徑 X Θ 新療效 X X BA+CT BA+CT** 新複方 X Θ BA+CT * 臨床試驗之 CT: 國內臨床試驗 銜接性試驗評估 ** 新療效 ( 新適應症 ) 藥品, 得自行決定是否執行 CT 表示視個案而定 Θ 表示部分資料 53
54 新藥查驗登記應檢附之技術性資料表 (2) 新藥類別 新劑型 ( 控釋 ) 新劑型 ( 速放 ) 新使用劑量新單位含量 表示視個案而定 Θ 表示部分資料 技術性資料 CMC 安全性試驗藥理作用 PK (ADME) 臨床試驗 X Θ X X BE or BA+CT X X X X BE or BA+CT X Θ Θ X BA+CT X Θ X X BE or BA+CT 54
55 新藥查驗登記審查流程 廠商申請 TFDA 收件 Global New 美國及歐盟核准外之新成分新藥 植物新藥 Biosimilar NCE-2 等 藥品諮議小組 整合藥品審查辦公室 Integrated Medicinal Products Review Office (impro) 行政部門 技術部門 CMC Pharm/Tox PK/PD Clinical Statistics 審查報告 TFDA 呈判 必要時諮詢專家 PMF PIC/S GMP 函覆申請者 55
56 適用範圍 藥物安全監視管理辦法 藥事法第 7 條所稱之新藥 其他經本屬公告認定之適用者 增加適用範圍 ( 公告 ) 監視中成分之新劑型 新劑量 新單位含量及其學名藥等藥品 安全監視期間 藥品 : 發證日起 5 年 56
57 第 4 條 藥物安全監視管理辦法 藥物安全監視期間, 持有藥物許可證之藥商應積極收集國內 外藥物使用安全資料, 除依嚴重藥物不良反應通報辦法之規定為通報外, 其他藥物不良反應需一併收錄, 並列於藥物定期安全性報告內, 依本署指定時間通報之 藥商未依前項規定進行通報者, 本署得重新評估其安全性 57
58 資料公開與資料專屬 藥事法第 40 條之 1 ( 資料公開 ) 中央衛生主管機關為維護公益之目的, 於必要時, 德公開所持有及保管藥商申請製造或輸入藥物所檢附之藥物成分 仿單等相關資料 但對於藥商申請新藥查驗登記屬於營業秘密之資料, 應保密之 前項得公開事項之範圍及方式, 其辦法由中央衛生主管機關定之 58
59 資料公開與資料專屬 藥事法第 40 條之 2 ( 資料專屬 ) 中央衛生主管機關於核發新藥許可證時, 應公開申請人檢附之已揭露專利字號或案號 新成分新藥許可證自核發之日起至五年內, 其他藥商非經許可證所有人同意, 不得引據其申請資料申請查驗登記 新成分新藥許可證核發之日起三年內, 其他藥上得依本法及相關法規有關藥品查驗登記審查之規定提出同成分 同劑型 同劑量及同單位含量藥品之查驗登記申請, 符合規定者, 得於新成分新藥許可證核發屆滿五年之翌日起發給藥品許可證 59
60 資料公開與資料專屬 藥事法第 40 條之 2 ( 資料專屬 ) ( 續 ) 新成分新藥在國外取得上市許可後三年內, 必須向中央衛生主管機關申請查驗登記, 始得準用第二項之規定 新藥專利權不及於藥商申請查驗登記前所進行之研究 教學或試驗 補充公告 ( ) 前開藥事法增訂條文生效後, 新成分新藥許可證核發時, 本署將暫給予五年資料專屬期間 其他藥商可依前開條文第四項規定, 舉証該新成分新藥是否在國外取得上市許可後三年內在我國申請查驗登記, 以作為得取消該新成分新藥資料專屬期之依據 60
61 TFDA 對藥品審查改革之努力 61
62 藥品審查改革目標 62
63 藥品管理審查改革方向 藥品管理審查規範與國際接軌 新藥審查技術法規協合化 (ICH, CTD, Guidance) 加強風險管理加強國際合作強化藥品審查品質 效率 透明 公開 一致性 Good Review Practice, GRevP 新興生技製藥產品管理規範 藥品及醫療器材複合性新產品奈米科技 新興傳輸性產品 基因工程, 體細胞治療產品 Regulate Product, Not Technology 63
64 完善法規環境, 與國際接軌 陸續更新修訂 NDA 相關規範 公告我國 新成分新藥審查核准摘要格式, 公開我國新核准之新成分新藥審查報告供各界參考 ( ) 新成分新藥查驗登記療效及安全性之考量重點 ( ) 藥品風險管理計畫及內容格式參考指引 ( ) 合理化 CPP ( ) 實施通用技術文件格式 (CTD)( ) 修正藥事法施行細則第二條新藥定義 ( ) 已在十大醫藥先進國核准上市滿十年, 但屬國內新成分新藥 ( 不包括生物藥品 ; 即 NCE-2) 之查驗登記審查重點 ( ) 64
65 藥品管理審查未來挑戰 新興生技製藥產品管理規範 植物新藥 生物相似性藥品 結合生物技術 製藥 材料 奈米及醫學工程 生醫材料及組織工程技術與產品 膠原蛋白 玻尿酸 聚乳酸等生醫材料 人工皮膚 人工軟骨等組織工程產品 醫用或研究用生物晶片 ( 蛋白質或基因 ) 基因治療 / 細胞治療 兼具藥品及醫療器材性質之複合式新產品 含藥血管支架 含降血糖輸液幫浦之血糖計 離子電導入法的藥物經皮傳送 配合光源之抗癌光感藥物緊急使用授權 (Emergency Use Authorization, EUA ) 藥物之輸入 製造, 應申請查驗登記並取得藥物許可證後, 始得為之 擬修正藥事法, 定義未取得許可證藥物, 例外可進行輸入製造之類型 : 針對目前國內尚無可比較或適宜的替代療法之危及生命或嚴重失能疾病 因應公共衛生需求之緊急狀況, 而有緊急使用之必要者等情形 65
66 新興生技產品管理挑戰 案例 :NBTXR3 癌症放射線治療提升劑 (Radioenhancer) 為奈米鉿氧化物 (nanoparticle formulation of hafnium oxide crystals, HfO2), 直接注射於腫瘤組織, 因帶負電之特性, 可與表面偏正電之腫瘤細胞結合並吞噬於細胞內, 再藉由外部給予放射線, 透過鉿金屬之電子交換, 激發水分子產生過氧化物, 以破壞癌細胞, 等腫瘤縮小後再以外科手術將腫瘤及奈米金屬產品取出 藥品? 注射方式投與 可能涉及劑量差異 透過化學反應產生作用 美國目前認定為藥品 醫療器材? 不涉及藥理作用, 不被代謝, 於原產國 ( 歐盟國 ) 被認定為醫材, 我國藥事法醫療器材之定義亦係比照歐盟 暫定為藥品考量我國臨床環境, 透過藥師調劑及把關, 以提升民眾用藥安全 66
67 合理化 NDA 審查流程 新藥審查機制 NCE 非 NCE 一般審查 優先審查 一般審查 國產創新藥品專案試辦計畫 標準審查精簡審查標準審查精簡審查 優先審查 :NCE+ 嚴重疾病 + 醫療迫切需求 精簡審查 :NCE+US FDA 及 EMA 已核准 + 無人種族群差異 1. 新療效 複方 使用途徑 劑量 單位含量 使用劑量之藥品, 不含生物藥品 植物新藥及 NCE 2. 國內製造, 並符合 PIC/S GMP 3. 專案試辦計畫 67
68 合理化 NDA 審查流程 新成分新藥製售證明 (CPP) 合理化 NCE 審查 Non-CPP 1-CPP 2-CPP 全套技術性文件 + 早期國內臨床試驗 + GCP/GLP/GMP 查核 + 藥品風險管理計畫 (REMS) 全套技術性文件 + 國內臨床試驗 + 必要時, 藥品風險管理計畫 (REMS) 十大先進國任兩國 CPP 全套技術性文件 + 必要時, 藥品風險管理計畫 (REMS) USFDA+EMA ( 精簡審查 ) ( 無人種差異 相同適應症 ) 部分技術性文件 + 必要時, 藥品風險管理計畫 (REMS) 68
69 提供藥品諮詢輔導機制 藥品諮詢輔導機制 線上資訊及出版品 函詢及諮詢 主動輔導 產業溝通平台 ( 定期 ) 藥品專案諮詢輔導 ( 早收清單 ) 關鍵途徑 國家型科技發展計畫 69
70 主動輔導機制 藥品專案諮詢輔導 藥品專案諮詢輔導要點 ( ) 針對國內準備上市或研發中之新藥 ( 含生物藥品 ) 進行專案諮詢輔導協助專案進入臨床試驗 (First in human, next phase or pivotal trial) 申請藥品查驗登記 取得藥證等目標 在藥品研發過程及時融入法規要求 70
71 TFDA 在生技製藥產業扮演之角色 保障國民健康之前提下, 兼顧製藥產業發展 全民健康的提升者 (Public Health Protection) 健康產業的推動者 (Public Health Promotion)
學 名 藥
 藥 品 組 新 手 上 路 手 冊 103 年 2 月 0 目 錄 藥 品 查 驗 登 記 概 述... 0 藥 品 查 驗 登 記 新 手 上 路... 2 新 藥 及 新 劑 型 新 使 用 劑 量 新 單 位 含 量 製 劑 查 驗 登 記 查 檢 表... 8 國 產 學 名 藥 品 查 驗 登 記 查 檢 表... 15 輸 入 學 名 藥 品 查 驗 登 記 查 檢 表... 18 生
藥 品 組 新 手 上 路 手 冊 103 年 2 月 0 目 錄 藥 品 查 驗 登 記 概 述... 0 藥 品 查 驗 登 記 新 手 上 路... 2 新 藥 及 新 劑 型 新 使 用 劑 量 新 單 位 含 量 製 劑 查 驗 登 記 查 檢 表... 8 國 產 學 名 藥 品 查 驗 登 記 查 檢 表... 15 輸 入 學 名 藥 品 查 驗 登 記 查 檢 表... 18 生
国内外相关的临床研究资料综述撰写的格式与内容
 化 学 药 物 申 报 资 料 撰 写 的 格 式 和 内 容 的 技 术 指 导 原 则 临 床 试 验 资 料 综 述 目 录 一 概 述... 3 二 资 料 格 式 与 内 容... 4 ( 一 ) 临 床 试 验 与 文 献 总 结... 4 1 临 床 试 验 总 结... 5 1.1 生 物 药 剂 学 研 究 总 结... 5 1.2 临 床 药 理 学 研 究 总 结... 5 1.3
化 学 药 物 申 报 资 料 撰 写 的 格 式 和 内 容 的 技 术 指 导 原 则 临 床 试 验 资 料 综 述 目 录 一 概 述... 3 二 资 料 格 式 与 内 容... 4 ( 一 ) 临 床 试 验 与 文 献 总 结... 4 1 临 床 试 验 总 结... 5 1.1 生 物 药 剂 学 研 究 总 结... 5 1.2 临 床 药 理 学 研 究 总 结... 5 1.3
吸入制剂质量控制研究技术指导原则
 指 导 原 则 编 号 : H G P H 9-1 吸 入 制 剂 质 量 控 制 研 究 技 术 指 导 原 则 二 〇 〇 七 年 九 月 目 录 一 概 述 2 二 吸 入 制 剂 的 分 类 3 三 质 量 控 制 研 究 3 ( 一 ) 吸 入 制 剂 质 量 控 制 的 主 要 指 标 和 参 数 3 ( 二 ) 气 雾 剂 4 ( 三 ) 喷 雾 剂 12 ( 四 ) 粉 雾 剂 14
指 导 原 则 编 号 : H G P H 9-1 吸 入 制 剂 质 量 控 制 研 究 技 术 指 导 原 则 二 〇 〇 七 年 九 月 目 录 一 概 述 2 二 吸 入 制 剂 的 分 类 3 三 质 量 控 制 研 究 3 ( 一 ) 吸 入 制 剂 质 量 控 制 的 主 要 指 标 和 参 数 3 ( 二 ) 气 雾 剂 4 ( 三 ) 喷 雾 剂 12 ( 四 ) 粉 雾 剂 14
Microsoft PowerPoint - SAGE 2010
 SAGE Journals Online -Communication Studies 大綱 SAGE 簡介 Communication Studies 收錄內容 SJO 平台功能介紹 首頁 瀏覽功能 檢索功能 進階服務 SAGE Content 超過 520 種人文 社會科學 理工 科技領域電子期刊 SAGE 與超過 245 個國際知名的學會合作 ( 包括 American Sociological
SAGE Journals Online -Communication Studies 大綱 SAGE 簡介 Communication Studies 收錄內容 SJO 平台功能介紹 首頁 瀏覽功能 檢索功能 進階服務 SAGE Content 超過 520 種人文 社會科學 理工 科技領域電子期刊 SAGE 與超過 245 個國際知名的學會合作 ( 包括 American Sociological
<4D6963726F736F667420576F7264202D2030373139C2E5C0F8BEB9A7F7B7BEB371A5ADA578B77CC4B3ACF6BFFD2E646F63>
 經 濟 部 工 業 局 會 議 紀 錄 經 濟 部 衛 生 署 與 業 者 溝 通 平 台 局 處 層 級 會 議 ( II ): 醫 療 器 材 產 業 會 議 紀 錄 一 時 間 :94 年 7 月 19 日 ( 星 期 二 ) 上 午 9 時 30 分 二 地 點 : 經 濟 部 工 業 局 第 一 會 議 室 三 主 持 人 : 經 濟 部 工 業 局 陳 局 長 昭 義 政 處 廖 處 長
經 濟 部 工 業 局 會 議 紀 錄 經 濟 部 衛 生 署 與 業 者 溝 通 平 台 局 處 層 級 會 議 ( II ): 醫 療 器 材 產 業 會 議 紀 錄 一 時 間 :94 年 7 月 19 日 ( 星 期 二 ) 上 午 9 時 30 分 二 地 點 : 經 濟 部 工 業 局 第 一 會 議 室 三 主 持 人 : 經 濟 部 工 業 局 陳 局 長 昭 義 政 處 廖 處 長
<4D6963726F736F667420576F7264202D20B1C0BC73B1D0A87CBEC7A4C0AF5AC2B2B3B92DB773C3C4313032303332372D31>
 立 陽 明 大 學 新 藥 及 中 草 藥 轉 譯 醫 學 推 廣 教 育 碩 士 學 分 班 102 學 年 度 招 生 簡 章 開 辦 系 所 : 國 立 陽 明 大 學 藥 理 學 研 究 所 國 立 中 國 醫 藥 研 究 所 民 國 102 年 4 月 30 日 目 錄 重 要 日 程 表... - 1 - 主 旨... - 2 - 一 開 課 時 間... - 4 - 二 課 程 規 劃...
立 陽 明 大 學 新 藥 及 中 草 藥 轉 譯 醫 學 推 廣 教 育 碩 士 學 分 班 102 學 年 度 招 生 簡 章 開 辦 系 所 : 國 立 陽 明 大 學 藥 理 學 研 究 所 國 立 中 國 醫 藥 研 究 所 民 國 102 年 4 月 30 日 目 錄 重 要 日 程 表... - 1 - 主 旨... - 2 - 一 開 課 時 間... - 4 - 二 課 程 規 劃...
Microsoft Word - 簡章.doc
 社 區 衛 生 護 理 師 認 證 考 試 100 年 考 試 簡 章 主 辦 單 位 : 台 灣 護 理 學 會 聯 絡 地 址 : 台 北 市 大 安 區 信 義 路 四 段 281 號 四 樓 聯 絡 電 話 :(02)2755-2291 網 址 :http://www.twna.org.tw/ 1 簡 章 目 錄 社 區 衛 生 護 理 師 認 證 辦 法... 1 社 區 衛 生 護 理
社 區 衛 生 護 理 師 認 證 考 試 100 年 考 試 簡 章 主 辦 單 位 : 台 灣 護 理 學 會 聯 絡 地 址 : 台 北 市 大 安 區 信 義 路 四 段 281 號 四 樓 聯 絡 電 話 :(02)2755-2291 網 址 :http://www.twna.org.tw/ 1 簡 章 目 錄 社 區 衛 生 護 理 師 認 證 辦 法... 1 社 區 衛 生 護 理
<4D6963726F736F667420576F7264202D20D5E3BDADB0C2CFE8D2A9D2B5B9C9B7DDD3D0CFDEB9ABCBBECAD7B4CEB9ABBFAAB7A2D0D0B9C9C6B1D5D0B9C9CBB5C3F7CAE9A3A8C9EAB1A8B8E532303135C4EA35D4C23239C8D5B1A8CBCDA3A92E646F63>
 浙 江 奥 翔 药 业 股 份 有 限 公 司 Zhejiang Ausun Pharmaceutical Co., Ltd. ( 住 所 : 浙 江 省 化 学 原 料 药 基 地 临 海 园 区 东 海 第 四 大 道 5 号 ) 首 次 公 开 发 行 A 股 股 票 招 股 说 明 书 ( 申 报 稿 ) 保 荐 机 构 ( 主 承 销 商 ) ( 住 所 : 四 川 省 成 都 市 东 城
浙 江 奥 翔 药 业 股 份 有 限 公 司 Zhejiang Ausun Pharmaceutical Co., Ltd. ( 住 所 : 浙 江 省 化 学 原 料 药 基 地 临 海 园 区 东 海 第 四 大 道 5 号 ) 首 次 公 开 发 行 A 股 股 票 招 股 说 明 书 ( 申 报 稿 ) 保 荐 机 构 ( 主 承 销 商 ) ( 住 所 : 四 川 省 成 都 市 东 城
歐盟EMA於2012年7月提出「A型血友病患者產生抑制抗體(Inhibitors)之免疫耐受性誘導療法(Immune Tolerance Induction)」回應文件,諮詢公眾意見
 臨床試驗中未預期之嚴重藥品不良反應 新藥科技組黃齡慧前言在藥品的研發階段, 除了驗證藥品的療效外, 蒐集受試者 ( 病人 ) 使用藥品的安全資訊是為最需要注意並重視的環節 當有重大事件發生時, 尤其是臨床試驗階段, 採取必要措施以維護受試者安全, 更是主管機關無可避免之責任 建立臨床試驗藥品安全快速通報機制的目的, 即為當受試者發生了未預期嚴重藥品不良反應時, 法規單位 試驗主持人 試驗委託者以及所有與此藥品臨床試驗相關的人員,
臨床試驗中未預期之嚴重藥品不良反應 新藥科技組黃齡慧前言在藥品的研發階段, 除了驗證藥品的療效外, 蒐集受試者 ( 病人 ) 使用藥品的安全資訊是為最需要注意並重視的環節 當有重大事件發生時, 尤其是臨床試驗階段, 採取必要措施以維護受試者安全, 更是主管機關無可避免之責任 建立臨床試驗藥品安全快速通報機制的目的, 即為當受試者發生了未預期嚴重藥品不良反應時, 法規單位 試驗主持人 試驗委託者以及所有與此藥品臨床試驗相關的人員,
 臺 灣 生 物 經 濟 產 業 發 展 方 案 Taiwan Bioeconomy Industry Development Program 中 華 民 國 105 年 1 月 5 日 105 年 1 月 5 日 行 政 院 核 定 摘 要 生 物 經 濟 係 指 在 生 物 資 源 或 生 物 技 術 基 礎 上, 發 展 成 產 品 與 服 務 的 一 種 經 濟 型 態, 包 括 所 引 導
臺 灣 生 物 經 濟 產 業 發 展 方 案 Taiwan Bioeconomy Industry Development Program 中 華 民 國 105 年 1 月 5 日 105 年 1 月 5 日 行 政 院 核 定 摘 要 生 物 經 濟 係 指 在 生 物 資 源 或 生 物 技 術 基 礎 上, 發 展 成 產 品 與 服 務 的 一 種 經 濟 型 態, 包 括 所 引 導
<4D6963726F736F667420576F7264202D20BFADC0B3D3A2D2BDD2A9BCAFCDC5A3A8CCECBDF2A3A9B9C9B7DDD3D0CFDEB9ABCBBECAD7B4CEB9ABBFAAB7A2D0D0B9C9C6B1D5D0B9C9CBB5C3F7CAE9A3A8C9EAB1A8B8E532303136C4EA33D4C23330C8D5B1A8CBCDA3A92E646F63>
 凯 莱 英 医 药 集 团 ( 天 津 ) 股 份 有 限 公 司 天 津 经 济 技 术 开 发 区 洞 庭 三 街 6 号 首 次 公 开 发 行 股 票 招 股 说 明 书 ( 申 报 稿 ) 本 公 司 的 发 行 申 请 尚 未 得 到 中 国 证 监 会 核 准 本 招 股 说 明 书 ( 申 报 稿 ) 不 具 有 据 以 发 行 股 票 的 法 律 效 力 仅 供 预 先 披 露 使
凯 莱 英 医 药 集 团 ( 天 津 ) 股 份 有 限 公 司 天 津 经 济 技 术 开 发 区 洞 庭 三 街 6 号 首 次 公 开 发 行 股 票 招 股 说 明 书 ( 申 报 稿 ) 本 公 司 的 发 行 申 请 尚 未 得 到 中 国 证 监 会 核 准 本 招 股 说 明 书 ( 申 报 稿 ) 不 具 有 据 以 发 行 股 票 的 法 律 效 力 仅 供 预 先 披 露 使
证券简称:信邦制药 证券代码:002390 股票上市地点:深圳证券交易所
 证 券 简 称 : 信 邦 制 药 证 券 代 码 :002390 股 票 上 市 地 点 : 深 圳 证 券 交 易 所 贵 州 信 邦 制 药 股 份 有 限 公 司 发 行 股 份 及 支 付 现 金 购 买 资 产 并 募 集 配 套 资 金 暨 关 联 交 易 报 告 书 ( 修 订 稿 ) 交 易 对 方 UCPHARM COMPANY LIMITED 琪 康 国 际 有 限 公 司 杭
证 券 简 称 : 信 邦 制 药 证 券 代 码 :002390 股 票 上 市 地 点 : 深 圳 证 券 交 易 所 贵 州 信 邦 制 药 股 份 有 限 公 司 发 行 股 份 及 支 付 现 金 购 买 资 产 并 募 集 配 套 资 金 暨 关 联 交 易 报 告 书 ( 修 订 稿 ) 交 易 对 方 UCPHARM COMPANY LIMITED 琪 康 国 际 有 限 公 司 杭
 医 药 和 生 命 科 学 行 业 中 国 医 药 行 业 展 望 第 二 版 目 录 引 言 3 第 一 章 现 代 医 学 起 源 传 统 中 医 药 : 敢 问 路 在 何 方? 5 第 二 章 非 处 方 药 市 场 : 迎 来 东 西 方 的 较 量 6 第 三 章 医 疗 器 械 孕 育 无 限 商 机 7 第 四 章 研 发 外 包 机 构 : 制 药 企 业 价 值 链 提 升 的
医 药 和 生 命 科 学 行 业 中 国 医 药 行 业 展 望 第 二 版 目 录 引 言 3 第 一 章 现 代 医 学 起 源 传 统 中 医 药 : 敢 问 路 在 何 方? 5 第 二 章 非 处 方 药 市 场 : 迎 来 东 西 方 的 较 量 6 第 三 章 医 疗 器 械 孕 育 无 限 商 机 7 第 四 章 研 发 外 包 机 构 : 制 药 企 业 价 值 链 提 升 的
Microsoft Word - 大陸化粧品進口程序與法規1220(16K)
 大 陸 化 粧 品 進 出 口 程 序 與 法 規 出 版 機 關 : 經 濟 部 工 業 局 化 粧 保 養 品 產 業 輔 導 計 畫 出 版 日 期 :102 年 11 月 序 臺 灣 化 粧 保 養 品 產 業 近 年 來 外 銷 成 長 表 現 優 異, 外 銷 值 自 2007 年 新 臺 幣 59 億 元, 成 長 至 2012 年 新 臺 幣 110 億 元, 成 長 幅 度 達
大 陸 化 粧 品 進 出 口 程 序 與 法 規 出 版 機 關 : 經 濟 部 工 業 局 化 粧 保 養 品 產 業 輔 導 計 畫 出 版 日 期 :102 年 11 月 序 臺 灣 化 粧 保 養 品 產 業 近 年 來 外 銷 成 長 表 現 優 異, 外 銷 值 自 2007 年 新 臺 幣 59 億 元, 成 長 至 2012 年 新 臺 幣 110 億 元, 成 長 幅 度 達
 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 243,1052,272 791222101452 2014719 58339347 396634355 196413164 28269 26 27 28 29 () () () () () () () () () () () () () () () () () () ()
2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 243,1052,272 791222101452 2014719 58339347 396634355 196413164 28269 26 27 28 29 () () () () () () () () () () () () () () () () () () ()
第六篇
 國 家 發 展 前 瞻 規 劃 委 辦 研 究 計 畫 - 產 業 人 力 供 需 評 估 ( 含 模 型 建 立 ) ( 第 二 年 度 計 畫 ) 編 號 : 國 家 發 展 前 瞻 規 劃 委 辦 研 究 計 畫 - 產 業 人 力 供 需 評 估 ( 含 模 型 建 立 ) 委 託 單 位 : 行 政 院 國 家 發 展 委 員 會 執 行 單 位 : 財 團 法 人 台 灣 經 濟 研
國 家 發 展 前 瞻 規 劃 委 辦 研 究 計 畫 - 產 業 人 力 供 需 評 估 ( 含 模 型 建 立 ) ( 第 二 年 度 計 畫 ) 編 號 : 國 家 發 展 前 瞻 規 劃 委 辦 研 究 計 畫 - 產 業 人 力 供 需 評 估 ( 含 模 型 建 立 ) 委 託 單 位 : 行 政 院 國 家 發 展 委 員 會 執 行 單 位 : 財 團 法 人 台 灣 經 濟 研
II
 I II 目 录 前 言...3 内 容 提 要...4 1 加 速 生 物 技 术 药 物 产 业 发 展 具 有 重 大 的 战 略 意 义...6 2 发 展 生 物 技 术 药 物 产 业 的 关 键 成 功 因 素...8 3 中 国 生 物 技 术 药 物 产 业 发 展 所 面 临 的 主 要 挑 战...14 4 打 造 世 界 先 进 的 创 新 型 生 物 技 术 药 物 产 业
I II 目 录 前 言...3 内 容 提 要...4 1 加 速 生 物 技 术 药 物 产 业 发 展 具 有 重 大 的 战 略 意 义...6 2 发 展 生 物 技 术 药 物 产 业 的 关 键 成 功 因 素...8 3 中 国 生 物 技 术 药 物 产 业 发 展 所 面 临 的 主 要 挑 战...14 4 打 造 世 界 先 进 的 创 新 型 生 物 技 术 药 物 产 业
目 錄
 臺 北 醫 大 會 議 紀 錄 會 議 名 稱 三 年 度 第 二 期 第 次 校 課 程 委 員 會 會 議 會 議 日 期 104 年 5 月 22 日 時 間 :104 年 5 月 22 日 10:00-12:00 地 點 : 醫 綜 合 大 樓 後 棟 4 樓 教 務 處 試 務 工 作 室 主 席 : 朱 娟 秀 教 務 長 記 錄 : 林 玉 靖 小 姐 出 席 人 員 : 方 德 昭
臺 北 醫 大 會 議 紀 錄 會 議 名 稱 三 年 度 第 二 期 第 次 校 課 程 委 員 會 會 議 會 議 日 期 104 年 5 月 22 日 時 間 :104 年 5 月 22 日 10:00-12:00 地 點 : 醫 綜 合 大 樓 後 棟 4 樓 教 務 處 試 務 工 作 室 主 席 : 朱 娟 秀 教 務 長 記 錄 : 林 玉 靖 小 姐 出 席 人 員 : 方 德 昭
013-020-台灣醫藥行銷師認證推動與展望.indd
 台 灣 醫 藥 行 銷 師 認 證 推 動 與 展 望 綜 中 華 民 國 行 銷 暨 管 理 協 會 常 務 理 事 李 勝 文 摘 要 (Taiwan Pharmaceutical Marketing & Management Association TPMMA) MR 33 MR MR33 壹 醫 藥 行 銷 師 在 醫 療 供 應 鏈 扮 演 的 角 色 () (Medical Representative
台 灣 醫 藥 行 銷 師 認 證 推 動 與 展 望 綜 中 華 民 國 行 銷 暨 管 理 協 會 常 務 理 事 李 勝 文 摘 要 (Taiwan Pharmaceutical Marketing & Management Association TPMMA) MR 33 MR MR33 壹 醫 藥 行 銷 師 在 醫 療 供 應 鏈 扮 演 的 角 色 () (Medical Representative
<4D6963726F736F667420576F7264202D20C4CFBEA9BDA1D3D1C9FABBAFD6C6D2A9B9C9B7DDD3D0CFDEB9ABCBBECAD7B4CEB9ABBFAAB7A2D0D041B9C9B9C9C6B1B2A2C9CFCAD0D5D0B9C9CBB5C3F7CAE9A3A8C9EAB1A8B8E532303136C4EA33D4C238C8D5B1A8CBCDA3A92E646F63>
 南 京 健 友 生 化 制 药 股 份 有 限 公 司 ( 南 京 高 新 开 发 区 MA010-1 号 地 ) ( 申 报 稿 ) 保 荐 人 ( 主 承 销 商 ) ( 四 川 省 成 都 市 东 城 根 上 街 95 号 ) 1-1-1 声 明 : 本 公 司 的 发 行 申 请 尚 未 得 到 中 国 证 券 监 督 管 理 委 员 会 核 准 本 招 股 说 明 书 ( 申 报 稿 )
南 京 健 友 生 化 制 药 股 份 有 限 公 司 ( 南 京 高 新 开 发 区 MA010-1 号 地 ) ( 申 报 稿 ) 保 荐 人 ( 主 承 销 商 ) ( 四 川 省 成 都 市 东 城 根 上 街 95 号 ) 1-1-1 声 明 : 本 公 司 的 发 行 申 请 尚 未 得 到 中 国 证 券 监 督 管 理 委 员 会 核 准 本 招 股 说 明 书 ( 申 报 稿 )
% % % 獨立 廉正 專業 創新
 101 99 102 101 1. 2. 3. 4. 5. 6. 7. 8. 9. 10. 99 102 8 4 34 11 101826 594 71.91% 160 19.37% 72 8.72% 101 100 27 18100 21 101 35 獨立 廉正 專業 創新 1. 7,290 8,677 26,180 26,011 1,272 1,346 142 157 7 7 1,757 1,795
101 99 102 101 1. 2. 3. 4. 5. 6. 7. 8. 9. 10. 99 102 8 4 34 11 101826 594 71.91% 160 19.37% 72 8.72% 101 100 27 18100 21 101 35 獨立 廉正 專業 創新 1. 7,290 8,677 26,180 26,011 1,272 1,346 142 157 7 7 1,757 1,795
Microsoft PowerPoint - Eisenstein_ABET_Presentation_Beijing_Oct_2007-Chinese.ppt [兼容模式]
![Microsoft PowerPoint - Eisenstein_ABET_Presentation_Beijing_Oct_2007-Chinese.ppt [兼容模式] Microsoft PowerPoint - Eisenstein_ABET_Presentation_Beijing_Oct_2007-Chinese.ppt [兼容模式]](/thumbs/43/23125636.jpg) Bruce Eisenstein 博 士 是 Drexel 大 学 电 气 和 计 算 机 工 程 系 的 Arthur J. Rowland 教 授, 同 时 是 电 气 和 计 算 机 工 程 系 的 前 任 系 主 任 (1980-1995) 他 是 一 个 受 尊 敬 的 IEEE 的 领 导 者, 在 2000 年 担 任 IEEE 的 主 席 在 担 任 主 席 以 前,Eisenstein
Bruce Eisenstein 博 士 是 Drexel 大 学 电 气 和 计 算 机 工 程 系 的 Arthur J. Rowland 教 授, 同 时 是 电 气 和 计 算 机 工 程 系 的 前 任 系 主 任 (1980-1995) 他 是 一 个 受 尊 敬 的 IEEE 的 领 导 者, 在 2000 年 担 任 IEEE 的 主 席 在 担 任 主 席 以 前,Eisenstein
Umschlag_Primer_AIQ_final_Umschlag_Primer_AIQ_final.qxd
 USP 21 CFR Part 11 入 门 指 南 GxP cgmp PIC/S SOP www.agilent.com/chem/cn 安 捷 伦 科 技 版 权 所 有,2009 2009 年 1 月 1 日 中 国 印 刷 发 行 号 5990-3288CHCN 分 析 仪 器 验 证 和 系 统 认 证 ISO 17025 QA/QC GLP ICH FDA OECD GCP
USP 21 CFR Part 11 入 门 指 南 GxP cgmp PIC/S SOP www.agilent.com/chem/cn 安 捷 伦 科 技 版 权 所 有,2009 2009 年 1 月 1 日 中 国 印 刷 发 行 号 5990-3288CHCN 分 析 仪 器 验 证 和 系 统 认 证 ISO 17025 QA/QC GLP ICH FDA OECD GCP
/
 Tel:03-5732682, E-mail:[email protected] 101 04 30 1 1. 2. 3. / 4. 5. 6. 7. 8. 9. 2 3 4.1 4.1.1 4.1.2 4.1.3 4 4.1 4.1.4 ( ) ( ) 1. 2. 5 4.1.5 101/04/30 4.1 6 4.1.5 101/04/30 4.1 (e) (f) ( ) (g) (
Tel:03-5732682, E-mail:[email protected] 101 04 30 1 1. 2. 3. / 4. 5. 6. 7. 8. 9. 2 3 4.1 4.1.1 4.1.2 4.1.3 4 4.1 4.1.4 ( ) ( ) 1. 2. 5 4.1.5 101/04/30 4.1 6 4.1.5 101/04/30 4.1 (e) (f) ( ) (g) (
类 抗 肿 瘤 药 物 临 床 研 究, 由 于 非 细 胞 毒 类 药 物 ( 如 信 号 传 导 抑 制 剂, 生 物 反 应 调 节 剂, 激 素 类 等 ) 是 目 前 新 药 开 发 的 主 要 方 向, 本 指 导 原 则 也 将 尽 可 能 对 此 类 别 药 物 临 床 研 究 的
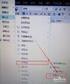
 抗 肿 瘤 药 物 临 床 试 验 技 术 指 导 原 则 一 概 述 恶 性 肿 瘤 是 严 重 威 胁 人 类 生 命 的 一 类 疾 病, 尽 管 现 有 治 疗 手 段 取 得 了 一 定 疗 效, 但 多 数 肿 瘤 患 者 生 存 时 间 有 限, 缺 乏 有 效 的 可 以 治 愈 的 药 物, 亟 需 开 发 新 的 药 物 来 满 足 需 要 在 抗 肿 瘤 药 物 的 风 险 效
抗 肿 瘤 药 物 临 床 试 验 技 术 指 导 原 则 一 概 述 恶 性 肿 瘤 是 严 重 威 胁 人 类 生 命 的 一 类 疾 病, 尽 管 现 有 治 疗 手 段 取 得 了 一 定 疗 效, 但 多 数 肿 瘤 患 者 生 存 时 间 有 限, 缺 乏 有 效 的 可 以 治 愈 的 药 物, 亟 需 开 发 新 的 药 物 来 满 足 需 要 在 抗 肿 瘤 药 物 的 风 险 效
股份有限公司
 公 司 代 码 :600267 公 司 简 称 : 海 正 药 业 浙 江 海 正 药 业 股 份 有 限 公 司 2016 年 半 年 度 报 告 重 要 提 示 一 本 公 司 董 事 会 监 事 会 及 董 事 监 事 高 级 管 理 人 员 保 证 半 年 度 报 告 内 容 的 真 实 准 确 完 整, 不 存 在 虚 假 记 载 误 导 性 陈 述 或 重 大 遗 漏, 并 承 担 个
公 司 代 码 :600267 公 司 简 称 : 海 正 药 业 浙 江 海 正 药 业 股 份 有 限 公 司 2016 年 半 年 度 报 告 重 要 提 示 一 本 公 司 董 事 会 监 事 会 及 董 事 监 事 高 级 管 理 人 员 保 证 半 年 度 报 告 内 容 的 真 实 准 确 完 整, 不 存 在 虚 假 记 载 误 导 性 陈 述 或 重 大 遗 漏, 并 承 担 个
PowerPoint プレゼンテーション
 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 Enabling Technologies Safety Assurance 2015 2016 2017 2018 2019 Future Forecast of Enabling Technologies Driver Acceptance of Automated Vehicle Systems
2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 Enabling Technologies Safety Assurance 2015 2016 2017 2018 2019 Future Forecast of Enabling Technologies Driver Acceptance of Automated Vehicle Systems
 24 24. Special Issue 名 人 講 堂 專 題 研 究 表3 新加坡政府對銷售給不同屬性投資人的對沖基金管理指引 25 焦 點 視 界 27 26 市 場 掃 描 證 交 集 錦 資料來源 新加坡金融管理局(Monetary Authority of Singapore)網站 25 機構投資人定義 (1)依銀行法設立的銀行 (2)商業銀行 (3)財務公司 (4)保險公司 (5)信託公司
24 24. Special Issue 名 人 講 堂 專 題 研 究 表3 新加坡政府對銷售給不同屬性投資人的對沖基金管理指引 25 焦 點 視 界 27 26 市 場 掃 描 證 交 集 錦 資料來源 新加坡金融管理局(Monetary Authority of Singapore)網站 25 機構投資人定義 (1)依銀行法設立的銀行 (2)商業銀行 (3)財務公司 (4)保險公司 (5)信託公司
<4D6963726F736F667420576F7264202D20312D3120D5D0B9C9CBB5C3F7CAE9A3A8C9EAB1A8B8E5A3A92E646F63>
 76 贵 阳 新 天 药 业 股 份 有 限 公 司 Guiyang Xintian Pharmaceutical Co.,Ltd. ( 贵 阳 国 家 高 新 技 术 产 业 开 发 区 新 添 大 道 114 号 ) 首 次 公 开 发 行 股 票 招 股 说 明 书 ( 申 报 稿 ) 保 荐 人 ( 主 承 销 商 ) ( 北 京 市 朝 阳 区 建 国 路 81 号 华 贸 中 心 德 意
76 贵 阳 新 天 药 业 股 份 有 限 公 司 Guiyang Xintian Pharmaceutical Co.,Ltd. ( 贵 阳 国 家 高 新 技 术 产 业 开 发 区 新 添 大 道 114 号 ) 首 次 公 开 发 行 股 票 招 股 说 明 书 ( 申 报 稿 ) 保 荐 人 ( 主 承 销 商 ) ( 北 京 市 朝 阳 区 建 国 路 81 号 华 贸 中 心 德 意
University of Science and Technology of China A dissertation for master s degree Research of e-learning style for public servants under the context of
 中 国 科 学 技 术 大 学 硕 士 学 位 论 文 新 媒 体 环 境 下 公 务 员 在 线 培 训 模 式 研 究 作 者 姓 名 : 学 科 专 业 : 导 师 姓 名 : 完 成 时 间 : 潘 琳 数 字 媒 体 周 荣 庭 教 授 二 一 二 年 五 月 University of Science and Technology of China A dissertation for
中 国 科 学 技 术 大 学 硕 士 学 位 论 文 新 媒 体 环 境 下 公 务 员 在 线 培 训 模 式 研 究 作 者 姓 名 : 学 科 专 业 : 导 师 姓 名 : 完 成 时 间 : 潘 琳 数 字 媒 体 周 荣 庭 教 授 二 一 二 年 五 月 University of Science and Technology of China A dissertation for
衞 衞 ii
 衞 衞 66 43 衞 [email protected] ii 2 4 4 7 7 8 13 13 14 15 I 18 II 19 iii - 1 - ( ) ( ) 52 30-2 - 30 0.5 11 5 1 000 ( 0.1%) 0.5% 1. 2. 3. 1. 2. 3. - 3 - 2. ( ) 1 3. 4. 5. 6. 2 ( ) 3 着 - 4 - 7. 85 30
衞 衞 66 43 衞 [email protected] ii 2 4 4 7 7 8 13 13 14 15 I 18 II 19 iii - 1 - ( ) ( ) 52 30-2 - 30 0.5 11 5 1 000 ( 0.1%) 0.5% 1. 2. 3. 1. 2. 3. - 3 - 2. ( ) 1 3. 4. 5. 6. 2 ( ) 3 着 - 4 - 7. 85 30
X 傳統育種技術 分子育種技術 基因改良育種
 06 2015 7 511 72 92? 2010? X 傳統育種技術 1960 1980 30 60 20 分子育種技術 5 10 3 5 基因改良育種 2015 7 511 07 改良後的基因及其生產的蛋白質都需經過嚴格的動物及田間生物安全試驗才會上市, 程序就跟新藥一樣 20 基改產品禁得起考驗 12 2013 1.75 50 1 5 1996 80 2013 156 35 21 6 90 08
06 2015 7 511 72 92? 2010? X 傳統育種技術 1960 1980 30 60 20 分子育種技術 5 10 3 5 基因改良育種 2015 7 511 07 改良後的基因及其生產的蛋白質都需經過嚴格的動物及田間生物安全試驗才會上市, 程序就跟新藥一樣 20 基改產品禁得起考驗 12 2013 1.75 50 1 5 1996 80 2013 156 35 21 6 90 08
深圳翰宇药业股份有限公司2016年半年度报告全文
 深 圳 翰 宇 药 业 股 份 有 限 公 司 2016 年 半 年 度 报 告 2016 年 8 月 第 一 节 重 要 提 示 释 义 本 公 司 董 事 会 监 事 会 及 董 事 监 事 高 级 管 理 人 员 保 证 本 报 告 所 载 资 料 不 存 在 任 何 虚 假 记 载 误 导 性 陈 述 或 者 重 大 遗 漏, 并 对 其 内 容 的 真 实 性 准 确 性 完 整 性 承
深 圳 翰 宇 药 业 股 份 有 限 公 司 2016 年 半 年 度 报 告 2016 年 8 月 第 一 节 重 要 提 示 释 义 本 公 司 董 事 会 监 事 会 及 董 事 监 事 高 级 管 理 人 员 保 证 本 报 告 所 载 资 料 不 存 在 任 何 虚 假 记 载 误 导 性 陈 述 或 者 重 大 遗 漏, 并 对 其 内 容 的 真 实 性 准 确 性 完 整 性 承
貳 肆 公司治理報告 一 組織系統 ( 一 ) 組織結構 ( 二 ) 組織系統圖 14 中華民國 98 年中華郵政年報
 14 16 24 30 24 25 26 26 27 27 28 29 29 一 組織系統二 董事 監察人 總經理 副總經理 各部門及分支機構主管資料三 公司治理運作情形 ( 一 ) 董事會運作情形 ( 二 ) 公司治理運作情形及其與上市上櫃公司治理實務守則差異情形及原因 ( 三 ) 揭露公司治理守則及相關規章之查詢方式 ( 四 ) 揭露其他足以增進對公司治理運作情形瞭解之重要資訊 ( 五 ) 內部控制制度執行狀況
14 16 24 30 24 25 26 26 27 27 28 29 29 一 組織系統二 董事 監察人 總經理 副總經理 各部門及分支機構主管資料三 公司治理運作情形 ( 一 ) 董事會運作情形 ( 二 ) 公司治理運作情形及其與上市上櫃公司治理實務守則差異情形及原因 ( 三 ) 揭露公司治理守則及相關規章之查詢方式 ( 四 ) 揭露其他足以增進對公司治理運作情形瞭解之重要資訊 ( 五 ) 內部控制制度執行狀況
藥品查驗登記審查準則
 1 USPDI 2 ( FDA) Approved Prescription Drug Product With Therapeutic Equivalence EvaluationsOrange Book FDA European Union The European Agency for the Evaluation of Medicinal Products EMEA EMEA 3 Physicians'
1 USPDI 2 ( FDA) Approved Prescription Drug Product With Therapeutic Equivalence EvaluationsOrange Book FDA European Union The European Agency for the Evaluation of Medicinal Products EMEA EMEA 3 Physicians'
募集样本
 华 鲁 控 股 集 团 有 限 公 司 2015 年 度 第 一 期 中 期 票 据 募 集 说 明 书 发 行 人 : 注 册 金 额 : 本 期 发 行 金 额 : 发 行 期 限 : 信 用 评 级 机 构 : 信 用 评 级 结 果 : 担 保 情 况 : 华 鲁 控 股 集 团 有 限 公 司 人 民 币 24 亿 元 人 民 币 3 亿 元 5 年 中 诚 信 国 际 信 用 评 级 有
华 鲁 控 股 集 团 有 限 公 司 2015 年 度 第 一 期 中 期 票 据 募 集 说 明 书 发 行 人 : 注 册 金 额 : 本 期 发 行 金 额 : 发 行 期 限 : 信 用 评 级 机 构 : 信 用 评 级 结 果 : 担 保 情 况 : 华 鲁 控 股 集 团 有 限 公 司 人 民 币 24 亿 元 人 民 币 3 亿 元 5 年 中 诚 信 国 际 信 用 评 级 有
<4D6963726F736F667420576F7264202D20312D3120D5D0B9C9CBB5C3F7CAE9A3A8C9EAB1A8B8E5A3A92E646F63>
 第 一 章 及 发 行 公 告 吉 林 紫 鑫 药 业 股 份 有 限 公 司 吉 林 省 柳 河 县 英 利 路 88 号 首 次 公 开 发 行 股 票 ( 申 报 稿 ) 保 荐 机 构 ( 主 承 销 商 ) 江 苏 省 苏 州 市 爱 河 桥 路 28 号 第 一 章 及 发 行 公 告 声 明 : 本 公 司 的 发 行 申 请 尚 未 得 到 中 国 证 监 会 核 准 本 ( 申 报
第 一 章 及 发 行 公 告 吉 林 紫 鑫 药 业 股 份 有 限 公 司 吉 林 省 柳 河 县 英 利 路 88 号 首 次 公 开 发 行 股 票 ( 申 报 稿 ) 保 荐 机 构 ( 主 承 销 商 ) 江 苏 省 苏 州 市 爱 河 桥 路 28 号 第 一 章 及 发 行 公 告 声 明 : 本 公 司 的 发 行 申 请 尚 未 得 到 中 国 证 监 会 核 准 本 ( 申 报
Form: RWPRR401-B
 Form: RWPRR401-B C C S 通 函 Circular 中 国 船 级 社 (2011 年 ) 通 函 第 81 号 总 第 145 号 2011 年 10 月 17 日 ( 共 4+26 页 ) 发 : 总 部 有 关 处 室 上 海 规 范 所 各 审 图 中 心 各 分 社 本 社 验 船 师 有 关 船 厂 产 品 制 造 厂 设 计 院 及 航 运 公 司 实 施 有 关
Form: RWPRR401-B C C S 通 函 Circular 中 国 船 级 社 (2011 年 ) 通 函 第 81 号 总 第 145 号 2011 年 10 月 17 日 ( 共 4+26 页 ) 发 : 总 部 有 关 处 室 上 海 规 范 所 各 审 图 中 心 各 分 社 本 社 验 船 师 有 关 船 厂 产 品 制 造 厂 设 计 院 及 航 运 公 司 实 施 有 关
Microsoft Word - 793-797 tb20150504赵宏宇s-高校教改纵横.doc
 微 生 物 学 通 报 Microbiology China [email protected] Apr. 20, 2016, 43(4): 793 797 http://journals.im.ac.cn/wswxtbcn DOI: 10.13344/j.microbiol.china.150504 高 校 教 改 纵 横 生 物 工 程 专 业 发 酵 课 程 群 建 设 探 索 * 赵 宏 宇
微 生 物 学 通 报 Microbiology China [email protected] Apr. 20, 2016, 43(4): 793 797 http://journals.im.ac.cn/wswxtbcn DOI: 10.13344/j.microbiol.china.150504 高 校 教 改 纵 横 生 物 工 程 专 业 发 酵 课 程 群 建 设 探 索 * 赵 宏 宇
智慧財產合作平台規劃
 How Taiwan Pharmaceutical Industries Affected by and Cope with the U.S. Patent Linkage System 台 灣 製 藥 產 業 受 美 國 專 利 連 結 制 度 之 影 響 及 因 應 對 策 羅 麗 珠 總 經 理 Dec. 2 nd, 2014 @@ 1 簡 報 大 綱 背 景 Hatch-Waxman Act
How Taiwan Pharmaceutical Industries Affected by and Cope with the U.S. Patent Linkage System 台 灣 製 藥 產 業 受 美 國 專 利 連 結 制 度 之 影 響 及 因 應 對 策 羅 麗 珠 總 經 理 Dec. 2 nd, 2014 @@ 1 簡 報 大 綱 背 景 Hatch-Waxman Act
rate extent (2-3) 40-50 physiological availability systematic availability bio-phase availability biological availability bioavailability 1977 FDA Bio
 Drug Bioavailability and Therapeutic Effects 1. efficacy2. safety3. applicability4. uniformity (1) E = k 1 f (A, C, S) E A C S k 1 A E = k 2 f (C, S) k 2 ( ) bioavailability 191 rate extent (2-3) 40-50
Drug Bioavailability and Therapeutic Effects 1. efficacy2. safety3. applicability4. uniformity (1) E = k 1 f (A, C, S) E A C S k 1 A E = k 2 f (C, S) k 2 ( ) bioavailability 191 rate extent (2-3) 40-50
投影片 1
 國內藥品與藥政管理概況 衛生福利部食品藥物管理署 藥品組 組長鄒玫君博士 102 年 9 月 27 日臨床藥學與藥品科技研究所 1 內容大綱 我國藥政管理組織 體系藥品之分類與定義藥品管理架構 藥品生命週期管理 上市前管理上市後管理 藥品流通管理藥事服務管理我國藥政管理法規演變藥政管理之改革與展望 2 我國藥政管理組織 體系 3 衛生福利部食品藥物管理署沿革 食品衛生處藥政處藥物食品檢驗局管制藥品管理局
國內藥品與藥政管理概況 衛生福利部食品藥物管理署 藥品組 組長鄒玫君博士 102 年 9 月 27 日臨床藥學與藥品科技研究所 1 內容大綱 我國藥政管理組織 體系藥品之分類與定義藥品管理架構 藥品生命週期管理 上市前管理上市後管理 藥品流通管理藥事服務管理我國藥政管理法規演變藥政管理之改革與展望 2 我國藥政管理組織 體系 3 衛生福利部食品藥物管理署沿革 食品衛生處藥政處藥物食品檢驗局管制藥品管理局
股份有限公司
 公 司 代 码 :600671 公 司 简 称 : 天 目 药 业 杭 州 天 目 山 药 业 股 份 有 限 公 司 2015 年 年 度 报 告 重 要 提 示 一 本 公 司 董 事 会 监 事 会 及 董 事 监 事 高 级 管 理 人 员 保 证 年 度 报 告 内 容 的 真 实 准 确 完 整, 不 存 在 虚 假 记 载 误 导 性 陈 述 或 重 大 遗 漏, 并 承 担 个 别
公 司 代 码 :600671 公 司 简 称 : 天 目 药 业 杭 州 天 目 山 药 业 股 份 有 限 公 司 2015 年 年 度 报 告 重 要 提 示 一 本 公 司 董 事 会 监 事 会 及 董 事 监 事 高 级 管 理 人 员 保 证 年 度 报 告 内 容 的 真 实 准 确 完 整, 不 存 在 虚 假 记 载 误 导 性 陈 述 或 重 大 遗 漏, 并 承 担 个 别
Construction of Chinese pediatric standard database A Dissertation Submitted for the Master s Degree Candidate:linan Adviser:Prof. Han Xinmin Nanjing
 密 级 : 公 开 学 号 :20081209 硕 士 学 位 论 文 中 医 儿 科 标 准 数 据 库 建 设 研 究 研 究 生 李 楠 指 导 教 师 学 科 专 业 所 在 学 院 毕 业 时 间 韩 新 民 教 授 中 医 儿 科 学 第 一 临 床 医 学 院 2011 年 06 月 Construction of Chinese pediatric standard database
密 级 : 公 开 学 号 :20081209 硕 士 学 位 论 文 中 医 儿 科 标 准 数 据 库 建 设 研 究 研 究 生 李 楠 指 导 教 师 学 科 专 业 所 在 学 院 毕 业 时 间 韩 新 民 教 授 中 医 儿 科 学 第 一 临 床 医 学 院 2011 年 06 月 Construction of Chinese pediatric standard database
我国原奶及乳制品安全生产和质量安全管理研究
 密 级 论 文 编 号 中 国 农 业 科 学 院 硕 士 学 位 论 文 我 国 原 奶 及 乳 制 品 质 量 安 全 管 理 研 究 Study on Quality and Safety Management of Raw Milk and Dairy Products in China 申 请 人 : 段 成 立 指 导 教 师 : 叶 志 华 研 究 员 张 蕙 杰 研 究 员 申 请
密 级 论 文 编 号 中 国 农 业 科 学 院 硕 士 学 位 论 文 我 国 原 奶 及 乳 制 品 质 量 安 全 管 理 研 究 Study on Quality and Safety Management of Raw Milk and Dairy Products in China 申 请 人 : 段 成 立 指 导 教 师 : 叶 志 华 研 究 员 张 蕙 杰 研 究 员 申 请
Grant proposal
 科 技 部 106 年 度 跨 領 域 整 合 型 研 究 計 畫 徵 求 公 告 一 規 劃 案 說 明 ( 一 ) 研 究 主 題 與 承 辦 單 位 項 目 研 究 主 題 主 辦 學 術 司 共 同 主 辦 學 術 司 1 以 尖 端 物 理 化 學 方 法 探 索 生 物 科 學 之 跨 領 域 研 究 自 然 司 生 科 司 2 空 間 資 訊 與 人 文 社 會 經 濟 跨 領 域 研
科 技 部 106 年 度 跨 領 域 整 合 型 研 究 計 畫 徵 求 公 告 一 規 劃 案 說 明 ( 一 ) 研 究 主 題 與 承 辦 單 位 項 目 研 究 主 題 主 辦 學 術 司 共 同 主 辦 學 術 司 1 以 尖 端 物 理 化 學 方 法 探 索 生 物 科 學 之 跨 領 域 研 究 自 然 司 生 科 司 2 空 間 資 訊 與 人 文 社 會 經 濟 跨 領 域 研
目 录
 安 全 生 产 职 业 体 系 建 设 及 职 业 资 格 管 理 ( 英 国 ) 人 事 司 乔 树 清 二 〇 一 三 年 十 二 月 1 目 录 一 基 本 情 况... 3 二 英 国 职 业 健 康 与 安 全 管 理... 3 ( 一 ) 政 府 层 面... 3 ( 二 ) 民 间 层 面... 6 ( 三 ) 法 律 层 面... 6 三 英 国 国 家 职 业 资 格 制 度 概
安 全 生 产 职 业 体 系 建 设 及 职 业 资 格 管 理 ( 英 国 ) 人 事 司 乔 树 清 二 〇 一 三 年 十 二 月 1 目 录 一 基 本 情 况... 3 二 英 国 职 业 健 康 与 安 全 管 理... 3 ( 一 ) 政 府 层 面... 3 ( 二 ) 民 间 层 面... 6 ( 三 ) 法 律 层 面... 6 三 英 国 国 家 职 业 资 格 制 度 概
中山大學學位論文典藏
 -- IEMBA 3 ii 4W2H Who( ) When( ) What( ) Why( ) How much( ) How to do( ) iii Abstract Pharmaceutical industry can be regard as one of the knowledge-intensive industries. Designing a sales promotion for
-- IEMBA 3 ii 4W2H Who( ) When( ) What( ) Why( ) How much( ) How to do( ) iii Abstract Pharmaceutical industry can be regard as one of the knowledge-intensive industries. Designing a sales promotion for
医学科研方法
 医 学 科 研 方 法 主 讲 苏 秀 兰 细 胞 生 物 学 教 授 第 一 讲 绪 论 一 概 念 : 在 医 学 科 学 研 究 活 动 中, 运 用 科 学 的 实 践 和 理 论 思 维 的 技 巧, 充 分 发 挥 自 己 的 智 慧, 去 寻 找 观 念 世 界 与 现 实 世 界 之 间 的 联 系 或 规 律, 从 而 发 现 新 现 象, 提 出 新 理 论 的 手 段 二 医
医 学 科 研 方 法 主 讲 苏 秀 兰 细 胞 生 物 学 教 授 第 一 讲 绪 论 一 概 念 : 在 医 学 科 学 研 究 活 动 中, 运 用 科 学 的 实 践 和 理 论 思 维 的 技 巧, 充 分 发 挥 自 己 的 智 慧, 去 寻 找 观 念 世 界 与 现 实 世 界 之 间 的 联 系 或 规 律, 从 而 发 现 新 现 象, 提 出 新 理 论 的 手 段 二 医
3-3.tpf
 第 三 節 藥 品 領 域 New Emergency Health Kit 98, NEHK 98 Supply Management System, SUMA 97 NEHK98 Asian Emergency Health Kit, AEHK 97 96 Radio-Frequency Identification, RFID RFID 97 RFID RFID 97 第 三 節 藥 品 領
第 三 節 藥 品 領 域 New Emergency Health Kit 98, NEHK 98 Supply Management System, SUMA 97 NEHK98 Asian Emergency Health Kit, AEHK 97 96 Radio-Frequency Identification, RFID RFID 97 RFID RFID 97 第 三 節 藥 品 領
0B职责及违规
 杜 邦 行 爲 守 則 確 保 永 續 發 展 的 未 來 核 心 價 値 的 實 踐 二 O 一 三 年 六 月 執 行 長 的 話 親 愛 的 杜 邦 同 仁 們 : 幾 個 世 紀 以 來, 杜 邦 員 工 一 直 利 用 以 市 場 為 導 向 的 科 學 在 這 個 變 幻 莫 測 的 世 界 中 作 出 業 績 雖 然 我 們 公 司 和 世 界 都 在 不 斷 進 步 和 發 展, 但
杜 邦 行 爲 守 則 確 保 永 續 發 展 的 未 來 核 心 價 値 的 實 踐 二 O 一 三 年 六 月 執 行 長 的 話 親 愛 的 杜 邦 同 仁 們 : 幾 個 世 紀 以 來, 杜 邦 員 工 一 直 利 用 以 市 場 為 導 向 的 科 學 在 這 個 變 幻 莫 測 的 世 界 中 作 出 業 績 雖 然 我 們 公 司 和 世 界 都 在 不 斷 進 步 和 發 展, 但
I 我国中药在国际市场上的竞争优势分析
 中 国 中 药 行 业 分 析 报 告 (2002 年 4 季 度 ) 出 版 日 期 : 2003 年 2 月 WWW.CEI.GOV.CN 编 写 说 明 本 期 报 告 由 中 药 协 会 军 事 医 学 科 学 院 专 家 分 析 撰 写 而 成 报 告 还 附 上 第 四 批 国 家 非 处 方 药 药 品 目 录 之 中 成 药 部 分, 力 图 为 专 业 市 场 沟 通 提 供 最
中 国 中 药 行 业 分 析 报 告 (2002 年 4 季 度 ) 出 版 日 期 : 2003 年 2 月 WWW.CEI.GOV.CN 编 写 说 明 本 期 报 告 由 中 药 协 会 军 事 医 学 科 学 院 专 家 分 析 撰 写 而 成 报 告 还 附 上 第 四 批 国 家 非 处 方 药 药 品 目 录 之 中 成 药 部 分, 力 图 为 专 业 市 场 沟 通 提 供 最
untitled
 VOL 18 NO 4 (Supplement 1) Oct - Dec 2011 ISSN 1727-2874 The Pharmaceutical Society of Hong Kong The Practising Pharmacists Association of Hong Kong The Society of Hospital Pharmacists of Hong Kong HK$80.00
VOL 18 NO 4 (Supplement 1) Oct - Dec 2011 ISSN 1727-2874 The Pharmaceutical Society of Hong Kong The Practising Pharmacists Association of Hong Kong The Society of Hospital Pharmacists of Hong Kong HK$80.00
PowerPoint 簡報
 從我國藥政管理制度與展望 看藥界未來與對藥師期待 食品藥物管理署藥品組劉麗玲組長 2014.6.15 台灣年輕藥師協會 25X35X45 生涯沙龍講座 衛生福利部食品藥物管理署 Food and Drug Administration, Ministry of Health and Welfare http://www.fda.gov.tw/ 1 內容大綱 從新聞回顧藥政管理源頭 從製藥開發看藥政管理角色
從我國藥政管理制度與展望 看藥界未來與對藥師期待 食品藥物管理署藥品組劉麗玲組長 2014.6.15 台灣年輕藥師協會 25X35X45 生涯沙龍講座 衛生福利部食品藥物管理署 Food and Drug Administration, Ministry of Health and Welfare http://www.fda.gov.tw/ 1 內容大綱 從新聞回顧藥政管理源頭 從製藥開發看藥政管理角色
Micromedex CALIS PPT
 MICROMEDEX 临 专 题 报 MICROMEDEX 权 区 理 资 术 ( ) 2004/09/22 报 : 梁 铭 内 纲 数 库 内 绍 例 , 年 约 2.9% 3.7% 疗 伤 疗, 约 8.8% ~ 13.6% 伤 导 ; 不 过, 这 过, 过 数 预 (Brennan et al, NEJM 1991;324:370-376; Gawande et al, Surgery 1999;126:66-75)
MICROMEDEX 临 专 题 报 MICROMEDEX 权 区 理 资 术 ( ) 2004/09/22 报 : 梁 铭 内 纲 数 库 内 绍 例 , 年 约 2.9% 3.7% 疗 伤 疗, 约 8.8% ~ 13.6% 伤 导 ; 不 过, 这 过, 过 数 预 (Brennan et al, NEJM 1991;324:370-376; Gawande et al, Surgery 1999;126:66-75)
THE CHINESE CERTIFIED PUBLIC ACCOUNTANT Academic Research 39 Brandr, 意 思 是 烧 灼 烙 印, 最 早 用 这 种 方 式 来 标 记 家 畜 等 来 区 别 私 有 财 产 朗 文 当 代 高 级 英 语 词 典 21 世 纪
 38 中 国 注 册 会 计 师 学 术 研 究 商 标 战 略 : 升 级 会 计 师 事 务 所 品 牌 战 略 的 必 由 之 路 基 于 2013 年 度 前 百 家 事 务 所 商 标 相 关 情 况 的 实 证 分 析 吴 杰 周 鑫 泽 摘 要 品 牌 战 略 是 推 动 行 业 做 强 做 大 走 出 去 的 有 力 法 宝 本 文 从 全 新 的 商 标 角 度, 以 2013 年
38 中 国 注 册 会 计 师 学 术 研 究 商 标 战 略 : 升 级 会 计 师 事 务 所 品 牌 战 略 的 必 由 之 路 基 于 2013 年 度 前 百 家 事 务 所 商 标 相 关 情 况 的 实 证 分 析 吴 杰 周 鑫 泽 摘 要 品 牌 战 略 是 推 动 行 业 做 强 做 大 走 出 去 的 有 力 法 宝 本 文 从 全 新 的 商 标 角 度, 以 2013 年
Microsoft Word - 邁進新紀元.DOC
 目 錄 前 言 第 一 章 香 港 中 醫 藥 發 展 的 歷 史 背 景 一 歷 史 淵 源 二 中 醫 藥 發 展 的 概 況 1. 香 港 市 民 普 遍 使 用 中 醫 藥 2. 香 港 中 醫 師 行 醫 的 基 本 情 況 3. 中 醫 藥 教 育 培 訓 4. 香 港 的 中 藥 資 源 及 中 藥 貿 易 5. 香 港 中 藥 的 零 售 批 發 及 生 產 第 二 章 積 極 籌
目 錄 前 言 第 一 章 香 港 中 醫 藥 發 展 的 歷 史 背 景 一 歷 史 淵 源 二 中 醫 藥 發 展 的 概 況 1. 香 港 市 民 普 遍 使 用 中 醫 藥 2. 香 港 中 醫 師 行 醫 的 基 本 情 況 3. 中 醫 藥 教 育 培 訓 4. 香 港 的 中 藥 資 源 及 中 藥 貿 易 5. 香 港 中 藥 的 零 售 批 發 及 生 產 第 二 章 積 極 籌
菸 害 防 治 預 防 改 善 措 施 (1) 第 一 階 段 - 裝 設 自 動 語 音 警 告 感 應 設 施 地 點 A 棟 二 側 樓 梯 未 裝 機 (11/1~11/30) 裝 機 時 (12/1~12/31) 6A 7A 8A 9A 10A 總 數 82 652 125 1153 39
 機 構 名 稱 : 戴 德 森 醫 療 財 團 法 人 嘉 義 基 督 教 醫 院 4.1.1 Working conditions comply with national/regional directives and indicators [Evidence: e.g. national and international (EU) regulations are recognized]. 工
機 構 名 稱 : 戴 德 森 醫 療 財 團 法 人 嘉 義 基 督 教 醫 院 4.1.1 Working conditions comply with national/regional directives and indicators [Evidence: e.g. national and international (EU) regulations are recognized]. 工
論 文 摘 要 本 文 乃 係 兩 岸 稅 務 爭 訟 制 度 之 研 究, 蓋 稅 務 爭 訟 在 行 訴 訟 中 一 直 占 有 相 當 高 的 比 例, 惟 其 勝 訴 率 一 直 偏 低, 民 87 年 10 月 28 日 行 訴 訟 法 經 幅 修 正 後, 審 級 部 分 由 一 級 一
 法 院 碩 士 在 職 專 班 碩 士 論 文 指 導 教 授 : 王 文 杰 博 士 兩 岸 稅 務 爭 訟 制 度 之 比 較 研 究 A comparative study on the system of cross-straits tax litigation 研 究 生 : 羅 希 寧 中 華 民 一 0 一 年 七 月 論 文 摘 要 本 文 乃 係 兩 岸 稅 務 爭 訟 制 度 之
法 院 碩 士 在 職 專 班 碩 士 論 文 指 導 教 授 : 王 文 杰 博 士 兩 岸 稅 務 爭 訟 制 度 之 比 較 研 究 A comparative study on the system of cross-straits tax litigation 研 究 生 : 羅 希 寧 中 華 民 一 0 一 年 七 月 論 文 摘 要 本 文 乃 係 兩 岸 稅 務 爭 訟 制 度 之
1
 全 民 健 康 保 險 提 升 民 眾 用 藥 品 質 方 案 中 華 民 國 98 年 10 月 1 日 健 保 審 字 第 0980095575 號 公 告 中 華 民 國 101 年 3 月 14 日 署 授 保 字 第 10100000800 號 公 告 修 正 壹 目 的 提 升 健 保 用 藥 品 質 及 便 利 性 貳 依 據 全 民 健 康 保 險 藥 價 基 準 參 定 義 : 一
全 民 健 康 保 險 提 升 民 眾 用 藥 品 質 方 案 中 華 民 國 98 年 10 月 1 日 健 保 審 字 第 0980095575 號 公 告 中 華 民 國 101 年 3 月 14 日 署 授 保 字 第 10100000800 號 公 告 修 正 壹 目 的 提 升 健 保 用 藥 品 質 及 便 利 性 貳 依 據 全 民 健 康 保 險 藥 價 基 準 參 定 義 : 一
 学 校 编 码 :10384 分 类 号 密 级 学 号 :X2007155130 UDC 厦 门 怡 福 养 生 健 康 管 理 有 限 公 司 创 业 计 划 王 韬 指 导 教 师 姓 名 : 郭 霖 教 授 厦 门 大 学 硕 士 学 位 论 文 厦 门 怡 福 养 生 健 康 管 理 有 限 公 司 创 业 计 划 A Business Plan for Xiamen Eve Health
学 校 编 码 :10384 分 类 号 密 级 学 号 :X2007155130 UDC 厦 门 怡 福 养 生 健 康 管 理 有 限 公 司 创 业 计 划 王 韬 指 导 教 师 姓 名 : 郭 霖 教 授 厦 门 大 学 硕 士 学 位 论 文 厦 门 怡 福 养 生 健 康 管 理 有 限 公 司 创 业 计 划 A Business Plan for Xiamen Eve Health
公 共 衛 生 教 育 與 人 力 現 況 與 展 望 第 四 節 對 台 灣 的 啟 示 30 第 三 章 國 內 公 共 衛 生 教 育 : 現 況 與 發 展 第 一 節 背 景 35 第 二 節 國 內 現 況 36 ( 一 ) 國 內 公 共 衛 生 校 系 設 置 概 況 36 ( 二
 目 錄 院 長 序 1 總 召 集 人 序 2 小 組 召 集 人 序 4 誌 謝 6 研 議 團 隊 7 執 行 摘 要 8 前 言 10 第 一 章 公 共 衛 生 之 定 義 與 範 疇 第 一 節 公 共 衛 生 概 念 的 演 進 15 第 二 節 公 共 衛 生 概 念 下 健 康 的 定 義 17 ( 一 ) 生 理 心 理 和 社 會 18 ( 二 ) 平 等 與 正 義 19 第
目 錄 院 長 序 1 總 召 集 人 序 2 小 組 召 集 人 序 4 誌 謝 6 研 議 團 隊 7 執 行 摘 要 8 前 言 10 第 一 章 公 共 衛 生 之 定 義 與 範 疇 第 一 節 公 共 衛 生 概 念 的 演 進 15 第 二 節 公 共 衛 生 概 念 下 健 康 的 定 義 17 ( 一 ) 生 理 心 理 和 社 會 18 ( 二 ) 平 等 與 正 義 19 第
Microsoft Word - 手冊(只有培訓單位)--V9
 目 錄 01 財 團 法 人 工 業 技 術 院 1 02 財 團 法 人 生 技 醫 療 科 技 政 策 中 心 8 03 財 團 法 人 生 物 技 術 開 中 心 10 04 財 團 法 人 金 屬 工 業 中 心 13 05 財 團 法 人 國 家 衛 生 院 18 06 財 團 法 人 農 業 科 技 院 21 07 財 團 法 人 醫 藥 工 業 技 術 中 心 24 08 財 團 法
目 錄 01 財 團 法 人 工 業 技 術 院 1 02 財 團 法 人 生 技 醫 療 科 技 政 策 中 心 8 03 財 團 法 人 生 物 技 術 開 中 心 10 04 財 團 法 人 金 屬 工 業 中 心 13 05 財 團 法 人 國 家 衛 生 院 18 06 財 團 法 人 農 業 科 技 院 21 07 財 團 法 人 醫 藥 工 業 技 術 中 心 24 08 財 團 法
Time Estimation of Occurrence of Diabetes-Related Cardiovascular Complications by Ching-Yuan Hu A thesis submitted in partial fulfillment of the requi
 Time Estimation of Occurrence of Diabetes-Related Cardiovascular Complications by Ching-Yuan Hu Master of Science 2011 Institute of Chinese Medical Sciences University of Macau Time Estimation of Occurrence
Time Estimation of Occurrence of Diabetes-Related Cardiovascular Complications by Ching-Yuan Hu Master of Science 2011 Institute of Chinese Medical Sciences University of Macau Time Estimation of Occurrence
Zytiga... Zytiga... Zytiga Zytiga Zytiga
 250 本資料僅提供醫護人員衛教使用 ............... Zytiga... Zytiga... Zytiga... 2 3 4 5 6 7 8 9 Zytiga... 10 Zytiga... 10...... 13 18 Zytiga Zytiga 2 25% 3 PSA PSA 3~4 ng/ml PSA bone scan CT scan MRI 4 5 攝護腺癌之治療 治療方面
250 本資料僅提供醫護人員衛教使用 ............... Zytiga... Zytiga... Zytiga... 2 3 4 5 6 7 8 9 Zytiga... 10 Zytiga... 10...... 13 18 Zytiga Zytiga 2 25% 3 PSA PSA 3~4 ng/ml PSA bone scan CT scan MRI 4 5 攝護腺癌之治療 治療方面
衞 66 43 衞 ii
 衞 衞 66 43 衞 [email protected] ii 2 4 4 9 9 10 15 18 18 20 22 iii - 1 - ( ) 衞 ( ) ( ) 1 256 (i) (ii) (iii) (iv) (v) (vi) (vii) 10 ( 100 320 ) ( 250 ) ( 160 ) ( 120 ) ( 91 ) ( 1 200 ) 60 0.60 60% - 2
衞 衞 66 43 衞 [email protected] ii 2 4 4 9 9 10 15 18 18 20 22 iii - 1 - ( ) 衞 ( ) ( ) 1 256 (i) (ii) (iii) (iv) (v) (vi) (vii) 10 ( 100 320 ) ( 250 ) ( 160 ) ( 120 ) ( 91 ) ( 1 200 ) 60 0.60 60% - 2
untitled
 01 HACCP (GHP) HACCP GMP CAS HACCP HACCP (hazard analysis and critical control point, HACCP) HACCP 2 Chapter 1 2000 2012 5,905 1,568 296 18.9% 101 527 104 46.2%(48/104) (hazard analysis and critical control
01 HACCP (GHP) HACCP GMP CAS HACCP HACCP (hazard analysis and critical control point, HACCP) HACCP 2 Chapter 1 2000 2012 5,905 1,568 296 18.9% 101 527 104 46.2%(48/104) (hazard analysis and critical control
杜邦行为守则
 确 保 将 来 可 持 续 发 展 践 行 我 们 的 核 心 价 值 观 二 O 一 三 年 六 月 杜 邦 首 席 执 行 官 致 辞 亲 爱 的 杜 邦 同 事 : 几 个 世 纪 以 来, 杜 邦 员 工 一 直 利 用 以 市 场 为 导 向 的 科 学 在 这 个 变 幻 莫 测 的 世 界 中 作 出 业 绩 虽 然 我 们 的 公 司 和 世 界 都 在 不 断 进 步 和 发 展,
确 保 将 来 可 持 续 发 展 践 行 我 们 的 核 心 价 值 观 二 O 一 三 年 六 月 杜 邦 首 席 执 行 官 致 辞 亲 爱 的 杜 邦 同 事 : 几 个 世 纪 以 来, 杜 邦 员 工 一 直 利 用 以 市 场 为 导 向 的 科 学 在 这 个 变 幻 莫 测 的 世 界 中 作 出 业 绩 虽 然 我 们 的 公 司 和 世 界 都 在 不 断 进 步 和 发 展,
运动员治疗用药豁免申报审批办法
 运 动 员 治 疗 用 药 豁 免 管 理 办 法 第 一 条 为 了 保 护 运 动 员 的 身 心 健 康, 保 证 运 动 员 的 伤 病 得 到 及 时 安 全 的 治 疗, 保 障 运 动 员 公 平 参 与 体 育 运 动 的 权 利, 根 据 国 务 院 反 兴 奋 剂 条 例, 参 照 世 界 反 兴 奋 剂 条 例 和 治 疗 用 药 豁 免 国 际 标 准 的 有 关 条 款,
运 动 员 治 疗 用 药 豁 免 管 理 办 法 第 一 条 为 了 保 护 运 动 员 的 身 心 健 康, 保 证 运 动 员 的 伤 病 得 到 及 时 安 全 的 治 疗, 保 障 运 动 员 公 平 参 与 体 育 运 动 的 权 利, 根 据 国 务 院 反 兴 奋 剂 条 例, 参 照 世 界 反 兴 奋 剂 条 例 和 治 疗 用 药 豁 免 国 际 标 准 的 有 关 条 款,
Microsoft PowerPoint - 101教師升等說明會
 2 1 3 4 2 5 並以該刊物出具接受證明之日起 6 3 7 8 4 9 10 5 11 12 6 13 14 7 15 靜宜大學教師升等資料 ( 僅供參考 ) 一 姓名 : 二 單位 : 三 現職 : 四 學歷 ( 請詳填起訖日期 ): 五 經歷 ( 請詳填起訖日期 ): 六 教師證書字號 : 年資起算日 : 七 學術專長領域 : 八 任現職期間教學工作 : ( 一 ) 授課記錄 ( 二 )
2 1 3 4 2 5 並以該刊物出具接受證明之日起 6 3 7 8 4 9 10 5 11 12 6 13 14 7 15 靜宜大學教師升等資料 ( 僅供參考 ) 一 姓名 : 二 單位 : 三 現職 : 四 學歷 ( 請詳填起訖日期 ): 五 經歷 ( 請詳填起訖日期 ): 六 教師證書字號 : 年資起算日 : 七 學術專長領域 : 八 任現職期間教學工作 : ( 一 ) 授課記錄 ( 二 )
Microsoft Word - 2目录.doc
 目 录 2014 年 度 获 证 企 业 年 会 会 议 日 程 安 排 1 会 议 资 料 1 强 化 管 理 是 企 业 经 营 必 由 之 路 --- 浅 谈 掌 握 法 律 法 规 知 识 对 企 业 管 理 的 重 要 意 义 5 2 ISO14001-2015(DIS) 标 准 修 订 的 最 新 动 态 及 主 要 变 化 22 3 实 施 环 境 管 理 体 系 的 绩 效 29 4
目 录 2014 年 度 获 证 企 业 年 会 会 议 日 程 安 排 1 会 议 资 料 1 强 化 管 理 是 企 业 经 营 必 由 之 路 --- 浅 谈 掌 握 法 律 法 规 知 识 对 企 业 管 理 的 重 要 意 义 5 2 ISO14001-2015(DIS) 标 准 修 订 的 最 新 动 态 及 主 要 变 化 22 3 实 施 环 境 管 理 体 系 的 绩 效 29 4
??? 1
 浙 江 省 肿 瘤 预 防 与 控 制 工 作 介 绍 Introduction to cancer control and prevention in Zhejiang Province 浙 江 省 疾 病 预 防 控 制 中 心 Zhejiang Provincial Center for Disease Control and Prevention 1 提 纲 (Outline) 流 行 病
浙 江 省 肿 瘤 预 防 与 控 制 工 作 介 绍 Introduction to cancer control and prevention in Zhejiang Province 浙 江 省 疾 病 预 防 控 制 中 心 Zhejiang Provincial Center for Disease Control and Prevention 1 提 纲 (Outline) 流 行 病
Microsoft Word - 刘 慧 板.doc
 中 国 环 境 科 学 2012,32(5):933~941 China Environmental Science 系 统 动 力 学 在 空 港 区 域 规 划 环 境 影 响 评 价 中 的 应 用 刘 慧 1,2, 郭 怀 成 1*, 盛 虎 1, 都 小 尚 1,3, 李 娜 1 1, 杨 永 辉 (1. 北 京 大 学 环 境 科 学 与 工 程 学 院, 北 京 100871; 2.
中 国 环 境 科 学 2012,32(5):933~941 China Environmental Science 系 统 动 力 学 在 空 港 区 域 规 划 环 境 影 响 评 价 中 的 应 用 刘 慧 1,2, 郭 怀 成 1*, 盛 虎 1, 都 小 尚 1,3, 李 娜 1 1, 杨 永 辉 (1. 北 京 大 学 环 境 科 学 与 工 程 学 院, 北 京 100871; 2.
東吳大學
 律 律 論 論 療 行 The Study on Medical Practice and Coercion 林 年 律 律 論 論 療 行 The Study on Medical Practice and Coercion 林 年 i 讀 臨 療 留 館 讀 臨 律 六 礪 讀 不 冷 療 臨 年 裡 歷 練 禮 更 老 林 了 更 臨 不 吝 麗 老 劉 老 論 諸 見 了 年 金 歷 了 年
律 律 論 論 療 行 The Study on Medical Practice and Coercion 林 年 律 律 論 論 療 行 The Study on Medical Practice and Coercion 林 年 i 讀 臨 療 留 館 讀 臨 律 六 礪 讀 不 冷 療 臨 年 裡 歷 練 禮 更 老 林 了 更 臨 不 吝 麗 老 劉 老 論 諸 見 了 年 金 歷 了 年
标题
 医 药 导 报 2016 年 8 月 第 35 卷 第 8 期 803 特 约 稿 鱼 腥 草 制 剂 上 市 后 安 全 性 再 评 价 吴 健 鸿 1 ꎬ 杨 晓 燕 2 ꎬ 柳 强 妮 2 ꎬ 尹 平 2 2 ꎬ 曾 繁 典 (1. 武 汉 药 品 医 疗 器 械 检 验 所 ꎬ 武 汉 430075ꎻ2. 华 中 科 技 大 学 同 济 医 学 院 ꎬ 武 汉 430030) 摘 要 目 的
医 药 导 报 2016 年 8 月 第 35 卷 第 8 期 803 特 约 稿 鱼 腥 草 制 剂 上 市 后 安 全 性 再 评 价 吴 健 鸿 1 ꎬ 杨 晓 燕 2 ꎬ 柳 强 妮 2 ꎬ 尹 平 2 2 ꎬ 曾 繁 典 (1. 武 汉 药 品 医 疗 器 械 检 验 所 ꎬ 武 汉 430075ꎻ2. 华 中 科 技 大 学 同 济 医 学 院 ꎬ 武 汉 430030) 摘 要 目 的
公開發行公司年報應行記載事項準則相關附表(98.12.22)
 股 票 代 碼 :4166 一 年 度 年 報 中 華 民 國 一 一 年 五 月 二 十 二 日 刊 印 本 年 報 相 關 內 容 請 至 公 開 資 訊 觀 測 站 查 詢 網 址 : http://newmops.twse.com.tw 一 本 公 司 發 言 人 : 發 言 人 : 楊 正 梅 電 話 :(02)2325-7621 代 理 發 言 人 : 張 奕 欣 電 話 :(02)2325-7621
股 票 代 碼 :4166 一 年 度 年 報 中 華 民 國 一 一 年 五 月 二 十 二 日 刊 印 本 年 報 相 關 內 容 請 至 公 開 資 訊 觀 測 站 查 詢 網 址 : http://newmops.twse.com.tw 一 本 公 司 發 言 人 : 發 言 人 : 楊 正 梅 電 話 :(02)2325-7621 代 理 發 言 人 : 張 奕 欣 電 話 :(02)2325-7621
Abstract The Research Origin: Since its enactment in 28 th December 2005, the Freedom of Government Information Law has been enforced for six years. S
 法 務 部 民 國 100 年 委 託 研 究 案 政 府 資 訊 限 制 公 開 或 提 供 事 由 審 查 基 準 及 改 進 救 濟 程 序 之 研 究 研 究 成 果 報 告 書 計 畫 編 號 : Lee100406 執 行 單 位 : 銘 傳 大 學 科 技 法 律 學 系 計 畫 主 持 人 : 范 姜 真 媺 副 教 授 協 同 主 持 人 : 郭 介 恒 副 教 授 王 毓 正 副
法 務 部 民 國 100 年 委 託 研 究 案 政 府 資 訊 限 制 公 開 或 提 供 事 由 審 查 基 準 及 改 進 救 濟 程 序 之 研 究 研 究 成 果 報 告 書 計 畫 編 號 : Lee100406 執 行 單 位 : 銘 傳 大 學 科 技 法 律 學 系 計 畫 主 持 人 : 范 姜 真 媺 副 教 授 協 同 主 持 人 : 郭 介 恒 副 教 授 王 毓 正 副
1.2 资 金 的 管 理 1.1 权 利 义 务 来 源 MOU 1.3 数 据 的 使 用 和 保 护 2 国 际 空 间 站 资 源 分 配 方 案 54
 第 29 卷 第 12 期 全 球 科 技 经 济 瞭 望 Vol. 29 No. 12 2014 年 12 月 Global Science, Technology and Economy Outlook Dec. 2014 刘 阳 子 ( 中 国 科 学 技 术 信 息 研 究 所, 北 京 ) 摘 要 : 空 间 探 索 既 复 杂 艰 巨 又 耗 资 甚 大, 因 此, 世 界 各 国 无
第 29 卷 第 12 期 全 球 科 技 经 济 瞭 望 Vol. 29 No. 12 2014 年 12 月 Global Science, Technology and Economy Outlook Dec. 2014 刘 阳 子 ( 中 国 科 学 技 术 信 息 研 究 所, 北 京 ) 摘 要 : 空 间 探 索 既 复 杂 艰 巨 又 耗 资 甚 大, 因 此, 世 界 各 国 无
关 于 瓶 装 水, 你 不 得 不 知 的 8 件 事 情 关 于 瓶 装 水, 你 不 得 不 知 的 8 件 事 情 1 水 质 : 瓶 装 的, 不 一 定 就 是 更 好 的 2 生 产 : 监 管 缺 位, 消 费 者 暴 露 于 风 险 之 中 人 们 往 往 假 定 瓶 装 水 是
 关 于 瓶 装 水, 你 不 得 不 知 的 件 事 情 关 于 瓶 装 水, 你 不 得 不 知 的 8 件 事 情 关 于 瓶 装 水, 你 不 得 不 知 的 8 件 事 情 1 水 质 : 瓶 装 的, 不 一 定 就 是 更 好 的 2 生 产 : 监 管 缺 位, 消 费 者 暴 露 于 风 险 之 中 人 们 往 往 假 定 瓶 装 水 是 干 净 安 全 健 康 的, 广 告 传 递
关 于 瓶 装 水, 你 不 得 不 知 的 件 事 情 关 于 瓶 装 水, 你 不 得 不 知 的 8 件 事 情 关 于 瓶 装 水, 你 不 得 不 知 的 8 件 事 情 1 水 质 : 瓶 装 的, 不 一 定 就 是 更 好 的 2 生 产 : 监 管 缺 位, 消 费 者 暴 露 于 风 险 之 中 人 们 往 往 假 定 瓶 装 水 是 干 净 安 全 健 康 的, 广 告 传 递
基 本 資 料 - 本 報 告 書 以 環 保 再 生 紙 影 印
 基 本 資 料 103 年 度 臺 北 市 推 動 資 源 回 收 形 象 改 造 暨 物 業 管 理 工 作 計 畫 基 本 資 料 表 甲 委 辦 單 位 臺 北 市 政 府 環 境 保 護 局 乙 執 行 單 位 綠 信 環 境 科 技 股 份 有 限 公 司 丙 年 度 103 年 計 畫 編 號 103 環 勞 025 號 丁 專 案 性 質 非 屬 財 務 之 工 程 或 勞 務 戊 計
基 本 資 料 103 年 度 臺 北 市 推 動 資 源 回 收 形 象 改 造 暨 物 業 管 理 工 作 計 畫 基 本 資 料 表 甲 委 辦 單 位 臺 北 市 政 府 環 境 保 護 局 乙 執 行 單 位 綠 信 環 境 科 技 股 份 有 限 公 司 丙 年 度 103 年 計 畫 編 號 103 環 勞 025 號 丁 專 案 性 質 非 屬 財 務 之 工 程 或 勞 務 戊 計
Microsoft Word - 98全國大學校長會議
 目 錄 壹 會 議 議 程 1 貳 專 題 演 講 4 專 題 演 講 ( 一 ): 校 園 民 主 與 學 術 自 由 4 專 題 演 講 ( 二 ): 高 等 教 育 新 視 界 - 彈 性 化 優 質 化 國 際 化 6 專 題 演 講 ( 三 ): 從 學 校 到 工 作 - 談 尊 嚴 勞 動 14 專 題 演 講 ( 四 ): 如 何 重 建 道 德 推 廣 大 學 有 品 運 動 24
目 錄 壹 會 議 議 程 1 貳 專 題 演 講 4 專 題 演 講 ( 一 ): 校 園 民 主 與 學 術 自 由 4 專 題 演 講 ( 二 ): 高 等 教 育 新 視 界 - 彈 性 化 優 質 化 國 際 化 6 專 題 演 講 ( 三 ): 從 學 校 到 工 作 - 談 尊 嚴 勞 動 14 專 題 演 講 ( 四 ): 如 何 重 建 道 德 推 廣 大 學 有 品 運 動 24
0-80-10() ISO ISO ISO/IEC Directives2012 (High Level Structure, HLS) () ISO31000 ISO31000 () () 2005 ISO 2.(Normative references) ISO27001:20132005 27
 ISO27001:2013ISO27001:2005 International Organization for StandardizationISO2013 10ISO27001:2005ISO 27001:2013ISO 270012005ISO27001:2005 24 ISO 27001:20052015930 (Mobile Payment)(BYOD) (Social Media)(Big
ISO27001:2013ISO27001:2005 International Organization for StandardizationISO2013 10ISO27001:2005ISO 27001:2013ISO 270012005ISO27001:2005 24 ISO 27001:20052015930 (Mobile Payment)(BYOD) (Social Media)(Big
,7 8,9 10,11 (1) (2) (3)
 J Chin Med 18(3,4): 129-146, 2007 129 1,3 2 2 2 4 4 4 1 2 3 4 96 10 5 96 11 7 Delphi Method Content Validity Index, CVI0.81 2 3 1 2 123 03-3196200 3302 E-mail [email protected] 130 3 4 5 6,7 8,9 10,11
J Chin Med 18(3,4): 129-146, 2007 129 1,3 2 2 2 4 4 4 1 2 3 4 96 10 5 96 11 7 Delphi Method Content Validity Index, CVI0.81 2 3 1 2 123 03-3196200 3302 E-mail [email protected] 130 3 4 5 6,7 8,9 10,11
Microsoft Word - 博士班學校及系組招生規定_20151118_060130_.docx
 海 外 聯 合 招 生 委 員 會 2016 年 秋 季 入 學 僑 生 及 港 澳 學 生 申 請 就 讀 博 士 班 校 系 分 則 及 招 生 一 覽 表 一 本 表 招 生 校 系 及 業 經 教 育 部 104 年 9 月 30 日 臺 教 高 ( 四 ) 字 第 1040130610 號 104 年 10 月 14 日 臺 教 高 ( 四 ) 字 第 1040139409 號 104 年
海 外 聯 合 招 生 委 員 會 2016 年 秋 季 入 學 僑 生 及 港 澳 學 生 申 請 就 讀 博 士 班 校 系 分 則 及 招 生 一 覽 表 一 本 表 招 生 校 系 及 業 經 教 育 部 104 年 9 月 30 日 臺 教 高 ( 四 ) 字 第 1040130610 號 104 年 10 月 14 日 臺 教 高 ( 四 ) 字 第 1040139409 號 104 年
