Hepsera
|
|
|
- 诊摘 黄
- 7 years ago
- Views:
Transcription
1 TM 干適能錠 HEPSERA TM Tablets 衛署藥輸字第 號 警語 : 嚴重的肝炎急性惡化 腎毒性 HIV 抗藥性 乳酸中毒, 以及伴隨脂肪變性之嚴重肝腫大 曾有中斷使用抗 B 型肝炎療法 ( 包括干適能 ) 的病患, 發生嚴重肝炎急性惡化的報告, 因此, 應針對中斷抗 B 型肝炎治療的病患, 進行臨床與實驗室檢測追蹤, 以密切監測肝功能, 且至少必須持續監測數個月 若有需要, 應考慮重新開始進行抗 B 型肝炎治療 [ 請參閱警語及注意事項 (5.1)] 有腎功能障礙風險或已有腎功能障礙的病患長期使用干適能, 可能會造成腎毒性, 應密切追蹤其腎功能, 且可能需要調整其劑量 [ 請參閱警語及注意事項 (5.2) 與用法用量 (2.2)] 不知已感染或未接受治療人類免疫缺乏病毒 (HIV) 的慢性 B 型肝炎患者, 在接受可能具有抗 HIV 效用的抗 B 型肝炎療法 ( 例如干適能 ) 治療時, 都可能會出現 HIV 抗藥性 [ 請參閱警語及注意事項 (5.3)] 曾有單獨使用核苷類似物 (nucleoside analogs) 或併用其他抗反轉錄病毒藥物時, 發生乳酸中毒與伴隨脂肪變性之嚴重肝腫大 ( 包括致死病例 ) 的報告 [ 請參閱警語及注意事項 (5.4)] 1 適應症 治療有 B 型肝炎病毒複製跡象的成人慢性 B 型肝炎患者 說明 : 根據少數病患身上所進行的支持性研究而得到的有限資料顯示, 針對具有 lamivudine 抗藥性的慢性 B 型肝炎患者 ( 包括併有代償性或代償不全性肝病的病患以及合併感染 HIV 的病患 ), 本藥可產生使病毒複製作用降低以及改善肝功能的作用 ( 參見警語及注意事項 )
2 2 用法用量 本藥須由醫師處方使用 2.1 慢性 B 型肝炎 成人 (18-65 歲 ): 干適能錠的建議劑量為一天一次, 一次一顆 與食物併服或不與食物併服皆可 此項建議劑量主要根據為期 48 週之臨床試驗結果 目前仍不確定最理想的治療期間 兒童與青少年 (< 18 歲 ): 干適能錠對 18 歲以下之患者的安全性與療效尚未確立 ( 參見警語及注意事項 ) 老年人 (> 65 歲 ): 干適能錠對 65 歲以上之患者的安全性與療效尚未確立 ( 參見警語及注意事項 ) 肝功能不全者 : 對肝功能不全的患者, 並不須調整其劑量 2.2 腎功能不全病患的劑量調整 曾在使用干適能之腎功能不全的成人病患體內, 觀察到曝藥量顯著增加的情形 [ 請參閱警語及注意事項 (5.2) 與臨床藥理學 (12.3)], 因此, 於基準點時, 肌酸酐清除率低於 50 ml/ 分鐘的成人病患, 應依據下列建議準則調整干適能的用藥間隔 ( 詳見表 1) 惟該等用藥間隔調整準則的安全性與有效性, 尚未經臨床評估 此外, 請務必注意, 該等準則係根據基準點時已存有腎功能不全 (pre-existing renal impairment at baseline) 之病患的相關資料而擬定, 可能不適用在干適能治療期間出現腎功能不全的病患, 因此, 應密切監測這些病患對治療的臨床反應及其腎功能 表 1 腎功能不全成人病患之干適能用藥間隔的調整 肌酸酐清除率 (ml/min) a 血液透析病患 建議劑量與用藥間隔 10 mg, 每 24 小時一次 10 mg, 每 48 小時一次 10 mg, 每 72 小時一次 10 mg, 每 7 天一次, 血液 透析後服用 a. 肌酸酐清除率係以 Cockcroft-Gault 方法, 使用瘦肉體重 (lean body weight) 或理想體重進行計算 尚未針對肌酸酐清除率低於 10 ml/ 分鐘的非血液透析病患, 進行 adefovir 的藥物動力學評估, 因此無法為該等病患提供用藥建議 尚未有腎功能不全之青少年病患的臨床資料, 故無法擬定用藥建議 [ 請參閱警語及注意事項 (5.2)] 3 劑型與藥物含量 10 毫克干適能錠為白至灰白色, 邊緣呈斜角的圓形平面錠劑 一面刻有 "GS KNU" 字樣, 另一面空白
3 4 禁忌 先前曾對本產品之任何成分過敏的病患, 不可使用干適能 5 警語及注意事項 5.1 中斷治療後肝炎惡化曾有中斷使用抗 B 型肝炎療法 ( 包括干適能 ) 的病患, 發生嚴重肝炎急性惡化的報告, 因此, 應針對中斷干適能治療的病患, 進行臨床與實驗室檢測追蹤, 以定期監測肝功能, 且至少必須持續監測數個月 若有需要, 應考慮重新開始進行抗 B 型肝炎治療 [ 請參閱警語及注意事項 (5.1)] 在干適能的臨床試驗中, 於中斷干適能治療後出現肝炎惡化 (ALT 升高至正常值上限的 10 倍或更高 ) 的受試者, 高達 25% 在 GS 與 GS 試驗 (N=492) 中皆曾觀察到該等事件, 且大多發生於中斷用藥後 12 週內, 而在發生這些惡化時通常未伴隨 HBeAg 血清轉變 (seroconversion), 表現方式除了再出現病毒複製外, 血清 ALT 亦會升高 在針對具有代償性肝功能的病患進行的 HBeAg- 陽性與 HBeAg- 陰性研究中, 肝炎惡化通常未伴隨發生肝功能代償不全 (hepatic decompensation), 不過, 末期肝臟疾病或肝硬化之病患出現肝功能代償不全風險的可能性較高 雖然大部分事件皆具有自限性或於重新開始治療後消失, 但亦曾有出現嚴重肝炎惡化 ( 包括致死 ) 的報告, 因此, 在停止治療後, 病患應接受密切追蹤 5.2 腎毒性 HIV 感染者使用高劑量時 ( 一天 60 與 120 mg) 與慢性 B 型肝炎患者使用高劑量時 ( 一天 30 mg) 的組織學分析顯示, 腎毒性 ( 特徵為延遲性血清肌酸酐逐漸增加及血清磷減少 ) 為 adefovir dipivoxil 療法的限制性毒性 若長期使用干適能 (10 mg, 一天一次 ) 可能會造成延遲性腎毒性, 惟腎功能正常者的整體腎毒性風險低, 然而, 對於有腎功能障礙風險或已有腎功能障礙的病患, 以及正在同時使用具腎毒性之藥物 ( 例如環孢靈 [cyclosporine] tacrolimus 胺基醣苷類藥物[aminoglycosides] 萬古黴素[vancomycin] 與非類固醇抗發炎藥物 ) 的病患而言, 非常重要 [ 請參閱不良反應 (6.2) 與臨床藥理學 (12.3)] 建議所有的病患皆應在開始進行干適能治療之前, 先接受肌酸酐清除率評估 在接受干適能治療之期間, 所有病患均應接受腎功能監測, 尤其是已有腎功能不全狀況者或具有其他腎功能不全風險者 於基準點時或治療期間有腎功能不全狀況的病患, 可能必須調整劑量 [ 請參閱用法用量 (2.2)], 而於治療時出現腎毒性的病患, 則應在中斷干適能治療之前, 先謹慎評估干適能治療的風險與效益
4 兒童病患 尚未針對不同之腎功能不全程度的 18 歲以下病患, 進行干適能的療效與安全性分析, 因此, 無資料可供提出該等病患的劑量建議 [ 請參閱用法用量 (2.2)] 5.3 HIV 抗藥性在開始進行干適能治療之前, 應先檢測所有病患的 HIV 抗體 未發現已感染 HIV 或未進行 HIV 治療的慢性 B 型肝炎病患, 可能會在接受具有抗 HIV 效用之抗 B 型肝炎療法 ( 例如干適能 ) 治療時, 出現 HIV 抗藥性 目前尚無研究顯示干適能可抑制病患的 HIV RNA, 不過, 已有極少數使用干適能治療合併感染 HIV 之慢性 B 型肝炎患者的資料 同時感染 HIV 以 HEPSERA 10 毫克進行治療並未顯示能有效抑制 HIV 複製 同時感染 HIV 之患者應該在 HEPSERA 10 毫克治療前, 以核准之抗反轉錄病毒療法控制 HIV RNA (< 400 copies/ml) 對合併感染 HIV 但不須採取抗反轉錄病毒療法的患者, 在單獨使用 adefovir 治療慢性 B 型肝炎時, 有使 HIV 突變的危險 5.4 乳酸中毒 / 伴隨脂肪變性 (Steatosis) 之嚴重肝腫大曾有單獨使用核苷類似物 (nucleoside analogs) 或併用抗反轉錄病毒藥物時, 發生乳酸中毒與伴隨脂肪變性之嚴重肝腫大 ( 包括致死病例 ) 的報告 該等病例大多為婦女, 肥胖與長期核苷暴露可能為危險因子 具有已知肝臟疾病危險因子的任何病患, 在使用核苷類似物時, 均應特別謹慎, 但是, 亦曾有無已知危險因子者發生病例的報告 在臨床或實驗室檢測中, 發現出現可顯示乳酸中毒或明顯肝毒性 ( 可能包括肝腫大與脂肪變性, 即使轉胺酶未明顯升高 ) 的病患, 應暫時停止干適能治療 5.5 與其他藥品併用干適能不可與 VIREAD(tenofovir disoproxil fumarate) 或含有 tenofovir disoproxil fumarate 的產品 ( 包括 ATRIPLA [efavirenz/emtricitabine/tenofovir disoproxil fumarate 複合錠劑 ] COMPLERA [emtricitabine/rilpivirine/tenofovir disoproxil fumarate 複合錠劑 ] STRIBILD [elvitegravir/cobicistat/emtricitabine/tenofovir disoproxil fumarate 複合錠劑 ] 與 TRUVADA [emtricitabine/tenofovir disoproxil fumarate 複合錠劑 ]) 併用 5.6 臨床抗藥性
5 對 adefovir dipivoxil 產生抗藥性, 可能會造成病毒量反彈而導致 B 型肝炎惡化, 若肝功能下降, 則可能會導致肝功能代償不全及可能致命的結果 adefovir dipivoxil 應與 lamivudine 併用, 切勿單獨使用 adefovir dipivoxil, 以降低有 lamivudine 抗藥性之 HBV 感染者的抗藥性風險 若在持續治療時, 血清 HBV DNA 仍高於 1000 copies/ml, 即應考慮調整療法, 以降低所有接受 adefovir dipivoxil 單一療法之病患的抗藥性風險 從 438 號研究 (N=124) 取得之長期 ( 144 週 ) 資料顯示, 相較於治療第 48 週時血清 HBV DNA 量低於 1000 copies/ml 的病患, 第 48 週時 HBV DNA 量高於 1000 copies/ml 者接受干適能治療時出現抗藥性的風險較高 6 不良反應以下不良反應將會在本藥品標示的其他章節中討論 : 嚴重的肝炎急性惡化 [ 請參閱加框警語及注意事項 (5.1)] 腎毒性 [ 請參閱加框警語及注意事項 (5.2)] 6.1 臨床試驗經驗由於臨床試驗係在各種不同的狀況下進行, 因此在臨床試驗中觀察到一種藥物的不良反應發生率, 無法直接與在臨床試驗中觀察到另一種藥物的發生率進行比較, 也可能無法反映出臨床上實際觀察到的發生率 曾有臨床與實驗室證據顯示, 病患在干適能治療中斷後出現肝炎惡化 在安慰劑對照及開放標示的試驗中, 確認干適能的不良反應包括 : 虛弱無力 頭痛 腹痛 腹瀉 噁心 消化不良 胃腸脹氣 肌酸酐增加與低磷酸鹽血症 (hypophosphatemia) 在 437 與 438 號試驗中, 總計有 522 位併有代償性肝臟疾病的慢性 B 型肝炎患者, 接受雙盲的干適能 (N=294) 或安慰劑 (N=228) 治療 48 週, 這兩項試驗中的不良反應發生率如表 2 所示 在 438 號試驗中, 接受開放標示之干適能治療最長 240 週之病患發生的不良反應, 與前 48 週報告者的性質與嚴重程度皆相近
6 表 號試驗中, 所有接受干適能治療者之發生率 3% 的不良反應 ( 第 1 4 級 )(0 48 週 ) a 不良反應 干適能 10mg (N=294) 安慰劑 (N=228) 虛弱無力 13% 14% 頭痛 9% 10% 腹痛 9% 11% 噁心 5% 8% 胃腸脹氣 4% 4% 腹瀉 3% 4% 消化不良 3% 2% a. 於該等試驗中, 干適能的不良反應整體發生率皆與安慰劑相近 不良反應發生率係依據試驗主持人確認的治療相關事件計算 第 48 週時, 無任何接受干適能治療者, 經確認血清肌酸酐濃度較基準點增加 0.5 mg/dl 或更多, 亦無人經確認磷濃度降至 2 mg/dl 或更低, 至第 96 週時, 根據 Kaplan-Meier 估計值, 顯示有 2% 接受干適能治療者的血清肌酸酐, 較基準點增加 0.5 mg/dl 或更多 ( 第 48 週之後無安慰劑對照的結果可供比較 ) 在 438 號試驗中決定繼續接受干適能治療最長 240 週的 125 位受試者, 有 4 人 (3%) 經確認血清肌酸酐較基準點增加 0.5 mg/dl, 其中有一位病患在終止治療後, 肌酸酐升高的情形已消失,3 位繼續接受治療的病患則維持穩定 在 437 號試驗中決定繼續接受干適能治療最長 240 週的 65 位受試者, 有 6 人經確認血清肌酸酐較基準點增加 0.5 mg/dl 或更多, 其中 2 人因血清肌酸酐濃度升高而退出試驗 於基準點時, 腎功能不全者的血清肌酸酐變化相關資料, 請參閱 不良反應 (6.2) 一節 6.2 有特殊風險的病患肝臟移植前與移植後的病患在針對有慢性 B 型肝炎與 lamivudine 抗藥性 B 型肝炎之肝臟移植前與移植後病患 ( 接受一天一次干適能治療最長 203 週 ) 進行的開放標示試驗 (435 號試驗 ) 中, 觀察到的其他不良反應包括 : 腎功能異常 腎衰竭 嘔吐 皮疹與搔癢 具腎功能障礙危險因子 ( 包括併用環孢靈與 tacrolimus 基準點時腎功能不全 高血壓 糖尿病與研究期間接受移植 ) 的肝臟移植前與移植後病患, 曾出現腎功能變化, 因此, 很難評估干適能在促成腎功能變化上扮演何種角色
7 根據 Kaplan-Meier 估計值, 顯示在第 48 週與第 96 週時, 肝臟移植前病患分別有 37% 與 53%, 而肝臟移植後病患則分別有 32% 與 51% 的血清肌酸酐濃度, 較基準點時增加 0.3 mg/dl 或更多, 至最後一次研究回診時, 有 3/226(1.3%) 的肝臟移植前病患及 6/241(2.5%) 的肝臟移植後病患, 血清磷濃度低於 2 mg/dl 此外, 有 4%(19/467) 的病患因腎臟不良事件而中斷干適能治療 6.4 上市後經驗除臨床試驗報告的不良反應外, 在 adefovir dipivoxil 獲准上市後, 亦發現以下可能的不良反應, 由於該等事件是由人數不明的族群自發通報, 因此無法估計其發生率 代謝與營養疾患 : 低磷血症 腸胃疾患 : 胰臟炎 肌肉骨骼系統與結締組織疾患 : 肌肉病變 軟骨症 (osteomalacia, 有骨頭疼痛之表徵, 且可能會造成骨折 ), 兩者皆伴隨近端腎小管病變 (proximal renal tubulopathy) 腎臟與泌尿疾患 : 腎衰竭 Fanconi 症候群 近端腎小管病變
8 7 藥物交互作用 由於 adefovir 是由腎臟排除, 因此干適能與可能降低腎功能或競爭腎小管主動分泌作用 (active tubular secretion) 的藥物併用時, 可能會使血清中之 adefovir 及 / 或併用藥物的濃度增加 [ 請參閱臨床藥理學 (12.3)] 當干適能與經由腎臟排除或已知會影響腎功能之其他藥物併用時, 應密切監測病患是否發生不良事件 [ 請參閱警語及注意事項 (5.2)] 干適能不可與 tenofovir disoproxil fumarate 併用 [ 請參閱警語及注意事項 (5.5)] 8 特定族群的使用 8.1 懷孕致畸胎性 : 懷孕用藥級數屬於 C 級 干適能尚未針對懷孕婦女進行具良好對照組的適當試驗 慢性 B 型肝炎為需要治療的嚴重狀況, 因此僅可在干適能對母親的可能效益, 超過對胎兒的可能風險時, 才可使用此藥物 懷孕大鼠與兔子的生殖研究顯示, 以口服方式給予 adefovir dipivoxil 後, 未在全身曝藥量相當於人類使用治療劑量之曝藥量的 23 倍 ( 大鼠 ) 與 40 倍 ( 兔子 ) 時, 發現胚胎毒性或致畸胎性, 但是, 在懷孕大鼠接受靜脈注射 adefovir 後, 曝藥量為人類使用治療劑量之曝藥量的 38 倍時, 即可發現胚胎毒性與畸胎 ( 全身水腫 扁平性凸眼 臍疝與尾巴捲縮 ) 發生率增高的現象 於靜脈注射後, 曝藥量約為人類使用治療劑量之曝藥量的 12 倍時, 未出現這些不良生殖影響 因為動物生殖研究不一定可預測人體的反應, 因此僅可在明確需要以及謹慎考量風險與益處之後, 使用干適能 [ 請參閱非臨床毒理學 (13.2)] 8.2 分娩目前尚無針對懷孕婦女進行的研究, 亦無干適能對於母親將 HBV 垂直傳染給嬰兒之狀況有何影響的相關資料, 可供參考, 因此, 應給予嬰兒適當的免疫接種, 避免新生兒感染 B 型肝炎病毒
9 8.3 哺乳婦女 目前不瞭解 adefovir 是否會分泌至人乳 由於許多藥物皆可分泌至人乳, 且哺乳嬰兒可能會對干適能產生嚴重不良反應, 因此, 必須考量藥物對母親的重要性, 而決定是否中斷哺乳或中斷使用藥物 8.5 老年人的使用干適能之臨床試驗納入的 65 歲以上病患不足, 因此無法決定其反應是否與較年輕病患有差異 一般而言, 在開立處方給老年病患時, 應謹慎, 因為老年病患通常會同時罹患其他疾病, 或併用其他藥物治療, 而提高其腎功能或心臟功能降低的機率 8.6 腎功能不全的病患建議為基準點肌酸酐清除率 (baseline creatinine clearance) 低於 50 ml/ 分鐘的成人病患, 調整干適能的用藥間隔 目前尚未針對肌酸酐清除率低於 10 ml/ 分鐘的非血液透析病患或腎功能不全的青少年病患, 進行 adefovir 的藥物動力學評估, 因此, 無法針對這些病患提出用藥方法建議 [ 請參閱用法用量 (2.2) 與警語及注意事項 (5.2)] 10 過量以一天一次 500 mg 劑量的 adefovir dipivoxil 治療 2 週, 以及以一天一次 250 mg 治療 12 週, 可能會引發腸胃副作用 若發生用藥過量時, 必須監測病患是否出現毒性證據, 並視需要給予支持性治療
10 在服用單劑 10 毫克干適能之後, 進行血液透析 4 小時, 大約可移除 35% 的 adefovir 劑量 11 性質說明 干適能為 adefovir dipivoxil 的商品名稱,adefovir dipivoxil 為 adefovir 的二酯前驅藥物, 而 Adefovir 為具有對抗人類 B 型肝炎病毒 (HBV) 感染之活性的非環狀核苷類似物 Adefovir dipivoxil 的化學名為 9-[2-[[bis[(pivaloyloxy)methoxy]-phosphinyl]- methoxy]ethyl]adenine, 分子式為 C 20 H 32 N 5 O 8 P, 分子量 , 構造式如下 : Adefovir dipivoxil 為白至灰白色的結晶粉末, 在 ph 2.0 的水中溶解度為 19 mg/ml, 在 ph 7.2 時為 0.4 mg/ml 於 octanol/ 磷酸鹽緩衝液 (ph 7) 中的分布係數 (partition coefficient)(log p) 為 1.91 干適能為口服型錠劑, 每顆錠劑含有 10 毫克 adefovir dipivoxil 與以下不具活性的成分 :croscarmellose sodium lactose monohydrate magnesium stearate pregelatinized starch 與 talc 12 臨床藥理學 12.1 作用機轉 Adefovir 為抗病毒藥物 [ 請參閱臨床藥理學 (12.4)] 12.3 藥物動力學成人病患已針對健康自願受試者與慢性 B 型肝炎患者進行 adefovir 的藥物動力學評估 此二族群具有相似的 adefovir 藥物動力學特性
11 吸收 Adefovir dipivoxil 為活性成分 adefovir 的二酯前驅藥 (diester prodrug) 根據一項交叉研究比較 (cross study comparison) 的結果顯示, 由干適能轉化成 adefovir 的口服生體可用率約為 59% 慢性 B 型肝炎患者 (N=14) 在口服單劑 10 毫克干適能後 0.58 至 4.00 小時 ( 中位數 = 1.75 小時 ) 達最高血漿濃度, adefovir 的最高血漿濃度 (C max ) 為 18.4 ± 6.26 ng/ml ( 平均值 ± 標準差 ),Adefovir 的血漿濃度 - 時間曲線下面積 (AUC 0- ) 為 220 ± 70.0 ng h/ml 血漿 adefovir 濃度係以雙指數 (biexponential) 方式下降, 終端排除半衰期為 7.48 ± 1.65 小時 腎功能正常之病患的 adefovir 藥物動力學狀況, 不受連續 7 天每天服用一次 10 毫克干適能的影響 目前尚未評估長期每天服用一次 10 毫克干適能, 對 adefovir 的藥物動力學有何影響 食物對口服吸收狀況的影響單劑 10 毫克干適能與食物 ( 大約 1000 大卡高脂飲食 ) 併服時,adefovir 的曝藥量不會受到影響 干適能可配食物服用或單獨服用 分佈在 0.1 至 25 μg/ml 濃度範圍內,adefovir 與人類血漿或人類血清蛋白的體外結合率為 4% 在靜脈注射 1.0 或 3.0 mg/kg/day 劑量之後, 達穩定狀態時的分佈體積, 分別為 392 ± 75 與 352 ± 9 ml/kg 代謝與排除口服之後,adefovir dipivoxil 會快速地轉化為 adefovir 在口服 10 毫克干適能之後, 達到穩定狀態的 24 小時期間, 會有 45% 的干適能口服劑量以 adefovir 的形式至尿液中回收,Adefovir 係經由腎臟的腎小球過濾作用與腎小管主動分泌作用排出體外 [ 請參閱藥物交互作用 (7) 與臨床藥理學 (12.3)] 藥物交互作用的評估 Adefovir dipivoxil 可在體內快速轉化為 adefovir adefovir 在比體內觀察到之濃度高出甚多 ( 大於 4000 倍 ) 的濃度下, 不會抑制任何常見之人類 CYP450 酵素 (CYP1A2 CYP2C9 CYP2C19 CYP2D6 與 CYP3A4) 的作用, 且 Adefovir 非這些酵素的受質, 但是, 尚不瞭解 adefovir 是否可誘發 CYP450 酵素 根據這些體外實驗的結果以及 adefovir 的腎臟排除路徑,adefovir 與其他藥物藉由 CYP450 產生交互作用 (adefovir 做為 CYP450 酵素之抑制劑或受質 ) 的可能性極低
12 現已針對健康成人自願受試者, 在投予多劑干適能 (10 毫克, 一天一次 ), 且併用 lamivudine(100 毫克, 一天一次 ) (N=18) trimethoprim/sulfamethoxazole(160/800 毫克, 一天兩次 ) (N=18) acetaminophen(1000 毫克, 一天四次 )(N=20) ibuprofen(800 毫克, 一天三次 )(N=18) 及包有腸溶衣的 didanosine (400 mg) (N=21) 之後, 評估 adefovir 的藥物動力學 亦已針對肝臟移植後的病患, 在已投予多劑干適能 (10 毫克, 一天一次 ) 且併用 tacrolimus (N=16) 之後, 評估 adefovir 的藥物動力學, 並已針對健康成人自願受試者, 在投予單劑聚乙二醇化干擾素 α-2a(pegylated interferon α-2a,pegifn))(180 μg) (N=15) 之後, 評估 adefovir 的藥物動力學 Adefovir 未改變 lamivudine trimethoprim/sulfamethoxazole acetaminophen ibuprofen 包有腸溶衣的 didanosine (didanosine EC) 或 tacrolimus 的藥物動力學 由於聚乙二醇化干擾素 α-2a 的變動性極大, 因此尚不確定 adefovir 對其藥物動力學有何影響 干適能與 lamivudine trimethoprim/sulfamethoxazole acetaminophen didanosine EC tacrolimus( 根據交叉研究比較結果 ) 和聚乙二醇化干擾素 α-2a 併用時, 不會改變 adefovir 的藥物動力學 干適能與 ibuprofen(800 毫克, 一天三次 ) 併用時, 會提高 adefovir C max (33%) 及 AUC (23%) 與尿中的排泄量, 此可能為口服生體可用率較高所致, 而非 adefovir 的腎臟清除率降低 除了 lamivudine trimethoprim/sulfamethoxazole 與 acetaminophen 外, 尚未評估干適能與經由腎臟排除之藥物, 或已知可影響腎臟功能之其他藥物併用的影響 尚不瞭解 Adefovir 對 cyclosporine 濃度有何影響 尚未針對 12 歲至 18 歲以下的青少年病患, 進行藥物交互作用研究 特族群群性別男性與女性病患具有相似的 adefovir 藥物動力學 人種研究顯示, 白種人與亞洲人具有相近的 adefovir 藥物動力學, 尚無其他人種的藥物動力學資料 老年病患目前尚未針對老年人進行藥物動力學研究
13 兒童病患針對 53 位患有代償性肝臟疾病的 HBeAg 陽性 B 型肝炎兒童病患, 以血中濃度進行 adefovir 藥物動力學評估的結果顯示,12 歲至 18 歲以下兒童病患, 在接受一天一次 10 毫克 adefovir dipivoxil 錠劑治療 48 週後的 adefovir 曝藥量 ( C max = 23.3 ng/ml;auc 0-24 = ng h/ml), 與成人相近 腎功能不全腎功能中度或重度不全, 或患有末期腎臟病 (ESRD) 且需血液透析之成人病患的 C max AUC 與半衰期 (T 1/2 ), 都較腎功能正常者高, 建議這些病患應改變干適能的投藥間隔 [ 請參閱用法用量 (2.2)] 各種腎功能不全程度之非慢性 B 型肝炎患者的 adefovir 藥物動力學, 如表 3 所示 在該試驗中, 受試者係接受單劑 10 毫克的干適能 表 3 各種腎功能程度之病患的 Adefovir 藥物動力學參數 ( 平均值 ± 標準差 ) 腎功能族群無腎功能不全輕度腎功能不全中度腎功能不全重度腎功能不全 肌酸酐清除率的基準值 (ml/min) >80 (N=7) (N=8) (N=7) (N=10) C max (ng/ml) 17.8 ± ± ± ± 10.3 AUC 0- (ng h/ml) 201 ± ± ± ± 629 CL/F (ml/min) 469 ± ± ± ± 51.3 CL renal (ml/min) 231 ± ± ± ± 18.4 四小時的血液透析大約可移除 35% 的 adefovir 劑量, 但尚未評估腹膜透析對 adefovir 的移除效果 尚未針對腎功能不全之青少年病患, 進行 adefovir 的藥物動力學研究 [ 請參閱特定族群的使用 (8.4)]
14 肝功能不全針對肝功能不全的非慢性 B 型肝炎病患, 進行投予單劑 10 毫克干適能後的 adefovir 藥物動力學研究顯示, 相較於無肝功能不全的病患, 中度與重度肝功能不全病患的 adefovir 藥物動力學未大幅改變, 因此無需改變肝功能不全病患的干適能用藥方法 12.4 微生物學作用機轉 Adefovir 為單磷酸腺苷的非環狀核苷酸類似物, 可在細胞激酶 (kinase) 磷酸化後, 轉變為具活性的代謝產物 adefovir 二磷酸 (adefovir diphosphate) adefovir 二磷酸可藉由與天然受質去氧腺苷三磷酸 (deoxyadenosine triphosphate) 競爭, 以及在併入病毒 DNA 後導致 DNA 鏈終止複製, 而抑制 HBV DNA 聚合酶 ( 反轉錄酶 ) 的作用 adefovir 二磷酸對 HBV DNA 聚合酶的抑制常數 (inhibition constant,k i ) 為 0.1 μm, 而 Adefovir 二磷酸亦為人類 DNA 聚合酶 α 與 γ 的微弱抑制劑,K i 值分別為 1.18 μm 與 0.97 μm 抗病毒活性在 HBV 轉染的人類肝癌細胞株, 抑制 50% 病毒 DNA 合成的 adefovir 濃度 (EC 50 ) 範圍在 0.2 至 2.5 μm Adefovir 與 lamivudine 併用時, 具有加成的抗 -HBV 活性 抗藥性在部分臨床分離株觀察到的基因型改變, 會降低在細胞培養中, 對用於治療 HBV 感染之核苷類似物反轉錄酶抑制劑的感受性 針對取自所有接受 adefovir dipivoxil 治療, 且可偵測到血清 HBV DNA 之病患的基因型檢測檢體進行的長期抗藥性分析顯示, 氨基酸取代型突變 rtn236t 和 rta181t/v 皆與 adefovir 抗藥性有關 在細胞培養中, rtn236t rta181v 與 rta181t 之氨基酸取代型突變, 對 adefovir 的感受性分別降低了 4 至 14 倍 2.5 至 4.2 倍與 1.3 至 1.9 倍 在第 48 週時, 先前未曾接受核苷治療之 HBeAg- 陽性受試者分離的病毒株 (GS 試驗,N=171) 中, 未觀察到與 adefovir 抗藥性有關的取代突變 試驗中有 65 位受試者, 在接受 adefovir dipivoxil 治療 235 週 ( 中位數, 範圍為 週 ) 之後, 繼續接受長期治療, 在 38 位受試者的病毒學治療失敗中 ( 證實 HBV DNA 濃度至少較最低點增加 10 倍, 或從未抑制在 10 3 copies/ml 以下 ), 有 16 人 (42%) 的分離株出現與 adefovir 抗藥性有關的取代突變 這些取代突變, 包括 rtn236t (N=2) rta181v (N=4) rta181t (N=3) rta181t+rtn236t (N=5) 與 rta181v+rtn236t (N=2) 在未曾接受核苷治療之 HBeAg 陰性受試者 (GS 試驗 ) 中, 有 30 位受試者分離的病毒株, 經確認具有與 adefovir 抗藥性有關的取代突變, 在第 與 240 週時的累積機率, 分別為 0% 3% 11% 19% 與 30% 在這 30 位受試者中, 有 22 人的 HBV DNA 濃度經證實至少較最低點增加 10 倍, 或從未低於 10 3 copies/ml, 另有 8 人具有與 adefovir 抗藥性有關的取代突變, 但病毒學治療未失敗 此外, 相較於第 48 週時血清 HBV DNA 高於 1,000 copies/ml 的受試者, 第 48 週時血清 HBV DNA 濃度低於定量下限 ( 低於 1,000 copies/ml) 的受試者, 長期 (4 至 5 年 ) 出現 adefovir dipivoxil 抗藥性的比例顯著較低
15 一項針對肝臟移植前與移植後病患進行的開放標示試驗 (GS 試驗 ), 評估了 129 位於基準點時, 具有 lamivudine- 抗藥性 B 型肝炎病毒之臨床證據之受試者分離的病毒株, 是否存有與 adefovir 抗藥性有關的取代突變, 結果在第 48 週時, 與 adefovir 抗藥性有關之取代突變 (rtn236t 或 rta181t/v) 的發生率為 0%, 但有 4 位受試者分離的病毒株, 於 adefovir dipivoxil 治療 72 週後出現 rtn236t 取代突變, 且併有血清 HBV DNA 反彈 HBV 出現 rtn236t 取代突變的 4 位受試者, 皆在出現基因型抗藥性之前停止 lamivudine 治療, 且隨後皆失去於基準點時即存在與 lamivudine 抗藥性有關的取代突變 在針對 35 位同時感染 HIV/HBV, 且具有 lamivudine 抗藥性 HBV 之病患 ( 添加 adefovir dipivoxil 至 lamivudine 療法 ) 進行的試驗中 (460i 試驗 ), 有 15 人分離的 HBV 病毒株在最長 144 週治療後進行的檢測中, 未發現與 adefovir 抗藥性有關的取代突變 交叉抗藥性 在細胞培養中, 含有與 lamivudine 抗藥性有關之取代突變 (rtl180m rtm204i rtm204v rtl180m + rtm204v rtv173l + rtl180m + rtm204v) 的重組型 HBV 變異株, 皆對 adefovir 敏感 adefovir dipivoxil 對於感染含有與 lamivudine 抗藥性有關之取代突變的 HBV 病患, 亦具有抗 HBV 活性 ( 血清 HBV DNA 降幅中位數為 4.1 log 10 copies/ml)( 435 號試驗 ), 在細胞培養中,adefovir 對含有與 entecavir 抗藥性有關之取代突變 (rtt184g rts202i rtm250v) 的 HBV 變異株, 亦具有抗病毒活性 在細胞培養中, 含有 DNA 聚合酶取代突變的 rtt128n 和 rtr153q, 或含有與 B 型肝炎病毒免疫球蛋白抗藥性有關之 rtw153q 的 HBV 變異株, 皆對 adefovir 敏感 在細胞培養中, 具有與 adefovir 抗藥性有關之 rtn236t 取代突變的 HBV 變異株, 對 entecavir 的敏感性未改變, 對 lamivudine 的敏感性則降低了 2 至 3 倍, 而含有與 adefovir 抗藥性有關之 rta181v 取代突變的 HBV 突變株, 對 lamivudine 的敏感性降低了 1 至 14 倍不等, 對 entecavir 的敏感性則降低了 12 倍 將 lamivudine 添加至 adefovir dipivoxil 療法時, 感染具 rta181v 取代突變 (N=2) 或 rtn236t 取代突變 (N=3) 之 HBV 的受試者, 血清 HBV DNA 分別降低 2.4 至 3.1 與 2.0 至 5.1 log 10 copies/ml
16 13 非臨床毒理學 13.1 致癌性 致突變性 生育力損害 小鼠與大鼠進行的長期口服 adefovir dipivoxil 致癌性研究, 是在曝藥量最高約為人類治療 HBV 感染時使用之治療劑量之曝藥量的 10 倍 ( 小鼠 ) 與 4 倍 ( 大鼠 ) 下進行, 結果, 小鼠與大鼠的研究皆顯示,adefovir dipivoxil 不具致癌性, 但體外小鼠淋巴瘤細胞分析 ( 有或無經過代謝活化作用 ) 則顯示,adefovir dipivoxil 具有致突變性 未經代謝活化作用之體外人類周邊血液淋巴球分析的結果顯示,adefovir 可誘發染色體畸變, 而體內小鼠微核分析顯示,adefovir dipivoxil 不具染色體損壞作用 (clastogenic), 使用 S. typhimurium 與 E. coli 菌株的 Ames 細菌反向突變分析 (reverse mutation assay) 結果則顯示, 不論是否經過代謝活化作用,adefovir 皆不具致突變性 生殖毒理學研究結果顯示, 在全身曝藥量約為人類使用治療劑量之曝藥量的 19 倍時, 皆未見到雄性或雌性大鼠生育力受損的證據 13.2 動物毒理學及 / 或藥理學毒理學研究針對大鼠與兔子進行 adefovir dipivoxil 口服與 adefovir 靜脈注射的動物生殖研究 在母體劑量產生的全身曝藥量, 約為人類在使 10 mg/ 天治療劑量之曝藥量的 23 倍 ( 大鼠 ) 與 40 倍 ( 兔子 ) 時, 口服的 adefovir dipivoxil 不會使大鼠與兔子出現胚胎毒性或致畸胎性 當懷孕大鼠接受靜脈注射 adefovir 時, 可在全身性曝藥量為人類之母體毒性劑量的 38 倍下, 發現胚胎毒性與畸胎 ( 全身水腫 扁平性凸眼 臍疝與尾巴捲縮 ) 發生率增高的現象, 而在懷孕大鼠接受曝藥量約為人類 12 倍之劑量的 adefovir 靜脈注射時, 未發現會對發育造成不良影響 動物毒理學研究讓動物服用 adefovir dipivoxil 引起的主要劑量限制性毒性作用, 包括以組織變化為特徵的腎小管腎病變, 及 / 或血中尿素氮 (BUN) 與血清肌酸酣升高 在全身性曝藥量約較人類使用建議治療劑量 (10 mg/ 天 ) 之曝藥量高 3 10 倍時, 可發現腎毒性
17 14 臨床試驗 號與 438 號試驗 ( 樞紐試驗 ) HBeAg- 陽性慢性 B 型肝炎 437 號試驗, 為針對 HBeAg- 陽性慢性 B 型肝炎患者進行之隨機分組 雙盲 安慰劑對照 分為三組的試驗, 旨於比較安慰劑與干適能 受試者的年齡中位數為 33 歲, 有 74% 的受試者為男性,59% 為亞洲人,36% 為白種人,24% 先前曾接受干擾素治療, 且受試者在基準點時的總 Knodell 組織活性指數 (Histology Activity Index, 簡稱 HAI) 中位數為 10, 以 Roche Amplicor Monitor 聚合酶連鎖反應 (PCR) 檢測法 (LLOQ = 1000 copies/ml) 測量的血清 HBV DNA 濃度中位數為 8.36 log 10 copies/ml,alt 濃度中位數為正常值上限的 2.3 倍 HBeAg- 陰性 ( 抗 -HBe 陽性 /HBV DNA 陽性 ) 慢性 B 型肝炎 438 號試驗, 為針對篩選時為 HBeAg- 陰性 ( 抗 -HBe 陽性 ) 慢性 B 型肝炎患者進行之隨機分組 雙盲 安慰劑對照的試驗 受試者的年齡中位數為 46 歲, 有 83% 的受試者為男性,66% 為白種人,30% 為亞洲人,41% 先前曾接受干擾素治療, 且受試者在基準點時的總 Knodell 組織活性指數 (HAI) 分數中位數為 10, 以 Roche Amplicor Monitor 聚合酶連鎖反應 (PCR) 檢測法 (LLOQ = 1000 copies/ml) 測量的血清 HBV DNA 濃度中位數為 7.08 log 10 copies/ml,alt 濃度中位數為正常值上限的 2.3 倍 這兩項試驗的主要療效評估指標, 皆為第 48 週時的組織學檢測結果改善情形, 結果如表 4 所示 a 表 4 第 48 週的組織學反應 437 號試驗 438 號試驗 干適能 安慰劑 干適能 安慰劑 10 mg (N=161) 10 mg (N=57) (N=168) (N=121) b 獲改善 53% 25% 64% 35% 未改善 37% 67% 29% 63% 資料遺漏 / 無法評估 10% 7% 7% 2% a. 具有可評估之基準點組織切片檢查資料的意圖治療族群 ( 接受 1 劑試驗藥物的受試者 ) b. 組織學檢測結果獲改善之定義 :Knodell 壞死 - 發炎分數降低 2 分, 而且 Knodell 纖維化分數未惡化
18 表 5 所示為兩治療組的 Ishak 纖維化分數變化 表 5 第 48 週時 Ishak 纖維化分數的變化 適當可用之組織切片的成對數目 干適能 10 mg (N=152) 437 號試驗 438 號試驗干適能安慰劑 10 mg (N=149) (N=113) 安慰劑 (N=56) Ishak 纖維化分數獲 a 34% 19% 34% 14% 得改善 無變化 55% 60% 62% 50% a 惡化 11% 21% 4% 36% a. Ishak 纖維化分數改變 1 分或更多 第 48 週時, 相較於安慰劑, 接受干適能治療者的血清 HBV DNA (log10 copies/ml) 平均變化 ALT 恢復正常, 以及 HBeAg 血清轉變皆獲得改善 ( 表 6) 表 6 第 48 週時的血清 HBV DNA 濃度變化 ALT 恢復正常與 HBeAg 血清轉變 437 號試驗 438 號試驗 干適能 10 mg (N=171) 安慰劑 (N=167) 干適能 10 mg (N=123) 安慰劑 (N=61) 相較於基準點, 血清 HBV DNA 濃度變化平均 ± SD (log 10 copies/ml) 3.57 ± ± ± ± 1.25 ALT 恢復正常 48% 16% 72% 29% HBeAg 血清轉變 12% 6% NA a NA a a. HBeAg- 陰性肝炎患者無法進行 HBeAg 血清轉變 超過 48 週的治療在 437 號試驗中, 繼續接受干適能治療至 72 週, 可持續維持第 48 週時觀察到血清 HBV DNA 濃度的平均降幅, 在 437 號試驗中亦可觀察到 ALT 恢復正常的受試者比例增加, 但目前尚不瞭解持續接受干適能治療, 對血清轉變的影響 在 438 號試驗中, 持續以設盲方式將前 48 週接受干適能治療之受試者, 隨機分派接受干適能或安慰劑繼續治療 48 週, 直至第 96 週時, 繼續接受干適能治療的受試者中, 有 50/70 (71%) 無法偵測到 HBV DNA( 低於 1000 copies/ml), 有 47/64 (73%) 的 ALT 恢復正常 停止干適能治療之大部分受試者的 HBV DNA 與 ALT 濃度, 則皆回到基準值
19 在 438 號試驗中,141 位符合參與資格的受試者, 有 125 人 (89%) 選擇繼續接受干適能治療至 192 週或 240 週 (4 年或 5 年 ), 由於這些受試者已接受干適能治療至少 48 週且已出現治療效益, 因此, 他們不一定能代表初次接受干適能的病患 這些受試者在第 192 週或 240 週時, 分別有 89/125 (71%) 與 47/70 (67%) 無法偵測到 HBV DNA( 低於 1000 copies/ml) 基準點時 ALT 升高之受試者在第 192 週或 240 週時, 分別有 77/104 (74%) 與 42/64 (66%) 之受試者的 ALT 正常, 有 6 位 (5%) 受試者的 HBsAg 消失 號試驗 ( 肝臟移植前與移植後的受試者 ) 同時有一項針對 467 位有 lamivudine 抗藥性 B 型肝炎臨床證據之肝臟移植前 (N=226) 與移植後 (N=241) 慢性 B 型肝炎患者, 評估干適能的開放標示 無對照組試驗 (435 號試驗 ) 顯示, 在基準點時, 有 60% 的肝臟移植前病患, 根據 Child-Pugh-Turcotte 分數歸為 B 或 C 類 肝臟移植前與移植後的病患, 以 Roche Amplicor Monitor PCR 檢測法 (LLOQ = 1000 copies/ml) 測量的基準點 HBV DNA 濃度中位數, 分別為 7.4 與 8.2 log 10 copies/ml, 基準點 ALT 濃度中位數, 則分別為正常值上限的 1.8 與 2.0 倍 此項試驗的結果如表 7 所示, 無論基準點時之 lamivudine 抗藥性 HBV DNA 聚合酶的突變模式為何, 干適能治療皆可使血清 HBV DNA 產生相近的降幅, 但是, 目前不瞭解表 7 所列的療效結果, 對其與臨床結果的關係有何重要性 表 7 第 48 週時, 肝臟移植前與移植後病患的療效 a 療效參數 相較於基準點的變化,HBV DNA 濃度平均 ± SD (log 10 copies/ml) 肝臟移植前 (N=226) 3.7 ± 1.6 (N=117) 肝臟移植後 (N=241) 4.0 ± 1.6 (N=164) 無法偵測到 HBV DNA (< 1000 b 77/109 (71%) 64/159 (40%) copies/ml) 的受試者比例 Child-Pugh-Turcotte 分數穩定或獲得改善 86/90 (96%) 107/115 (93%) 恢復正常 c : ALT 61/82 (74%) 56/110 (51%) 白蛋白 43/54 (80%) 21/26 (81%) 膽紅素 38/68 (58%) 29/38 (76%) 凝血酶原時間 (Prothrombin time) 39/46 (85%) 5/9 (56%) a. 此項試驗收錄的所有受試者中, 有 29% (HBV DNA) 與 37%~45%(CPT 分數 ALT 恢復正常 白蛋白 膽紅素與凝血酶原時間 ) 的數據遺漏 b. 分母 : 基準點時, 以 Roche Amplicor Monitor PCR 檢測法 (LLOQ = 1000 copies/ml) 測量之血清 HBV DNA 濃度 1000 copies/ml, 且第 48 週之數值未遺漏的受試者人數 c. 分母 : 基準點時數值異常, 且第 48 週之數值未遺漏的受試者人數
20 號試驗 (Lamivudine 抗藥性的臨床證據 ) 461 號試驗, 為針對 59 位具 lamivudine 抗藥性 B 型肝炎病毒之臨床證據的慢性 B 型肝炎患者, 進行之雙盲 活性藥物對照的試驗, 受試者隨機分派接受干適能單一療法或干適能併用 lamivudine 100 毫克, 或 lamivudine 100 毫克單一療法治療 在第 48 週時接受干適能治療者, 以 Roche Amplicor Monitor PCR 檢測法 (LLOQ = 1000 copies/ml) 測量的血清 HBV DNA 濃度降幅 ( 平均 ± 標準差 ), 為 4.00 ± 1.41 log 10 copies/ml, 接受干適能與 lamivudine 合併療法治療者, 則為 3.46 ± 1.10 log 10 copies/ml, 而單獨接受 lamivudine 治療者的血清 HBV DNA 平均降幅為 0.31 ± 0.93 log 10 copies/ml 干適能治療組有 47% 受試者的 ALT 恢復正常, 接受干適能與 lamivudine 合併療法治療者為 53%, 單獨接受 lamivudine 治療者則為 5% 目前不瞭解這些發現對其與臨床結果之關係的重要性 16 供應形式 / 儲存與操作 干適能錠的包裝容器為高密度聚乙烯 (HDPE) 瓶, 並附有防止兒童開啟的瓶蓋 每瓶中均含有 30 顆錠劑以及矽膠乾燥劑 儲存溫度不可超過 30 若瓶口的密封膜破損或不見, 請勿使用
21 17 病患諮詢資訊 17.1 安全使用說明 請參閱核准的病患藥品標示 請醫師務必將干適能可能具有的風險與益處, 以及可選擇的其他療法告知病患 請醫師指導病患 : - 在開始干適能治療之前, 先閱讀藥品說明書 - 遵循規律的用藥時間表, 以免錯過用藥時間 - 若出現任何嚴重腹痛 肌肉痛 眼睛變黃 尿液顏色深 大便顏色淡, 及 / 或食慾不振, 必須立即通報 - 若出現任何不尋常的症狀, 或有任何已知的症狀持續存在或惡化, 必須立即告知醫師或藥劑師 在使用干適能的期間, 病患仍應繼續接受醫師照護 請務必告知病患 : - 目前尚不瞭解干適能最理想的治療持續時間, 以及治療反應與長期後果 ( 肝細胞癌或代償不全的肝硬化 ) 之間的關係 - 未事先告知醫師, 病患不可擅自中斷使用干適能 [ 請參閱警語及注意事項 (5.1)] - 在使用干適能治療的期間, 務必接受例行性的實驗室監測與醫師的追蹤 - 在開始使用干適能治療之前, 務必先進行 HIV 抗體檢測 [ 請參閱警語及注意事項 (5. 3)] - 干適能不可與 ATRIPLA 或 COMPLERA 或 STRIBILD, 或 TRUVADA 或 VIREAD 同時使用 [ 請參閱警語及注意事項 (5. 5)] - 具有 Lamivudine 抗藥性的病患, 在使用干適能時必須併用 lamivudine, 不可單獨使用干適能 [ 請參閱警語及注意事項 (5.6)]
22 17.2 懷孕與哺乳 醫師必須將懷孕期間使用干適能可能具有的風險, 告知育齡婦女 若病患在使用干適能之期間懷孕, 必須告知醫師 請將干適能的懷孕註冊系統告知正在使用干適能的懷孕病患, 並協助其登錄 必須告知病患, 目前還不清楚干適能是否會分泌至人乳中, 也不瞭解干適能是否會傷害哺乳的嬰兒, 因此, 必須決定是否要中斷哺乳或停用藥物 製造廠 :Patheon, Inc. 廠址 :2100 Syntex Court Mississauga, Ontario, Canada L5N 7K9 包裝廠 :GlaxoSmithKline Inc. 廠址 :7333 Mississauga Road North Mississauga, Ontario, Canada L5N 6L4 藥商 : 荷商葛蘭素史克藥廠股份有限公司台灣分公司地址 : 台北市忠孝西路一段六十六號二十四樓
提案一 報告人:賴貞橞
 全民健康保險藥品給付規定 修正規定 第 10 章抗微生物劑 Antimicrobial agents 修正後給付規定 10.7. 抗病毒劑 Antiviral drugs 10.7.3 Lamivudine( 限使用 Zeffix tablets 100mg);Entecavir ( 如 Baraclude 0.5mg); Telbivudine ( 如 Sebivo 600mg):(92/10/1
全民健康保險藥品給付規定 修正規定 第 10 章抗微生物劑 Antimicrobial agents 修正後給付規定 10.7. 抗病毒劑 Antiviral drugs 10.7.3 Lamivudine( 限使用 Zeffix tablets 100mg);Entecavir ( 如 Baraclude 0.5mg); Telbivudine ( 如 Sebivo 600mg):(92/10/1
Microsoft Word - Pegasys RP PI_ _clean version
 2006 10 18 2006 12 22 2007 11 14 2007 12 12 2008 05 28 2008 12 11 2010 10 14 2011 02 11 2011 08 04 2012 04 28 2012 12 20 2013 01 14 2014 12 05 2015 03 09 2016 9 27 2016 12 19 2017 05 04 2017 08 16 α-2a
2006 10 18 2006 12 22 2007 11 14 2007 12 12 2008 05 28 2008 12 11 2010 10 14 2011 02 11 2011 08 04 2012 04 28 2012 12 20 2013 01 14 2014 12 05 2015 03 09 2016 9 27 2016 12 19 2017 05 04 2017 08 16 α-2a
Pegasys vials,PFS Hep B & C_Chinesen.doc
 135 /180 /, 135 /0.5 180 /0.5 Pegasys vials 135mcg/ml, 180 mcg/ml Pegasys prefilled syringes 135mcg/0.5ml, 180 mcg/0.5ml 1. (vial) (prefilled syringe) 1.0ml 135mcg Peginterferon alfa-2a 1.0ml 180mcg Peginterferon
135 /180 /, 135 /0.5 180 /0.5 Pegasys vials 135mcg/ml, 180 mcg/ml Pegasys prefilled syringes 135mcg/0.5ml, 180 mcg/0.5ml 1. (vial) (prefilled syringe) 1.0ml 135mcg Peginterferon alfa-2a 1.0ml 180mcg Peginterferon
38 嬰兒猝死症候群 (SIDS) 急性支氣管炎及急性細支 其他 9, 臺灣地區 總計 0 歲 死亡數 名 原因 Number Crude 名 原因 Number of Deaths Death Rate of Deaths 所有死亡原因 64,
 臺灣地區 總計 0 歲 死亡數 名 原因 Number Crude 名 原因 Number of Deaths Death Rate of Deaths 所有死亡原因 97,979 838.0 所有死亡原因 446 1 惡性腫瘤 28,476 243.6 1 源於周產期的特定病況 195 2 心臟疾病 ( 高血壓性疾病 11,484 98.2 2 先天性畸形變形及染色體 99 3 腦血管疾病 6,980
臺灣地區 總計 0 歲 死亡數 名 原因 Number Crude 名 原因 Number of Deaths Death Rate of Deaths 所有死亡原因 97,979 838.0 所有死亡原因 446 1 惡性腫瘤 28,476 243.6 1 源於周產期的特定病況 195 2 心臟疾病 ( 高血壓性疾病 11,484 98.2 2 先天性畸形變形及染色體 99 3 腦血管疾病 6,980
250 ZYTIGA Tablets 250 mg
 250 ZYTIGA Tablets 250 mg 026139 1 ZYTIGA CYP17 prednisone prednisolone 1 chemotherapy is not yet clinically indicated 2 docetaxel 3 2 2.1 ZYTIGA 1,000 4 250 prednisone prednisolone 5 1 ZYTIGA 1,000 4
250 ZYTIGA Tablets 250 mg 026139 1 ZYTIGA CYP17 prednisone prednisolone 1 chemotherapy is not yet clinically indicated 2 docetaxel 3 2 2.1 ZYTIGA 1,000 4 250 prednisone prednisolone 5 1 ZYTIGA 1,000 4
F A F G F H F F A F G F H doi : / NRD 1032 PK PK 攻防首部曲 在藥品查驗登記時, 必須檢附相關藥動學資料支持藥品的療效與安全性以備核准
 藥物在體內的 PK 攻防 36 藥物動力學 PharmacokineticsADME Absorption Z Disposition Distribution Elimination Metabolism D Excretion T C T C Z pharmacokinetics PK absorption distribution metabolism excretion ADME 2015
藥物在體內的 PK 攻防 36 藥物動力學 PharmacokineticsADME Absorption Z Disposition Distribution Elimination Metabolism D Excretion T C T C Z pharmacokinetics PK absorption distribution metabolism excretion ADME 2015
 慢性腎病兒童第7 章兒童慢性腎病的主要臨床癥狀,包括食慾下降 疲勞 生長發育遲緩 高血壓 多尿及腎性骨病等 第 7 章 慢性腎病兒童 * 腎延敏行 積極面對慢性腎病60 醫療上的問題 * 慢性腎病兒童61 腎延敏行 積極面對慢性腎病62 5 6 慢性腎病兒童的身心發展需要 慢性腎病兒童63 腎延敏行 積極面對慢性腎病64 慢性腎病 : : : : : (1) (maltodextrin) (2)
慢性腎病兒童第7 章兒童慢性腎病的主要臨床癥狀,包括食慾下降 疲勞 生長發育遲緩 高血壓 多尿及腎性骨病等 第 7 章 慢性腎病兒童 * 腎延敏行 積極面對慢性腎病60 醫療上的問題 * 慢性腎病兒童61 腎延敏行 積極面對慢性腎病62 5 6 慢性腎病兒童的身心發展需要 慢性腎病兒童63 腎延敏行 積極面對慢性腎病64 慢性腎病 : : : : : (1) (maltodextrin) (2)
New Baraclude PI
 本藥須由醫師處方使用 貝樂克貝樂克 貝樂克膜衣錠 0.5 毫克 1 毫克 貝樂克口服液劑 0.05 毫克 / 毫升 Brclude* Tblets 0.5 mg, 1 mg Brclude* Orl Solution 0.05 mg/ml (entecvir) 0.5 毫克衛署藥輸字第 024469 號 1 毫克衛署藥輸字第 024468 號 0.05 毫克 / 毫升衛署藥輸字第 024467 號
本藥須由醫師處方使用 貝樂克貝樂克 貝樂克膜衣錠 0.5 毫克 1 毫克 貝樂克口服液劑 0.05 毫克 / 毫升 Brclude* Tblets 0.5 mg, 1 mg Brclude* Orl Solution 0.05 mg/ml (entecvir) 0.5 毫克衛署藥輸字第 024469 號 1 毫克衛署藥輸字第 024468 號 0.05 毫克 / 毫升衛署藥輸字第 024467 號
....V....VII.... VIII
 ....V....VII.... VIII................................. 002... 002... 004... 006... 012... 014... 019.... 022.... 023................................. 026... 026... 027... 039 XIII...043... 043... 045....
....V....VII.... VIII................................. 002... 002... 004... 006... 012... 014... 019.... 022.... 023................................. 026... 026... 027... 039 XIII...043... 043... 045....
Zytiga... Zytiga... Zytiga Zytiga Zytiga
 250 本資料僅提供醫護人員衛教使用 ............... Zytiga... Zytiga... Zytiga... 2 3 4 5 6 7 8 9 Zytiga... 10 Zytiga... 10...... 13 18 Zytiga Zytiga 2 25% 3 PSA PSA 3~4 ng/ml PSA bone scan CT scan MRI 4 5 攝護腺癌之治療 治療方面
250 本資料僅提供醫護人員衛教使用 ............... Zytiga... Zytiga... Zytiga... 2 3 4 5 6 7 8 9 Zytiga... 10 Zytiga... 10...... 13 18 Zytiga Zytiga 2 25% 3 PSA PSA 3~4 ng/ml PSA bone scan CT scan MRI 4 5 攝護腺癌之治療 治療方面
特点和作用
 2006 10 2007 02 2010 08 2010 11 2015 02 2015 05 2017 03 Valganciclovir Hydrochloride Tablets Yan Suan Xie Geng Xi Luo Wei Pian 1.L-,- 2[(2-- 1,6- -6-- 9H-- 9-) ]-3-- 2.9-[[2--1- ] ] L- O H H 2 N N N N
2006 10 2007 02 2010 08 2010 11 2015 02 2015 05 2017 03 Valganciclovir Hydrochloride Tablets Yan Suan Xie Geng Xi Luo Wei Pian 1.L-,- 2[(2-- 1,6- -6-- 9H-- 9-) ]-3-- 2.9-[[2--1- ] ] L- O H H 2 N N N N
SW cdr
 1~2 3 4 5~6 7~8 9~10 11 12 13 14 15 16~18 16 16 17 17 18 18 18 19 19 19 20 21 22 23~26 23 24 24 25 26 27 27 27 : 110V 1 110V 110V 15A 2 3 23 24 4 ( ) 5 6 1 2 26 20 l 1 7 3 4 5 15 17 18 12 7~13 6 ~ 8 ~
1~2 3 4 5~6 7~8 9~10 11 12 13 14 15 16~18 16 16 17 17 18 18 18 19 19 19 20 21 22 23~26 23 24 24 25 26 27 27 27 : 110V 1 110V 110V 15A 2 3 23 24 4 ( ) 5 6 1 2 26 20 l 1 7 3 4 5 15 17 18 12 7~13 6 ~ 8 ~
Microsoft Word - PI-Draft IM
 26 1 23 26 11 12 27 3 22 27 4 28 27 5 24 28 12 9 29 2 11 29 3 15 29 9 8 21 4 8 211 4 29 212 2 27 212 11 6 213 12 5 Tarceva Erlotinib Hydrochloride Tablets Yansuan Eluotini Pian N-(3-)-6,7- (2- )-4- C 22
26 1 23 26 11 12 27 3 22 27 4 28 27 5 24 28 12 9 29 2 11 29 3 15 29 9 8 21 4 8 211 4 29 212 2 27 212 11 6 213 12 5 Tarceva Erlotinib Hydrochloride Tablets Yansuan Eluotini Pian N-(3-)-6,7- (2- )-4- C 22
C 22H 23 N 3 O 4 HCl EGFR NSCLC ++ NSCLC NSCLC EGFR 15mg/
 26 1 23 26 11 12 27 3 22 27 4 28 27 5 24 28 12 9 29 2 11 29 3 15 29 9 8 21 4 8 211 4 29 212 2 27 212 11 6 213 12 5 217 1 17 217 3 1 Tarceva Erlotinib Hydrochloride Tablets Yansuan Eluotini Pian N-(3-)
26 1 23 26 11 12 27 3 22 27 4 28 27 5 24 28 12 9 29 2 11 29 3 15 29 9 8 21 4 8 211 4 29 212 2 27 212 11 6 213 12 5 217 1 17 217 3 1 Tarceva Erlotinib Hydrochloride Tablets Yansuan Eluotini Pian N-(3-)
Microsoft Word - statistics04-1_doc.docx
 入學新生體檢及異常統計表 (102 學年度 ) 國立成功大學 102 學年度新生體檢表概況 學院別 未檢 比例 不合格 比例 合格 比例 總 文學院 16 4.68 290 88.96 36 11.04 342 理學院 48 9.86 345 78.59 94 21.41 487 工學院 256 12.59 1432 80.54 346 19.46 2034 管理學院 42 5.10 672 85.93
入學新生體檢及異常統計表 (102 學年度 ) 國立成功大學 102 學年度新生體檢表概況 學院別 未檢 比例 不合格 比例 合格 比例 總 文學院 16 4.68 290 88.96 36 11.04 342 理學院 48 9.86 345 78.59 94 21.41 487 工學院 256 12.59 1432 80.54 346 19.46 2034 管理學院 42 5.10 672 85.93
CFDA BRAF V mg CFDA BRAF V600 BRAF 960 mg QTc mg 2
 2017 3 10 2017 5 26, Zelboraf Vemurafenib film-coated tablets Weimofeini Pian -1- {3-[5-(4- )-1H- [2,3- b] -3- ]-2,4- } - C 23H 18 ClF 2 N 3 O 3 S 489.93 1 CFDA BRAF V600 240 mg CFDA BRAF V600 BRAF 960
2017 3 10 2017 5 26, Zelboraf Vemurafenib film-coated tablets Weimofeini Pian -1- {3-[5-(4- )-1H- [2,3- b] -3- ]-2,4- } - C 23H 18 ClF 2 N 3 O 3 S 489.93 1 CFDA BRAF V600 240 mg CFDA BRAF V600 BRAF 960
144 ) 985 Da ( 80 RA DMARDs MTX DMARDs sjia NSAIDs 2 2 sjia 80mg/4ml 200mg/10ml 400mg/20ml RA 8mg/kg 4 1 MTX DMARDs 4mg/kg 0.9% 100ml 1 100kg 800mg sj
 2013 03 26 2014 06 03 2015 11 25 2016 10 25 2017 09 25 ACTEMRA Tocilizumab Injection Tuozhudankang Zhusheye 6IL-6 CHO DNA C 6428H 9976 N 1720 O 2018 S 42 () 1 144 ) 985 Da ( 80 RA DMARDs MTX DMARDs sjia
2013 03 26 2014 06 03 2015 11 25 2016 10 25 2017 09 25 ACTEMRA Tocilizumab Injection Tuozhudankang Zhusheye 6IL-6 CHO DNA C 6428H 9976 N 1720 O 2018 S 42 () 1 144 ) 985 Da ( 80 RA DMARDs MTX DMARDs sjia
臨床藥物治療學 Therapeutics of Clinical Drugs 參 C 型肝炎治療目標 (American Association for the Study of Liver Disease, AASLD) C (sustained virologic response, SVR)
 Therapeutics of Clinical Drugs 臨床藥物治療學 Thymalfasin 用於治療 C 型肝炎 光田綜合醫院藥劑部藥師白雅君 賴建名 摘要 C C interferon ribavirin Thymalfasin C phase III thymalfasin C C thymosin α1 thymalfasin 壹 前言 C interferon ribavirin
Therapeutics of Clinical Drugs 臨床藥物治療學 Thymalfasin 用於治療 C 型肝炎 光田綜合醫院藥劑部藥師白雅君 賴建名 摘要 C C interferon ribavirin Thymalfasin C phase III thymalfasin C C thymosin α1 thymalfasin 壹 前言 C interferon ribavirin
Microsoft Word - Tamiflu_CDS 13.0_redressing site_1016-TAM-01_clean
 1016-TAM-01 30 45 75 ( ) 75 () Capsules 30 mg Capsules 45 mg Capsules 75 mg Oseltamivir phosphate 1. 1.1 / 1.2 30 ROCHE 30 mg 45 ROCHE 45 mg 75 ROCHE 75 mg 1.3 1.4 / 1 1.5 : Oseltamivir phosphate 30 39.4
1016-TAM-01 30 45 75 ( ) 75 () Capsules 30 mg Capsules 45 mg Capsules 75 mg Oseltamivir phosphate 1. 1.1 / 1.2 30 ROCHE 30 mg 45 ROCHE 45 mg 75 ROCHE 75 mg 1.3 1.4 / 1 1.5 : Oseltamivir phosphate 30 39.4
Microsoft Word - 慢性B型肝炎藥物治療之進展_9610育靜的
 慢性 B 型肝炎藥物治療之進展文 / 朱育靜藥師審閱 / 陳宏毅組長一 前言台灣 B 型肝炎帶原的人口比例長久以來仍維持著 15~20% 的高盛行率,B 型肝炎疫苗接種以來, 雖然兒童 B 型肝炎帶原率及罹患率已經顯著降低, 但在成年人口中仍有相當多的帶原者面臨可能的慢性肝炎 肝硬化和肝癌的進展 根據 2004 年世界衛生組織統計, 全球超過有三億五千萬人感染慢性 B 型肝炎 1, 其中 50~75%
慢性 B 型肝炎藥物治療之進展文 / 朱育靜藥師審閱 / 陳宏毅組長一 前言台灣 B 型肝炎帶原的人口比例長久以來仍維持著 15~20% 的高盛行率,B 型肝炎疫苗接種以來, 雖然兒童 B 型肝炎帶原率及罹患率已經顯著降低, 但在成年人口中仍有相當多的帶原者面臨可能的慢性肝炎 肝硬化和肝癌的進展 根據 2004 年世界衛生組織統計, 全球超過有三億五千萬人感染慢性 B 型肝炎 1, 其中 50~75%
CellCept
 2007 02 14 2007 11 06 2008 01 22 2009 12 14 2010 01 18 2011 09 14 2012 07 16 2013 05 08 2014 11 03 2015 12 01 2016 06 03 2016 11 04 2018 02 01 Mycophenolate Mofetil Tablets / Matimaikaofenzhi Pian (E)-6-(4-
2007 02 14 2007 11 06 2008 01 22 2009 12 14 2010 01 18 2011 09 14 2012 07 16 2013 05 08 2014 11 03 2015 12 01 2016 06 03 2016 11 04 2018 02 01 Mycophenolate Mofetil Tablets / Matimaikaofenzhi Pian (E)-6-(4-
HIV JO Slide Template
 慢 性 乙 型 肝 炎 人 类 健 康 的 隐 形 杀 手 Gang Chen Hepatitis B Foundation 乙 型 肝 炎 基 金 会 提 要 : 乙 型 肝 炎 流 行 概 况 乙 型 肝 炎 病 毒 的 传 播 途 径 慢 性 乙 型 肝 炎 感 染 的 进 程 和 预 后 慢 性 乙 型 肝 炎 感 染 的 诊 断 和 治 疗 乙 型 肝 炎 病 毒 感 染 的 防 治 现
慢 性 乙 型 肝 炎 人 类 健 康 的 隐 形 杀 手 Gang Chen Hepatitis B Foundation 乙 型 肝 炎 基 金 会 提 要 : 乙 型 肝 炎 流 行 概 况 乙 型 肝 炎 病 毒 的 传 播 途 径 慢 性 乙 型 肝 炎 感 染 的 进 程 和 预 后 慢 性 乙 型 肝 炎 感 染 的 诊 断 和 治 疗 乙 型 肝 炎 病 毒 感 染 的 防 治 现
Microsoft Word - Simp_Chin_summary
 欢 迎 光 临 乙 型 肝 炎 基 金 会 中 文 网 站! 全 世 界 有 数 亿 华 人 患 有 乙 型 肝 炎 大 多 数 人 甚 至 都 不 知 道 他 们 已 经 受 到 感 染 但 是, 您 应 当 了 解 一 些 重 要 知 识 请 与 您 的 朋 友 家 人 和 社 区 中 的 其 它 人 士 共 享 这 一 信 息 乙 型 肝 炎 并 非 遗 传, 而 是 由 病 毒 引 起 已
欢 迎 光 临 乙 型 肝 炎 基 金 会 中 文 网 站! 全 世 界 有 数 亿 华 人 患 有 乙 型 肝 炎 大 多 数 人 甚 至 都 不 知 道 他 们 已 经 受 到 感 染 但 是, 您 应 当 了 解 一 些 重 要 知 识 请 与 您 的 朋 友 家 人 和 社 区 中 的 其 它 人 士 共 享 这 一 信 息 乙 型 肝 炎 并 非 遗 传, 而 是 由 病 毒 引 起 已
一般資訊:
 克 憂 果 TM 持 續 性 藥 效 錠 12.5 毫 克 SEROXAT TM CR Tablets 12.5 mg (Paroxetine) 衛 署 藥 輸 字 第 024256 號 定 性 與 定 量 組 成 錠 劑 : 每 錠 所 含 的 paroxetine hydrochloride 相 當 於 12.5 毫 克 paroxetine 游 離 鹽 基 劑 型 12.5 毫 克 錠 劑 :
克 憂 果 TM 持 續 性 藥 效 錠 12.5 毫 克 SEROXAT TM CR Tablets 12.5 mg (Paroxetine) 衛 署 藥 輸 字 第 024256 號 定 性 與 定 量 組 成 錠 劑 : 每 錠 所 含 的 paroxetine hydrochloride 相 當 於 12.5 毫 克 paroxetine 游 離 鹽 基 劑 型 12.5 毫 克 錠 劑 :
FULL PRESCRIBING INFORMATION
 普 利 他 膜 衣 錠 400 毫 克 Prezista Tablets 400mg 衛 署 藥 輸 字 第 025286 號 1 適 應 症 與 用 途 1.1 成 人 病 患 PREZISTA 適 用 於 與 ritonavir (PREZISTA/rtv) 及 其 它 抗 反 轉 錄 病 毒 藥 物 合 併 使 用, 以 治 療 人 類 免 疫 缺 乏 病 毒 (HIV-1) 感 染 之 成
普 利 他 膜 衣 錠 400 毫 克 Prezista Tablets 400mg 衛 署 藥 輸 字 第 025286 號 1 適 應 症 與 用 途 1.1 成 人 病 患 PREZISTA 適 用 於 與 ritonavir (PREZISTA/rtv) 及 其 它 抗 反 轉 錄 病 毒 藥 物 合 併 使 用, 以 治 療 人 類 免 疫 缺 乏 病 毒 (HIV-1) 感 染 之 成
Microsoft Word - 返利凝 膜衣錠 Revolade EU plus US leaflet Sep 07
 返 利 凝 25 毫 克 膜 衣 錠 Revolade 25mg film-coated tablets Eltrombopag olamine 本 藥 須 由 醫 師 處 方 使 用 衛 署 藥 輸 字 第 025272 號 返 利 凝 50 毫 克 膜 衣 錠 Revolade 50mg film-coated tablets Eltrombopag olamine 本 藥 須 由 醫 師 處
返 利 凝 25 毫 克 膜 衣 錠 Revolade 25mg film-coated tablets Eltrombopag olamine 本 藥 須 由 醫 師 處 方 使 用 衛 署 藥 輸 字 第 025272 號 返 利 凝 50 毫 克 膜 衣 錠 Revolade 50mg film-coated tablets Eltrombopag olamine 本 藥 須 由 醫 師 處
Valganciclovir
 0118-VAL-01 克毒癒 膜衣錠 450 毫克 film-coated tablets 450 mg Valganciclovir 抗病毒藥物 為 ganciclovir 的前驅藥物, 其臨床毒性包括顆粒性球減少 貧血及血小板 減少 動物試驗中,ganciclovir 具有致癌性 致畸胎性並暫時性或永久性抑制精子 形成 1. 說明 1.1 治療 / 藥理分類 抗病毒劑 ATC code: J05AB14
0118-VAL-01 克毒癒 膜衣錠 450 毫克 film-coated tablets 450 mg Valganciclovir 抗病毒藥物 為 ganciclovir 的前驅藥物, 其臨床毒性包括顆粒性球減少 貧血及血小板 減少 動物試驗中,ganciclovir 具有致癌性 致畸胎性並暫時性或永久性抑制精子 形成 1. 說明 1.1 治療 / 藥理分類 抗病毒劑 ATC code: J05AB14
Bonviva
 核 准 日 期 :26 年 1 月 修 改 日 期 :26 年 11 月 27 年 3 月 27 年 4 月 27 年 5 月 28 年 12 月 29 年 2 月 29 年 3 月 29 年 9 月 21 年 4 月 211 年 4 月 212 年 2 月 212 年 11 月 盐 酸 厄 洛 替 尼 片 说 明 书 请 仔 细 阅 读 说 明 书 并 在 医 师 指 导 下 使 用 药 品 名
核 准 日 期 :26 年 1 月 修 改 日 期 :26 年 11 月 27 年 3 月 27 年 4 月 27 年 5 月 28 年 12 月 29 年 2 月 29 年 3 月 29 年 9 月 21 年 4 月 211 年 4 月 212 年 2 月 212 年 11 月 盐 酸 厄 洛 替 尼 片 说 明 书 请 仔 细 阅 读 说 明 书 并 在 医 师 指 导 下 使 用 药 品 名
CellCept
 2006 10 16 2007 11 07 2008 01 22 2008 12 15 2009 12 14 2010 01 18 2011 09 14 2012 07 16 2013 05 08 2014 10 24 2015 12 01 2016 06 03 2016 11 11 2018 02 01 Mycophenolate Mofetil Capsules Matimaikaofenzhi
2006 10 16 2007 11 07 2008 01 22 2008 12 15 2009 12 14 2010 01 18 2011 09 14 2012 07 16 2013 05 08 2014 10 24 2015 12 01 2016 06 03 2016 11 11 2018 02 01 Mycophenolate Mofetil Capsules Matimaikaofenzhi
Ⅱ J Clini Hepatol August 2012 Vol. 28 No DNA cccdna HBV 2008 HBV 2008 HBV HBeAg HBV DNA > ~ IU/ml ALT 6
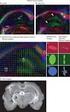 Ⅰ 2012 R512. 6 + 2 B 1001-5256 2012 08 - I - 21 Asian - pacific consensus statement on the management of chronic hepatitis B a 2012 update Yun - Fan Liaw 1 Jia - HorngKao 2 Teerha Piratvisuth 3 Henry Lik
Ⅰ 2012 R512. 6 + 2 B 1001-5256 2012 08 - I - 21 Asian - pacific consensus statement on the management of chronic hepatitis B a 2012 update Yun - Fan Liaw 1 Jia - HorngKao 2 Teerha Piratvisuth 3 Henry Lik
家具使用說明書_實體版2016.9
 續上頁 居家甲醛對策 保持室內空氣流通 甲醛會緩慢地釋放於空氣中 因此平時就需保持室內空氣流通 尤其新居落成時 請盡量將窗子開到最大 以利通風透氣 由於室內溫度 溼度升高時 會大量釋放甲醛 在夏季或梅雨季節 室內經常長時間處於密閉狀態 請特別謹慎注意 此外 若屋內有數個窗戶時 建議保持至少2 扇窗的通風 收納家具用游離甲醛吸附紙/4入 160元 主成分為多孔天然礦石與紙漿 並添加具吸附 分解效果的胺基酸
續上頁 居家甲醛對策 保持室內空氣流通 甲醛會緩慢地釋放於空氣中 因此平時就需保持室內空氣流通 尤其新居落成時 請盡量將窗子開到最大 以利通風透氣 由於室內溫度 溼度升高時 會大量釋放甲醛 在夏季或梅雨季節 室內經常長時間處於密閉狀態 請特別謹慎注意 此外 若屋內有數個窗戶時 建議保持至少2 扇窗的通風 收納家具用游離甲醛吸附紙/4入 160元 主成分為多孔天然礦石與紙漿 並添加具吸附 分解效果的胺基酸
Microsoft Word - Approved PI-clean (updated )
 2007 02 14 2007 03 23 2008 06 30 2008 07 01 2008 07 29 2010 02 12 2010 05 27 2011 09 14 2012 05 15 2012 08 24 2014 01 06 INR / 1 >60 Capecitabine Tablets Kapeitabin Pian 5 --5--N-[()]- O N H N O Me 4 3
2007 02 14 2007 03 23 2008 06 30 2008 07 01 2008 07 29 2010 02 12 2010 05 27 2011 09 14 2012 05 15 2012 08 24 2014 01 06 INR / 1 >60 Capecitabine Tablets Kapeitabin Pian 5 --5--N-[()]- O N H N O Me 4 3
表一特定辭彙縮寫定義 AASLD: American Association for the Study of Liver Disease APASL: Asian Pacific Association for the Study of the Liver EASL: European Assoc
 B 文薜帷 1 黃一城 2 黃煜庭 3 陳詩典 4 廖曜磐 5 病毒學 B DNA(partially-double stranded DNA) Hepadnaviridae B 3, 200 (, o p e n reading frame) ORF-S( S ) (surface antigen) C (core antigen, nucleocapsid) precore antigen( e
B 文薜帷 1 黃一城 2 黃煜庭 3 陳詩典 4 廖曜磐 5 病毒學 B DNA(partially-double stranded DNA) Hepadnaviridae B 3, 200 (, o p e n reading frame) ORF-S( S ) (surface antigen) C (core antigen, nucleocapsid) precore antigen( e
Microsoft PowerPoint - CHB Tx講座 finalizedv.pptx
 B 型肝炎治療的臨床實務 劉俊人 台大醫學院臨床醫學研究所 台大醫院內科部暨肝炎研究中心 Features of CHB In Asia 75% in Asia Chronic hepatitis B virus infection: > 35 million chronic carriers globally Perinatally acquired HBV infection Prolonged
B 型肝炎治療的臨床實務 劉俊人 台大醫學院臨床醫學研究所 台大醫院內科部暨肝炎研究中心 Features of CHB In Asia 75% in Asia Chronic hepatitis B virus infection: > 35 million chronic carriers globally Perinatally acquired HBV infection Prolonged
[ 规 格 ] (1)80mg;( 2)125mg [ 用 法 用 量 ] 本 品 的 剂 型 为 口 服 胶 囊 在 阿 瑞 匹 坦 胶 囊 与 一 种 糖 皮 质 激 素 和 一 种 5-HT 3 拮 抗 剂 联 合 治 疗 方 案 中, 本 品 给 药 3 天 在 开 始 治 疗 前 需 仔
![[ 规 格 ] (1)80mg;( 2)125mg [ 用 法 用 量 ] 本 品 的 剂 型 为 口 服 胶 囊 在 阿 瑞 匹 坦 胶 囊 与 一 种 糖 皮 质 激 素 和 一 种 5-HT 3 拮 抗 剂 联 合 治 疗 方 案 中, 本 品 给 药 3 天 在 开 始 治 疗 前 需 仔 [ 规 格 ] (1)80mg;( 2)125mg [ 用 法 用 量 ] 本 品 的 剂 型 为 口 服 胶 囊 在 阿 瑞 匹 坦 胶 囊 与 一 种 糖 皮 质 激 素 和 一 种 5-HT 3 拮 抗 剂 联 合 治 疗 方 案 中, 本 品 给 药 3 天 在 开 始 治 疗 前 需 仔](/thumbs/42/23000951.jpg) 核 准 日 期 :2013 年 7 月 16 日 修 改 日 期 : 阿 瑞 匹 坦 胶 囊 说 明 书 请 仔 细 阅 读 说 明 书 并 在 医 师 指 导 下 使 用 [ 药 品 名 称 ] 通 用 名 称 : 阿 瑞 匹 坦 胶 囊 商 品 名 称 : 意 美 (EMEND) 英 文 名 称 :Aprepitant Capsules 汉 语 拼 音 : Aruipitan Jiaonang
核 准 日 期 :2013 年 7 月 16 日 修 改 日 期 : 阿 瑞 匹 坦 胶 囊 说 明 书 请 仔 细 阅 读 说 明 书 并 在 医 师 指 导 下 使 用 [ 药 品 名 称 ] 通 用 名 称 : 阿 瑞 匹 坦 胶 囊 商 品 名 称 : 意 美 (EMEND) 英 文 名 称 :Aprepitant Capsules 汉 语 拼 音 : Aruipitan Jiaonang
 2 3 13 17 22 26 1 2 8 100738 +86 (10) 8508 5000 +86 (10) 8518 5111 www.kpmg.com.cn 2006 4 2002 2006 1 28% 2006 17 8 500 2006 2006 2006 7 2.5 2 1 500 500 40% 500 10 16 14 12 10 8 6 4 2 2002-2006 5.1 5.9
2 3 13 17 22 26 1 2 8 100738 +86 (10) 8508 5000 +86 (10) 8518 5111 www.kpmg.com.cn 2006 4 2002 2006 1 28% 2006 17 8 500 2006 2006 2006 7 2.5 2 1 500 500 40% 500 10 16 14 12 10 8 6 4 2 2002-2006 5.1 5.9
藥訊102.01
 中華民國一百零二年三月 彰基藥訊 CCH Pharmacy 發行人 簡素玉 本期要目 Newsletter 主編 彰化基督教醫院藥學部 總編 江怡蓉 第二十一卷 第一期 72 2013年藥品警訊(Q1)... 陳薏如藥師 藥師參與HIV/AIDS國際臨床照護計畫認證之角色... 林雪香藥師 用藥安全 2013 年 藥 品 警 訊( Q 1 ) 陳薏如 藥師 撰寫 施雅分 藥師 審閱 衛生署食品藥物管理局對於國內外相關用藥安全警訊
中華民國一百零二年三月 彰基藥訊 CCH Pharmacy 發行人 簡素玉 本期要目 Newsletter 主編 彰化基督教醫院藥學部 總編 江怡蓉 第二十一卷 第一期 72 2013年藥品警訊(Q1)... 陳薏如藥師 藥師參與HIV/AIDS國際臨床照護計畫認證之角色... 林雪香藥師 用藥安全 2013 年 藥 品 警 訊( Q 1 ) 陳薏如 藥師 撰寫 施雅分 藥師 審閱 衛生署食品藥物管理局對於國內外相關用藥安全警訊
对乙酰氨基酚
 药 品 名 对 乙 酰 氨 基 酚 英 文 名 Paracetamol 别 名 扑 热 息 痛 ; 醋 氨 酚 ; 乙 酰 氨 基 酚 ; 百 服 宁 ; 必 理 通 ; 泰 诺 林 ; 日 立 清 ; 一 滴 清 ; 退 热 净 ; 赛 安 林 ;Acetaminophen 剂 型 1. 片 剂 :0.1g,0.3g,0.5g; 2. 咀 嚼 片 ( 百 服 宁 咀 嚼 片 ):160mg; 3.
药 品 名 对 乙 酰 氨 基 酚 英 文 名 Paracetamol 别 名 扑 热 息 痛 ; 醋 氨 酚 ; 乙 酰 氨 基 酚 ; 百 服 宁 ; 必 理 通 ; 泰 诺 林 ; 日 立 清 ; 一 滴 清 ; 退 热 净 ; 赛 安 林 ;Acetaminophen 剂 型 1. 片 剂 :0.1g,0.3g,0.5g; 2. 咀 嚼 片 ( 百 服 宁 咀 嚼 片 ):160mg; 3.
臺北市及死亡率 - 別 ( 續 1)( 修正 ) ( 二 ) 松山區 中華民國 105 年單 : 人 ; 人 / 十萬人 ;% 所有 1, 所有 所有 惡腫瘤 4
 臺北市及死亡率 - 別 ( 修正 ) ( 一 ) 臺北市 中華民國 105 年單 : 人 ; 人 / 十萬人 ;% 所有 18,039 668.05 33.75 100.00 所有 10,369 80.5 44.60 100.00 所有 7,670 544.83 55.48 100.00 1 惡腫瘤 5,19 193.8 105.00 8.93 惡腫瘤,90 5.9 17.78 8.16 惡腫瘤,99
臺北市及死亡率 - 別 ( 修正 ) ( 一 ) 臺北市 中華民國 105 年單 : 人 ; 人 / 十萬人 ;% 所有 18,039 668.05 33.75 100.00 所有 10,369 80.5 44.60 100.00 所有 7,670 544.83 55.48 100.00 1 惡腫瘤 5,19 193.8 105.00 8.93 惡腫瘤,90 5.9 17.78 8.16 惡腫瘤,99
383 圖 3 不同抗病毒藥物位於血清 HBV DNA 上的基因突變位點清 HBV DNA 載量檢測不到以及 ALT 正常為終點目標 ; 但由於干擾素本身費用較為昂貴, 也具有不等程度的副作用, 因而較難為一般病人所接受 Lamivudine( 干安能 ) Lamivudine 本身對抑制 HBV
 382 慢性B型肝炎抗病毒藥物的選擇 文 圖/譚健民 引 宏恩醫療財團法人宏恩綜合醫院肝膽胃腸科 言 根據流行病的統計 估計全球B型肝炎病毒 (hepatitis B, HBV)感染者約有3.5億人 而其中75%以 上的慢性HBV帶原者分佈在亞洲地區 而HBV感染 更是導致慢性肝炎 肝硬化以及肝細胞癌的主要原因 (1) 目前而言 在臨床上的藥物治療尚難以達到徹底 消滅HBV 但慢性HBV帶原者可在持續接受抗病毒藥
382 慢性B型肝炎抗病毒藥物的選擇 文 圖/譚健民 引 宏恩醫療財團法人宏恩綜合醫院肝膽胃腸科 言 根據流行病的統計 估計全球B型肝炎病毒 (hepatitis B, HBV)感染者約有3.5億人 而其中75%以 上的慢性HBV帶原者分佈在亞洲地區 而HBV感染 更是導致慢性肝炎 肝硬化以及肝細胞癌的主要原因 (1) 目前而言 在臨床上的藥物治療尚難以達到徹底 消滅HBV 但慢性HBV帶原者可在持續接受抗病毒藥
Middle East Respiratory Syndrome Coronavirus, MERS-CoV WHO Qatar 2013 MERS MERS 耗費巨大的社會成本 MERS V
 54 2015 1 505 新興的中東呼吸症候群 冠狀病毒 Those who cannot remember the past are condemned to repeat it. 忘記過去的人, 注定要重蹈覆轍 2012 4 Zarqa 13 2 2012 9 WHO Middle East Respiratory Syndrome Coronavirus, MERS 11 MERS 9 2
54 2015 1 505 新興的中東呼吸症候群 冠狀病毒 Those who cannot remember the past are condemned to repeat it. 忘記過去的人, 注定要重蹈覆轍 2012 4 Zarqa 13 2 2012 9 WHO Middle East Respiratory Syndrome Coronavirus, MERS 11 MERS 9 2
Microsoft Word - 文件1
 染牛隻的臨床症狀狀包括情緒不安 敏感 有攻擊性 磨牙 動作失調 後肢無力 躺臥死亡等症狀狀, 死亡後病理解剖, 會發現其腦部組織出 現空洞, 呈現海綿狀狀病變 被製成肉骨粉, 且掺入飼料中餵養牛隻, 因而使牛隻有受到感染的機 會 根據流行行病學調查研究顯示, 牛海綿狀狀腦病不會透過空氣傳播, 也不會因牛與牛之間的直接或間接接觸 ( 經口 鼻 交配 ) 而平行行感 切實檢驗食品安全
染牛隻的臨床症狀狀包括情緒不安 敏感 有攻擊性 磨牙 動作失調 後肢無力 躺臥死亡等症狀狀, 死亡後病理解剖, 會發現其腦部組織出 現空洞, 呈現海綿狀狀病變 被製成肉骨粉, 且掺入飼料中餵養牛隻, 因而使牛隻有受到感染的機 會 根據流行行病學調查研究顯示, 牛海綿狀狀腦病不會透過空氣傳播, 也不會因牛與牛之間的直接或間接接觸 ( 經口 鼻 交配 ) 而平行行感 切實檢驗食品安全
健康大百科
 A 系 E 健 康 大 百 科 E E E E E E AA AA AA AA AA AA 列 丛 书 编 委 会 主 任 丁 向 阳 北 京 市 人 民 政 府 主 编 方 来 英 北 京 市 卫 生 局 副 主 编 赵 春 惠 北 京 市 卫 生 局 编 委 ( 按 姓 氏 笔 画 排 序 ) 丁 辉 北 京 妇 产 医 院 马 长 生 北 京 安 贞 医 院 王 天 有 首 都 儿 科 研 究
A 系 E 健 康 大 百 科 E E E E E E AA AA AA AA AA AA 列 丛 书 编 委 会 主 任 丁 向 阳 北 京 市 人 民 政 府 主 编 方 来 英 北 京 市 卫 生 局 副 主 编 赵 春 惠 北 京 市 卫 生 局 编 委 ( 按 姓 氏 笔 画 排 序 ) 丁 辉 北 京 妇 产 医 院 马 长 生 北 京 安 贞 医 院 王 天 有 首 都 儿 科 研 究
繼續教育 Therapeutics of Clinical Drugs 臨床藥物治療學 (chemokinecoreceptors) CCR5 CXCR4 (CCR5) HIV-1 R5 (macrophage) M (M-tropic) (CXCR4) HIV X4 CD4+ T T (T-tro
 藥學雜誌 127 77 HIV 病毒及其相關治療藥物簡介 中山醫學大學附設醫院藥劑科藥師廖文聰 蕭如君 中山醫學大學醫學系兼任講師蔡敏鈴 摘要 (human Immunodeficiency Virus, HIV) (acquired immune deficiency syndrome, AIDS) HIV HIV HIV AIDS HAART acquired immune deficiency
藥學雜誌 127 77 HIV 病毒及其相關治療藥物簡介 中山醫學大學附設醫院藥劑科藥師廖文聰 蕭如君 中山醫學大學醫學系兼任講師蔡敏鈴 摘要 (human Immunodeficiency Virus, HIV) (acquired immune deficiency syndrome, AIDS) HIV HIV HIV AIDS HAART acquired immune deficiency
<B8BDB1EDD2BBA3BACDB3D2BBB6A8BCDBD2A9C6B7D7EEB8DFC1E3CADBBCDBB8F1B1ED2E786C73>
 附 表 一 : 统 一 定 价 药 品 表 金 额 : 元 定 价 目 1 293 追 风 透 骨 片 48 片 追 风 透 骨 片 24 片 追 风 透 骨 片 24 片 ( 薄 膜 追 风 透 骨 片 48 片 ( 薄 膜 ( 瓶 ) 30.0 * ( 瓶 ) 15.4 ( 瓶 ) 16.9 ( 瓶 ) 33.0 追 风 透 骨 丸 水 蜜 丸 6g 袋 1.8 * 追 风 透 骨 丸 水 蜜
附 表 一 : 统 一 定 价 药 品 表 金 额 : 元 定 价 目 1 293 追 风 透 骨 片 48 片 追 风 透 骨 片 24 片 追 风 透 骨 片 24 片 ( 薄 膜 追 风 透 骨 片 48 片 ( 薄 膜 ( 瓶 ) 30.0 * ( 瓶 ) 15.4 ( 瓶 ) 16.9 ( 瓶 ) 33.0 追 风 透 骨 丸 水 蜜 丸 6g 袋 1.8 * 追 风 透 骨 丸 水 蜜
FULL PRESCRIBING INFORMATION
 糖漸帄膜衣錠 5 毫克 Trajenta 5mg Film-Coated Tablets 衛署藥輸字第 025537 號 1 適應症第二型糖尿病 使用上的重要限制 : TRAJENTA 不可用於第一型糖尿病患者, 亦不可用於治療糖尿病酮酸中毒 (ketoacidosis), 因為 TRAJENTA 對於此並無效 尚未進行 TRAJENTA 與胰島素併用的相關研究 2 用法用量本藥須由醫師處方使用 2.1
糖漸帄膜衣錠 5 毫克 Trajenta 5mg Film-Coated Tablets 衛署藥輸字第 025537 號 1 適應症第二型糖尿病 使用上的重要限制 : TRAJENTA 不可用於第一型糖尿病患者, 亦不可用於治療糖尿病酮酸中毒 (ketoacidosis), 因為 TRAJENTA 對於此並無效 尚未進行 TRAJENTA 與胰島素併用的相關研究 2 用法用量本藥須由醫師處方使用 2.1
Herceptin Trastuzumab Injection Zhusheyong Qutuozhu Dankang DNA ( CHO) 1.1% 20ml L -L -α,α mg 21mg/ml HER2 1 HER2 5- HER2 HER2 HER2 IHC3+ IHC2+
 2009 07 31 2011 03 30 2011 12 13 2012 05 22 2012 08 15 2012 08 30 2012 11 29 2013 07 08 2015 01 26 2015 11 04 2016 04 12 2017 05 11 2018 07 04 2018 07 31 24 1 / 45 Herceptin Trastuzumab Injection Zhusheyong
2009 07 31 2011 03 30 2011 12 13 2012 05 22 2012 08 15 2012 08 30 2012 11 29 2013 07 08 2015 01 26 2015 11 04 2016 04 12 2017 05 11 2018 07 04 2018 07 31 24 1 / 45 Herceptin Trastuzumab Injection Zhusheyong
Microsoft Word - 西达本胺说明书 20150130.docx
 核 准 日 期 :2014 年 12 月 23 日 修 改 日 期 :2015 年 01 月 19 日 西 达 本 胺 片 说 明 书 请 仔 细 阅 读 说 明 书 并 在 医 师 指 导 下 使 用 药 品 名 称 通 用 名 称 : 西 达 本 胺 片 商 品 名 称 : 爱 谱 沙 ( 英 文 :Epidaza ) 英 文 名 称 :Chidamide Tablets 汉 语 拼 音 :Xidaben
核 准 日 期 :2014 年 12 月 23 日 修 改 日 期 :2015 年 01 月 19 日 西 达 本 胺 片 说 明 书 请 仔 细 阅 读 说 明 书 并 在 医 师 指 导 下 使 用 药 品 名 称 通 用 名 称 : 西 达 本 胺 片 商 品 名 称 : 爱 谱 沙 ( 英 文 :Epidaza ) 英 文 名 称 :Chidamide Tablets 汉 语 拼 音 :Xidaben
Microsoft Word - ACI chapter00-1ed.docx
 前言 Excel Excel - v - 財務管理與投資分析 -Excel 建模活用範例集 5 相關 平衡 敏感 - vi - 前言 模擬 If-Then 規劃 ERP BI - vii - 財務管理與投資分析 -Excel 建模活用範例集 ERP + BI + ERP BI Excel 88 Excel 1. Excel Excel 2. Excel 3. Excel - viii - 前言 1.
前言 Excel Excel - v - 財務管理與投資分析 -Excel 建模活用範例集 5 相關 平衡 敏感 - vi - 前言 模擬 If-Then 規劃 ERP BI - vii - 財務管理與投資分析 -Excel 建模活用範例集 ERP + BI + ERP BI Excel 88 Excel 1. Excel Excel 2. Excel 3. Excel - viii - 前言 1.
FULL PRESCRIBING INFORMATION
 福退癌膜衣錠 200 毫克 Votrient(Pazopanib HCL) film-coated tablets 200mg 衛署藥輸字第 025433 號本藥須由醫師處方使用 福退癌膜衣錠 400 毫克 Votrient(Pazopanib HCL) film-coated tablets 400mg 衛署藥輸字第 025434 號本藥須由醫師處方使用 警語 : 肝毒性 臨床試驗中曾觀察到嚴重且致命的肝毒性
福退癌膜衣錠 200 毫克 Votrient(Pazopanib HCL) film-coated tablets 200mg 衛署藥輸字第 025433 號本藥須由醫師處方使用 福退癌膜衣錠 400 毫克 Votrient(Pazopanib HCL) film-coated tablets 400mg 衛署藥輸字第 025434 號本藥須由醫師處方使用 警語 : 肝毒性 臨床試驗中曾觀察到嚴重且致命的肝毒性
Microsoft Word - Dilatrend_CDS 6.0_redressing site_1016-DIL-01_clean
 1016-DIL-01 6.25 /25 Tablets 6.25 mg/25 mg 022071 020452 Carvedilol 1. 1.1 / Alpha (α) beta (β) ATC code: C07AG02 1.2 1.3 1.4 / 1.5 : Carvedilol 6.25 6.25 carvedilol Lactose monohydrate, Sucrose, Povidone
1016-DIL-01 6.25 /25 Tablets 6.25 mg/25 mg 022071 020452 Carvedilol 1. 1.1 / Alpha (α) beta (β) ATC code: C07AG02 1.2 1.3 1.4 / 1.5 : Carvedilol 6.25 6.25 carvedilol Lactose monohydrate, Sucrose, Povidone
TDF 300 mg d -1 n =45 TDF 300 mg d -1 /FTC 200 mg d -1 2 HBV n = 45 ETV mg d - 1 n = HBV /HIV CHB HBV 2 mg dl - 1 < 2 mg dl - 1 TDF 1 3 1
 302 100039 5 R975. 5 A 1003-3734 2013 11-1269 - 06 Recent advances of the treatment of chronic hepatitis B with tenofovir ZHANG Ning LUO Sheng-qiang 302 Hospital of PLA Beijing 100039 China Abstract Tenofovir
302 100039 5 R975. 5 A 1003-3734 2013 11-1269 - 06 Recent advances of the treatment of chronic hepatitis B with tenofovir ZHANG Ning LUO Sheng-qiang 302 Hospital of PLA Beijing 100039 China Abstract Tenofovir
衛署藥製字第014550號
 衛 署 藥 製 字 第 057858 號 G-11891 息 骨 能 膠 囊 200 毫 克 Celecolen Capsules 200 mg 成 分 Celecoxib 的 化 學 名 為 4-[5-(4-methylphenyl)-3-(trifluoromethyl)-1H-pyrazol-1-yl] benzenesulfonamide, 為 具 有 兩 個 芳 香 族 取 代 基 的 pyrazole,
衛 署 藥 製 字 第 057858 號 G-11891 息 骨 能 膠 囊 200 毫 克 Celecolen Capsules 200 mg 成 分 Celecoxib 的 化 學 名 為 4-[5-(4-methylphenyl)-3-(trifluoromethyl)-1H-pyrazol-1-yl] benzenesulfonamide, 為 具 有 兩 個 芳 香 族 取 代 基 的 pyrazole,
1 500 表 1: 各國平均分數
 2012 年多益測驗全球考生資料統計報告 A < 1> 2012 B < 2> 100% 500 2012 2012 / 21 25 (38%) 57% (58%) 25% / 20% 35% 53% 31% 17% / 31% 12% 6 45 1-10% 81% 6 2012 48 3 30% 1 編註 1: 請見 P.15 編註 2: 請見 P.17 1 500 表 1: 各國平均分數 466
2012 年多益測驗全球考生資料統計報告 A < 1> 2012 B < 2> 100% 500 2012 2012 / 21 25 (38%) 57% (58%) 25% / 20% 35% 53% 31% 17% / 31% 12% 6 45 1-10% 81% 6 2012 48 3 30% 1 編註 1: 請見 P.15 編註 2: 請見 P.17 1 500 表 1: 各國平均分數 466
<4D F736F F D20BA43A9CA42ABACA878AAA2A4A7B773AA76C0F82E646F63>
 慢性 B 型肝炎之新治療 張定宗 B 型肝炎病毒 (HBV) 慢性感染為傷害人類健康的重要疾病, 尤其在亞洲 非洲 中東 太平洋島嶼的居民有 10 % ~ 20 %的 HBV 帶原率, 其絕大部分是在嬰兒期及孩童期感染的 台灣地區約有 80% 成人曾經感染過 B 型肝炎,15~20%成為帶原者 近年來估計全世界有超過三億的人口為 HBV 帶原者, 其中 50 % ~ 75 %的帶原者有活躍的病毒複製及慢性肝炎的情形,25~40%將發展成肝硬化及肝癌等併發症
慢性 B 型肝炎之新治療 張定宗 B 型肝炎病毒 (HBV) 慢性感染為傷害人類健康的重要疾病, 尤其在亞洲 非洲 中東 太平洋島嶼的居民有 10 % ~ 20 %的 HBV 帶原率, 其絕大部分是在嬰兒期及孩童期感染的 台灣地區約有 80% 成人曾經感染過 B 型肝炎,15~20%成為帶原者 近年來估計全世界有超過三億的人口為 HBV 帶原者, 其中 50 % ~ 75 %的帶原者有活躍的病毒複製及慢性肝炎的情形,25~40%將發展成肝硬化及肝癌等併發症
Microsoft Word - Twynsta_US PI_201106_CA
 倍 必 康 平 錠 40/5 毫 克 衛 署 藥 輸 字 第 025444 號 40/10 毫 克 衛 署 藥 輸 字 第 025445 號 80/5 毫 克 衛 署 藥 輸 字 第 025446 號 80/10 毫 克 衛 署 藥 輸 字 第 025447 號 完 整 處 方 資 訊 警 語 : 避 免 於 懷 孕 期 間 使 用 於 懷 孕 期 間 使 用 直 接 作 用 於 腎 素 - 血 管
倍 必 康 平 錠 40/5 毫 克 衛 署 藥 輸 字 第 025444 號 40/10 毫 克 衛 署 藥 輸 字 第 025445 號 80/5 毫 克 衛 署 藥 輸 字 第 025446 號 80/10 毫 克 衛 署 藥 輸 字 第 025447 號 完 整 處 方 資 訊 警 語 : 避 免 於 懷 孕 期 間 使 用 於 懷 孕 期 間 使 用 直 接 作 用 於 腎 素 - 血 管
X 傳統育種技術 分子育種技術 基因改良育種
 06 2015 7 511 72 92? 2010? X 傳統育種技術 1960 1980 30 60 20 分子育種技術 5 10 3 5 基因改良育種 2015 7 511 07 改良後的基因及其生產的蛋白質都需經過嚴格的動物及田間生物安全試驗才會上市, 程序就跟新藥一樣 20 基改產品禁得起考驗 12 2013 1.75 50 1 5 1996 80 2013 156 35 21 6 90 08
06 2015 7 511 72 92? 2010? X 傳統育種技術 1960 1980 30 60 20 分子育種技術 5 10 3 5 基因改良育種 2015 7 511 07 改良後的基因及其生產的蛋白質都需經過嚴格的動物及田間生物安全試驗才會上市, 程序就跟新藥一樣 20 基改產品禁得起考驗 12 2013 1.75 50 1 5 1996 80 2013 156 35 21 6 90 08
其 化 学 结 构 式 为 : F O COOH H 3 C N N O N H CH 3. CH 3 SO 3 H. H 2 O 分 子 式 :C 18H 20FN 3O 4 CH 3SO 3H H 2O 分 子 量 :475.50 本 品 其 他 成 份 为 : 氯 化 钠 性 状 本 品 为
 核 准 日 期 2007 年 04 月 02 日 修 改 日 期 2010 年 09 月 09 日 2011 年 09 月 29 日 2012 年 06 月 05 日 2013 年 05 月 15 日 甲 磺 酸 左 氧 氟 沙 星 注 射 液 说 明 书 请 仔 细 阅 读 说 明 书 并 在 医 师 指 导 下 使 用 警 告 : 在 所 有 年 龄 组 中, 氟 喹 诺 酮 类 药 物, 包
核 准 日 期 2007 年 04 月 02 日 修 改 日 期 2010 年 09 月 09 日 2011 年 09 月 29 日 2012 年 06 月 05 日 2013 年 05 月 15 日 甲 磺 酸 左 氧 氟 沙 星 注 射 液 说 明 书 请 仔 细 阅 读 说 明 书 并 在 医 师 指 导 下 使 用 警 告 : 在 所 有 年 龄 组 中, 氟 喹 诺 酮 类 药 物, 包
藥訊 cdr
 中華民國一百零二年六月 彰基藥訊 CCH Pharmacy 發行人 簡素玉 本期要目 Newsletter 主編 彰化基督教醫院藥學部 總編 江怡蓉 第二十一卷 第二期 73 2013年藥品警訊(Q2)... 施雅分藥師 淺談糖尿病神經病變藥物治療... 林水木藥師 用藥安全 2013 年 藥 品 警 訊( Q 2 ) 施雅分 藥師 撰寫 陳薏如 藥師 審閱 衛生署食品藥物管理局對於國內外相關用藥安全警訊
中華民國一百零二年六月 彰基藥訊 CCH Pharmacy 發行人 簡素玉 本期要目 Newsletter 主編 彰化基督教醫院藥學部 總編 江怡蓉 第二十一卷 第二期 73 2013年藥品警訊(Q2)... 施雅分藥師 淺談糖尿病神經病變藥物治療... 林水木藥師 用藥安全 2013 年 藥 品 警 訊( Q 2 ) 施雅分 藥師 撰寫 陳薏如 藥師 審閱 衛生署食品藥物管理局對於國內外相關用藥安全警訊
老人憂鬱症的認識與老人自殺問題
 18-24 25-44 45-64 65 10 8 6 4 2 0 ( 40% 15% Affect Cognition : drive Behavior DSM-V major depressive episode 2 9 5 Electronic Convulsion Therapy; ECT Rabins65 1% Rabins, 1992 20%-30% Blazer, 1994 65 12.9
18-24 25-44 45-64 65 10 8 6 4 2 0 ( 40% 15% Affect Cognition : drive Behavior DSM-V major depressive episode 2 9 5 Electronic Convulsion Therapy; ECT Rabins65 1% Rabins, 1992 20%-30% Blazer, 1994 65 12.9
