或罕見疾病藥物者, 可向保險人建議收載 保險人每年將暫予收載結果, 報請主管機關公告收載於本標準中 第五條經保險人暫予收載或調整支付價格之品項, 或增修之給付規定, 於主管機關公告收載或修正前, 暫依保險人收載或調整結果支付 第六條有關保險人暫予收載之生效日期如下 : 一 新建議收載之品項或增修之藥
|
|
|
- 稳 吕
- 7 years ago
- Views:
Transcription
1 全民健康保險藥物給付項目及支付標準 行政院衛生署 101 年 12 月 28 日衛署健保字第 號令修正發布 全民健康保險藥價基準 名稱修正為 全民健康保險藥物給付項目及支付標準 ; 並自 102 年 1 月 1 日施行衛生福利部 102 年 8 月 29 日衛部保字第 號令修正發布第 條條文 ; 增訂第 條條文衛生福利部 103 年 6 月 17 日衛部保字第 號令修正發布第 條條文 ; 增訂第 條條文衛生福利部 103 年 9 月 25 日衛部保字第 號令修正發布第 條條文 ; 增訂第 53-2 條條文衛生福利部 103 年 12 月 5 日衛部保字第 號令修正發布第 條條文衛生福利部 104 年 4 月 23 日衛部保字第 號令修正發布第 85 條條文衛生福利部 104 年 7 月 3 日衛部保字第 號令修正發布第 條條文 ; 增訂第 條條文衛生福利部 105 年 3 月 10 日衛部保字第 號令修正發布第 條條文 ; 增訂第 條條文 ; 刪除第 條條文 第一編總則第一條全民健康保險藥物給付項目及支付標準 ( 以下稱本標準 ) 係依據全民健康保險法 ( 以下稱本法 ) 第四十一條第二項訂定 原則上, 每年檢討一次 第二條全民健康保險支付及給付之藥物, 以記載於本標準者為限 第三條本標準所列特殊材料項目係指於相關診療項目收費外, 可向保險人另行申報之項目 本標準未列項目之支付價格已包含於全民健康保險醫療服務給付項目及支付標準相關手術材料費 處置費 麻醉費或檢查費項目支付點數內, 不另支付 第四條本標準未收載之品項, 由藥物許可證之持有廠商或保險醫事服務機構, 檢具本保險藥物納入給付建議書, 向保險人建議收載 新藥及新功能類別特殊材料品項者, 其建議書應含財務衝擊分析資料, 經保險人同意後, 始得納入支付品項 前述未收載品項, 保險人應依本標準之收載及支付價格訂定原則, 並經全民健康保險藥物給付項目及支付標準共同擬訂會議 ( 以下稱藥物擬訂會議 ) 擬訂後, 暫予收載 未符合國際醫藥品稽查協約組織藥品優良製造規範 ( 以下稱 PIC/S GMP) 之藥品, 不得建議收載 中藥藥品項目收載及異動, 應由中藥相關藥業公會於每年四月十五日及十月十五日前向保險人提出建議, 經每半年於藥物擬訂會議擬訂後, 由保險人暫予收載 依本標準第三十三條之二以同分組藥品之支付價格核價者, 得不經藥物擬訂會議, 由保險人暫予收載 新藥取得主管機關核發之查驗登記技術與行政資料審核通過核准函者, 可先行向保險人建議收載 經主管機關核准專案進口或專案製造而未領有藥物許可證之藥物且屬必要藥品 1
2 或罕見疾病藥物者, 可向保險人建議收載 保險人每年將暫予收載結果, 報請主管機關公告收載於本標準中 第五條經保險人暫予收載或調整支付價格之品項, 或增修之給付規定, 於主管機關公告收載或修正前, 暫依保險人收載或調整結果支付 第六條有關保險人暫予收載之生效日期如下 : 一 新建議收載之品項或增修之藥物給付規定 : 當月十五日前 ( 含 ) 同意者, 於次月一日生效 ; 當月十五日後同意者, 於次次月一日生效 二 已收載品項調整支付價格者 : ( 一 ) 依同意日起算, 次次一季一日生效 ; 惟屬配合本法第四十六條及本標準第三編第三章 第五編之藥物支付價格調整者, 其時間不在此限 ( 二 ) 個案特別處理案件, 自通知新藥物價格至新藥物價格實施生效, 給予一個月緩衝期 第六條之一本標準收載之藥物, 其藥物許可證逾期或經主管機關註銷 廢止者, 自保險人通知日之次次月一日起取消給付 但有特殊醫療急迫性或無替代品者, 經廠商檢附主管機關核定之文件後, 延長給付日期至該品項最後一批之有效期限截止日之前一季第一個月一日 前項許可證逾期之藥物, 經廠商檢具許可證效期申請展延中 變更或涉及藥事法尚未辦理完成之文件者, 自原訂取消給付日起延長給付六個月, 必要時得再延長 第一項註銷或廢止原因, 如與藥物之安全或療效有關者, 自主管機關公告註銷或廢止日起取消給付 第七條每一特殊材料品項每半年申復以一次為限, 申復案件自保險人回復函文到之日起六個月內, 同品項不得再提申復 第八條特材管理費用按實際核付特材費用之百分之五支付, 惟最高上限不得超過一千五百點, 如係整組使用者, 應以整組計價後加計 第九條特材管理費用包括特材耗損 包裝 高壓滅菌 倉儲 管理等費用 第十條義肢項目支付價格包括人員 設備 材料 裝置 管理及行政作業成本等費用, 不得另行加計特材管理費用 第二編藥品第一章健保藥品收載原則第十一條可建議納入全民健康保險給付之藥品如下 : 一 主管機關核准通過查驗登記並取得藥品許可證之藥品, 且其許可證類別為下列之一者 : ( 一 ) 限由醫師使用 ( 二 ) 須由醫師處方使用 ( 三 ) 由醫師或檢驗師使用 ( 四 ) 限由牙醫師使用 ( 五 ) 限由麻醉醫師使用 ( 六 ) 限由眼科醫師使用 2
3 ( 七 ) 限由醫師及牙醫師使用 二 醫師指示用藥依法不在全民健康保險給付範圍, 原前公 勞保核准使用之指示用藥, 經醫師處方暫予支付 但保險人應逐步檢討並縮小該類品項之給付範圍 三 可建議納入全民健康保險給付之中藥藥品 : ( 一 ) 依中藥新藥查驗登記須知之規定, 依 藥品優良臨床試驗規範 (GCP) 進行臨床試驗, 且通過新藥查驗登記 (NDA) 各項審查作業, 取得主管機關核發藥品許可證之新藥 ( 二 ) 主管機關核准經由 GMP 中藥濃縮廠製造之 調劑專用 及 須由醫師 ( 中醫師 ) 處方使用 之濃縮中藥為限 ; 複方濃縮中藥並應列屬主管機關整編之 臨床常用中藥方劑基準方 前項中藥藥品支付應依據全民健康保險醫療服務給付項目及支付標準規定辦理 第十二條全民健康保險不予給付之藥品如下 : 一 主管機關核准屬避孕用藥 生髮劑 黑斑漂白劑 戒菸用貼片 洗髮精等非屬醫療所必需者 二 預防接種所用之疫苗 三 經保險人認定, 非屬醫療所必需或缺乏經濟效益者 四 不符藥品許可證所載適應症及本標準藥品給付規定者 惟特殊病例得以個案向保險人申請事前審查, 並經核准後給付 五 其他經主管機關公告不給付之藥品 對於醫藥團體提出臨床實證於療效上有疑慮之藥品, 於保險人接獲相關事證後, 經藥物擬訂會議審議, 得先暫停給付, 自保險人公告日至實施生效, 給予三個月緩衝期, 俟藥物主管機關確認其無療效上疑慮後之次月, 始得恢復給付 第十二條之一本標準收載之藥品品項, 有替代性品項可供病人使用且符合下列情形之一者, 保險人得將該品項不列入健保給付範圍一年..一 藥商以高於支付價供應予本保險特約醫事服務機構, 經通知許可證持有藥商改善, 仍未改善者 二 許可證持有藥商因故不再供應且未於六個月前通報保險人者 有不可抗力因素, 致無法供應時, 未於該發生日起十日內通報保險人 第十二條之二本標準已收載之藥品品項, 如連續五年以上無醫令申報量, 且有替代性品項可供病人使用者, 該品項不列入本標準 但如有特殊情形, 藥物許可證之持有廠商或保險醫事服務機構得向保險人提出說明, 並提藥物擬訂會議審議 第十三條含於全民健康保險醫療服務給付項目及支付標準相關費用不另支付之品項如下 : 一 清潔劑 賦型劑 放射線製劑 診斷用藥 二 其他經全民健康保險醫療服務給付項目及支付標準明列內含於相關費用, 不另支付之品項 第二章健保藥品支付價格訂定原則第十四條新建議收載全民健康保險藥品之分類如下 : 3
4 一 新藥 : 指新建議收載之品項, 於本標準收載品項中, 屬新成分 新劑型 新給藥途徑及新療效複方者 ( 一 ) 第 1 類新藥 : 藥品許可證之持有商須提出與現行最佳常用藥品之藥品 - 藥品直接比較 (head-to-head comparison) 或臨床試驗文獻間接比較 (indirect comparison), 顯示臨床療效有明顯改善之突破創新新藥 倘該藥品為有效治療特定疾病之第一個建議收載新藥, 而無現有最佳治療藥品可供比較, 則可用該疾病現行標準治療 ( 如 : 外科手術 支持性療法等 ) 做為療效比較之對象 ; 前述臨床療效包含減少危險副作用 ( 二 ) 第 2 類新藥 : 1. 第 2A 類 : 與現行最佳常用藥品比較, 顯示臨床價值有中等程度改善 (moderate improvement) 之新藥 2. 第 2B 類 : 臨床價值相近於已收載核價參考品之新藥 二 本標準已收載成分 劑型之新品項 : ( 一 ) 複方及特殊規格藥品 1. 水 醣類及電解質補充調節液 2. 氨基酸及注射營養劑 3. 綜合維生素 4. 綜合感冒藥 5. 制酸劑 ( 二 ) 其他處方藥品 1. 原開發廠藥品 : (1) 原開發公司之母廠或子廠所生產之同一成分 劑型及劑量之產品 (2) 具有原開發公司以書面授權在本國委託製造或共同販售, 且在授權期間所產 售之同一成分 劑型及劑量之產品 2.BA/BE 學名藥品 : 實施生體可用率或生體相等性 (BA/BE) 實驗, 並經主管機關認可之藥品 3. 一般學名藥品 : 其他非屬 BA/BE 學名藥之學名藥品 三 生物相似性藥品 : 經主管機關依生物相似性藥品之相關查驗登記規定核准認定之藥品 第十五條原開發廠藥品之認定標準如下 : 一 原開發公司係指該藥品之有效成分取得成分專利之公司 二 倘同一原開發公司製造之產品, 授權在臺由不同公司取得藥品許可證販售, 須為相同之英文品名 三 廠商在向保險人提出核價建議之同時, 須檢附下列相關文件之一, 始得認定為原開發廠藥品 : ( 一 ) 該藥品之有效成分具專利之證明文件, 以中華民國專利為優先, 若非為中文版本, 則需提供經政府立案之翻譯社所翻譯之中文譯本 ( 二 )The Merck Index 最新版記載該公司為該品項成分專利權人之影本, 認為有 4
5 必要時, 應提供專利證明文件 四 倘為授權在臺製造或共同販售之公司, 應提供原開發公司載明有效期間之書面授權文件, 且文件上所刊載商品名稱應與原開發公司之藥品相同, 該文件另須送交我國駐外單位簽證 若未提供上述相關資料, 則不予認定 五 複方藥品之原開發公司必須為擁有全部有效成分之專利權或經專利權人授權者 第十六條 BA/BE 學名藥品之認定標準如下 : 一 生體相等性 (BE) 試驗 :BE 試驗計畫經主管機關核准通過實施, 並取得該試驗報告之同意或核備函者 二 生體可利用率 (BA) 併臨床試驗 : 同時符合下列各項 : ( 一 )BA 試驗計畫經主管機關核准通過實施, 並取得該報告之同意或核備函 ( 二 ) 臨床試驗計畫經主管機關核准通過實施, 並取得該報告之同意或核備函 ; 或於藥品許可證上有已執行臨床試驗之註記 三 BA/BE 學名藥品委託他廠製造時, 須經主管機關核准委託他廠製造或變更製造廠, 並檢附主管機關核發得以取代 BE 學名藥品或變更前後藥品無安全療效差異所核發可視為 BA/BE 學名藥品之認定函 四 一般學名藥品委託他廠製造時, 使用被委託廠持有同分組之 BA/BE 學名藥品之相同配方 製程 ( 含設備 ) 製造時, 除應取得該同分組藥品之 BE 試驗報告或 BA 併臨床試驗報告同意核備函及其授權書, 併同時檢具主管機關核發二者配方 製程 ( 含設備 ) 均相同之證明函 第十七條新藥支付價格之訂定原則如下 : 一 第 1 類新藥 : 以十國藥價中位數核價 對於致力於國人族群特異性療效及安全性之研發, 在國內實施臨床試驗達一定規模, 以十國藥價中位數之 1.1 倍 ( 即加算百分之十 ) 核價 二 第 2 類新藥 : ( 一 ) 以十國藥價中位數為上限 ( 二 ) 得依其臨床價值改善情形, 從下列方法擇一核價 : 1. 十國藥價最低價 2. 原產國藥價 3. 國際藥價比例法 4. 療程劑量比例法 5. 複方製劑得採各單方健保支付價合計乘以百分之七十, 或單一主成分價格核算藥價 ( 三 ) 依上述核價原則計算後, 若符合下列條件者, 則另予加算, 惟仍不得高於十國藥價中位數 : 1. 對於致力於國人族群特異性療效及安全性之研發, 在國內實施臨床試驗達一定規模, 依相關原則核價後加算百分之十 2. 在國內進行藥物經濟學 (PE) 之臨床研究者, 最高加算百分之十 三 建議收載二項以上同成分劑型但不同規格之藥品, 依上述核價方式核價後, 其餘 5
6 品項得採規格量換算法計算藥價 第十七條之一在我國為國際間第一個上市, 且臨床療效有明顯改善之新成分新藥或為治療特定疾病之第一個新成分新藥, 得自下列方法, 擇一訂定其支付價格 : 一 參考市場交易價 二 參考成本計算法 廠商須切結所提送之成本資料無誤, 且須經保險人邀集成本會計 財務及醫藥專家審議 三 參考核價參考品或治療類似品之十國藥價, 且不得高於該十國藥價中位價 第十八條第十七條國際藥價比例法及療程劑量比例法之執行方式如下 : 一 國際藥價比例法 : ( 一 ) 分別計算十國新藥與核價參考品之藥價比值, 並取各國藥價比值之中位數乘以核價參考品之健保藥價, 計算該新藥之健保價格 ( 二 ) 若可供參考之藥價比值國家數為奇數, 取最中間一國藥價比值為之 ; 若為偶數, 取最中間二國藥價比值之平均值為之 二 療程劑量比例法 : ( 一 ) 依新藥療程劑量及參考品療程劑量及單價, 計算每單位新藥之初始藥價 ( 二 ) 依療程劑量比例法核價者, 得考慮新藥與參考品之療效 安全性及方便性, 以下列方式加算 : 1. 比核價參考品療效佳, 並有客觀證據 (evidence base) 者, 最高加算百分之十五 2. 比核價參考品安全性高, 並有客觀證據者, 最高加算百分之十五 3. 在使用上, 較核價參考品更具方便性者, 如用藥間隔較長 用藥途徑較優 療效與安全性監測作業較簡化 安定性較穩定 效期較長 攜帶方便 調製較方便 使用較方便 安全包裝者, 最高加算百分之十五 4. 具臨床意義之兒童製劑者, 最高加算百分之十五 第十九條新藥之核價參考品選取原則如下 : 一 依解剖治療化學分類系統 (Anatomical Therapeutic Chemical classification,atc classification) 為篩選基礎 二 原則上以同藥理作用或同治療類別之藥品為選取對象 三 若有執行臨床對照試驗 (head-to-head comparison) 之藥品, 列為重要參考 四 新藥經藥物擬訂會議審議認屬第 2A 類新藥者 : ( 一 ) 依選取參考品之同成分規格之原開發廠藥品為核算基準 ( 二 ) 核價參考品以最近五年收載之療效類似藥品為主要參考 第二十條第 1 類或第 2 類新藥以十國藥價中位數或最低價核價者, 其查有藥價之國家少於或等於五國, 應自新藥收載生效之次年起, 逐年於每年第四季以十國藥價檢討支付價, 至有藥價之國家多於五國之次年或以十國藥價業檢討五次為止 原藥價高於以原核價方式所計算之新價格時, 應調整至原核價方式所計算之新價格, 並於次年一月一日生效 ; 原藥價低於以原核價方式所計算之新價格時, 維持原藥價 依第十七條之一第三款以參考類似品之十國藥價核價者, 比照前項規定辦理 6
7 第二十一條對於致力於國人族群特異性療效及安全性之新藥研發, 在國內實施臨床試驗達一定規模之認定基準, 為下列條件之一 : 一 比照藥品查驗登記審查準則第三十八條之一規定 : 新藥之研發階段, 在我國進行第一期 (Phase I ) 及與國外同步進行第三期樞紐性臨床試驗 (Phase III Pivotal Trial ), 或與國外同步在我國進行第二期臨床試驗 (Phase II) 及第三期樞紐性臨床試驗 (Phase III Pivotal Trial), 且符合下列基準者 : ( 一 ) 試驗性質屬第一期 (Phase I ), 如藥動學試驗 (PK study) 藥效學試驗 (PD study) 或劑量探索試驗 (Dose finding study) 等, 我國可評估之受試者人數至少十人為原則 ( 二 ) 第二期 (Phase II) 之臨床試驗, 我國可評估之受試者人數至少二十人為原則 ( 三 ) 第三期樞紐性臨床試驗 (Phase III Pivotal Trial ), 我國可評估之受試者人數至少八十人為原則, 且足以顯示我國與國外試驗結果相似 二 比照藥品查驗登記審查準則第三十八條之二第二項第四款規定 : 有十大醫藥先進國家之一參與之多國多中心第三期臨床試驗 (Phase III study), 且其試驗報告為向美國食品藥物管理局 (Food and Drug Administration,FDA) 或歐洲醫藥品管理局 (European Medicines Agency,EMA) 申請查驗登記之臨床資料, 並符合下列條件之一者 : ( 一 ) 單次試驗總受試者人數二百人以上, 我國可評估之受試者人數至少三十人為原則, 或我國受試者占總人數百分之五以上 ( 二 ) 單次試驗總受試者人數未滿二百人, 我國可評估之受試者人數至少十人為原則 第二十二條新品項藥品支付價格之訂定原則如下 : 一 同一成分劑型藥品之價格, 以常用劑量為計算基準, 當劑量為倍數時, 其支付價格以不超過倍數之九成為原則 二 屬藥物許可證換證之新品項 : ( 一 ) 於舊證註銷日三個月以內提出建議者 : 得延用舊證藥品之價格 ( 二 ) 於舊證註銷日起超過三個月提出建議者 : 視同新品項, 依本標準第四條之程序辦理 三 建議收載之規格量, 應以藥品許可證登載之 包裝種類 為限 四 外用液劑 外用軟膏劑 口服液劑等劑型, 非屬本標準已收載之規格量品項 : ( 一 ) 本標準已收載同一張許可證不同規格之品項者, 依個別藥品之仿單 世界衛生組織 (WHO) 之 ATC 網站之每日劑量換算給付合理天數, 作為是否收載之依據, 惟以仿單之用法 用量為優先, 其支付價格以最近似之高低規格量換算, 取最低價核定之 ( 二 ) 醫療必須使用之特殊規格, 必要時提請臨床醫師及醫 藥專家提供專業認定 ( 三 ) 屬新複方製劑, 與已收載品項無同分組者, 依新藥核價程序處理 7
8 五 授權在臺製造或販售之原開發廠藥品, 若經停止授權, 應依其所屬藥品分類予以重新核價 六 全靜脈營養輸液按醫療機構提供之全靜脈營養處方箋中, 所使用本標準已收載品項之用量, 乘以各品項每 ml 之藥價單價, 加總後之藥價, 再換算該全靜脈營養輸液每 ml 之藥價 ( 四捨五入至小數點第二位 ) 核算 七 新品項核價參考品之價格所依據之時間點, 依新品項預計之生效日為準 ; 若其參考品之價格於該時間點已有後續即將調整價格之資訊時, 核予二個先後生效之健保支付價 八 屬本標準第十四條第二款第二目, 且為二種有效成分以上之複方製劑之核價原則如下 : ( 一 ) 新品項之單位含量組成與已收載同成分劑型品項之單位含量組成, 具比例關係且等於一時, 依本標準第二十七條至第三十三條辦理 ( 二 ) 新品項之單位含量組成與已收載同成分劑型品項之單位含量組成, 具比例關係且非等於一時, 取下列條件之最低價 : 1. 單位含量組成具比例關係之同成分劑型品項最低價, 以規格量換算後價格 2. 該品項或同單位含量組成之原開發廠藥品之十國藥價最低價 3. 同單位含量之各單方藥品最低價 ( 各單方以同廠牌藥品之健保支付價優先 ) 合計乘以百分之七十後價格 4. 廠商建議價格 ( 三 ) 新品項之單位含量組成與已收載同成分劑型品項之單位含量組成, 不具比例關係時, 取下列條件之最低價 : 1. 該品項或同單位含量組成之原開發廠藥品之十國藥價最低價 2. 以同單位含量之各單方藥品最低價 ( 各單方以同廠牌藥品之健保支付價優先 ) 合計乘以百分之七十後價格 3. 廠商建議價格 第二十三條 ( 刪除 ) 第二十四條 ( 刪除 ) 第二十五條具標準包裝之藥品, 指交付病人自行使用之口服錠劑 膠囊劑藥品, 其包裝符合藥事法第七十五條及藥品查驗登記審查準則第二十條相關規定, 具有下列可讓民眾清楚辨識藥品之條件如下 : 一 交付病人之藥品包裝為主管機關核准之包裝 ; 或交付病人鋁箔片裝之藥品, 其藥品每一片鋁箔紙上所刊印之內容符合藥品查驗登記審查準則相關規定 二 慢性病之藥品為常用包裝規格之包裝數, 以供藥事人員以藥品原包裝提供予病人 三 前述包裝均應完整呈現可供病患或其家屬辨識之藥品資訊, 如藥品中文名稱 藥品英文名稱 含量 有效期間, 若能更明確提供服用日期者尤佳 ( 如星期一至星期日 ) 第二十六條下列複方及特殊規格藥品以同類品最低價支付, 且不得高於所列之支付上限 8
9 價 : 一 水 醣類及 / 或電解質補充調節液 ( 一 ) 醣類注射液規格支付上限價 500mL 1000mL 濃度 5% 31.5 元 56.7 元 10% 31.5 元 56.7 元 20% 35.0 元 50% 63.0 元 10% Maltose 元 ( 二 ) 電解質或醣類電解質注射液 類 別 規 格 支付上限價 Saline Solution 500mL 31.5 元 Dextrose +Saline 500mL 31.5 元 Ringers Solution 500mL 31.5 元 Lactated Ringers 500mL 40.0 元 Lactated Ringers+ 醣類 500mL 60.0 元 Lactated Ringers +Maltose 500mL 元 醣類 + 電解質溶液 400mL 60.0 元 800mL 元 附註 : 此處所稱 醣類 係指 Dextrose 或 Maltose 以外之任何種類醣類, 包括 Fructose Xylitol Sorbitol 等 二 胺基酸及注射營養劑 ( 一 ) 胺基酸大型注射液 類 別 規格 支付上限價 一般胺基酸注射液濃度小於或等於 3% 500mL 200 元 濃度大於 3% 小於或等於 5% 500mL 220 元 濃度大於 5% 小於或等於 7% 500mL 240 元 濃度大於 7% 500mL 310 元 肝疾病用胺基酸注射液 500mL 630 元 ( 二 ) 脂肪乳劑規格 支付上限價 100mL mL 500mL 濃度 10% 元 元 元 9
10 20% 元 元 三 制酸劑 : ( 一 ) 口服錠劑 膠囊 顆粒 : 支付上限價 2.0 元 ( 二 ) 單一劑量包裝之懸浮液 : 支付上限價 10.0 元 / 包 ( 三 ) 瓶裝懸浮劑液類別支付上限價 一般懸浮劑液 添加 Simethicone 添加 Oxethazine 1.2 元 /5mL 1.5 元 /5mL 1.9 元 /5mL 四 綜合感冒藥 : ( 一 ) 口服錠劑 膠囊 顆粒 : 支付上限價 4.0 元 ( 二 ) 糖漿劑類別支付上限價 不含植物抽提物或 Codeine 含植物抽提物 0.2 元 /ml 0.3 元 /ml 含 Codeine 0.45 元 /ml 五 綜合維生素 : ( 一 ) 口服 : 支付上限價 3.0 元 ( 二 ) 注射 : 支付上限價 15.0 元 / 毫升前項含葡萄糖 胺基酸及脂肪乳劑之三合一營養輸注液, 以同分組每單位熱量單價之最低價格為基準, 經總熱量換算後之價格與廠商建議價格相較, 取其低者為支付價格 第二十七條新品項屬原開發廠藥品之同藥品分類支付價格訂定原則如下 : 一 原開發廠藥品在國內已有實施 BA/BE 之同成分規格藥品者, 分為監視中藥品與非監視中藥品 : ( 一 ) 監視中藥品 : 以該品於十大先進國家藥價中位數為支付價格上限 ( 二 ) 非監視中藥品 : 以該品於十大先進國家藥價中位數之 0.85 倍為支付價格上限 二 原開發廠藥品其在國內沒有實施 BA/BE 之同成分規格藥品者, 以該品於十大先進國家藥價中位數為支付價格上限 三 上述所稱十大先進國家藥價係指英國 德國 日本 瑞士 美國 比利時 澳洲 法國 瑞典 加拿大等十國藥價並加上匯率予以換算得之 有關參考各國之藥價公定書及匯率, 由保險人定期公布 第二十八條新品項屬原開發廠藥品之同藥品分類核價方式如下 : 10
11 一 本標準未收載同成分 劑型原開發廠藥品者, 取下列條件之最低價 : ( 一 ) 同規格原開發廠藥品於十大先進國家藥價中位數或中位數之 0.85 倍為支付價格上限 : 1. 本標準已收載有實施 BA/BE 之同成分劑型藥品, 且原開發廠藥品非屬於監視中藥品, 以十大先進國家藥價中位數之 0.85 倍為支付價格上限 2. 本標準未收載有實施 BA/BE 之同成分劑型藥品或本標準已收載有實施 BA/BE 同成分劑型藥品, 且原開發廠藥品屬於監視中藥品者, 以十大先進國家藥價中位數為支付價格上限 ( 二 ) 廠商建議價格 二 本標準有收載具同成分 劑型原開發廠藥品者 : ( 一 ) 有同規格原開發廠藥品者, 取下列條件之最低價 : 1. 同規格原開發廠藥品最低價 2. 同規格原開發廠藥品於十大先進國家藥價中位數或中位數之 0.85 倍為支付價格上限 : (1) 本標準已收載實施 BA/BE 同成分劑型藥品, 且原開發廠藥品非屬於監視中藥品, 以十大先進國家藥價中位數之 0.85 倍為支付價格上限 (2) 本標準未收載有實施 BA/BE 之同成分劑型藥品或本標準已收載有實施 BA/BE 同成分劑型藥品, 且原開發廠藥品屬於監視中藥品者, 以十大先進國家藥價中位數為支付價格上限 3. 廠商建議價格 ( 二 ) 無同規格原開發廠藥品者 : 1. 有收載同規格學名藥品, 取下列條件之最低價 : (1) 原開發廠藥品最低價規格量換算後價格 (2) 同規格原開發廠藥品於十大先進國家藥價中位數或中位數之 0.85 倍為支付價格上限 : 本標準已收載有實施 BA/BE 同成分劑型藥品, 且原開發廠藥品非屬於監視中藥品, 以十大先進國家藥價中位數之 0.85 倍為支付價格上限 本標準未收載有實施 BA/BE 之同成分劑型藥品或本標準已收載有實施 BA/BE 同成分劑型藥品, 且原開發廠藥品屬於監視中藥品者, 以十大先進國家藥價中位數為支付價格上限 (3) 廠商建議價格 2. 無收載同規格學名藥品者 : (1) 劑量與國際藥價具一定比例關係 ( 國際藥價比值中位數於劑量比率之 ±30% 間, 且無任一國際藥價比值 =1) 者, 取下列條件之最低價 : 原開發廠藥品最低價規格量換算後價格 同規格原開發廠藥品於十大先進國家藥價中位數或中位數之 0.85 倍為支付價格上限 : 本標準已收載有實施 BA/BE 同成分劑型藥品, 且原開發廠藥品非屬於監 11
12 視中藥品, 以十大先進國家藥價中位數之 0.85 倍為支付價格上限 本標準未收載有實施 BA/BE 之同成分劑型藥品或本標準已收載有實施 BA/BE 同成分劑型藥品, 且原開發廠藥品屬於監視中藥品者, 以十大先進國家藥價中位數為支付價格上限 廠商建議價格 (2) 劑量與國際藥價無一定比例關係 ( 國際藥價比值中位數不在劑量比率之 ± 30% 間, 或一國以上國際藥價比值 =1): 廠商建議價低於藥價比例法及原開發廠藥品最低價規格換算, 取下列條件之最低價 : 原開發廠藥品最低價規格量換算後價格 同規格原開發廠藥品於十大先進國家藥價中位數或中位數之 0.85 倍為支付價格上限 : A. 本標準已收載有實施 BA/BE 同成分劑型藥品, 且原開發廠藥品非屬於監視中藥品, 以十大先進國家藥價中位數之 0.85 倍為支付價格上限 B. 本標準未收載有實施 BA/BE 之同成分劑型藥品或本標準已收載有實施 BA/BE 同成分劑型藥品, 且原開發廠藥品屬於監視中藥品者, 以十大先進國家藥價中位數為支付價格上限 廠商建議價格 廠商建議價不低於藥價比例法及原開發廠藥品最低價規格換算, 提藥物擬訂會議討論 第二十九條新品項屬 BA/BE 學名藥品之同藥品分類支付價格訂定原則如下 : 一 新建議收載通過 BA/BE 藥品, 以不高於本標準收載之已實施 BA/BE 之同成分 規格 劑型 劑量之最低支付價格核價 二 學名藥品如實施 BE 後, 可重新建議核價 三 BA/BE 以不超過同成分原開發廠藥品支付價格為原則 第三十條新品項屬 BA/BE 學名藥品之同藥品分類核價方式如下 : 一 有收載同規格 BA/BE 學名藥品或原開發廠藥品者, 取下列條件之最低價 : ( 一 ) 同規格原開發廠藥品最低價之百分之八十或百分之九十 : 1. 原開發廠藥品尚在專利期內或仍屬監視期中藥品者, 以同規格原開發廠藥品最低價之百分之八十為支付價格 2. 其他條件者, 以同規格原開發廠藥品最低價之百分之九十為支付價格 ( 二 ) 同規格 BA/BE 學名藥品最低價 ( 三 )BE 對照品藥價 ( 四 ) 廠商建議價格 二 未收載同規格 BA/BE 學名藥品及原開發廠藥品 : ( 一 ) 有收載不同規格 BA/BE 學名藥品或原開發廠藥品者, 取下列條件之最低價 : 1. 原開發廠藥品最低價規格量換算後價格之百分之八十或百分之九十 : 12
13 (1) 原開發廠藥品尚在專利期內或仍屬監視期中藥品者, 以原開發廠藥品最低價規格量換算後價格之百分之八十為支付價格 (2) 其他條件者, 以原開發廠藥品最低價規格量換算後價格之百分之九十為支付價格 2.BA/BE 學名藥品最低價規格量換算後之價格 3. 同規格原開發廠藥品十大先進國家藥價中位數之 0.85 倍 4.BE 對照品藥價 5. 廠商建議價格 ( 二 ) 未收載不同規格 BA/BE 學名藥品及原開發廠藥品者 : 1. 同規格原開發廠藥品有國際藥價者, 取下列條件之最低價 : (1) 同規格原開發廠藥品應核算藥價之百分之八十或百分之九十 : 原開發廠藥品尚在專利期內或仍屬監視期中藥品者, 以同規格原開發廠藥品應核算藥價之百分之八十為支付價格 其他條件者, 以同規格原開發廠藥品應核算藥價之百分之九十為支付價格 (2) BE 對照品藥價 (3) 廠商建議價格 2. 同規格原開發廠藥品無國際藥價者, 取下列條件之最低價 : (1) 同規格一般學名藥最高價 ; 一般學名藥無同規格時, 依最高價規格量換算後之價格 (2)BE 對照品藥價 (3) 廠商建議價格 第三十一條新品項屬一般學名藥品之同藥品分類支付價格訂定原則如下 : 一 新建議收載之藥品, 以不高於本標準收載一般學名藥之同成分 規格 劑型 劑量之最低支付價格核價 二 一般學名藥品之支付價格, 不得大於 BA/BE 之藥品支付價格, 且不高於原開發廠藥品支付價格之百分之八十為原則 第三十二條新品項屬一般學名藥品之同藥品分類核價方式如下 : 一 有收載同規格一般學名藥 BA/BE 學名藥品或原開發廠藥品者, 取下列條件之最低價 : ( 一 ) 同規格一般學名藥最低價 ( 二 ) 同規格 BA/BE 學名藥最低價 ( 三 ) 同規格原開發廠藥品藥價之百分之八十 ( 四 ) 廠商建議價格 二 未收載同規格一般學名藥 BA/BE 學名藥及原開發廠藥品者, 取下列條件之最低價 : ( 一 ) 一般學名藥最低價規格量換算後之價格 ( 二 )BA/BE 學名藥最低價規格量換算後之價格 13
14 ( 三 ) 原開發廠藥品最低價規格量換算後價格之百分之八十 ( 四 ) 同規格原開發廠藥品於十大先進國家藥價中位數或中位數之 0.85 倍為支付價格上限 : 1. 本標準已收載有實施 BA/BE 同成分劑型藥品, 且原開發廠藥品非屬於監視中藥品, 以十大先進國家藥價中位數之 0.85 倍為支付價格上限 2. 本標準未收載有實施 BA/BE 之同成分劑型藥品或本標準已收載有實施 BA/BE 同成分劑型藥品, 且原開發廠藥品仍屬監視中藥品者, 以十大先進國家藥價中位數為支付價格上限 ( 五 ) 廠商建議價格 第三十二條之一生物相似性藥品之核價方式, 取下列條件之最低價 : 一 本標準已收載原開發廠藥品支付價之. 八五倍 二 原開發廠藥品在十國藥價中位數之. 八五倍 三 該藥品在十國藥價中位數之. 八五倍 四 廠商建議價格 第三十三條新品項藥品基本價之核價方式如下 : 一 劑型別基本價如下 : ( 一 ) 錠劑或膠囊劑, 為一. 五元 ; 具標準包裝, 為二元 ( 二 ) 口服液劑, 為二十五元 ( 三 ) 一百毫升以上未滿五百毫升之輸注液, 為二十二元 ( 四 ) 五百毫升以上大型輸注液, 為二十五元 ( 五 ) 前二目以外之其他注射劑, 為十五元 ( 六 ) 栓劑, 為五元 ( 七 ) 眼藥水, 為十二元, 單一劑量包裝不適用 ( 八 ) 口服鋁箔小包 ( 顆粒劑 粉劑 懸浮劑 ), 為六元 二 同分組基本價按下列條件之最高價格核價 : ( 一 ) 同分組最高價藥品價格之 八倍, 與同分組之 PIC/S GMP 品項之最低價, 二項方式取其最低價 ( 二 ) 劑型別基本價 ( 三 ) 以同藥品分類之核價方式核算之藥價 ( 四 ) 原品項之現行健保支付價 三 下列品項不適用前二款之核價方式.. ( 一 ) 指示用藥 ( 二 ) 含葡萄糖 胺基酸及脂肪乳劑之三合一營養輸注液 ( 三 ) 健保代碼末二碼為 99 之品項 第三十三條之一本標準中華民國一百零五年三月十日修正施行時, 依修正前第二十四條規定條件收載者, 其原料藥具備藥品主檔案 (Drug Master File,DMF) 或便民包裝條件有異動時, 由保險人依下列原則重新核價 : 一 以同分組健保代碼第二碼為 C 之最低價核價 ; 同分組無健保代碼第二碼為 C 者, 以 14
15 原健保支付價之 八倍核價 但不得高於同分組健保代碼第二碼為 A 或 B 之藥品支付價格 二 屬全民健康保險藥品價格調整作業辦法第二十一條規定調整之同成分 同劑型藥品, 以本標準收載之同分組且符合 PIC/S GMP 藥品之支付價格核價 前項重新核給健保代碼及藥品價格之生效方式, 依本標準新品項規定辦理 ; 原健保支付價應歸零, 其生效方式, 自保險人公布日至實施生效, 給予一個月緩衝期 藥廠之 GMP 證明被廢止 註銷或失效前所生產之藥品, 未經主管機關認定不得販售者, 得繼續支付 但藥品經主管機關認定不得販售者, 自主管機關函知保險人之發文日起, 暫停支付, 暫停支付後六個月內, 廠商未檢附製造許可移轉經主管機關核定或備查之證明文件者, 取消該品項之健保給付 第一項及前項支付價格處理結果, 由保險人公布生效後, 提藥物擬訂會議報告 第三十三條之二符合 PIC/S GMP 之新品項, 屬全民健康保險藥品價格調整作業辦法第二十一條規定調整之同成分 同劑型藥品, 其藥品支付價格訂定原則如下 : 一 以本標準收載之同分組且符合 PIC/S GMP 藥品之支付價格核價, 不適用本標準第二十六條至第三十三條規定 二 若無同分組之 PIC/S GMP 藥品作為核價參考品, 依本標準第二十六條至第三十二條規定核價 三 適用本標準第二十五條標準包裝藥品之訂價原則及劑型別基本價 四 下列品項不得作為核價參考品 : ( 一 ) 健保代碼末二碼為 99 之品項 ( 二 ) 指示用藥 ( 三 ) 因藥品市場實際交易價格調查未申報或不實申報而尚於支付價格調降期間之藥品 第三十四條有關必要藥品及罕見疾病用藥原則上尊重市場價格, 且品項種類由醫藥團體視需要依規定隨時提報 適用之藥品如下 : 一 罕見疾病用藥 : 經主管機關公告為罕見疾病用藥, 已收載於本標準或新建議納入收載者 二 不可替代必要藥品 : 於治療特定適應症無其他成分藥品可供替代之必要藥品, 並經藥物擬訂會議認定者 三 必要藥品 : 本標準已收載品項, 非屬不可替代但具臨床價值, 且相較於其他可替代成分藥品價格便宜, 並經藥物擬訂會議認定者 第三十五條本標準必要藥品及罕見疾病用藥支付價格訂定原則如下 : 一 罕見疾病用藥 不可替代必要藥品及必要藥品, 屬本標準已收載成分 劑型新品項之核價, 依本標準新品項之核價方式辦理 二 罕見疾病用藥屬新藥者, 得依下列方式核價 : ( 一 ) 依新藥之藥品支付價格訂定原則辦理 ( 二 ) 參考該品項或國外類似品之十國藥價 : 1. 每月申報金額小於等於五十萬元者, 以十國藥價中位數加百分之二十為上限 15
16 價 2. 每月申報金額大於五十萬元 小於等於一百萬元者, 以十國藥價中位數加百分之十為上限價 3. 每月申報金額大於一百萬元者, 以十國藥價中位數為上限價 ( 三 ) 參考成本價 : 1. 進口產品依其進口成本 ( 含運費 保險費 關稅 報關費用 特殊倉儲保管費 ) 加計百分之二十五管銷費用為上限價 2. 國內製造產品則依其製造成本 ( 不含研發費用 ) 加計百分之二十五管銷費用為上限價 3. 領有藥物許可證者, 得加計繳納藥害救濟徵收金比率及營業稅 適用前條之藥品, 因匯率或成本變動等因素, 致不敷成本, 廠商可提出調高健保價之建議, 由保險人提藥物擬訂會議討論, 其訂定方式得依前項第二款第二目及第三目之規定辦理 本標準已收載未領有藥物許可證之罕見疾病用藥, 應於三年內取得藥物許可證或主管機關認定其安全及療效無虞之證明文件, 未於期限內取得相關文件者, 取消給付, 但取得美國或歐盟上市許可者, 不在此限, 並得逐年調降其支付價格 不可替代必要藥品須與保險人簽訂合約, 並應確保供貨無虞, 若因不可抗力, 無法供貨者, 應提出替代方案, 並於六個月前向保險人提出 經簽訂供貨無虞合約之不可替代必要藥品及罕見疾病用藥, 若購買價仍高於健保支付價格, 保險醫事服務機構得依購買價格向保險人申請藥品費用, 但申報價格以健保支付價格之 1.3 倍為上限 第三十六條第一級及第二級管制藥品或抗蛇毒血清, 不論由主管機關所屬機關自行製造 委託製造或依政府採購法招標購置者, 其藥品支付價格, 保險人得依主管機關備查後之價格公告實施, 其因成本變動而須調整藥價時亦同 第三十七條特約醫事服務機構及藥品許可證之持有藥商可提出或由保險人公開徵求藥品論質計酬或發展實證醫學給付試辦計畫, 並經藥物擬訂會議審議後, 報請主管機關核定後施行 第三十八條十國藥價計算方式如下 : 一 十國藥價係指英國 德國 日本 瑞士 美國 比利時 澳洲 法國 瑞典 加拿大等十國藥價並加上匯率予以換算得之 二 依新藥或新品項受理日當季保險人公告之匯率計算 三 若具有兩種以上包裝者, 以單價最低者為計算基準 第三十九條藥品規格量換算法如下 : 一 以高規格藥價換算低規格之藥價 : 高規格藥價乘以 低規格品項規格量 ( 總含量 ) 除以高規格品項規格量 ( 總含量 ) 除以 0.9 二 以低規格藥價換算高規格之藥價 : 低規格藥價乘以 高規格品項規格量 ( 總含量 ) 除以低規格品項規格量 ( 總含量 ) 乘以 0.9 第四十條核算價格小數點之處理方式如下 : 16
17 一 核算價小於五元者, 取小數點後兩位, 第三位 ( 含 ) 以後無條件捨去 二 核算價大於或等於五元且小於五十元者, 取小數點後一位, 第二位 ( 含 ) 以後無條件捨去 三 核算價大於或等於五十元者, 取至整數, 小數點以後無條件捨去 第三章價量協議第四十一條列入價量協議之條件如下 : 一 新藥案件 : 廠商提供之財務預估資料, 預估於給付後之五年間, 有任一年之藥費支出高於新臺幣二億元者 二 擴增給付範圍案件 : 廠商提供之財務預估資料, 預估於擴增給付範圍後之五年間, 有任一年擴增部分之藥費支出高於新臺幣一億元者 三 未達上述二項條件之藥品, 於納入給付或擴增給付範圍後之五年間, 有任一年之實際藥費支出較原預估高出百分之五十以上, 且總金額高於新臺幣一億元 ( 新藥案件 ) 或新臺幣五仟萬元 ( 擴增給付範圍案件 ) 者 第四十二條價量協議期限如下 : 一 原則上為四年, 必要時得縮短或延長 二 以藥價或擴增給付範圍生效日為價量協議起日, 每十二個月為一個觀察年 第四十三條中止價量協議之條件, 須符合下列其中一項條件 : 一 協議期限屆滿 二 取消健保給付 三 協議期限內已另收載二種 ( 含 ) 以上同成分不同廠牌藥品 第四十四條價量協議方案得視個案情況擇一或多項併行處理 : 一 檢討價格方案:擴增給付範圍案件, 下列二項可併行處理 : ( 一 ) 以十國藥價檢討 1. 調整原則 (1) 健保支付價大於等於十國藥價中位價時, 調整至十國藥價中位價 (2) 健保支付價介於十國藥價中位價與十國藥價最低價時, 調整至十國藥價最低價 (3) 健保支付價小於十國最低價, 維持健保支付價 2. 調整時以保險人當季公告之匯率為換算基礎 ( 二 ) 以擴增額度檢討之調整比例公式, 為給付範圍擴增部分所預估增加之費用 (P) 與原給付範圍之費用 (B) 加上擴增範圍之比值乘上分攤比例值 (R 值 )[P (P+B) R] 二 還款方案 : 下列方式擇一執行 : ( 一 ) 設定各觀察年費用限量額度, 倘健保特約醫事服務機構申報之醫令金額超過限量額度, 則廠商償還一定比例金額予保險人 ( 二 ) 廠商於各觀察年償還健保特約醫事服務機構申報醫令金額之一定比例金額予保險人, 償還比例不設上限 三 降價方案 : 下列方式擇一執行 : 17
18 ( 一 ) 設定各觀察年費用限量額度, 倘健保特約醫事服務機構申報之醫令金額超過限量額度, 則調降健保支付價 ( 二 ) 於各觀察年調降一定比例之健保支付價, 調降比例不設上限 四 協議分擔方案 : 同成分不同廠牌或同藥理分類藥品設定共同分攤之還款方案或降價方案 採還款方案時, 依各藥品費用申報之比例分攤各廠商償還之金額 ; 採降價方案時, 則各藥品之價格調整比例一致 第四十五條限量額度之換算方式, 依廠商提供之財務預估資料 ( 適用人數乘以預估年使用量 ), 以暫予收載之健保支付價換算, 作為限量額度設定基準 第四十六條符合第四十一條第一項第三款之案件, 即廠商於提出建議案時, 預估藥費未達列入價量協議之藥品, 於納入給付或擴增給付範圍後之五年間, 任一年 ( 一月一日至十二月三十一日 ) 之實際藥費已達列入價量協議之條件時, 保險人將於次一年之三月三十一日前通知廠商進行價量協議 倘廠商未於保險人通知進行價量協議之該年五月三十一日完成價量協議, 則自該年十月一日起, 健保支付價以原藥價之 0.9 倍重新核價生效 ; 若於次一年五月底仍無法完成價量協議, 則再調降藥價百分之十, 並依此原則逐年調降藥價百分之十, 直至完成價量協議或已連續五年調降藥價 第三編特殊材料第一章健保特殊材料收載原則第四十七條可建議納入本標準支付之特殊材料品項如下 : 一 屬於本標準特殊材料所收載之類別 二 屬新功能類別之特殊材料, 經藥物擬訂會議評估可收載者 第四十八條全民健康保險不予支付之特殊材料如下 : 一 經保險人認定非屬醫療所必須, 或缺乏經濟效益者 二 不符醫療器材許可證及本標準所訂適應症者 三 未納入全民健康保險醫療服務給付項目及支付標準之診療項目所使用之醫療器材 四 本法第五十一條所訂之材料 : 義齒 義眼 眼鏡 助聽器 輪椅 拐杖及其他非具積極治療性之裝具 第四十九條販售之特殊材料, 其製造產地應與原醫療器材許可證相符, 經查證不符者, 該品項不列入健保給付範圍, 一年之內不得建議收載新品項 第五十條本標準已收載之特殊材料品項, 如連續三年 ( 含 ) 無醫令申報量, 且有替代性品項可供病人使用者, 該品項不予列入本標準 但如有特殊情形, 藥物許可證之持有廠商或保險醫事服務機構得向保險人提出說明, 經提藥物擬訂會議審議同意後, 得保留二年, 並以一次為限 第五十一條經保險人收載之特殊材料, 廠商有供貨給保險醫事服務機構之義務 如欲停止供貨一個月以上者, 應於二個月前向保險人提出說明 未提出說明者, 按下列方式處理 : 一 將未供貨之品項不列入健保給付範圍 18
19 二 三年內, 該醫療器材商不得建議收載新品項核價 第二章健保特殊材料支付點數訂定原則第五十二條無同功能類別之特殊材料, 經由藥物擬訂會議擬訂時, 參考下列因素核算支付點數 : 一 新研發品項之功能 效用 效果 二 功能相近之既有特殊材料支付點數 三 其他國家之市場及保險支付價格 四 於保險醫療上之經濟效益分析 五 預估之全年使用量 ( 自開始販售起算之第一年至第三年 ) 六 前述點數生效後, 保險人得視實際市場銷售量再評估其支付價格 第五十二條之一建議收載納入本標準之新功能類別特殊材料, 其分類如下 : 一 創新功能特殊材料 : 醫療器材許可證之持有廠商須提出與現行最佳同功能或類似功能類別特殊材料之臨床試驗文獻比較證據, 顯示臨床功能或療效有明顯改善之突破創新特殊材料 ; 該特殊材料為現有治療之第一個建議收載特殊材料, 且無現有最佳特殊材料可供比較者, 得以該疾病現行標準治療方法, 包括外科手術 支持性療法等, 作為療效比較之對象 二 功能改善特殊材料 : 與現行最佳同功能或類似功能類別特殊材料比較, 顯示具有臨床價值之功能改善之特殊材料 第五十二條之二新功能類別特殊材料支付點數之訂定原則如下 : 一 創新功能特殊材料, 得自下列方法擇一訂定 : ( 一 ) 原產國特材價格 ( 二 ) 國際價格中位數 ( 三 ) 公立醫院依政府採購法採購決標價格之中位數, 除以收載時最近四季結算之醫院總額部門浮動點值之平均值 ( 四 ) 各層級醫療院所收取自費價格之中位數 ( 五 ) 依成本計算 廠商須切結所提送之成本資料無誤, 且須經保險人邀集成本會計 財務及醫療專家審議 ( 六 ) 廠商之建議點數低於前五目訂定之點數者, 得採該建議點數 二 功能改善特殊材料, 得自下列方法擇一訂定 : ( 一 ) 國際價格最低價 ( 二 ) 國際價格比例法 ( 三 ) 公立醫院依政府採購法採購決標價格之中位數 平均價或最低價, 除以收載時最近四季結算之醫院總額部門浮動點值之平均值 ( 四 ) 各層級醫療院所收取自費價格之中位數 平均價或最低價 ( 五 ) 療程費用比例法 ( 六 ) 既有類似功能類別特殊材料之支付點數 ( 七 ) 既有功能類別特殊材料有無附加功能之比例換算 ( 八 ) 廠商之建議點數低於前七目訂定之點數者, 得採該建議點數 19
20 三 依療程費用比例法 既有類似功能類別特殊材料之支付點數核價者, 得考慮以下因素, 並與本標準已收載之既有類似功能類別特殊材料比較, 依下列方式加算 : ( 一 ) 更具臨床有效性, 最高加算百分之十五 ( 二 ) 對病人或醫療從業人員更具安全性, 最高加算百分之十五 ( 三 ) 可改善疾病或外傷的治療方法, 最高加算百分之十五 ( 四 ) 能降低對病人的侵襲性, 最高加算百分之十五 ( 五 ) 能明顯減少醫療或藥品費用支出, 按比例加算, 最高加算百分之十五 ( 六 ) 利於兒童之使用及操作者, 最高加算百分之十五 ( 七 ) 用於罕見疾病病人或相較於既有類似功能類別特殊材料, 推算使用對象病人人數較少者, 最高加算百分之十五 經藥物擬訂會議同意依前項第一款第三目 第四目, 或第二款第三目 第四目訂定支付點數後, 納入本標準 如廠商對功能分類或支付點數有不同意見者, 得自保險人通知日起三十日內提出 建議收載二項以上同功能類別但不同規格 ( 指體積 面積 長度 數量 ) 之特殊材料品項者, 依第一項訂定方法計算常用規格品項之支付點數後, 其餘品項得依規格比例換算之, 並得按一定比例折算或加成 第五十二條之三前條各層級醫療院所收取自費價格 國際價格比例法及療程費用比例法之執行方式如下 : 一 各層級醫療院所收取自費價格 : 蒐集該新建議品項於各層級醫療院所之收費價格, 應至少取得五筆資料 二 國際價格比例法 ( 一 ) 蒐集該新建議品項於韓國 日本 美國 澳洲等四國及其他具官方公開網站可供查詢的國家之價格及類似品項之價格, 並加上該建議案受理日當季保險人公告之匯率予以換算之 ( 二 ) 依新建議品項與類似品項之比值, 乘以類似品項之健保支付點數得之 ( 三 ) 有多國數值者, 取其平均數 三 療程費用比例法 : 以使用本標準已收載之類似品項之支付點數計算一個療程, 或一定期間使用或相同規格量之特殊材料點數, 換算新建議品項之支付點數 第五十三條具有同功能類別之特殊材料, 依同功能類別品項之最低支付點數核價 第五十三條之一核算支付點數小數點之處理方式如下 : 一 支付點數小於一百點者, 取小數點後一位, 第二位 ( 含 ) 以後, 無條件捨去 二 支付點數大於或等於一百點者, 取至整數, 小數點以後, 無條件捨去 第三章特殊材料支付點數之調整第五十三條之二必要或不可替代之特殊材料, 因成本變動等因素致不敷成本, 且屬相同功能類別者, 亦無廠商可依現行健保支付點數供應時, 該醫療器材許可證之持有廠商得提出該特殊材料調高健保支付點數之建議, 由保險人提藥物擬訂會議討論 前項特殊材料支付點數之訂定原則如下, 得擇一訂定..一 參考廠商進口或製造成本價 20
21 二 參考醫事服務機構購買價 三 同功能類別特殊材料有多家廠商可供應, 採其中建議價最低者 前項價格之訂定, 得考量合理因素加算, 最高加算百分之十 第五十四條保險人為建立公開 合理 透明之特殊材料點數調整制度, 應實施特殊材料市場實際交易價格調查 第五十五條特殊材料支付點數調整之目標如下 : 一 逐步縮小特殊材料各廠牌同類品項間之價差 二 逐步調整特殊材料支付點數, 使更接近特殊材料市場實際之加權平均銷售價格 第五十六條逐步縮小特殊材料同類品項間價差之方法如下 : 一 同功能同類品項, 訂定統一支付點數 二 支付點數高於同功能同類特殊材料支付點數中位數一定倍數之品項, 予以調整支付點數 第五十七條縮小特殊材料支付點數與市場銷售價格差異之方法, 指參考特殊材料市場實際交易價格調查資料, 調整特殊材料支付點數, 使其更接近特殊材料之市場銷售價格 第五十八條特殊材料市場實際交易價格調查之方法如下 : 一 調查對象 : ( 一 ) 直接銷售給本保險特約醫事服務機構之所有特殊材料供應商 ( 二 ) 有採購調查品項之特約醫事服務機構 二 調查品項 : 由保險人公告 ( 一 ) 本標準支付特殊材料品項以四年為一週期, 循序辦理 ( 二 ) 部分給付項目及新功能類別品項, 每二年調查一次 ( 三 ) 特殊材料申報點數成長快速, 或市場價格明顯扭曲者, 得列入機動調查 三 調查內容 : 廠商及醫療院所之特殊材料銷售及購買之價量資料 四 價量調查時程表 : 每年一月公布調查品項及調整後新點數生效實施日期 五 資料申報方式 : 採網路連線申報並填寫確認書 第五十九條所稱不實申報係指特殊材料申報資料有下列情事之一者 : 一 未申報贈品特殊材料量或交易金額未扣除折讓者 二 僅申報部分醫事服務機構交易資料者 三 其他足以影響調查結果正確性或完整性之情節 第六十條廠商及本保險醫事服務機構應配合特殊材料市場實際交易價格調查, 據實申報, 不申報或申報不實者, 以下列方式處理 : 一 廠商部分, 該品項不列入健保給付範圍, 一年內不得建議收載新品項 二 保險醫事服務機構部分, 以其所申報同類品項 ( 特材代碼前五碼 ) 之五折價格支付, 並追溯一年 第六十一條利用特殊材料市場實際交易價格調整特殊材料支付點數之處理原則如下 : 一 核價類別 : 係依功能來分類 二 各核價類別特殊材料市場實際加權平均價格 (GWAP) 之核算, 依下列原則辦理 : 21
22 ( 一 ) 資料採計期間 : 依公告價量調查之申報資料期間為調整計算基礎 ( 二 ) 以公告期間同核價類別所有品項特殊材料廠商申報之價量調查資料做為 GWAP 計算之基礎為原則 廠商如未申報價量, 則逕按特約醫事服務機構申報價量計算 ( 三 ) 對於同時無醫院及廠商申報之核價類別, 則不列入健保給付範圍 ( 四 ) 部分給付品項, 其市場加權平均價格如低於或接近現行收載類似功能品項時, 則可研議收載 ( 五 ) 對於會影響診療服務之特殊核價類別之特殊材料, 其年使用量少或無其他替代品之必要核價類別品項, 經價量調查之 GWAP 高於醫療費用申報同核價類別加權平均支付價格 ( 或個別支付價格 ) 者, 得提藥物擬訂會議擬訂後, 重新核價 三 特殊材料支付點數之調整 : ( 一 ) 調整後之新特殊材料點數, 依 相同核價類別特殊材料市場實際加權平均價格 加計一定百分比後調整, 且必須小於等於醫療費用申報同核價類別加權平均支付點數 Pnew = GWAP (1+ A),Pnew Pold Pnew: 新特殊材料點數 GWAP: 相同核價類別特殊材料市場實際加權平均價格 Pold: 同核價類別特殊材料加權平均支付點數 ( 指最近完整一年之醫療費用申報資料 ) A:X % ( 二 ) 舊核價類別調整後點數應不高於新核價類別調整後點數 ( 三 ) 調整後之特殊材料點數, 依核價類別之區隔, 次一等級之類別調整後點數不得高於較高等級類別之點數 第三章之一價量協議第六十一條之一本標準新收載之新功能類別特殊材料, 保險人得於收載前, 依廠商提供之財務預估年使用量及納入給付後三年間之費用支出, 與廠商訂定價量協議 本標準新功能類別新收載之第一件特殊材料, 依下列條件列為價量協議之品項 : 一 依廠商提供之財務預估年使用量, 並以暫予收載之健保支付點數換算, 於給付後之三年間, 有任一年 ( 一月一日至十二月三十一日 ) 之費用支出高於新臺幣三千萬元者 二 收載時之預估費用未達前款條件, 於納入給付後之三年間, 任一年 ( 一月一日至十二月三十一日 ) 之費用支出已達新臺幣三千萬元者 同屬價量協議類別之新收載同功能類別特殊材料, 於前項價量協議期間, 併同辦理 第六十一條之二保險人得參考廠商提供之三年販售量, 依同功能類別不分規格 不分廠牌特殊材料品項之合計銷售量, 分二階段訂定協議內容, 進行支付價格調整 : 一 合計銷售量達第一階段數量者 : 依原支付點數百分之九十五計算 22
23 二 合計銷售量達第二階段數量者 : 依原支付點數百分之九十計算 三 前二款折算比例, 保險人得視情況調整 為使雙方有所依據, 保險人與廠商得簽訂價量協議書 協議完成後, 支付價格始得生效 價量協議之品項仍屬保險人特殊材料價量調查及調價作業之範圍 第六十一條之三本章價量協議之期限如下 : 一 原則上為四年, 必要時得縮短或延長 二 以第一件收載之特殊材料支付點數生效日為價量協議起日, 並以該生效日之次年一月一日起算, 每十二個月為一個觀察年 三 同屬價量協議類別之新收載同功能類別特殊材料, 與該類別第一件收載品項之價量協議期限一致 第六十一條之四符合下列情形之一者, 保險人得中止價量協議 : 一 已屆該功能類別協議之最後段折扣數 二 依價量調查調整之支付點數已低於價量協議最後段應調降支付點數 三 取消健保給付 第四編事前審查第六十二條對於高危險 昂貴或易浮濫使用之特殊材料及藥品, 保險人應依本標準規定辦理事前審查 保險醫事服務機構應依前項規定申請事前審查 第六十三條保險醫事服務機構向保險人申請事前審查時, 應檢附下列文件 : 一 事前審查申請書 二 足供審查判斷之病歷及相關資料 三 前條第一項應事前審查項目規定之必備文件資料 前項第一款事前審查申請書如附件一 第六十四條保險人應於收到保險醫事服務機構送達事前審查申請文件起二週內完成核定, 逾期未核定者, 視同完成事前審查 但資料不全經保險人通知補件者, 不在此限 第六十五條保險醫事服務機構如因事出緊急, 得以書面說明電傳保險人報備後, 先行處理治療, 並立即備齊應附文件補件審查 第六十六條依規定應事前審查項目, 保險醫事服務機構未於事前提出申請或報備, 或未經保險人核定即施予者, 得依程序審查不支付費用 事前審查案件, 申請或報備後未及經審查回復即因急迫需要而施行者, 應依專業審查核定結果辦理 第五編藥品支付價格之調整第六十七條藥品支付價格調整目標如下 : 一 逐步縮小智慧財產權或品質較無爭議之同成分 同含量 同規格 同劑型藥品之價差 二 逐步調整藥品支付價格, 使更接近藥品市場實際之加權平均銷售價格 23
24 第六十八條縮小同成分 同含量 同規格 同劑型之不同廠牌藥品價差之方法如下 : 一 針對智慧財產權較無爭議之同成分 同含量 同規格 同劑型藥品, 逐步以分類分組 (Grouping) 方式調整健保支付價格 ( 一 ) 適用於分類分組調整支付價格藥品之條件 : 1. 智慧財產權較無爭議或年代久遠之藥品 2. 品質較無爭議之同成分規格藥品 ( 二 ) 上述品項 分類分組及價格調整之方法由保險人參考醫 藥相關專家學者意見後訂定之 二 對支付價格高於同成分 含量 劑型 規格藥品支付價中位數一定倍數之藥品, 予以調整支付價格 第六十九條藥品品質宜對實施製劑之原料藥具備 DMF 符合 PIC/S GMP 及便民藥品包裝等項目, 予以提升品質誘因 第七十條縮小藥品支付價格與市場銷售價格差異之方法如下 : 一 參考 藥品市場實際交易價格調查, 調整藥品支付價格, 使其更接近藥品之市場銷售價格 二 專利逾期採即時調整與及時反映市場價格 三 藥價調查及調整應集中於專利逾期後之中 短期 第七十一條藥品市場實際交易價格調查之方法如下 : 一 甲調查 ( 一 ) 調查品項 : 本標準支付藥品品項 ( 二 ) 調查對象 : 直接銷售給特約醫事服務機構之所有藥品供應商 ( 三 ) 調查內容 : 銷售保險特約醫事服務機構之藥品摘要資料, 其內容包括 : 藥品代碼 藥品名稱 藥商代號 藥商名稱 申報期間 聯絡電話 傳真電話 藥商統一編號 聯絡地址 院所代號 藥品銷售量( 應包含贈品量 藥品耗損, 並扣除退貨數量 ) 銷售總金額( 應包含營業稅, 並扣除折讓金額及退貨金額 ) 銷售量合計及金額合計等 ( 四 ) 調查時程 : 按季申報, 且於每季結束後第二個月二十日前, 申報前一季各月份之藥品銷售資料 二 乙調查 ( 一 ) 調查品項 : 由保險人公告 ( 二 ) 調查對象 : 以醫療院所為調查對象, 其中地區醫院以上全面普查, 必要時, 基層院所抽樣 1/10 調查 ( 三 ) 調查內容 : 調查對象在保險人指定期間之所有藥品銷售明細資料 包括藥商代號 藥商名稱 藥商統一編號 聯絡電話 許可執照字號 聯絡地址 申報資料年月 傳真電話 發票日期 院所代號 藥品代碼 包裝規格 ( 單位 ) 藥品銷售量( 應包含贈品量 藥品耗損, 並扣除退貨數量 ) 售藥總金額 ( 應包含營業稅, 並扣除折讓金額及退貨金額 ) 發票號碼 發票註記等 ( 四 ) 調查時程 : 在保險人公告之申報期限內申報 24
25 三 丙調查 ( 一 ) 調查品項 : 價量異常之品項, 如市場實際交易價格加權平均值高於健保支付價格之藥品 ( 二 ) 調查方式 : 由保險人前往藥品供應商與特約院所實地訪查 第七十二條機動性藥品市場實際交易價格調查 ( 以下簡稱機動性調查 ) 如下 : 一 針對外界檢舉有明確事證案件, 且符合下列三項條件時, 保險人應進行機動性調查 : ( 一 ) 藥商或藥局藥品販售價格低於健保支付價之百分之六十 ( 二 ) 同分組藥品有三個以上 ( 三 ) 同分組最近一年特約醫事服務機構申報總計金額大於新臺幣五千萬元以上 二 機動性調查之方式.. ( 一 ) 保險人得抽取一定比例特約醫事服務機構之藥品採購資料, 進行價格調整 ( 二 ) 保險人應將被檢舉品項之同分組品項併同調查及處理 三 利用機動性調查調整藥品支付價格之處理原則, 若被檢舉之藥品或併同調查之藥品販售價格, 同品質條件之藥品有低於現有健保支付價格之百分之五十者, 依調查醫事服務機構之最低交易價格計算調整健保支付價格, 公式如下 : Pnew =2 Pmin Pnew: 調整後新藥價 Pmin: 市場交易最低價第七十三條所稱不實申報係指申報資料有下列情事之一, 致墊高市場平均交易價格者 : 一 未申報贈藥量或交易金額未扣除折讓者 二 僅申報部分院所交易資料者 三 其他足以影響調查結果正確性或完整性之情節 第七十四條未申報或不實申報之藥品, 經掛號通知藥品許可證持有藥商及交貨廠商或醫療院所後, 自發文日期三週內未補齊正確資料或提出合理說明者, 以下列方式處理 : 一 藥商 ( 一 ) 未申報或不實申報品項無同成分 同劑型其他產品可供替代, 致影響民眾用藥權益者 : 以該品項之加權平均價格之 0.8 倍調整且不得高於現行健保支付價格 0.8 倍 ( 二 ) 未申報之品項, 不列入健保給付範圍一年 ( 含標準包裝規格 ), 生效日自發文日起次次一季一日生效 ( 三 ) 不實申報品項有同成分 同劑型其他產品可供替代者 : 1. 不實申報不影響藥價調整結果者 : 調降藥品支付價格 ( 以同分組最低價之 0.8 倍調整且不得高於現行健保支付價格 0.8 倍 ) 25
26 2. 不實申報會影響藥價調整結果者, 按下列方式處理 : (1) 不實申報者為下列情形之一者 : 該品項不列入健保給付範圍一年 ( 含標準包裝規格 ) 許可證持有藥商 許可證持有藥商相關子公司 經銷商為不實申報係許可證持有藥商授意者 (2) 不實申報者係為經銷商所為 : 不實申報數量占率 百分之十 : 該品項不列入健保給付範圍一年 ( 含標準包裝規格 ) 不實申報數量占率 < 百分之十 : 影響藥價調整幅度 百分之六 : 該品項不列入健保給付範圍一年 ( 含標準包裝規格 ) 影響藥價調整幅度 < 百分之六 : 由許可證持有藥商選擇下列任一種方式辦理 : A. 調降藥品支付價格 ( 以同分組最低價之 0.8 倍調整且不得高於現行健保支付價格 0.8 倍 ), 並返還因不實申報而增加健保藥費支出金額 ( 金額 = 前後價差 * 前一次藥價調整後至調降藥價生效日之使用量 ) B. 該品項不列入健保給付範圍一年 ( 含標準包裝規格 ) (3) 若有多家經銷商不實申報同一品項時, 不實申報占率為各不實申報經銷商之總和 (4) 上述 不實申報數量占率 計算公式 : 該不實申報品項該經銷商申報銷售予所有醫事服務機構之數量 該品項所有藥商之申報數量 百分之百 (5) 上述影響 藥價調整幅度 計算公式 :( 原調整後價格 - 更正後調整價格 ) 原健保支付價格 百分之百 ; 或 ( 原同分組加權平均銷售價格 - 更正後同分組加權平均銷售價格 ) 原同分組加權平均銷售價格 百分之百 3. 不實申報不列入健保給付範圍一年 ( 含標準包裝規格 ) 之品項, 生效日自發文日起次次一季一日生效 二 醫療院所 ( 一 ) 不實申報品項之同藥理分類藥品均以同成分 含量 劑型藥品之最低價給付 ( 自核定生效日期回溯一年 ) ( 二 ) 依本保險特約醫事服務機構合約辦理 第七十五條利用市場實際交易價格調整藥品支付價格之處理原則如下 : 一 調整時程 : 主成分於專利期內 專利權逾期五年以上及無專利權之藥品, 每兩年調整一次 二 藥品分組分類 ( 一 ) 同核價成分 同核價劑型 同規格量藥品歸為同分組 ( 二 ) 同分組藥品依專利與否分為二大類 : 1. 專利期內藥品 26
27 2. 逾 ( 無 ) 專利藥品, 再分為下列二類 : 第一類包含原開發廠藥品 符合 PIC/S GMP 之藥品 BA/BE 學名藥品 BE 學名藥品之對照品 ; 第二類為非屬第一類之一般學名藥品 三 藥品支付價格之調整 : ( 一 ) 計算調整期間 : 自最近一次支付價格調整生效日起至調查截止日止 ( 二 ) 專利期內藥品調整方式 : 1. 個別藥品之市場加權平均價格大於等於調整前支付價格乘以 0.85 者, 不予調整 ; 個別藥品之市場加權平均價格小於調整前支付價格乘以 0.85 者, 調整其支付價格為 調整前支付價格 乘以 0.15 加其 市場加權平均價格 藥價調整公式 : (1)WAP (1-R) Pold: 不予調整 (2)WAP < (1- R) Pold: 依下列公式調整 Pnew=WAP+ Pold R Pnew: 新藥價 WAP: 藥價調查申報之個別藥品市場加權平均價格 Pold: 調整前支付價格 R:15 % 2. 設定調整下限價 : 錠劑或膠囊劑最低調降至 1 元 ; 口服液劑最低調降至 25 元 ; 100~500mL( 不含 ) 輸注液最低調降至 22 元 ;500mL( 含 ) 以上大型輸注液最低調降至 25 元 ; 其他注射劑最低調降至 15 元 以上不含健保代碼末二碼為 99 者 3. 設定最大調降幅度為百分之四十 4. 設定同分組最低價 : 經上述公式調整後, 同分組品項之最低價不得低於同分組品項最高價之 0.7 倍 ( 不含 ); 低於最高價 0.7 倍 ( 不含 ) 之品項, 其健保支付價格依最高價之 0.7 倍調整, 惟調整後之新藥價不高於調整前支付價格 5. 新收載之品項 : 指收載生效日期距調查期限六個月以內且符合下列要件之品項 其價格調整於次一年依上述調整公式計算之 (1) 新收載之新藥且無銷售紀錄之藥品品項 (2) 經主管機關核准通過生體相等性試驗 (BE) 重新建議核價之品項 ( 三 ) 逾 ( 無 ) 專利期藥品調整方式 : 1. 設定暫調價格 : (1) 依其 同分組分類藥品之加權平均價格 ( 以下稱 GWAP) 為目標值 第二類藥品之目標值應以第一類藥品之目標值為上限 (2) 個別藥品市場加權平均價格 (WAP) 高於或等於目標值之 1.05 倍者, 以目標值之 1.05 倍為暫調價格 ; 個別藥品 WAP 低於目標值之 1.05 倍者, 以 WAP 為暫調價格, 並以目標值之 0.9 倍為下限 但暫調價格不得高於調整前支付價格 2. 設定最大調降幅度 : 暫調價格與調整前支付價格比較, 二者差距之百分比, 稱為調幅 ; 依調幅範圍, 設定最大調降幅度如下 : (1) 調幅於 15%( 含 ) 以下 : 不予調整 27
28 (2) 調幅介於 15%( 不含 ) 至 20%( 含 ): 最大調降幅度 2.5% (3) 調幅介於 20%( 不含 ) 至 25%( 含 ): 最大調降幅度 7.5% (4) 調幅介於 25%( 不含 ) 至 30%( 含 ): 最大調降幅度 12.5% (5) 調幅介於 30%( 不含 ) 至 35%( 含 ): 最大調降幅度 17.5% (6) 調幅介於 35%( 不含 ) 至 40%( 含 ): 最大調降幅度 22.5% (7) 調幅介於 40%( 不含 ) 至 45%( 含 ): 最大調降幅度 27.5% (8) 調幅介於 45%( 不含 ) 至 50%( 含 ): 最大調降幅度 32.5% (9) 調幅介於 50%( 不含 ) 至 55%( 含 ): 最大調降幅度 37.5% (10) 調幅介於 55%( 不含 ) 以上 : 最大調降幅度 40% 3. 以調幅減百分之十五及最大調降幅度取低者, 予以核算調整後支付價格, 並以調整前支付價格為上限 4. 設定調整下限價 : 錠劑或膠囊劑最低調降至 1 元 ; 口服液劑最低調降至 25 元 ; 100~500mL( 不含 ) 輸注液最低調降至 22 元 ;500mL( 含 ) 以上大型輸注液最低調降至 25 元 ; 其他注射劑最低調降至 15 元 以上不含健保代碼末二碼為 99 者 ( 四 ) 專利期內藥品無 WAP, 或逾 ( 無 ) 專利期藥品無 GWAP 之調整 : 1. 單方及含二或三個主成分之複方 : 依同核價成分藥品之平均調幅調整, 若無同核價成分藥品之平均調幅, 則以同藥理分類 (ATC 前五碼相同 ) 藥品之平均調幅調整, 若無同藥理分類藥品之平均調幅, 則以單方及含二或三個主成分之複方之平均調幅調整 2. 含四個主成分以上之複方 : 依含四個主成分以上之複方之平均調幅調整 3. 設定調整下限價 : 錠劑或膠囊劑最低調降至 1 元 ; 口服液劑最低調降至 25 元 ; 100~500mL( 不含 ) 輸注液最低調降至 22 元 ;500mL( 含 ) 以上大型輸注液最低調降至 25 元 ; 其他注射劑最低調降至 15 元 以上不含健保代碼末二碼為 99 者 ( 五 ) 同分組 同廠牌品項之調整 : 1. 專利期內藥品 : 同分組 同廠牌及同品質條件藥品有二個品項 ( 含 ) 以上者, 以最低價調整 2. 逾 ( 無 ) 專利期藥品 : 同分組 同廠牌 同分類及同品質條件藥品有二個品項 ( 含 ) 以上者, 以最低價調整 ( 六 ) 藥價調整後, 同分組品項之最低價不得低於同分組品項最高價之 0.6 倍 ( 不含 ); 低於最高價 0.6 倍 ( 不含 ) 之品項, 其健保支付價格依最高價之 0.6 倍調整 ; 惟不得高於調整前支付價之二倍 ( 含 ), 本規定不適用指示用藥 ( 七 ) 調整後同廠牌之同成分 劑型藥品, 低規格量藥品支付價格不高於高規格量藥品支付價格 高低規格量品項之調整如下 : 1. 同成分劑型以各規格同分組之最近一年醫令申報量最高之規格量為常用規格量, 以該常用規格量之品項調整後藥價為基準價 2. 各廠牌同成分之錠劑及膠囊劑, 低規格量品項之藥價不高於該基準價, 高規格量品項之藥價不低於該基準價 3. 非屬錠劑及膠囊劑且屬同許可證之品項, 其低規格量品項之藥價不高於該基 28
29 準價, 高規格量品項之藥價不低於該基準價 4. 若無常用規格量者, 低規格量品項之藥價不高於高規格量品項之藥價 5. 同分組藥品經高低規格量品項之調整後, 其無銷售量之品項, 以同分組分類其他有銷售量品項之最高價為上限 ( 八 ) 經保險人核定屬標準包裝之口服錠劑 口服膠囊劑 ( 健保代碼末三碼為 1G0 ) 者, 以 1.5 元為最低價, 本規定不適用指示用藥 ( 九 ) 符合 PIC/S GMP 藥品之最低價 : 錠劑或膠囊劑為 1.5 元 ( 倘同時具標準包裝者為 2 元 ) 口服液劑為 25 元 100~500mL( 不含 ) 輸注液為 22 元 500mL( 含 ) 以上大型輸注液為 25 元 其他注射劑為 15 元 以上不適用於健保代碼末二碼為 99 者及指示用藥 ( 十 ) 供醫事服務機構申報屬大包裝品項之最小單位 ( 健保代碼末二碼為 99 者 ): 以同許可證各規格調整後之最小單位之單價最低者調整 ( 十一 ) 調整後之新藥價, 學名藥品之藥價, 不得高於原開發廠藥品之藥價, 標準包裝及符合 PIC/S GMP 之藥品不在此限 四 相關價格之核算原則如下 : ( 一 ) 加權平均價格之核算原則 : 藥價調查申報之個別藥品市場加權平均價格 ( 小數以下第五位四捨五入 ) ( 二 ) 同分組分類藥品之加權平均價格之核算原則 : 藥價調查申報之同分組分類市場加權平均價格 ( 小數以下第五位四捨五入 ) ( 三 ) 新藥價之核算原則 : 1. 小於 5 元者, 取小數點後兩位, 第三位 ( 含 ) 以後無條件捨去 2. 大於或等於 5 元且小於 50 元者, 取小數點後一位, 第二位 ( 含 ) 以後無條件捨去 3. 大於或等於 50 元者, 取至整數, 小數點以後無條件捨去 第七十六條必要藥品 罕見疾病用藥及其他經保險人公告之特殊品項, 由保險人與該項藥品廠商協商調整事宜 與保險人簽有供應無虞合約之不可替代必要藥品及罕見疾病用藥, 按下列方式調整價格 : 一 同類藥品, 即同成分 劑型 劑量, 具有相同品質條件者, 調整為相同價格 二 依實際市場交易價格調整, 配合一般藥品之例行調整時程, 每二年計算調整一次 : ( 一 ) 採計前前一年第四季至前一年第三季之甲調查資料 ( 二 ) 新收載之品項, 無同類藥品, 而生效未滿一年者, 不進行調整 有同類藥品者, 將生效後應申報之甲調查資料併同類既有品項調整 三 調整方式 : ( 一 )0.80 Pold GWAP 1.05 Pold: 不予調整 ( 二 )GWAP>1.05 Pold,Pnew=GWAP ( 並以 1.3 Pold 為上限 ) ( 三 )GWAP<0.80 Pold,Pnew=GWAP+0.20 Pold 29
30 Pnew: 調整後支付價格 Pold: 調整前支付價格 GWAP: 同成分 劑型 劑量, 具有相同品質條件之藥品, 以交易價量資料計算所得之加權平均價格四 前述健保支付價格之調整, 以初次收載之健保支付價之二倍為上限 第七十七條利用市場實際交易價格調整藥品支付價格之資料引用之條件, 經重新調整價格之品項, 其生效日期前之銷售量不予計算, 另自生效日期以後之銷售量, 若於公立醫院因合約問題無法調整售價者, 該資料得排除不列入計算, 並應檢附舉證文件資料影印本, 併同甲調查向保險人申報 第七十八條保險人得依本法第六十二條規定, 其支付之藥品費用超出全民健康保險會協定之藥品費用總額時, 依該超出之比例, 於下年度調整本標準 第六編附則第七十九條本標準之藥品給付品項暨支付標準表, 詳附件二 第八十條本標準之特殊材料給付品項暨支付標準表, 詳附件三 第八十一條本標準之中藥用藥品項表 ( 單方 ), 詳附件四 第八十二條本標準之中藥用藥品項表 ( 複方 ), 詳附件五 第八十三條本標準之藥品給付規定, 詳附件六 第八十四條本標準之特殊材料給付規定, 詳附件七 第八十五條本標準自中華民國一百零二年一月一日施行 本標準修正條文, 除第七十九條附件二至第八十四條附件七之施行日期由主管機關另定者外, 自發布日施行 30
Microsoft Word - w 附件-第6次調整原則.DOC
 全民健康保險第 6 次年度藥品支付價格調整原則 98.07.16 壹 藥品分類 一 專利期內藥品 ( 含監視中新藥 ) 二 逾 ( 無 ) 專利保護藥品 ( 不含監視中新藥 ) 貳 加權平均價格 (WAP) 之核算原則 藥價調查申報資料採用期間 : 以 96 年第 4 季至 97 年第 3 季甲調查資料為藥價調整計算基礎 參 藥價調整原則 附件 一 下列藥品, 不列入藥價調整, 由保險人依全民健康保險藥品支付價格調整作業要點辦理
全民健康保險第 6 次年度藥品支付價格調整原則 98.07.16 壹 藥品分類 一 專利期內藥品 ( 含監視中新藥 ) 二 逾 ( 無 ) 專利保護藥品 ( 不含監視中新藥 ) 貳 加權平均價格 (WAP) 之核算原則 藥價調查申報資料採用期間 : 以 96 年第 4 季至 97 年第 3 季甲調查資料為藥價調整計算基礎 參 藥價調整原則 附件 一 下列藥品, 不列入藥價調整, 由保險人依全民健康保險藥品支付價格調整作業要點辦理
稅之鼓勵措施 ( 修正條文第三十五條 ) 七 增訂抗蛇毒血清之支付價格, 比照第一級及第二級管制藥品之訂定方式 ( 修正條文第三十六條 ) 八 將現行特殊材料無申報數量取消給付之年限, 由一年延長為三年, 並明訂作業流程 ( 修正條文第五十條 ) 九 為維護民眾使用新特材之權益, 針對市場實際交易價
 全民健康保險藥物給付項目及支付標準部分條文修正總說明 全民健康保險藥價基準於八十八年三月三十日訂定發布, 並於一百零一年 十二月二十八日修正名稱為全民健康保險藥物給付項目及支付標準 ( 以下稱本 標準 ), 最近一次修正係於一百零四年七月三日發布 為使本標準規定之內容更能切合臨床醫療實際需求, 並兼顧民眾之醫療權 益, 經檢討後認為有修正之必要, 爰擬具本標準修正案, 藥品部分共計修正八 條 新增二條
全民健康保險藥物給付項目及支付標準部分條文修正總說明 全民健康保險藥價基準於八十八年三月三十日訂定發布, 並於一百零一年 十二月二十八日修正名稱為全民健康保險藥物給付項目及支付標準 ( 以下稱本 標準 ), 最近一次修正係於一百零四年七月三日發布 為使本標準規定之內容更能切合臨床醫療實際需求, 並兼顧民眾之醫療權 益, 經檢討後認為有修正之必要, 爰擬具本標準修正案, 藥品部分共計修正八 條 新增二條
中期 12 中期 % 報告期 報告 44 中期 報 年中期報告 中國鋁業股份有限公司
 2016 2016 6 30 6 2016 2016 www.hkex.com.hk www.chalco.com.cn 2 6 8 10 中期 12 中期 12 13 16 22 25 26 27 5% 28 29 29 報告期 29 30 31 31 31 32 35 35 36 38 報告 44 中期 報 46 1 2016 年中期報告 中國鋁業股份有限公司 1. ALUMINUM CORPORATION
2016 2016 6 30 6 2016 2016 www.hkex.com.hk www.chalco.com.cn 2 6 8 10 中期 12 中期 12 13 16 22 25 26 27 5% 28 29 29 報告期 29 30 31 31 31 32 35 35 36 38 報告 44 中期 報 46 1 2016 年中期報告 中國鋁業股份有限公司 1. ALUMINUM CORPORATION
( ) (1) (2) (3) (4) 2
 2007 11 29 1. ( ) 2. ( ) 3. 1 ( ) 1. 2. (1) (2) (3) (4) 2 1. (1) (2) 2. ( ) $20,000,000 X1 1 1 $3,000,000 X1 1 1 1,000,000 $12,000,000 $4,000,000 $5,000,000 $10 X1 1 1 $13 (1) ( ) $5,000,000 $8,000,000
2007 11 29 1. ( ) 2. ( ) 3. 1 ( ) 1. 2. (1) (2) (3) (4) 2 1. (1) (2) 2. ( ) $20,000,000 X1 1 1 $3,000,000 X1 1 1 1,000,000 $12,000,000 $4,000,000 $5,000,000 $10 X1 1 1 $13 (1) ( ) $5,000,000 $8,000,000
注入新能量明確新方向
 股份代號 598 Stock Code : 598 注入新能 量 明 確 新方 向 2015 Interim Report 2015 中 期 報 告 中期報告 R O F A Y NE W D T I L A T I V IR E C New Ti Interim Report on 2015 注入新能量明確新方向 2 3 4 5 7 9 10 38 49 50 公司資料 公司 公司 SINOTRANS
股份代號 598 Stock Code : 598 注入新能 量 明 確 新方 向 2015 Interim Report 2015 中 期 報 告 中期報告 R O F A Y NE W D T I L A T I V IR E C New Ti Interim Report on 2015 注入新能量明確新方向 2 3 4 5 7 9 10 38 49 50 公司資料 公司 公司 SINOTRANS
 2014 : 706 2 3 4 5 6 12 15 簡明綜合損益及其他全面收入報表 截至二零一四年六月三十日止六個月 二零一三年 3 3,796 4,738 3,796 4,738 4 1,983 1,837 (27,319) (26,934) (21,540) (20,359) 5 (64) (92) (21,604) (20,451) 6 159 196 期 7 (21,445) (20,255)
2014 : 706 2 3 4 5 6 12 15 簡明綜合損益及其他全面收入報表 截至二零一四年六月三十日止六個月 二零一三年 3 3,796 4,738 3,796 4,738 4 1,983 1,837 (27,319) (26,934) (21,540) (20,359) 5 (64) (92) (21,604) (20,451) 6 159 196 期 7 (21,445) (20,255)
(Microsoft Word - \244\345\245\3635)
 衛生福利部中央健康保險署公告 發布日期 :103.09.10 健保審字第 1030081502 號 主旨 : 公告暫予支付新增及異動 全民健康保險藥物給付項目及支付標準 之藥 物品項計 1,662 項 依據 : 全民健康保險法第 41 條 第 62 條第 1 項暨全民健康保險藥物給付項目及 支付標準 公告事項 : 全民健康保險藥品新收載品項明細表 及 全民健康保險藥品已收 載品項異動明細表 如附件
衛生福利部中央健康保險署公告 發布日期 :103.09.10 健保審字第 1030081502 號 主旨 : 公告暫予支付新增及異動 全民健康保險藥物給付項目及支付標準 之藥 物品項計 1,662 項 依據 : 全民健康保險法第 41 條 第 62 條第 1 項暨全民健康保險藥物給付項目及 支付標準 公告事項 : 全民健康保險藥品新收載品項明細表 及 全民健康保險藥品已收 載品項異動明細表 如附件
規格藥商項次健保代碼藥品名稱成分及含量量名稱 1 TPN TPN-A 1ML 南基醫院 2 TPN TPN-B 1ML 南基 醫院 3 TPN TPN-C 1ML 南基 醫院 全民健康保險藥品新收載品項明細表 原支付初核價初核說明價格 一 依
 規格藥商量名稱 1 TPN4227299 TPN-A 1ML 南基醫院 2 TPN4228299 TPN-B 1ML 南基 醫院 3 TPN4229299 TPN-C 1ML 南基 醫院 原支付初核價初核說明價格 -- 0.26 一 依下列原則取低者, 暫予支付每 ML 0.26 元 : ( 一 ) 依核價原則計算, 每 ML 為 0.26 元 (208+67+67)/1300=0.26 ; ( 二
規格藥商量名稱 1 TPN4227299 TPN-A 1ML 南基醫院 2 TPN4228299 TPN-B 1ML 南基 醫院 3 TPN4229299 TPN-C 1ML 南基 醫院 原支付初核價初核說明價格 -- 0.26 一 依下列原則取低者, 暫予支付每 ML 0.26 元 : ( 一 ) 依核價原則計算, 每 ML 為 0.26 元 (208+67+67)/1300=0.26 ; ( 二
全民健康保險新收載品項明細表 項次 健保代碼 藥品名稱 成分及含量 規格量 藥商名稱 1 TPN TPN A3(1464ML) 1 仁愛醫 療財團 法人大 里仁愛 醫院 原支付價初核價格初核說明 一 依全靜脈營養輸液核價原則計算, 暫予支付每 ML 0.65 元 : (
 項次 健保代碼 藥品名稱 成分及含量 規格量 藥商名稱 1 TPN4407299 TPN A3(1464ML) 1 仁愛醫 療財團 法人大 里仁愛 醫院 原支付價初核價格初核說明 -- 0.65 一 依全靜脈營養輸液核價原則計算, 暫予支付每 ML 0.65 元 : (67/400 400)+(67/400 400)+(154/200 400)+(220/10 10)+(64/4 4)+(221/250
項次 健保代碼 藥品名稱 成分及含量 規格量 藥商名稱 1 TPN4407299 TPN A3(1464ML) 1 仁愛醫 療財團 法人大 里仁愛 醫院 原支付價初核價格初核說明 -- 0.65 一 依全靜脈營養輸液核價原則計算, 暫予支付每 ML 0.65 元 : (67/400 400)+(67/400 400)+(154/200 400)+(220/10 10)+(64/4 4)+(221/250
項次健保代碼藥品名稱成分及含量 1 K NOVOMIX 30 FLEXPEN 2 K NOVORAPID FLEXPEN 3 K NOVOMIX 50 FLEXPEN 4 B PLETAAL OD TABLETS 50MG 5
 1 K000820266 NOVOMIX 30 FLEXPEN 2 K000823266 NOVORAPID FLEXPEN 3 K000908266 NOVOMIX 50 FLEXPEN 4 B025994100 PLETAAL OD TABLETS 50MG 5 B025993100 PLETAAL OD TABLETS 100MG INSULIN ASPART 100U/ML (UNIT/ML)
1 K000820266 NOVOMIX 30 FLEXPEN 2 K000823266 NOVORAPID FLEXPEN 3 K000908266 NOVOMIX 50 FLEXPEN 4 B025994100 PLETAAL OD TABLETS 50MG 5 B025993100 PLETAAL OD TABLETS 100MG INSULIN ASPART 100U/ML (UNIT/ML)
F A F G F H F F A F G F H doi : / NRD 1032 PK PK 攻防首部曲 在藥品查驗登記時, 必須檢附相關藥動學資料支持藥品的療效與安全性以備核准
 藥物在體內的 PK 攻防 36 藥物動力學 PharmacokineticsADME Absorption Z Disposition Distribution Elimination Metabolism D Excretion T C T C Z pharmacokinetics PK absorption distribution metabolism excretion ADME 2015
藥物在體內的 PK 攻防 36 藥物動力學 PharmacokineticsADME Absorption Z Disposition Distribution Elimination Metabolism D Excretion T C T C Z pharmacokinetics PK absorption distribution metabolism excretion ADME 2015
一 者 : ( 一 ) 限 由 醫 師 使 用 ( 二 ) 須 由 醫 師 處 方 使 用 ( 三 ) 由 醫 師 或 檢 驗 師 使 用 ( 四 ) 限 由 牙 醫 師 使 用 ( 五 ) 限 由 麻 醉 醫 師 使 用 ( 六 ) 限 由 眼 科 醫 師 使 用 ( 七 ) 限 由 醫 師 及
 全民健康保險藥物給付項目及支付標準 第一編 總則 第一條 全民健康保險藥物給付項目及支付標準(以下稱本標準)係依據全民健康保險 法(以下稱本法)第四十一條第二項訂定 原則上 每年檢討一次 第二條 全民健康保險支付及給付之藥物 以記載於本標準者為限 第三條 本標準所列特殊材料項目係指於相關診療項目收費外 可向保險人另行申報之 項目 本標準未列項目之支付價格已包含於全民健康保險醫療服務給付項目及支付標
全民健康保險藥物給付項目及支付標準 第一編 總則 第一條 全民健康保險藥物給付項目及支付標準(以下稱本標準)係依據全民健康保險 法(以下稱本法)第四十一條第二項訂定 原則上 每年檢討一次 第二條 全民健康保險支付及給付之藥物 以記載於本標準者為限 第三條 本標準所列特殊材料項目係指於相關診療項目收費外 可向保險人另行申報之 項目 本標準未列項目之支付價格已包含於全民健康保險醫療服務給付項目及支付標
公司
 (Incorporated in the Cayman Islands with limited liability) (於開曼群島註冊成立之有限公司) Stock Code : 00953 股份代號: 00953 年報 2014 ANNUAL REPORT 2014 Annual Report 2014 年 報 公司 2 3 4 14 24 28 38 40 41 43 44 46 99 1 Cricket
(Incorporated in the Cayman Islands with limited liability) (於開曼群島註冊成立之有限公司) Stock Code : 00953 股份代號: 00953 年報 2014 ANNUAL REPORT 2014 Annual Report 2014 年 報 公司 2 3 4 14 24 28 38 40 41 43 44 46 99 1 Cricket
投影片 1
 全民健康保險藥品費用分配比率 目標制 試辦方案之評估與檢討 暨藥價政策之問題研析 衛生福利部中央健康保險署 104 年 7 月 24 日 1 報告大綱 藥品費用分配比率目標制藥價調整原則 藥價政策之問題研析 2 歷次藥價調整減少藥費支出金額 調整次數 調整年度 調整金額 1 89 年 5 億元 2 90 年 46 億元 3 92 年 57 億元 4 93 年 0.68 億元 94 年 23.6 億元
全民健康保險藥品費用分配比率 目標制 試辦方案之評估與檢討 暨藥價政策之問題研析 衛生福利部中央健康保險署 104 年 7 月 24 日 1 報告大綱 藥品費用分配比率目標制藥價調整原則 藥價政策之問題研析 2 歷次藥價調整減少藥費支出金額 調整次數 調整年度 調整金額 1 89 年 5 億元 2 90 年 46 億元 3 92 年 57 億元 4 93 年 0.68 億元 94 年 23.6 億元
全民健康保險新收載品項異動明細表 項次健保代碼藥品名稱成分及含量規格量藥商名稱原支付價初核價格初核說明生效方式 / 日期 1 AC PROGESTERONE INJECTION 25MG "Y.Y." 2 AC AZAPRINE F.C. TABLETS
 項次健保代碼藥品名稱成分及含量規格量藥商名稱原支付價初核價格初核說明生效方式 / 日期 1 AC59840209 PROGESTERONE INJECTION 25G "Y.Y." 2 AC59675100 AZAPRINE F.C. TABLETS 50G 3 AC59771100 EXNORTAN F.C. TABLETS 5/160G PROGESTERONE 25.000G/L 1L 應元
項次健保代碼藥品名稱成分及含量規格量藥商名稱原支付價初核價格初核說明生效方式 / 日期 1 AC59840209 PROGESTERONE INJECTION 25G "Y.Y." 2 AC59675100 AZAPRINE F.C. TABLETS 50G 3 AC59771100 EXNORTAN F.C. TABLETS 5/160G PROGESTERONE 25.000G/L 1L 應元
全民健康保險藥品新收載品項明細表 項次健保代碼藥品名稱成分及含量 1 A A A A A TOPSYM CREAM (FLUOCINONID E) TOPSYM OINTMENT (FLUOCI
 1 A018063338 2 A018088338 3 A023592100 4 A045183412 5 A048083265 TOPSYM CREAM (FLUOCINONID E) TOPSYM OINTMENT (FLUOCINONID E) CIMETIDINE TABLETS 200MG"D.T.S" ZINE ORABASE 0.1% TILAM FOR INJECTION FLUOCINONIDE
1 A018063338 2 A018088338 3 A023592100 4 A045183412 5 A048083265 TOPSYM CREAM (FLUOCINONID E) TOPSYM OINTMENT (FLUOCINONID E) CIMETIDINE TABLETS 200MG"D.T.S" ZINE ORABASE 0.1% TILAM FOR INJECTION FLUOCINONIDE
 24 24. Special Issue 名 人 講 堂 專 題 研 究 表3 新加坡政府對銷售給不同屬性投資人的對沖基金管理指引 25 焦 點 視 界 27 26 市 場 掃 描 證 交 集 錦 資料來源 新加坡金融管理局(Monetary Authority of Singapore)網站 25 機構投資人定義 (1)依銀行法設立的銀行 (2)商業銀行 (3)財務公司 (4)保險公司 (5)信託公司
24 24. Special Issue 名 人 講 堂 專 題 研 究 表3 新加坡政府對銷售給不同屬性投資人的對沖基金管理指引 25 焦 點 視 界 27 26 市 場 掃 描 證 交 集 錦 資料來源 新加坡金融管理局(Monetary Authority of Singapore)網站 25 機構投資人定義 (1)依銀行法設立的銀行 (2)商業銀行 (3)財務公司 (4)保險公司 (5)信託公司
貳 肆 公司治理報告 一 組織系統 ( 一 ) 組織結構 ( 二 ) 組織系統圖 14 中華民國 98 年中華郵政年報
 14 16 24 30 24 25 26 26 27 27 28 29 29 一 組織系統二 董事 監察人 總經理 副總經理 各部門及分支機構主管資料三 公司治理運作情形 ( 一 ) 董事會運作情形 ( 二 ) 公司治理運作情形及其與上市上櫃公司治理實務守則差異情形及原因 ( 三 ) 揭露公司治理守則及相關規章之查詢方式 ( 四 ) 揭露其他足以增進對公司治理運作情形瞭解之重要資訊 ( 五 ) 內部控制制度執行狀況
14 16 24 30 24 25 26 26 27 27 28 29 29 一 組織系統二 董事 監察人 總經理 副總經理 各部門及分支機構主管資料三 公司治理運作情形 ( 一 ) 董事會運作情形 ( 二 ) 公司治理運作情形及其與上市上櫃公司治理實務守則差異情形及原因 ( 三 ) 揭露公司治理守則及相關規章之查詢方式 ( 四 ) 揭露其他足以增進對公司治理運作情形瞭解之重要資訊 ( 五 ) 內部控制制度執行狀況
 100 9/5 E-mail 88 ( ) 20098 21 100-2 88-3 - - 4 - 5-6 - 7-8 (1) - 9 (2)- () 1. 9912 2. 3. 4. 5. () 1. 2. 3. 4. 5. 6. / 7. / - 10 (2)- () 1. 2. 3. 4. 5. 6. () 9912-11 (2)- - 12 13 - (2)- 1. 2. 3. 4. 5.
100 9/5 E-mail 88 ( ) 20098 21 100-2 88-3 - - 4 - 5-6 - 7-8 (1) - 9 (2)- () 1. 9912 2. 3. 4. 5. () 1. 2. 3. 4. 5. 6. / 7. / - 10 (2)- () 1. 2. 3. 4. 5. 6. () 9912-11 (2)- - 12 13 - (2)- 1. 2. 3. 4. 5.
目 錄
 Zhongzhi Pharmaceutical Holdings Limited 3737 2015 目 錄 2 4 5 10 18 20 24 36 38 39 40 42 43 45 104 公司資料 Clifton House 75 Fort House P.O. Box 1350 Grand Cayman KY1-1108 Cayman Islands 3 141 2102 2103 1 22
Zhongzhi Pharmaceutical Holdings Limited 3737 2015 目 錄 2 4 5 10 18 20 24 36 38 39 40 42 43 45 104 公司資料 Clifton House 75 Fort House P.O. Box 1350 Grand Cayman KY1-1108 Cayman Islands 3 141 2102 2103 1 22
威 發 國 際 集 團 有 限 公 司 於 百 慕 達 註 冊 成 立 之 有 限 公 司 股份代號 : 765 2O15
 威 發 國 際 集 團 有 限 公 司 於 百 慕 達 註 冊 成 立 之 有 限 公 司 股份代號 : 765 2O15 2 3-4 5-6 7-10 11-12 13-31 32-40 41-42 43 44-45 46 47-48 49-132 133 134 公司資料 02 年 公司 44 9 C D MUFG Fund Services (Bermuda) Limited The Belvedere
威 發 國 際 集 團 有 限 公 司 於 百 慕 達 註 冊 成 立 之 有 限 公 司 股份代號 : 765 2O15 2 3-4 5-6 7-10 11-12 13-31 32-40 41-42 43 44-45 46 47-48 49-132 133 134 公司資料 02 年 公司 44 9 C D MUFG Fund Services (Bermuda) Limited The Belvedere
目錄 2 公司資料 3 董事及高級管理層簡歷 5 主席報告 6 管理層討論及分析 10 企業管治報告 17 董事會報告 26 獨立核數師報告 28 綜合全面收益報表 29 綜合財務狀況報表 30 綜合權益變動表 31 綜合現金流量表 32 綜合財務報表附註 94 五年財務摘要 95 主要物業之詳情
 Great China Properties Holdings Limited 大中華地產控股有限公司 ( 於香港註冊成立之有限公司 ) 股份代號 : 21 同一夢想 共創未來 2015 年報 目錄 2 公司資料 3 董事及高級管理層簡歷 5 主席報告 6 管理層討論及分析 10 企業管治報告 17 董事會報告 26 獨立核數師報告 28 綜合全面收益報表 29 綜合財務狀況報表 30 綜合權益變動表
Great China Properties Holdings Limited 大中華地產控股有限公司 ( 於香港註冊成立之有限公司 ) 股份代號 : 21 同一夢想 共創未來 2015 年報 目錄 2 公司資料 3 董事及高級管理層簡歷 5 主席報告 6 管理層討論及分析 10 企業管治報告 17 董事會報告 26 獨立核數師報告 28 綜合全面收益報表 29 綜合財務狀況報表 30 綜合權益變動表
5 AC TROPINE EYE DROPS 0.5% (ATROPINE SULFATE) ATROPINE SULFATE MG/ 藥商名稱 麥迪 森 原支付初核價價格 本品項之藥品分類 : 一般學名藥 2. 本品項之品質條件 :C 級, 符合 PIC/S P
 1 KC00895248 BAXTER KIOVIG 100 MG/ SOLUTION FOR INFUSION IMMUNOGLOBULIN HUMAN 100.000MG/ 全民健康保險新收載品項明細表 50.00 0 百特 -- 9000 1. 本品項之藥品分類 : 一般學名藥 2. 本品項之品質條件 :C 級, 符合 PIC/S P 3. 有收載同規格藥品, 依藥品分類核價原則取最低價, 暫核為每支
1 KC00895248 BAXTER KIOVIG 100 MG/ SOLUTION FOR INFUSION IMMUNOGLOBULIN HUMAN 100.000MG/ 全民健康保險新收載品項明細表 50.00 0 百特 -- 9000 1. 本品項之藥品分類 : 一般學名藥 2. 本品項之品質條件 :C 級, 符合 PIC/S P 3. 有收載同規格藥品, 依藥品分類核價原則取最低價, 暫核為每支
1
 2015 www.hkgem.com www.kwanonconstruction.com 1 目錄 3 4 6 7 11 20 30 42 44 45 47 48 49 51 114 2 公司資料 公司 Cricket Square Hutchins Drive P.O. Box 2681 Grand Cayman KY1-1111 Cayman Islands 41 43 45 47 5 Codan
2015 www.hkgem.com www.kwanonconstruction.com 1 目錄 3 4 6 7 11 20 30 42 44 45 47 48 49 51 114 2 公司資料 公司 Cricket Square Hutchins Drive P.O. Box 2681 Grand Cayman KY1-1111 Cayman Islands 41 43 45 47 5 Codan
完全照護手冊
 20 13.6 9.910 17.8 13.3 20 1996 () 1. 2. 1998 20012000 2014 0800-507272 5 55% 30.1% 16.9% 40.7% 25.3%13.2 72.5%30-6012.1% 3015.4%60 60.8%22.3% 45 2013 3700 37.4% 2-319.8%121 0800-507272 1421 11 5 70% 7
20 13.6 9.910 17.8 13.3 20 1996 () 1. 2. 1998 20012000 2014 0800-507272 5 55% 30.1% 16.9% 40.7% 25.3%13.2 72.5%30-6012.1% 3015.4%60 60.8%22.3% 45 2013 3700 37.4% 2-319.8%121 0800-507272 1421 11 5 70% 7
<4D F736F F D20A4A4C3C4B2A3B77EB56FAE69ABD8C4B3AED15F66756C6C>
 ... 3... 10... 12... 13 3.1... 13 3.2... 13 3.3... 14 3.4... 15 3.5... 17 3.6... 21 3.7... 23 3.8 GMP... 24 3.9... 26... 28 4.1... 28 4.2... 29... 30 5.1... 30 5.2.... 30 5.3... 37 5.4... 38 5.5... 39
... 3... 10... 12... 13 3.1... 13 3.2... 13 3.3... 14 3.4... 15 3.5... 17 3.6... 21 3.7... 23 3.8 GMP... 24 3.9... 26... 28 4.1... 28 4.2... 29... 30 5.1... 30 5.2.... 30 5.3... 37 5.4... 38 5.5... 39
年報 2014 中裕燃氣控股有限公司
 Stock Code 股份代號: 3633 ZHONGYU GAS HOLDINGS LIMITED www.zhongyugas.com Annual Report 2014 年 報 (Incorporated in the Cayman Islands with limited liability) (於 開 曼 群 島 註 冊成立之有限公司) 2014 Annual 年 Report 報 年報
Stock Code 股份代號: 3633 ZHONGYU GAS HOLDINGS LIMITED www.zhongyugas.com Annual Report 2014 年 報 (Incorporated in the Cayman Islands with limited liability) (於 開 曼 群 島 註 冊成立之有限公司) 2014 Annual 年 Report 報 年報
 第一篇文概說第七章公文的用語及標點符號公本篇內容 第一章 緒論 第二章 公文的意義 第三章 公文與高 普 特各類考試 第四章 公文程式之意義及演變 第五章 公文之分類及其行文系統 第六章 公文之結構與行款 第一篇 第一章緒論 003 第一章緒論 等 等 004 最新應用公文 第一篇 第二章公文的意義 005 第二章公文的意義 第一節 一 須為公務員製作之文書 二 須為公務員 職務上 製作之文書 006
第一篇文概說第七章公文的用語及標點符號公本篇內容 第一章 緒論 第二章 公文的意義 第三章 公文與高 普 特各類考試 第四章 公文程式之意義及演變 第五章 公文之分類及其行文系統 第六章 公文之結構與行款 第一篇 第一章緒論 003 第一章緒論 等 等 004 最新應用公文 第一篇 第二章公文的意義 005 第二章公文的意義 第一節 一 須為公務員製作之文書 二 須為公務員 職務上 製作之文書 006
目錄
 ( ) (: 00059) 2015 目錄 2 3 4 5 8 21 41 53 61 63 64 66 67 68 150 151 1 公司資料 公司 股 00059 0.1% 05821 0.1% 05580 0.1% 05855 0.1% 05567 0.1% 05602 業 8 32 33 86 20 2208 2888 86 20 2208 2777 業 151 14 1401 (852)
( ) (: 00059) 2015 目錄 2 3 4 5 8 21 41 53 61 63 64 66 67 68 150 151 1 公司資料 公司 股 00059 0.1% 05821 0.1% 05580 0.1% 05855 0.1% 05567 0.1% 05602 業 8 32 33 86 20 2208 2888 86 20 2208 2777 業 151 14 1401 (852)
(Microsoft Word - \244\345\245\3638)
 衛生福利部中央健康保險署公告 發布日期 :104.03.13 健保審字第 1040080965 號 主旨 : 公告支付新增及異動 全民健康保險藥物給付項目及支付標準 之藥物品 項計 1,710 項 依據 : 全民健康保險法第 41 條暨全民健康保險藥物給付項目及支付標準 公告事項 : 及 全民健康保險藥品已收 載品項異動明細表 如附件 ( 附件電子檔已置於本署全球資訊網 (http://www.nhi.gov.tw),
衛生福利部中央健康保險署公告 發布日期 :104.03.13 健保審字第 1040080965 號 主旨 : 公告支付新增及異動 全民健康保險藥物給付項目及支付標準 之藥物品 項計 1,710 項 依據 : 全民健康保險法第 41 條暨全民健康保險藥物給付項目及支付標準 公告事項 : 及 全民健康保險藥品已收 載品項異動明細表 如附件 ( 附件電子檔已置於本署全球資訊網 (http://www.nhi.gov.tw),
表二 105 年國中教育會考英語科閱讀與聽力答對題數對應整體能力等級加標示對照表 閱讀答 對題數 聽力答對題數 待加強待加強待加強待加強待加強待加強待加強待加強待加強待加強待加強待加強
 表一 105 年國中教育會考國文科 社會科與自然科能力等級加標示與答對題數對照表 國文社會自然 A++ 46-48 60-63 51-54 A+ 42-48 44-45 54-63 58-59 46-54 49-50 A 42-43 54-57 46-48 B++ 37-41 45-53 37-45 B+ 20-41 31-36 24-53 38-44 20-45 30-36 B 20-30 24-37
表一 105 年國中教育會考國文科 社會科與自然科能力等級加標示與答對題數對照表 國文社會自然 A++ 46-48 60-63 51-54 A+ 42-48 44-45 54-63 58-59 46-54 49-50 A 42-43 54-57 46-48 B++ 37-41 45-53 37-45 B+ 20-41 31-36 24-53 38-44 20-45 30-36 B 20-30 24-37
製造廠名稱 6 A ZYPINE FILM COATED OLANZAPINE 5MG 中生生 TABLETS 5MG 技淡水 西藥新增品項 原支付初核價價格 屬 BA/BE 學名藥 行政院衛生署 101 年 12 月 20 日署授食字第 號
 製造廠名稱 1 B0260293C8 EXELON PATCH 10 RIVASTIGMINE 9.5MG LTS 18MG LOHMA NN 2 B025729148 BISOLVON (R) SOLUTION 2MG/ML 3 A057972155 LEVOTAM ORAL SOLUTON 100MG/ML "CENTER" 4 A057972166 LEVOTAM ORAL SOLUTON 100MG/ML
製造廠名稱 1 B0260293C8 EXELON PATCH 10 RIVASTIGMINE 9.5MG LTS 18MG LOHMA NN 2 B025729148 BISOLVON (R) SOLUTION 2MG/ML 3 A057972155 LEVOTAM ORAL SOLUTON 100MG/ML "CENTER" 4 A057972166 LEVOTAM ORAL SOLUTON 100MG/ML
CHANGSHOUHUA FOOD COMPANY LIMITED
 2014 CHANGSHOUHUA FOOD COMPANY LIMITED 2 3 5 12 22 34 38 40 41 42 43 44 46 102 公司資料 2 公司 股份 Royal Bank of Canada Trust Company (Cayman) Limited 4th Floor, Royal Bank House 24 Shedden Road, George Town
2014 CHANGSHOUHUA FOOD COMPANY LIMITED 2 3 5 12 22 34 38 40 41 42 43 44 46 102 公司資料 2 公司 股份 Royal Bank of Canada Trust Company (Cayman) Limited 4th Floor, Royal Bank House 24 Shedden Road, George Town
項次 健保代碼 藥品名稱 成分及含量 規格量 藥商名稱 原支付價 初核價格 初核說明 生效方式 / 日期 1 KC NUWIQ 250 IU Simoctocog alfa IU 1.000IU 艾科索 本品項之藥品分類 : 一般學名藥 2. 有收載同
 項次 健保代碼 藥品名稱 成分及含量 規格量 藥商名稱 原支付價 初核價格 初核說明 生效方式 / 日期 1 KC01068299 NUWIQ 250 IU Simoctocog alfa 250.000IU 1.000IU 艾科索 -- 23 1. 本品項之藥品分類 : 一般學名藥 2. 有收載同規格藥品, 依藥品分類 核價原則取最低價, 暫予支付每單位 23 元 (1) 同規格一般學名藥最低價
項次 健保代碼 藥品名稱 成分及含量 規格量 藥商名稱 原支付價 初核價格 初核說明 生效方式 / 日期 1 KC01068299 NUWIQ 250 IU Simoctocog alfa 250.000IU 1.000IU 艾科索 -- 23 1. 本品項之藥品分類 : 一般學名藥 2. 有收載同規格藥品, 依藥品分類 核價原則取最低價, 暫予支付每單位 23 元 (1) 同規格一般學名藥最低價
01 目錄 02 報 報 21 報 28 報 報 41 年 年報
 China Financial International Investments Limited 2012 01 目錄 02 報 03 04 05 18 報 21 報 28 報 35 36 37 38 39 40 報 41 年 104 2012 年報 公司資料 02 中國金融國際投資 有限公司 有限公司 Conyers Dill & Pearman Clarendon House 2 Church
China Financial International Investments Limited 2012 01 目錄 02 報 03 04 05 18 報 21 報 28 報 35 36 37 38 39 40 報 41 年 104 2012 年報 公司資料 02 中國金融國際投資 有限公司 有限公司 Conyers Dill & Pearman Clarendon House 2 Church
1
 2016 www.hkgem.com www.kwanonconstruction.com 1 目錄 3 4 6 10 21 32 47 49 50 52 54 56 126 2 公司資料 公司 Cricket Square Hutchins Drive P.O. Box 2681 Grand Cayman KY1-1111 Cayman Islands 41 43 45 47 5 Codan Trust
2016 www.hkgem.com www.kwanonconstruction.com 1 目錄 3 4 6 10 21 32 47 49 50 52 54 56 126 2 公司資料 公司 Cricket Square Hutchins Drive P.O. Box 2681 Grand Cayman KY1-1111 Cayman Islands 41 43 45 47 5 Codan Trust
% % % 獨立 廉正 專業 創新
 101 99 102 101 1. 2. 3. 4. 5. 6. 7. 8. 9. 10. 99 102 8 4 34 11 101826 594 71.91% 160 19.37% 72 8.72% 101 100 27 18100 21 101 35 獨立 廉正 專業 創新 1. 7,290 8,677 26,180 26,011 1,272 1,346 142 157 7 7 1,757 1,795
101 99 102 101 1. 2. 3. 4. 5. 6. 7. 8. 9. 10. 99 102 8 4 34 11 101826 594 71.91% 160 19.37% 72 8.72% 101 100 27 18100 21 101 35 獨立 廉正 專業 創新 1. 7,290 8,677 26,180 26,011 1,272 1,346 142 157 7 7 1,757 1,795
行政院金融監督管理委員會全球資訊網-行政院金融監督管理委員會
 本公司銷售富邦投信股票型基金所收取之通路報酬如 ㄧ 投資人支付 台端支付的基金申購手續費為 0%~2%, 其中本公司收取不多於 0%~2% 股票型基金經理費收入為年率 1.5%~2.0%, 台端持有本基金期 間, 本公司收取不多於年率 0%~1% 銷售獎勵金 (%) 基金募集期間, 富邦投信支付獎勵金 0%~0.15% 範例 : 富邦精準基金 之申購手續費 1% 及經理費 1.5%, 本公司銷售之申購手續費分成不多
本公司銷售富邦投信股票型基金所收取之通路報酬如 ㄧ 投資人支付 台端支付的基金申購手續費為 0%~2%, 其中本公司收取不多於 0%~2% 股票型基金經理費收入為年率 1.5%~2.0%, 台端持有本基金期 間, 本公司收取不多於年率 0%~1% 銷售獎勵金 (%) 基金募集期間, 富邦投信支付獎勵金 0%~0.15% 範例 : 富邦精準基金 之申購手續費 1% 及經理費 1.5%, 本公司銷售之申購手續費分成不多
第七章行政工作 7.1 預算 法律依據 預算收入 94
 第七章行政工作 93 第七章行政工作 7.1 預算 7.1.1 法律依據 7.1.2 預算收入 94 五 2006 年收入管理 圖表二十六 2006 年收入結構 7.1.3 預算支出 95 圖表二十七 2006 年支出管理 96 圖表二十八 2006 年實際支出結構 圖表二十九 2006 年預算支出與實際支出對比 97 7.2 人員 圖表三十 1999 2006 年人員數目比較表 98 附件行政申訴範疇立案調查個案撮要
第七章行政工作 93 第七章行政工作 7.1 預算 7.1.1 法律依據 7.1.2 預算收入 94 五 2006 年收入管理 圖表二十六 2006 年收入結構 7.1.3 預算支出 95 圖表二十七 2006 年支出管理 96 圖表二十八 2006 年實際支出結構 圖表二十九 2006 年預算支出與實際支出對比 97 7.2 人員 圖表三十 1999 2006 年人員數目比較表 98 附件行政申訴範疇立案調查個案撮要
100% 50% 50% 80% 20% 60% 40% 80% 20% 60% 40% 20
 2 II 19 100% 50% 50% 80% 20% 60% 40% 80% 20% 60% 40% 20 22 3 3 6 6 5 6 5 7 4 5 50 4 4 3 3 6 5 6 6 6 6 4 5 50 5 3 3 6 7 5 6 4 7 4 5 50 6 2 4 6 7 5 6 4 7 4 5 50 7 2 4 6 7 5 6 4 7 5 4 50 8 2 4 6 7 5 6 4 7
2 II 19 100% 50% 50% 80% 20% 60% 40% 80% 20% 60% 40% 20 22 3 3 6 6 5 6 5 7 4 5 50 4 4 3 3 6 5 6 6 6 6 4 5 50 5 3 3 6 7 5 6 4 7 4 5 50 6 2 4 6 7 5 6 4 7 4 5 50 7 2 4 6 7 5 6 4 7 5 4 50 8 2 4 6 7 5 6 4 7
低功率電波輻射性電機管理辦法 第十二條經型式認證合格之低功率射頻電機, 非經許可, 公司 商號或使用者均不得擅自變更頻率 加大功率或變更原設計之特性及功能 第十四條低功率射頻電機之使用不得影響飛航安全及干擾合法通訊 ; 經發現有干擾現象時, 應立即停用, 並改善至無干擾時方得繼續使用 前項合法通訊,
 使用說明書 TMAX 機車 在騎乘機車之前, 請務必仔細閱讀這本使用說明書 XP00 XP00A PW--T 低功率電波輻射性電機管理辦法 第十二條經型式認證合格之低功率射頻電機, 非經許可, 公司 商號或使用者均不得擅自變更頻率 加大功率或變更原設計之特性及功能 第十四條低功率射頻電機之使用不得影響飛航安全及干擾合法通訊 ; 經發現有干擾現象時, 應立即停用, 並改善至無干擾時方得繼續使用 前項合法通訊,
使用說明書 TMAX 機車 在騎乘機車之前, 請務必仔細閱讀這本使用說明書 XP00 XP00A PW--T 低功率電波輻射性電機管理辦法 第十二條經型式認證合格之低功率射頻電機, 非經許可, 公司 商號或使用者均不得擅自變更頻率 加大功率或變更原設計之特性及功能 第十四條低功率射頻電機之使用不得影響飛航安全及干擾合法通訊 ; 經發現有干擾現象時, 應立即停用, 並改善至無干擾時方得繼續使用 前項合法通訊,
全民健康保險已收載異動品項明細表 項次 健保代碼 藥品名稱 成分及含量 規格量 藥商名稱 原支付價 初核價格 初核說明 生效方式 / 日期 1 AC MEGAXIA ES ORAL SUSPENSION 125MG/ML MEGESTROL ACETATE MG/ML
 全民健康保險已收載異動品項明細表 項次 健保代碼 藥品名稱 成分及含量 規格量 藥商名稱 原支付價 初核價格 初核說明 生效方式 / 日期 1 AC58764161 MEGAXIA ES ORAL SUSPENSION 125MG/ML MEGESTROL ACETATE 125.000MG/ML 150.000M L 安成 3818 0 1. 依廠商 107 年 8 月 15 日安 ( 公 ) 字第
全民健康保險已收載異動品項明細表 項次 健保代碼 藥品名稱 成分及含量 規格量 藥商名稱 原支付價 初核價格 初核說明 生效方式 / 日期 1 AC58764161 MEGAXIA ES ORAL SUSPENSION 125MG/ML MEGESTROL ACETATE 125.000MG/ML 150.000M L 安成 3818 0 1. 依廠商 107 年 8 月 15 日安 ( 公 ) 字第
行政法概要 本章學習重點 本章大綱 第一節行政作用之概念 第二節行政作用之分類 一 行政程序法 第三節行政作用法之範圍 第四節行政作用之私法 行為 二 行政罰法三 行政執行法一 源起二 類型 第五節行政作用中的非 權力行為 一 類型 二 事實行為 第六節行政作用之內部 行為 一 行政規則
 第 6 章 行政作用及其分類 行政法概要 本章學習重點 1. 2. 本章大綱 第一節行政作用之概念 第二節行政作用之分類 一 行政程序法 第三節行政作用法之範圍 第四節行政作用之私法 行為 二 行政罰法三 行政執行法一 源起二 類型 第五節行政作用中的非 權力行為 一 類型 二 事實行為 第六節行政作用之內部 行為 一 行政規則 二 內部指令 CHAPTER 6 行政作用及其分類 內文教學區 1 行政法概要
第 6 章 行政作用及其分類 行政法概要 本章學習重點 1. 2. 本章大綱 第一節行政作用之概念 第二節行政作用之分類 一 行政程序法 第三節行政作用法之範圍 第四節行政作用之私法 行為 二 行政罰法三 行政執行法一 源起二 類型 第五節行政作用中的非 權力行為 一 類型 二 事實行為 第六節行政作用之內部 行為 一 行政規則 二 內部指令 CHAPTER 6 行政作用及其分類 內文教學區 1 行政法概要
目錄
 2017 目錄 2 3 5 11 22 35 50 56 57 59 61 63 122 1 公司資料 公司 Cricket Square Hutchins Drive P.O. Box 2681 Grand Cayman KY1-1111 Cayman Islands 41 43 45 47 5 Codan Trust Company (Cayman) Limited Cricket Square,
2017 目錄 2 3 5 11 22 35 50 56 57 59 61 63 122 1 公司資料 公司 Cricket Square Hutchins Drive P.O. Box 2681 Grand Cayman KY1-1111 Cayman Islands 41 43 45 47 5 Codan Trust Company (Cayman) Limited Cricket Square,
 2015 002 024 004 026 005 027 011 028 021 043 023 048 James William Beeke Howard Robert Balloch Peter Humphrey Owen Peter Humphrey Owen Peter Humphrey Owen Howard Robert Balloch Peter Humphrey Owen 中 Maples
2015 002 024 004 026 005 027 011 028 021 043 023 048 James William Beeke Howard Robert Balloch Peter Humphrey Owen Peter Humphrey Owen Peter Humphrey Owen Howard Robert Balloch Peter Humphrey Owen 中 Maples
目錄表 年中期報告
 目錄表 2 4 5 13 28 29 31 33 35 36 67 1 2015 年中期報告 公司資料 公司 22 公司 www.boyaa.com.hk 0434 博雅互動國際有限公司 2 公司資料 中 1001 TCL E D3 9B-C 518000 183 17 1712-1716 Maples Fund Services (Cayman) Limited PO Box 1093, Boundary
目錄表 2 4 5 13 28 29 31 33 35 36 67 1 2015 年中期報告 公司資料 公司 22 公司 www.boyaa.com.hk 0434 博雅互動國際有限公司 2 公司資料 中 1001 TCL E D3 9B-C 518000 183 17 1712-1716 Maples Fund Services (Cayman) Limited PO Box 1093, Boundary
Zytiga... Zytiga... Zytiga Zytiga Zytiga
 250 本資料僅提供醫護人員衛教使用 ............... Zytiga... Zytiga... Zytiga... 2 3 4 5 6 7 8 9 Zytiga... 10 Zytiga... 10...... 13 18 Zytiga Zytiga 2 25% 3 PSA PSA 3~4 ng/ml PSA bone scan CT scan MRI 4 5 攝護腺癌之治療 治療方面
250 本資料僅提供醫護人員衛教使用 ............... Zytiga... Zytiga... Zytiga... 2 3 4 5 6 7 8 9 Zytiga... 10 Zytiga... 10...... 13 18 Zytiga Zytiga 2 25% 3 PSA PSA 3~4 ng/ml PSA bone scan CT scan MRI 4 5 攝護腺癌之治療 治療方面
39% % 李兆基博士大紫荊勳賢 10
 旺角 香港 39%7.61 5.48 38% 4.89 3.54 李兆基博士大紫荊勳賢 10 38% 44% 3% The H Collection 62% 11 18 12 進行發展中物業及已建成主要存貨, 樓面總括如下 : 項目數目 集團自佔實用 / 樓面面積 ( 百萬平方呎 ) ( 註一 ) 備註 ( 甲 ) 可於二零一八年銷售之樓面 : 1. 24 1.1 2. 6 0.6 ( 乙 ) 市區項目
旺角 香港 39%7.61 5.48 38% 4.89 3.54 李兆基博士大紫荊勳賢 10 38% 44% 3% The H Collection 62% 11 18 12 進行發展中物業及已建成主要存貨, 樓面總括如下 : 項目數目 集團自佔實用 / 樓面面積 ( 百萬平方呎 ) ( 註一 ) 備註 ( 甲 ) 可於二零一八年銷售之樓面 : 1. 24 1.1 2. 6 0.6 ( 乙 ) 市區項目
 2013~2015 保健食品產業專業人才 供需調查 2011 5 2011529 2012 2013~2015 2012 44.67% 2011 11.96% 2013~2015 ... 1... 1... 5... 10... 12... 13... 14... 19... 20... 22... 24... 12... 19... 21... 22 III IV 1... 1 2... 3
2013~2015 保健食品產業專業人才 供需調查 2011 5 2011529 2012 2013~2015 2012 44.67% 2011 11.96% 2013~2015 ... 1... 1... 5... 10... 12... 13... 14... 19... 20... 22... 24... 12... 19... 21... 22 III IV 1... 1 2... 3
18 Prulifloxacin PLx Pharma PLx Pharma RegeneRx Biopharmaceuticals, Inc. Thymosin Beta 4 Treprestinil United Therapeutics Treprestinil United Therapeu
 業務回顧 Lee s Pharmaceutical Holdings Limited 李氏大藥廠控股有限公司 * 950 第一季度業績公佈截至二零一二年三月三十一日止三個月 109,889,000 49% 24,609,000 45.7% 5.24 44.8% 100% 93% 35% 77% 62% 60% 36% 35% 71% 2.7 1.4 22.4% 42.3% 37.2% * 1 18
業務回顧 Lee s Pharmaceutical Holdings Limited 李氏大藥廠控股有限公司 * 950 第一季度業績公佈截至二零一二年三月三十一日止三個月 109,889,000 49% 24,609,000 45.7% 5.24 44.8% 100% 93% 35% 77% 62% 60% 36% 35% 71% 2.7 1.4 22.4% 42.3% 37.2% * 1 18
業績 簡明綜合收益表 截至六月三十日止六個月 人民幣千元 ( 未經審核 ) 3 11,202,006 9,515,092 (7,445,829) (6,223,056) 3,756,177 3,292, , ,160 (2,995,823) (2,591,057) (391,
 POU SHENG INTERNATIONAL (HOLDINGS) LIMITED 寶勝國際 ( 控股 ) 有限公司 ( 股份代號 :3813) 截至二零一八年六月三十日止六個月未經審核中期業績 本集團財務摘要 截至六月三十日止六個月百分比 增幅 ( 未經審核 ) 11,202,006 9,515,092 17.7% 530,360 505,753 4.9% 306,833 298,612 2.8%
POU SHENG INTERNATIONAL (HOLDINGS) LIMITED 寶勝國際 ( 控股 ) 有限公司 ( 股份代號 :3813) 截至二零一八年六月三十日止六個月未經審核中期業績 本集團財務摘要 截至六月三十日止六個月百分比 增幅 ( 未經審核 ) 11,202,006 9,515,092 17.7% 530,360 505,753 4.9% 306,833 298,612 2.8%
本公司(銀行)銷售○○投信「○○基金」所收取之通路報酬如下:
 20180824 版 ( 都柏林 ) 本公司銷售 ( 都柏林 ) 法盛國際系列 法盛 - 盧米斯賽勒斯高收益債券基金 ( 原名稱 : 法儲銀 - 盧米斯賽勒斯高收益債券型基金 )( 本基金主要係投資於非投資等級之高風險債券 ) 所收取之通路報酬如下 : 台端支付的基金申購手續費不多於 2%, 其中本公司收取不多於 2% 台端支付的基金轉換手續費為 0% 二 基金公司 ( 或總代理人 / 境外基金機構
20180824 版 ( 都柏林 ) 本公司銷售 ( 都柏林 ) 法盛國際系列 法盛 - 盧米斯賽勒斯高收益債券基金 ( 原名稱 : 法儲銀 - 盧米斯賽勒斯高收益債券型基金 )( 本基金主要係投資於非投資等級之高風險債券 ) 所收取之通路報酬如下 : 台端支付的基金申購手續費不多於 2%, 其中本公司收取不多於 2% 台端支付的基金轉換手續費為 0% 二 基金公司 ( 或總代理人 / 境外基金機構
行政院所屬各機關公務出國報告書格式及應載事項
 出國報告 ( 出國類別 : 開會類 ) ( 裝 釘 線 ) 參加 藥品價格管理研討會 服務機關 : 衛生福利部中央健康保險署姓名職稱 : 署長黃三桂組長施如亮組長林阿明視察林裕能派赴國家 : 中國大陸出國期間 :2014/9/9~2014/9/11 報告日期 :2014/9/25 1 摘要由中國大陸中國價格協會於 103 年 9 月 10 日在北京舉辦 藥品價格管理研討會, 主題為藥品價格管理經驗交流,
出國報告 ( 出國類別 : 開會類 ) ( 裝 釘 線 ) 參加 藥品價格管理研討會 服務機關 : 衛生福利部中央健康保險署姓名職稱 : 署長黃三桂組長施如亮組長林阿明視察林裕能派赴國家 : 中國大陸出國期間 :2014/9/9~2014/9/11 報告日期 :2014/9/25 1 摘要由中國大陸中國價格協會於 103 年 9 月 10 日在北京舉辦 藥品價格管理研討會, 主題為藥品價格管理經驗交流,
一 0 六年度年報 中華民國一 0 七年四月十二日刊印 查詢本年報之網址如下 : (1) 主管機關指定之公開資訊觀測站 :newmops.twse.com.tw (2) 本公司網址 :
 一 0 六年度年報 中華民國一 0 七年四月十二日刊印 查詢本年報之網址如下 : (1) 主管機關指定之公開資訊觀測站 :newmops.twse.com.tw (2) 本公司網址 :www.chimeicorp.com 一 本公司發言人 代理人發言人姓名 : 公司發言人 : 姓名 : 陳世賢職稱 : 副總經理電話 :(06)2663000 電子郵件信箱 :service@mail.chimei.com.tw
一 0 六年度年報 中華民國一 0 七年四月十二日刊印 查詢本年報之網址如下 : (1) 主管機關指定之公開資訊觀測站 :newmops.twse.com.tw (2) 本公司網址 :www.chimeicorp.com 一 本公司發言人 代理人發言人姓名 : 公司發言人 : 姓名 : 陳世賢職稱 : 副總經理電話 :(06)2663000 電子郵件信箱 :service@mail.chimei.com.tw
TablesDivision_Chinois
 Exemple Tables de division Chinois http://www.memrise.com/ 除以 chúyǐ divisé par (diviser par) 等于 děngyú égale (être égal à) 八除以四等于二 bā chúyǐ sì děngyú èr 8 divisé par 4 égale 2 Table de division par 1 一除以一
Exemple Tables de division Chinois http://www.memrise.com/ 除以 chúyǐ divisé par (diviser par) 等于 děngyú égale (être égal à) 八除以四等于二 bā chúyǐ sì děngyú èr 8 divisé par 4 égale 2 Table de division par 1 一除以一
惠理基金管理香港有限公司 (852) (852)
 2017 惠理基金管理香港有限公司 (852) 2880 9263 (852) 2564 8487 operations@valueetf.com.hk www.valueetf.com.hk 2-3 理 4 ( ) 5 ( ) 6-7 ( ) 8 ( ) 9 ( ) 10 1 截至二零一七年九月三十日止六個月 管理人兼 RQFII 持有人惠理基金 理香港 香港 投資顧問 理香港 香港 管理人兼 RQFII
2017 惠理基金管理香港有限公司 (852) 2880 9263 (852) 2564 8487 operations@valueetf.com.hk www.valueetf.com.hk 2-3 理 4 ( ) 5 ( ) 6-7 ( ) 8 ( ) 9 ( ) 10 1 截至二零一七年九月三十日止六個月 管理人兼 RQFII 持有人惠理基金 理香港 香港 投資顧問 理香港 香港 管理人兼 RQFII
, , % , % 人民幣十億元 2011 年至 2020 年 ( 估計 ) 中國的保健開支總額 6, ,000.0 複合年增長率 (2011 年至 2015 年 ):1
 OEM OEM CMPI OBM 2015 87.3% 12.7% OEM OBM (i) (ii) CMPI (iii) (iv) 2015 39.1% 34.7% 16.5% 9.7% OEM OEM CMPI OEM OEM OBM OBM 2013 2014 2015 OBM 67.4% 71.6% 65.9% OBM 2011 70,169 2015 76,120 2.1% 2020 96,286
OEM OEM CMPI OBM 2015 87.3% 12.7% OEM OBM (i) (ii) CMPI (iii) (iv) 2015 39.1% 34.7% 16.5% 9.7% OEM OEM CMPI OEM OEM OBM OBM 2013 2014 2015 OBM 67.4% 71.6% 65.9% OBM 2011 70,169 2015 76,120 2.1% 2020 96,286
 前稱海王國際集團有限公司 於香港註冊成立之有限公司 股 份 代 號 : 00070 2 3 4 5-13 14-15 16-26 27-32 33-39 40-43 44-45 46-47 48 49-50 51-112 02 公司資料 Nicholas J. Niglio 二零一七年一 一 一 二零一七年 一 二零一七年 一 公司 二零一七年一 一 二零一七年二 一 一 二零一七年 一 二零一七年
前稱海王國際集團有限公司 於香港註冊成立之有限公司 股 份 代 號 : 00070 2 3 4 5-13 14-15 16-26 27-32 33-39 40-43 44-45 46-47 48 49-50 51-112 02 公司資料 Nicholas J. Niglio 二零一七年一 一 一 二零一七年 一 二零一七年 一 公司 二零一七年一 一 二零一七年二 一 一 二零一七年 一 二零一七年
0 0 = 1 0 = 0 1 = = 1 1 = 0 0 = 1
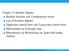 0 0 = 1 0 = 0 1 = 0 1 1 = 1 1 = 0 0 = 1 : = {0, 1} : 3 (,, ) = + (,, ) = + + (, ) = + (,,, ) = ( + )( + ) + ( + )( + ) + = + = = + + = + = ( + ) + = + ( + ) () = () ( + ) = + + = ( + )( + ) + = = + 0
0 0 = 1 0 = 0 1 = 0 1 1 = 1 1 = 0 0 = 1 : = {0, 1} : 3 (,, ) = + (,, ) = + + (, ) = + (,,, ) = ( + )( + ) + ( + )( + ) + = + = = + + = + = ( + ) + = + ( + ) () = () ( + ) = + + = ( + )( + ) + = = + 0
HKSTPC-Annual Report Chi
 企業管治報告 14 企業管治架構 股東 ( 香港特別行政區政府 ) 董事會 管理層 企業合規 - 90 - 企業發展 董事會 17 1 16 董事會成員組成 2015 11 20 80 85 簡介會 2016 1 成員與時並進 2015 利益申報 14 利益衝突 - 91 - 董事會職能 77% 專業建議 承擔責任 6 常務委員會 95 企業拓展及批租委員會 9 8 80% - 92 - 企業發展
企業管治報告 14 企業管治架構 股東 ( 香港特別行政區政府 ) 董事會 管理層 企業合規 - 90 - 企業發展 董事會 17 1 16 董事會成員組成 2015 11 20 80 85 簡介會 2016 1 成員與時並進 2015 利益申報 14 利益衝突 - 91 - 董事會職能 77% 專業建議 承擔責任 6 常務委員會 95 企業拓展及批租委員會 9 8 80% - 92 - 企業發展
untitled
 06 18 33 35 39 2012 04 08 32 34 37 40 2012 FCS (PE), FCIS PO Box 309, Ugland House Grand Cayman, KY1-1104 Cayman Islands 501 201203 1 28 183 17 1712 1716 www.microport.com.cn 6 2012 484,916 448,824 8.0%
06 18 33 35 39 2012 04 08 32 34 37 40 2012 FCS (PE), FCIS PO Box 309, Ugland House Grand Cayman, KY1-1104 Cayman Islands 501 201203 1 28 183 17 1712 1716 www.microport.com.cn 6 2012 484,916 448,824 8.0%
財金資訊-82期.indd
 / ( ) ( ) (waterfall model) (spiral model) 1 (output) (input) 1 www.fisc.com.tw 27 Barry Boehm 1988 2 (prototype) (agile) 2 ( ) 3 3 ( ) 28 / No.82 / 2015.04 (software testing) (peer review) ( ) V ( 4 )
/ ( ) ( ) (waterfall model) (spiral model) 1 (output) (input) 1 www.fisc.com.tw 27 Barry Boehm 1988 2 (prototype) (agile) 2 ( ) 3 3 ( ) 28 / No.82 / 2015.04 (software testing) (peer review) ( ) V ( 4 )
 2 3 13 17 22 26 1 2 8 100738 +86 (10) 8508 5000 +86 (10) 8518 5111 www.kpmg.com.cn 2006 4 2002 2006 1 28% 2006 17 8 500 2006 2006 2006 7 2.5 2 1 500 500 40% 500 10 16 14 12 10 8 6 4 2 2002-2006 5.1 5.9
2 3 13 17 22 26 1 2 8 100738 +86 (10) 8508 5000 +86 (10) 8518 5111 www.kpmg.com.cn 2006 4 2002 2006 1 28% 2006 17 8 500 2006 2006 2006 7 2.5 2 1 500 500 40% 500 10 16 14 12 10 8 6 4 2 2002-2006 5.1 5.9
三、醫藥制度
 三 醫藥制度 議題 16. 妥善使用醫療財源 1. 消弭藥價差 : 目前藥價差變成醫院重大之收入來源, 也使其成為選擇藥劑之標準 如此巨大的藥價差非但導致藥劑使用過剩, 也增加了健保的支出 學名藥之功用本即以便宜價格減輕健保財政之負擔, 若反將學名藥之藥價設定較高, 則只會擴大藥價差, 且絲毫無法減輕健保財政之負擔 主管單位辦理情形暨未來處理方向衛生署 1. 辦理情形 (1) 為逐步縮小藥價差, 中央健康保險局依據
三 醫藥制度 議題 16. 妥善使用醫療財源 1. 消弭藥價差 : 目前藥價差變成醫院重大之收入來源, 也使其成為選擇藥劑之標準 如此巨大的藥價差非但導致藥劑使用過剩, 也增加了健保的支出 學名藥之功用本即以便宜價格減輕健保財政之負擔, 若反將學名藥之藥價設定較高, 則只會擴大藥價差, 且絲毫無法減輕健保財政之負擔 主管單位辦理情形暨未來處理方向衛生署 1. 辦理情形 (1) 為逐步縮小藥價差, 中央健康保險局依據
1
 全 民 健 康 保 險 提 升 民 眾 用 藥 品 質 方 案 中 華 民 國 98 年 10 月 1 日 健 保 審 字 第 0980095575 號 公 告 中 華 民 國 101 年 3 月 14 日 署 授 保 字 第 10100000800 號 公 告 修 正 壹 目 的 提 升 健 保 用 藥 品 質 及 便 利 性 貳 依 據 全 民 健 康 保 險 藥 價 基 準 參 定 義 : 一
全 民 健 康 保 險 提 升 民 眾 用 藥 品 質 方 案 中 華 民 國 98 年 10 月 1 日 健 保 審 字 第 0980095575 號 公 告 中 華 民 國 101 年 3 月 14 日 署 授 保 字 第 10100000800 號 公 告 修 正 壹 目 的 提 升 健 保 用 藥 品 質 及 便 利 性 貳 依 據 全 民 健 康 保 險 藥 價 基 準 參 定 義 : 一
10 AC AC AB AC AC AC BIOZOLE TABLET 20MG OMP E.C CAPSULES 20MG OMEZOL CAP. 20MG OMELON ENTERIC
 附件 - 專利權期滿日於每年第二季之第二大類藥品支付價格調整結果序號 1 BC23221100 NEXIUM TAB. 40MG 2 AC43842100 3 AC9693100 4 AC9243100 BA26189100 OKWE ENTERIC- MICROENCAPSULAT ED CAPSULE 40 MG "N.K." EMAZOLE TABLETS 40MG AMIPASOLE ENTERIC
附件 - 專利權期滿日於每年第二季之第二大類藥品支付價格調整結果序號 1 BC23221100 NEXIUM TAB. 40MG 2 AC43842100 3 AC9693100 4 AC9243100 BA26189100 OKWE ENTERIC- MICROENCAPSULAT ED CAPSULE 40 MG "N.K." EMAZOLE TABLETS 40MG AMIPASOLE ENTERIC
全民健康保險已收載品項異動明細表 項次 健保代碼 藥品名稱 成分及含量 規格量 藥商名稱 原支付價初核價格 初核說明 生效方式 / 日期 1 KC RECORMON SOLUTION FOR EPOETIN BETA, 注射劑, 5 羅氏大藥廠股份 月許可證註銷 10
 項次 健保代碼 藥品名稱 成分及含量 規格量 藥商名稱 原支付價初核價格 初核說明 生效方式 / 日期 1 KC00645221 RECORMON SOLUTION FOR EPOETIN BETA, 注射劑, 5 羅氏大藥廠股份 910 0 8 月許可證註銷 IN PRE-FILLED SYRINGE 5000IU 5.00 KIU 有限公司 2 KC00646212 RECORMON SOLUTION
項次 健保代碼 藥品名稱 成分及含量 規格量 藥商名稱 原支付價初核價格 初核說明 生效方式 / 日期 1 KC00645221 RECORMON SOLUTION FOR EPOETIN BETA, 注射劑, 5 羅氏大藥廠股份 910 0 8 月許可證註銷 IN PRE-FILLED SYRINGE 5000IU 5.00 KIU 有限公司 2 KC00646212 RECORMON SOLUTION
untitled
 Ulferts International Limited Ulferts International Limited 200,000,000 20,000,000 2,000,000 180,000,000 0.62 0.38 1% 0.0027% 0.005% 1711 38D 0.62 0.38 0.621%0.005%0.0027% 0.62 www.hkexnews.hk www.ulferts.com.hk
Ulferts International Limited Ulferts International Limited 200,000,000 20,000,000 2,000,000 180,000,000 0.62 0.38 1% 0.0027% 0.005% 1711 38D 0.62 0.38 0.621%0.005%0.0027% 0.62 www.hkexnews.hk www.ulferts.com.hk
(Microsoft Word _ A-\255\327\245\277\263W\251w.doc)
 行政院衛生署中央健康保險局令 發布日期 :101.12.26 健保審字第 1010041241 號 修正 全民健康保險藥品給付規定 第 8 章免疫製劑 Immunologic agents 8.2. 免疫調節劑 Immunomodulators 第 10 章抗微生物劑 Antimicrobial agents 10.7. 抗病毒劑 Antiviral drugs 給付規定, 並自中華民國一百零二年二月一日生效
行政院衛生署中央健康保險局令 發布日期 :101.12.26 健保審字第 1010041241 號 修正 全民健康保險藥品給付規定 第 8 章免疫製劑 Immunologic agents 8.2. 免疫調節劑 Immunomodulators 第 10 章抗微生物劑 Antimicrobial agents 10.7. 抗病毒劑 Antiviral drugs 給付規定, 並自中華民國一百零二年二月一日生效
全民健康保險已收載品項異動明細表 項次 健保代碼 藥品名稱 成分及含量 規格量 藥商名稱 原支付價 初核價格 初核說明 生效方式 / 日期 1 BC DIMETRIOSE CAPSULES GESTRINONE, 一般錠劑膠囊劑, 賽諾菲股份有 許可證註銷 106/06/
 項次 健保代碼 藥品名稱 成分及含量 規格量 藥商名稱 原支付價 初核價格 初核說明 1 BC21526100 DIMETRIOSE CAPSULES GESTRINONE, 一般錠劑膠囊劑, 賽諾菲股份有 178 0 許可證註銷 106/06/01 2.50 MG 限公司 2 BC21613100 ROXANE 75MG ROXATIDINE, 緩釋錠劑膠囊劑, 75.00 MG 3 BC22884100
項次 健保代碼 藥品名稱 成分及含量 規格量 藥商名稱 原支付價 初核價格 初核說明 1 BC21526100 DIMETRIOSE CAPSULES GESTRINONE, 一般錠劑膠囊劑, 賽諾菲股份有 178 0 許可證註銷 106/06/01 2.50 MG 限公司 2 BC21613100 ROXANE 75MG ROXATIDINE, 緩釋錠劑膠囊劑, 75.00 MG 3 BC22884100
 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 243,1052,272 791222101452 2014719 58339347 396634355 196413164 28269 26 27 28 29 () () () () () () () () () () () () () () () () () () ()
2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 243,1052,272 791222101452 2014719 58339347 396634355 196413164 28269 26 27 28 29 () () () () () () () () () () () () () () () () () () ()
 (於中華人民共和國註冊成立的股份有限公司) (a joint stock limited company incorporated in the People s Republic of China with limited liability) (Stock Code: 1666) (股份代號:1666) 年 報 2013 ANNUAL REPORT 2013 Annual Report 2013
(於中華人民共和國註冊成立的股份有限公司) (a joint stock limited company incorporated in the People s Republic of China with limited liability) (Stock Code: 1666) (股份代號:1666) 年 報 2013 ANNUAL REPORT 2013 Annual Report 2013
季度財務報表 本公司 董事 本集團 季度業績 核數師 香港會計師公會 2410 業務回顧 232,262, % 710,165, % 34.2% 22.9% 7.3% 28.7% 24.5% % 28.0% 24.5% 61,583, % 164
 Lee s Pharmaceutical Holdings Limited 李氏大藥廠控股有限公司 * ( 股份代號 :950) 季度業績截至二零一五年九月三十日止九個月 財務摘要 截至九月三十日 截至九月三十日 止三個月 變動 止九個月 變動 二零一五年 二零一五年 千港元 千港元 收入 232,262 246,679 5.8% 710,165 689,395 +3.0% 毛利 161,863 170,807
Lee s Pharmaceutical Holdings Limited 李氏大藥廠控股有限公司 * ( 股份代號 :950) 季度業績截至二零一五年九月三十日止九個月 財務摘要 截至九月三十日 截至九月三十日 止三個月 變動 止九個月 變動 二零一五年 二零一五年 千港元 千港元 收入 232,262 246,679 5.8% 710,165 689,395 +3.0% 毛利 161,863 170,807
5. / / / / / / / / 6. * (
 19/2013 (19.3.2013 (a (b ( (2013-2014 ( 1. 2013 2. 3. / ( 1 2 3 4 5 6 7 8 9 10 11 12 1 2 3 4. $220,000 1 5. / / / / / / / / 6. * ( 2010 2012 181 120 1137 120 554 2 7. * 1. 2. 3. 4. 8. ( * (I 180 (15 x
19/2013 (19.3.2013 (a (b ( (2013-2014 ( 1. 2013 2. 3. / ( 1 2 3 4 5 6 7 8 9 10 11 12 1 2 3 4. $220,000 1 5. / / / / / / / / 6. * ( 2010 2012 181 120 1137 120 554 2 7. * 1. 2. 3. 4. 8. ( * (I 180 (15 x
SW cdr
 1~2 3 4 5~6 7~8 9~10 11 12 13 14 15 16~18 16 16 17 17 18 18 18 19 19 19 20 21 22 23~26 23 24 24 25 26 27 27 27 : 110V 1 110V 110V 15A 2 3 23 24 4 ( ) 5 6 1 2 26 20 l 1 7 3 4 5 15 17 18 12 7~13 6 ~ 8 ~
1~2 3 4 5~6 7~8 9~10 11 12 13 14 15 16~18 16 16 17 17 18 18 18 19 19 19 20 21 22 23~26 23 24 24 25 26 27 27 27 : 110V 1 110V 110V 15A 2 3 23 24 4 ( ) 5 6 1 2 26 20 l 1 7 3 4 5 15 17 18 12 7~13 6 ~ 8 ~
第二頁 n n n n 增值稅稅率和徵收率 % 11% 17% 5% 3% 36 1
 國富浩華稅務 ( 香港 ) 有限公司 Crowe Horwath Tax Services (HK) Limited Member Crowe Horwath International 第 13 期 2016 年 8 月 1 日 中國快訊 中國全面推進 營改增 改革 陳維端先生 : +852 2894 6818 : charles.chan@crowehorwath.hk 譚建國先生 : +852
國富浩華稅務 ( 香港 ) 有限公司 Crowe Horwath Tax Services (HK) Limited Member Crowe Horwath International 第 13 期 2016 年 8 月 1 日 中國快訊 中國全面推進 營改增 改革 陳維端先生 : +852 2894 6818 : charles.chan@crowehorwath.hk 譚建國先生 : +852
jrc_tmp_ rpt
 本公司銷售聯博證券投資信託股份有限公司總代理之 聯博 - 全球不動產證券基金 A 股美元 所收取之通路報酬如下 : 台端支付的基金申購手續費為 3.00%, 其中本公司收取不多於 3.00% 台端支付的基金轉換手續費為 0.00%, 其中本公司收取不多於 0.00% 本基金經理費收入為年率 1.50%, 台端持有本基金期間, 本公司收取不多於年率 0.60 % 三 其他報酬 : 計算 : 聯博 -
本公司銷售聯博證券投資信託股份有限公司總代理之 聯博 - 全球不動產證券基金 A 股美元 所收取之通路報酬如下 : 台端支付的基金申購手續費為 3.00%, 其中本公司收取不多於 3.00% 台端支付的基金轉換手續費為 0.00%, 其中本公司收取不多於 0.00% 本基金經理費收入為年率 1.50%, 台端持有本基金期間, 本公司收取不多於年率 0.60 % 三 其他報酬 : 計算 : 聯博 -
 Special Issue 名 人 講 堂 專 題 研 究 保證金收取 合格之擔保品種類為何 非現金擔保品之折扣率 haircut 為何 CCP是否將會員所繳擔保品用於投資 其孳息是否回饋給會員 限制措施 焦 點 視 界 是否對會員之委託金額 信用 部位及風險訂定限額 會員是否必須對其客戶制定限額 洗價 mark-to-market 之時間及方法為何 結算交割 市 場 掃 描 交割週期 T+1或T+3
Special Issue 名 人 講 堂 專 題 研 究 保證金收取 合格之擔保品種類為何 非現金擔保品之折扣率 haircut 為何 CCP是否將會員所繳擔保品用於投資 其孳息是否回饋給會員 限制措施 焦 點 視 界 是否對會員之委託金額 信用 部位及風險訂定限額 會員是否必須對其客戶制定限額 洗價 mark-to-market 之時間及方法為何 結算交割 市 場 掃 描 交割週期 T+1或T+3
全民健康保險藥物給付項目及支付標準共同擬訂會議藥品部分第 20 次 (105 年 6 月 ) 會議議程時間 :105 年 6 月 16 日及 6 月 23 日 ( 星期四 ) 上午 9 時 30 分地點 : 衛生福利部中央健康保險署 18 樓禮堂主席 : 陳代理主席昭姿壹 主席致詞貳 前次會議決定及
 全民健康保險藥物給付項目及支付標準共同擬訂會議藥品部分第 20 次 (105 年 6 月 ) 會議會議資料 中華民國 105 年 6 月 16 日 中華民國 105 年 6 月 23 日 全民健康保險藥物給付項目及支付標準共同擬訂會議藥品部分第 20 次 (105 年 6 月 ) 會議議程時間 :105 年 6 月 16 日及 6 月 23 日 ( 星期四 ) 上午 9 時 30 分地點 : 衛生福利部中央健康保險署
全民健康保險藥物給付項目及支付標準共同擬訂會議藥品部分第 20 次 (105 年 6 月 ) 會議會議資料 中華民國 105 年 6 月 16 日 中華民國 105 年 6 月 23 日 全民健康保險藥物給付項目及支付標準共同擬訂會議藥品部分第 20 次 (105 年 6 月 ) 會議議程時間 :105 年 6 月 16 日及 6 月 23 日 ( 星期四 ) 上午 9 時 30 分地點 : 衛生福利部中央健康保險署
費率表
 - 個人投保 基本保障 - 未滿 15 足歲以下適用 5% 醫療費用限額 10% 醫療費用限額 5% 醫療費用限額 10% 醫療費用限額 5% 海外醫療費用限額 10% 海外醫療費用限額 單位 : 元 保險金額醫療費用海外醫療 1 日 2 日 3 日 4 日 5 日 6 日 7 日 8 日 9 日 10 日 11 日 12 日 13 日 14 日 15 日 16 日 17 日 18 日 19 日 20
- 個人投保 基本保障 - 未滿 15 足歲以下適用 5% 醫療費用限額 10% 醫療費用限額 5% 醫療費用限額 10% 醫療費用限額 5% 海外醫療費用限額 10% 海外醫療費用限額 單位 : 元 保險金額醫療費用海外醫療 1 日 2 日 3 日 4 日 5 日 6 日 7 日 8 日 9 日 10 日 11 日 12 日 13 日 14 日 15 日 16 日 17 日 18 日 19 日 20
untitled
 R ( ) .5..5 2.. 2.. 2 4 5 7 7 7 7 7 8 8 8 0 0 2 4 5 5 5 7 8 8 PC 0 安全注意事項及緊急處理方法 請務必遵守 警告 發生異常或故障時 應立即停止使用 拔 下電源插頭 恐會導致冒煙 起火 觸 電 異常或故障事例 即使接上電源開關有時也不會運轉 插拔電源線時 有時通電有時不通電 運轉中 有燒焦味或異音 本體部分變形或異常發熱 請立即連絡服務站進行檢查及修理
R ( ) .5..5 2.. 2.. 2 4 5 7 7 7 7 7 8 8 8 0 0 2 4 5 5 5 7 8 8 PC 0 安全注意事項及緊急處理方法 請務必遵守 警告 發生異常或故障時 應立即停止使用 拔 下電源插頭 恐會導致冒煙 起火 觸 電 異常或故障事例 即使接上電源開關有時也不會運轉 插拔電源線時 有時通電有時不通電 運轉中 有燒焦味或異音 本體部分變形或異常發熱 請立即連絡服務站進行檢查及修理
N S ( ) 9975 (852) (852)
 2015 N S 2 6 8 40 41 N S www.chinaunicom.com.hk ( ) 9975 (852) 2126 2018 (852) 2126 2016 董事長報告書 中國聯通 股 公司 年 年 公司 國 聯網 + 網絡 公司 合 年 年 公司 1,202.75.3% 網 8.8 68.3% 公司 年 EBITDA 504.6 5.8% EBITDA 42.0%4.4 69.9
2015 N S 2 6 8 40 41 N S www.chinaunicom.com.hk ( ) 9975 (852) 2126 2018 (852) 2126 2016 董事長報告書 中國聯通 股 公司 年 年 公司 國 聯網 + 網絡 公司 合 年 年 公司 1,202.75.3% 網 8.8 68.3% 公司 年 EBITDA 504.6 5.8% EBITDA 42.0%4.4 69.9
10 AC TERNIBIN F.C. TABLETS 250MG GEFITINIB MG 中化新豐工廠 本品項原經 105 年 12 月共擬會議決議核予每粒 925 元, 因核價參考品依價量協議檢討結果調整支付價, 新藥價自 106 年 4 月
 項次健保代碼藥品名稱成分及含量規格量藥商名稱原支付價初核價格初核說明生效日期適應症 1 TPN2009299 TPN-1(1207ML) 1ML -- 0.37 依 全民健康保險藥物給付項目及支付標準 全靜脈營養輸液 ( 以下簡稱 TPN) 核價原則計算, 暫予 支付每 ML 0.37 元 : (108/200 400)+(67/400 400)+(67/400 400)+(95/10 2)+(63/4
項次健保代碼藥品名稱成分及含量規格量藥商名稱原支付價初核價格初核說明生效日期適應症 1 TPN2009299 TPN-1(1207ML) 1ML -- 0.37 依 全民健康保險藥物給付項目及支付標準 全靜脈營養輸液 ( 以下簡稱 TPN) 核價原則計算, 暫予 支付每 ML 0.37 元 : (108/200 400)+(67/400 400)+(67/400 400)+(95/10 2)+(63/4
雲南水務投資股份有限公司 Yunnan Water Investment Co., Limited* 於中華人民共和國註冊成立的股份有限公司 全球發售 全球發售的發售股份數目 287,521,000 股 H 股股份 視乎超額配股權行使與否而定 香港發售股份數目 28,754,000 股 H 股股份
 2015 5 13 1933 H 571 H 2015 6 17 H H 1 雲南水務投資股份有限公司 Yunnan Water Investment Co., Limited* 於中華人民共和國註冊成立的股份有限公司 全球發售 全球發售的發售股份數目 287,521,000 股 H 股股份 視乎超額配股權行使與否而定 香港發售股份數目 28,754,000 股 H 股股份 可予調整 國際發售股份數目
2015 5 13 1933 H 571 H 2015 6 17 H H 1 雲南水務投資股份有限公司 Yunnan Water Investment Co., Limited* 於中華人民共和國註冊成立的股份有限公司 全球發售 全球發售的發售股份數目 287,521,000 股 H 股股份 視乎超額配股權行使與否而定 香港發售股份數目 28,754,000 股 H 股股份 可予調整 國際發售股份數目
信託基金 ( 本基金主要係投資於非投資等級之高風險債券且基金之配息來源可能為本金 ) 國泰亞洲成長證券投資信託基金國泰歐洲精選證券投資信託基金 國泰中國高收益債券證券投資信託基金 ( 本基金主要係投資於非投資等級之高風險債券且基金之配息來源可能為本金 ) 國泰亞太入息平衡證券投資信託基金 ( 本基金
 國泰證券投資信託股份有限公司公告 日期 : 中華民國 105 年 10 月 6 日文號 :105 國泰投信系字第 0000000878 號 主旨 : 公告各基金投資資產 股票或債券達一定比例之主要投資所在國或地區及其次一季例假日 說明 : 一 依據各基金信託契約及公開說明書規定之公告方式辦理, 各項依據如下 : 基金依據主要投資所在國或地區定義 國泰全球環保趨勢證券投資信託基金國泰中港台證券投資信託基金國泰新興市場證券投資信託基金國泰全球資源證券投資信託基金國泰中國內需增長證券投資信託基金國泰新興高收益債券證券投資信託基金
國泰證券投資信託股份有限公司公告 日期 : 中華民國 105 年 10 月 6 日文號 :105 國泰投信系字第 0000000878 號 主旨 : 公告各基金投資資產 股票或債券達一定比例之主要投資所在國或地區及其次一季例假日 說明 : 一 依據各基金信託契約及公開說明書規定之公告方式辦理, 各項依據如下 : 基金依據主要投資所在國或地區定義 國泰全球環保趨勢證券投資信託基金國泰中港台證券投資信託基金國泰新興市場證券投資信託基金國泰全球資源證券投資信託基金國泰中國內需增長證券投資信託基金國泰新興高收益債券證券投資信託基金
(03) (03) (03) (03) (03)
 6147 R049 232524 CHIPBOND Technology Corporation 年報資訊申報網址 :http://sii.tse.com.tw 年報資訊查詢網址 ( 公開資訊觀測站 ):http://mops.tse.com.tw/ 中華民國九十二年五月三十一日刊印 (03)567-8788 davidc@chipbond.com.tw (03)567-8788 kulongc@chipbond.com.tw
6147 R049 232524 CHIPBOND Technology Corporation 年報資訊申報網址 :http://sii.tse.com.tw 年報資訊查詢網址 ( 公開資訊觀測站 ):http://mops.tse.com.tw/ 中華民國九十二年五月三十一日刊印 (03)567-8788 davidc@chipbond.com.tw (03)567-8788 kulongc@chipbond.com.tw
全民健康保險藥事小組第6屆第20次會議紀錄
 全民健康保險藥事小組第 8 屆第 17 次 (99 年 8 月 ) 會議紀錄時間 :99 年 8 月 5 日上午 9 時 15 分地點 : 中央健康保險局 9 樓第 1 會議室主席 : 陳召集人燕惠紀錄 : 何容甄壹 主席致詞貳 上次會議紀錄確認參 報告事項報告案一 案由 : 全民健康保險藥事小組待審議案件進度報告 決定 : 洽悉 報告案二 案由 : 有關通盤檢討 全民健康保險藥品給付規定 中 限許可證已核准適應症之藥品
全民健康保險藥事小組第 8 屆第 17 次 (99 年 8 月 ) 會議紀錄時間 :99 年 8 月 5 日上午 9 時 15 分地點 : 中央健康保險局 9 樓第 1 會議室主席 : 陳召集人燕惠紀錄 : 何容甄壹 主席致詞貳 上次會議紀錄確認參 報告事項報告案一 案由 : 全民健康保險藥事小組待審議案件進度報告 決定 : 洽悉 報告案二 案由 : 有關通盤檢討 全民健康保險藥品給付規定 中 限許可證已核准適應症之藥品
SOP Waiting Time
 專科門診 for Stable New Bookings at Specialist Out-patient Clinics 2017 年 10 月 1 日至 2018 年 9 月 30 日 1 October 2017 30 September 2018 專科門診診所實施分流制度 22201820182018, 確保病情緊急並需要及早診治的病人獲得優先跟進及治療 新轉介個案通常先由護士甄別, 再經有關專科醫生覆核,
專科門診 for Stable New Bookings at Specialist Out-patient Clinics 2017 年 10 月 1 日至 2018 年 9 月 30 日 1 October 2017 30 September 2018 專科門診診所實施分流制度 22201820182018, 確保病情緊急並需要及早診治的病人獲得優先跟進及治療 新轉介個案通常先由護士甄別, 再經有關專科醫生覆核,
簡明綜合損益表 未經審核 截至九月三十日止六個月 二零一八年 千港元 2 3,110,500 2,932,492 (2,799,721) (2,646,033) 310, ,459 25,697 27,522 (104,374) (100,775) (124,282) (117,822)
 SAMSON PAPER HOLDINGS LIMITED 森信紙業集團有限公司 * ( 股份代號 :731) 截至二零一八年九月三十日止六個月之中期業績公佈 1 簡明綜合損益表 未經審核 截至九月三十日止六個月 二零一八年 千港元 2 3,110,500 2,932,492 (2,799,721) (2,646,033) 310,779 286,459 25,697 27,522 (104,374)
SAMSON PAPER HOLDINGS LIMITED 森信紙業集團有限公司 * ( 股份代號 :731) 截至二零一八年九月三十日止六個月之中期業績公佈 1 簡明綜合損益表 未經審核 截至九月三十日止六個月 二零一八年 千港元 2 3,110,500 2,932,492 (2,799,721) (2,646,033) 310,779 286,459 25,697 27,522 (104,374)
<4C50352D B971B8A3B35DB3C6A655B2D5A9FAB2D32E786C73>
 [ 回中信局首頁 ] 一般型電腦 Pentium Gold G00(Windows 作業系統 )( 獨立主機不含螢幕 ) acer eriton M660G (0/0/)] NT$,00 一般型電腦 Pentium Gold G00(Windows 作業系統 )( 獨立主機不含螢幕 ) ASUS M60MB 90(0/08/0)] NT$,00 一般型電腦 Pentium Gold G00(Windows
[ 回中信局首頁 ] 一般型電腦 Pentium Gold G00(Windows 作業系統 )( 獨立主機不含螢幕 ) acer eriton M660G (0/0/)] NT$,00 一般型電腦 Pentium Gold G00(Windows 作業系統 )( 獨立主機不含螢幕 ) ASUS M60MB 90(0/08/0)] NT$,00 一般型電腦 Pentium Gold G00(Windows
關於我們 , ,600 2, 目錄
 2018 INTERIM REPORT 關於我們 2002 3 2,000 2018 6 3020 1,600 2,700 2 9 10 12 12 12 17 23 23 23 24 25 目錄 26 27 28 30 31 32 69 70 業務回顧 ( 除另有說明外, 所有金額均以港元列示 ) 業 2018 6 30 ( 報告期 ), 有 EBITDAEBITDA 期 6 30 2018 2017
2018 INTERIM REPORT 關於我們 2002 3 2,000 2018 6 3020 1,600 2,700 2 9 10 12 12 12 17 23 23 23 24 25 目錄 26 27 28 30 31 32 69 70 業務回顧 ( 除另有說明外, 所有金額均以港元列示 ) 業 2018 6 30 ( 報告期 ), 有 EBITDAEBITDA 期 6 30 2018 2017
惠理基金管理香港有限公司香港中環干諾道中四十一號盈置大廈九樓電話 :(852) 傳真 :(852) 電子郵箱 網址 :www.valuepartners.com.hk 本半年度報告之中英文內容如有歧義, 概以英文版本為準 本報告並
 A 2015 惠理基金管理香港有限公司香港中環干諾道中四十一號盈置大廈九樓電話 :(852) 2880 9263 傳真 :(852) 2565 7975 電子郵箱 :vpl@vp.com.hk 網址 :www.valuepartners.com.hk 本半年度報告之中英文內容如有歧義, 概以英文版本為準 本報告並不構成要約銷售或邀請購買任何基金單位 投資者在作出投資決定前, 請參閱有關基金章程, 並應參考基金最新之半年度及年度報告作補充資料
A 2015 惠理基金管理香港有限公司香港中環干諾道中四十一號盈置大廈九樓電話 :(852) 2880 9263 傳真 :(852) 2565 7975 電子郵箱 :vpl@vp.com.hk 網址 :www.valuepartners.com.hk 本半年度報告之中英文內容如有歧義, 概以英文版本為準 本報告並不構成要約銷售或邀請購買任何基金單位 投資者在作出投資決定前, 請參閱有關基金章程, 並應參考基金最新之半年度及年度報告作補充資料
選擇學校午膳供應商手冊適用於中、小學 (2014年9月版)
 2014 年 9 月版 選擇 學校午膳供應商手冊 適用於中 小學 i 1 1 2 3 4 5 6 7 8 9 1 2 2 i. ii. iii. iv. v. i. ii. iii. iv. v. vi. vii. 3 i. ii. iii. iv. v. 4 i. ii. 1. 2. 3. 4. 5. iii. iv. 5 6 3 4 5 6 i. ii. i. ii. iii. iv. v.
2014 年 9 月版 選擇 學校午膳供應商手冊 適用於中 小學 i 1 1 2 3 4 5 6 7 8 9 1 2 2 i. ii. iii. iv. v. i. ii. iii. iv. v. vi. vii. 3 i. ii. iii. iv. v. 4 i. ii. 1. 2. 3. 4. 5. iii. iv. 5 6 3 4 5 6 i. ii. i. ii. iii. iv. v.
附件十八之一運輸類飛機廣布性疲勞損傷檢查符合期限及使用限制 本附件依第一百四十四條之一之規定及參考 FAR 及 訂定 1. 航空器使用人以下列飛機營運者, 應於下表符合期限前將含機體使用限制之適航限制項目納入維護計畫 2. 機體使用限制於下表符合期限前仍未取
 附件十八之一運輸類飛機廣布性疲勞損傷檢查符合期限及使用限制 本附件依第一百四十四條之一之規定及參考 FAR 26.21 26.23 及 121.1115 訂定 1. 航空器使用人以下列飛機營運者, 應於下表符合期限前將含機體使用限制之適航限制項目納入維護計畫 2. 機體使用限制於下表符合期限前仍未取得設計國民航主管機關核准時, 應依下表所列預設機體使用限制辦理 3. 已將設計國民航主管機關核准之機體使用限制延展,
附件十八之一運輸類飛機廣布性疲勞損傷檢查符合期限及使用限制 本附件依第一百四十四條之一之規定及參考 FAR 26.21 26.23 及 121.1115 訂定 1. 航空器使用人以下列飛機營運者, 應於下表符合期限前將含機體使用限制之適航限制項目納入維護計畫 2. 機體使用限制於下表符合期限前仍未取得設計國民航主管機關核准時, 應依下表所列預設機體使用限制辦理 3. 已將設計國民航主管機關核准之機體使用限制延展,
900??indd
 900 432 中華民國一 二年七月十六日 中鋼半月刊 第九版 六月份公司業務概況 八 碳鋼產量 六九九 七 三公噸 碳 鋼銷量 七三六 九公噸 合併營收 二五 八七五 一七五千元 福利金收支統計 項 福 利 資 訊 請 參 閱 EIP 快速選 單 總務福利資訊平台 本公司福委會一 二年六月 份福利金收入及各項補助之人 數 金額統計如下表 至於各 一 二年合併累計營收 二千元 一七三 一五五
900 432 中華民國一 二年七月十六日 中鋼半月刊 第九版 六月份公司業務概況 八 碳鋼產量 六九九 七 三公噸 碳 鋼銷量 七三六 九公噸 合併營收 二五 八七五 一七五千元 福利金收支統計 項 福 利 資 訊 請 參 閱 EIP 快速選 單 總務福利資訊平台 本公司福委會一 二年六月 份福利金收入及各項補助之人 數 金額統計如下表 至於各 一 二年合併累計營收 二千元 一七三 一五五
LCIDC01_ doc
 華郵政臺字第㆕㈨㈦號執照登記認為第㆒類新聞紙類 華民國㈨㈩㆒年㈩㆒ ㆓㈩ (星期㆔)版出㈥. ㆔期星每卷㆒㈩㈨第期㈦㈩㈥第發行零售全年訂購處 址電話立法院公報處每冊新臺幣㈧ 元計㈧ 期㈧折優待立法院公報處 山南路㆒號㆓㆔㈤㈧㈤㆔㈤㆓頁次立法院第㈤屆第㆓會期第㈧次會議紀錄對行政院院長施政報告繼續質詢 繼續質詢 (㆕㈨ ㆓㈤㈧)國是論壇 (㆔㈤㈦ ㆔㈥㈧)立法院第㈤屆第㆓會期第㈦次會議議事錄 (㆔㈥㈨
華郵政臺字第㆕㈨㈦號執照登記認為第㆒類新聞紙類 華民國㈨㈩㆒年㈩㆒ ㆓㈩ (星期㆔)版出㈥. ㆔期星每卷㆒㈩㈨第期㈦㈩㈥第發行零售全年訂購處 址電話立法院公報處每冊新臺幣㈧ 元計㈧ 期㈧折優待立法院公報處 山南路㆒號㆓㆔㈤㈧㈤㆔㈤㆓頁次立法院第㈤屆第㆓會期第㈧次會議紀錄對行政院院長施政報告繼續質詢 繼續質詢 (㆕㈨ ㆓㈤㈧)國是論壇 (㆔㈤㈦ ㆔㈥㈧)立法院第㈤屆第㆓會期第㈦次會議議事錄 (㆔㈥㈨
創業板之特色 ii 釋義 預期時間表
 閣下如 有任何疑問 閣下如已 本公司 售出或轉讓 RUI KANG PHARMACEUTICAL GROUP INVESTMENTS LIMITED 銳康藥業集團投資有限公司 ( 股份代號 :8037) 建議股份合併及股東特別大會通告 69 2 SGM-1 SGM-2 48 33 A18 7 www.hkgem.com www.ruikang.com.hk 創業板之特色....................................................
閣下如 有任何疑問 閣下如已 本公司 售出或轉讓 RUI KANG PHARMACEUTICAL GROUP INVESTMENTS LIMITED 銳康藥業集團投資有限公司 ( 股份代號 :8037) 建議股份合併及股東特別大會通告 69 2 SGM-1 SGM-2 48 33 A18 7 www.hkgem.com www.ruikang.com.hk 創業板之特色....................................................
Chinasoft International Limited 中軟國際有限公司 * 於開曼群島註冊成立之有限公司 股份代號 0354 * 僅供識別
 Chinasoft International Limited * 於開曼群島註冊成立之有限公司 股份代號 0354 * 僅供識別 1 內容.......................................................... 2...................................................... 3...................................................
Chinasoft International Limited * 於開曼群島註冊成立之有限公司 股份代號 0354 * 僅供識別 1 內容.......................................................... 2...................................................... 3...................................................
 2 4 5 23 34 43 44 47 92 1. CRRC Corporation Limited CRRC 2. 16 16 010-51862188 010-51862188 010-63984785 010-63984785 crrc@crrcgc.cc crrc@crrcgc.cc 3. 16 100036 16 100036 www.crrcgc.cc crrc@crrcgc.cc 4.
2 4 5 23 34 43 44 47 92 1. CRRC Corporation Limited CRRC 2. 16 16 010-51862188 010-51862188 010-63984785 010-63984785 crrc@crrcgc.cc crrc@crrcgc.cc 3. 16 100036 16 100036 www.crrcgc.cc crrc@crrcgc.cc 4.
Microsoft Word
 141 102 9 25 146 1 8... 1... 2 40 1... 6 2 5... 10... 11... 12 19 1... 12 2 1 1... 14 9 4 1... 15 壽險訊息第 141 期 1 一 金融監督管理委員會令示保險業依保險法第 146 條第 1 項第 8 款規定投資不動產信託受益權之相關規範 102 8 29 10202508001 twbbb twbbb
141 102 9 25 146 1 8... 1... 2 40 1... 6 2 5... 10... 11... 12 19 1... 12 2 1 1... 14 9 4 1... 15 壽險訊息第 141 期 1 一 金融監督管理委員會令示保險業依保險法第 146 條第 1 項第 8 款規定投資不動產信託受益權之相關規範 102 8 29 10202508001 twbbb twbbb
