<4D F736F F D D313032ABFCA6D2A4C6BEC7A6D2B8D5BBA1A9FA5FA977BD5A5F2E646F63>
|
|
|
- 娥 昝
- 5 years ago
- Views:
Transcription
1 大學入學考試中心 指定科目考試 考試說明 ( 適用於 99 課綱 ) 中華民國 100 年 9 月 版權所有
2
3 指定科目考試化學考試說明 目 錄 壹 測驗目標... 1 貳 測驗內容... 參 試題舉例... 附件一 指定科目考試測驗內容 附件二 化學科 99 課綱與 95 暫綱的差異... 4
4
5 指定科目考試考試說明 民國 10 年開始, 指定科目考試 將依據 99 學年度實施之 普通高級中學課程綱要 ( 簡稱 99 課綱 ) 命題 1 本考試說明即針對實施 99 課綱後, 施測之指定科目考試, 說明命題方向與 99 課綱的關係, 俾使學生準備考試有所參考 本說明分成幾個重點, 分別是測驗目標 試題舉例 指定科目考試測驗內容 ( 附件一 ) 化學科 99 課綱與 95 暫綱的差異 ( 附件二 ) 壹 測驗目標 測驗目標是希望藉由不同的評量方式, 測量出考生的學習成果 不同課程的教學目標之間或有差異, 但一般教學的目標均包括下述學習成果 : 知識 推理思考的能力 實驗或實作技能 與他人溝通的能力 態度 興趣與鑑賞等 從化學科的角度而言, 是希望能夠測驗高中生下列四項在化學方面的學習成果 : 1. 基本知識與概念. 實驗技能 3. 推理與思考能力 4. 應用知識的能力指定科目考試的測驗目標及細目如下 : 一 測驗考生的基本化學知識與概念 1a. 基本的化學名詞 定義及現象 1b. 基本的化學規則 學說及定律二 測驗考生的基礎實驗技能 a. 化學實驗儀器 裝置的認識及操作 b. 化學實驗之觀察 記錄 分析及解釋能力 c. 化學實驗的安全 衛生及環保的認識及執行 1 99 學年度實施之 普通高級中學課程綱要 於民國 97 年 1 月 4 日發布, 係由 95 學年度實施之 普通 高級中學課程暫行綱要 ( 簡稱 95 暫綱 ) 修訂而成 1
6 三 測驗考生的推理與思考能力 3a. 理解化學資料的能力 3b. 化學計算的能力 3c. 分析 歸納 演繹及創造的能力 3d. 設計實驗以解決問題的能力四 測驗考生應用化學知識的能力 4a. 瞭解化學與生活之關係 4b. 瞭解化學與其他學科的關係 4c. 應用化學原理解決問題的能力 貳 測驗內容 指定科目考試的考試範圍包括基礎化學 ( 一 ) 基礎化學( 二 ) 基礎化學 ( 三 ) 選修化學與選修化學實驗 本中心所研擬的指定科目考試的測驗內容, 是將 99 課綱化學科的基礎化學 ( 一 ) 基礎化學( 二 ) 基礎化學( 三 ) 選修化學與選修化學實驗內容重新安排整理而得 參 試題舉例 一 測驗考生的基本化學知識與概念 例 1. 下列何者不能作為布 洛 (Brønsted-Lowry) 酸? (A) NH + 4 (B) HO 參考答案 :D 測驗目標 :1a. 基本的化學名詞 定義及現象 (C) HSO 3 (D) HPO (E) CH3COOH 測驗內容 : 選修化學物質性質四 水溶液中酸 鹼 鹽的平衡 說明 : (100 年度研究用試卷 ) + 依據布 洛酸鹼理論, 布 洛酸需要能釋放出質子, 選項中的 (A) NH 4 (B) HO (C) HSO 3 及 (E) CH3COOH 均可釋出 H +, 分別產生 NH 3 OH SO 3 及 (D) HPO 是次磷酸 H3PO 釋出 H + 所得到的共軛酸根, H 3 PO 僅有一 個 H 連接在 O 上 ( 如右圖所示 ), 另兩個 H 鍵結在 P 上, 無法以 H + 釋 出, 因此 (D) 為正確解答 CH3COO 而
7 例. 下列有關反應熱及物質能量轉換的敘述, 何者正確? (A) 一莫耳的純物質, 由液體汽化為氣體所需的熱量, 少於其由氣體凝結為液體所放出的熱量 (B) 有一化學反應, 其生成物的莫耳生成熱比反應物的莫耳生成熱小, 則此反應為吸熱反應 (C) 二氧化碳溶於水的莫耳溶解熱等於二氧化碳的莫耳凝結熱 (D) 二氧化碳的莫耳生成熱等於石墨的莫耳燃燒熱 (E) 二氧化碳的莫耳汽化熱等於乾冰的莫耳昇華熱 (98 學年度指考 ) 參考答案 :D 測驗目標 :1a. 基本的化學名詞 定義及現象測驗內容 : 選修化學物質狀態六 液態與溶液說明 : 各選項的說明如下 : (A) 一莫耳的純物質, 由液體汽化為氣體所需的熱量稱為莫耳汽化熱, 由氣體凝結為液體所放出的熱量稱為莫耳凝結熱, 兩者應該相等 (B) 化學反應的反應熱定義為 : 反應熱 =( 生成物的莫耳生成熱總和 )-( 反應物的莫耳生成熱總和 ), 依題意反應熱為負值, 所以是放熱反應 (C) 二氧化碳的莫耳凝結熱, 是指二氧化碳由氣體轉變成液態二氧化碳, 即 : CO(g) CO(l) 所放出的熱 二氧化碳溶於水, 即 : CO (g) CO (aq) 的莫耳溶解熱 ; 這兩者的熱量不同 (D) 二氧化碳的莫耳生成熱, 是指一莫耳二氧化碳, 由其最安定的成分元素反應生成時, 也就是 C(s, 石墨 ) + O(g) CO (g) 的能量的變化, 正好等於石墨的莫耳燃燒熱 因此,(D) 為正確解答 (E) 二氧化碳的莫耳汽化熱是二氧化碳液態變為氣態 : CO (l) CO (g) 所需要的熱量, 與乾冰的昇華是二氧化碳液態變為氣態 : CO (s) CO (g) 所需要的熱量不同, 兩者有所不同 例 3. 下列有關於週期表的敘述, 哪些正確? (A) 同一週期的氧化物水溶液酸性的趨勢, 大致為由左至右逐漸增加 (B) 類金屬的化學性質介於金屬與非金屬之間, 又稱為過渡金屬 (C) 週期表 A 族的元素, 其價電子數與所屬的族數相同 (D) 鹵族元素的電負度由上而下漸增 (E) 同一週期元素第一游離能的趨勢, 大致為隨原子序的增加而降低 (100 年度研究用試卷 ) 3
8 參考答案 :ACE 測驗目標 :1b. 基本的化學規則 學說及定律測驗內容 : 基礎化學 ( 一 ) 物質基本構造二 原子構造與元素週期表說明 : 本題選項 (B) 與 (D) 有錯誤, 選項 (B) 類金屬不是過渡金屬, 選項 (D) 中鹵族元素的電負度應該由上而下漸減 因此, 選項 (A) (C) (E) 的敘述正確 二 測驗考生的基礎實驗技能例 4. 於某實驗室中, 欲以下述反應製備化合物丙 首先, 將化合物甲與化合物乙溶於硫酸後, 並劇烈攪拌 然後, 將反應瓶加熱至 65, 反應過程中會有一紅棕色氣體, 不斷自儀器戊頂端冒出 為實驗的安全, 會將該氣體導入錐形瓶中, 與瓶中的飽和硫代硫酸鈉溶液作用 待反應完成後, 將雙頸瓶中的內容物經處理得固體丙, 反應式與實驗裝置如圖二與圖三所示 O O I OH + KBrO 3 H SO 4 OH I O O 甲乙丙 圖二 庚 己 戊 圖三 飽和 Na S O 3 水溶液 試根據上述實驗, 回答下列問題 : (1) 寫出化合物甲的苯環上兩種官能基名稱? () 化合物乙 ( KBrO ) 中 Br 的氧化數為何? 3 (3) 反應產生的紅棕色氣體為何? (4) 在錐形瓶中, 紅棕色氣體反應後所得的生成物為何? (5) 儀器戊的名稱為何? 儀器戊中冷水的入口端為何處? (100 年度研究用試卷 ) 4
9 參考答案 : (1) 化合物甲的官能基為羧基與鹵化物, 羧基亦可寫羧酸, 鹵化物亦可寫碘化物 () KBrO 3 中 Br 的氧化數, 可由右式推得 :1+ x 6 = 0 x = + 5 (3) 紅棕色的氣體為 Br (4) 反應所得的生成物 Br, 即溴離子 (5) 儀器戊是冷凝管 冷水應由下方, 即己的方向注入 測驗目標 :1a. 基本的化學名詞 定義及現象 a. 化學實驗儀器 裝置的認識及操作 3a. 理解化學資料的能力 測驗內容 : 基礎化學 ( 一 ) 物質變化四 常見的化學反應 說明 : 基礎化學 ( 二 ) 含碳元素的物質二 有機化合物 本題是藉由有機化合物的反應, 來測驗考生對氧化還原的了解, 屬於課程綱要中的 有機化合物 氧化還原反應 無機化合物與化學實驗的綜合內容 三 測驗考生的推理與思考能力例 5. 水的相變化如圖一所示, 下列敘述哪些正確? 甲 (A) 甲點為三相點, 在此壓力與溫度的條件下, 水的三態共存 (B) 乙點表示水的氣態與液態共存 (C) 在乙點時, 若壓力維持 1 大氣壓, 但增高溫度, 水將變為液態 (D) 將冰維持在 3 毫米汞柱壓力下, 但增高溫度, 則冰會昇華 (E) 當固態與液態共存時, 增大壓力, 水的溫度隨之增加 (100 年度研究用試卷 ) 參考答案 :ABD 5
10 測驗目標 :3a. 理解化學資料的能力測驗內容 : 選修化學物質狀態六 液態與溶液說明 : 本題測試考生對水的相變化之理解, 包括三相點, 任二態共存曲線隨溫度與壓力的變化, 以及產生昇華的條件 本題的答案皆可藉由圖表的理解而推得, 避免考生死背這些內容 例 6. 王同學取.00 克的柳酸 ( 分子量 =138) 與 4.00 毫升的乙酐 ( 分子量 =10, 比重 =1.08), 在濃硫酸的催化下反應, 所得產物經純化 再結晶及烘乾後, 得到 1.80 克的阿司匹靈 柳酸與乙酐反應生成阿司匹靈的反應式如下 : H 3 C O O OH O H 3 C 濃 H + SO 4 OH O + OH H 3 C O O O 柳酸乙酐阿司匹靈 CH 3 COOH 試問 : 參考答案 : 1. 理論上, 本實驗最多可產生多少克的阿司匹靈?. 王同學在本實驗所得的產率為何 (%)? 3. 本實驗完成後, 可取出少許產物, 以 1% 氯化鐵溶液 ( FeCl 溶液呈藍紫色, 則其所含的不純物為何? 1. 由反應 : 柳酸 + 乙酐 阿司匹靈 + 乙酸, 需先求何者為限量試劑 柳酸莫耳數 : (mol) 138 = 乙酐莫耳數 : = (mol) 10 故知柳酸為限量試劑 阿司匹靈理論產量 : =.61 (g). 產率 : % 68.9% 69%.61 = 3( aq) ), 檢驗其純度 若 ( 改寫自 96 學年度指考 ) 3. 氯化鐵是用來檢測產物中是否殘留柳酸, 柳酸會與鐵離子產生藍紫色的錯合物 6
11 測驗目標 :a. 化學實驗儀器 裝置的認識及操作 b. 化學實驗之觀察 記錄 分析及解釋能力 3b. 化學計算的能力測驗內容 : 基礎化學 ( 一 ) 物質變化三 化學反應選修化學實驗 10. 化學合成說明 : 本題是屬於課程綱要中化學反應計量 限量試劑 產率 有機化合物的結構與反應的內容 例 7. 將反應物 A 和 B 各 0.040M 置於一密閉容器中, 使其反應生成 C, 反應過程中各 物種濃度隨時間的變化如圖 4 所示 濃度 (M ) A C B 時間 ( 時 ) 圖 4 下列有關此反應之敘述何者正確? (A) 此反應可表示為 A + 3B C (B) 當 B 和 C 的濃度相同時,A 的濃度約為 0.03M (C) 此反應初速率的絕對值大小順序為 B>C>A 4 (D) 此反應之平衡常數約為 ( 係數為最簡單整數者 ) (E) 在圖中 B 和 C 的交點處,B 的消耗速率與 C 的形成速率相同 (98 學年度指考 ) 參考答案 :ABCD 測驗目標 :3a. 理解化學資料的能力 3b. 化學計算的能力 3c. 分析 歸納 演繹及創造的能力測驗內容 : 基礎化學 ( 三 ) 物質變化二 化學反應速率三 化學平衡 7
12 說明 : 各選項說明如下 : (A) 反應物 A 與 B 各 0.040M 置於一密閉容器中, 達平衡時, (B) A 用去 = (M),B 用去 = (M),C 產生 0.00M, 因此, aa + bb cc 的係數比 a : b : c = 1: 3:, 選項 (A) 正確 由 A + 3B C 初 中 x -3x +x 後 0.04-x x x 在 [B] = [C] 時, 即 x = x, 解出 x = 0.008, 所以,[A] = 0.04 x = = 0.03, 選項 (B) 正確 (C) 若 A,B 及 C 的初速率分別為 R B R A, ( )M ( )M = ; R C = 0小時 0小時 R B 及 R C, 則 R, 故 R A : R B : RC = 1:3: 初速率大小的順序為 RB > RC > RA, 選項 (C) 正確 [ ] [ ][ ] C (0.0) 4 (D) 此反應之平衡常數 K = = = 10 = A B (0.03)(0.01) 3 A 4 4 ( )M = ; 0小時 (E) 對此反應而言, R A : R B : R C = 1:3:, 所以,B 的消耗速率與 C 的形成速率比為 3:, 兩者並不相同 根據以上 (A) 至 (E) 的敘述可知, 本題答案為 (A)(B)(C)(D) 例 8. 以 MnO 催化 KClO 3 熱分解產生氧氣的反應式如下 : KClO 3O + KCl MnO 3(s) (g) (s) 雖然上列反應極近於完全, 但不是唯一的反應, 亦即尚有少量的副反應, 導致所產 出的氣體有異常的氣味 為了探究臭味的成分, 做了下列的實驗 : (1) 將產生的氣體通過潤濕的碘化鉀 - 澱粉試紙 ( 如圖 4), 結果試紙顯現紫藍色 KClO 3 +MnO 8 橡皮管 圖 4 潤濕的 KI- 澱粉試紙
13 () 將產生的氣體通過硝酸銀溶液, 則產生白色沉澱 (3) 所產生的氣體經質譜儀分析, 在複雜的質譜圖中, 有質量尖峰 ( 相當於分子量 ) 出現在 67 與 69 的位置, 而其強度比約為 3:1 試問依上述實驗結果, 能夠確認在熱分解 KClO 3 時, 所逸出的氣體中有下列哪些 物質? (A) 氧氣 (B) 氯氣 (C) 臭氧 (D) 氯化鉀 參考答案 :ABE (E) 二氧化氯 測驗目標 :1b. 基本的化學規則 學說及定律 b. 化學實驗之觀察 記錄 分析及解釋能力 3c. 分析 歸納 演繹及創造的能力 測驗內容 : 基礎化學 ( 一 ) 物質基本組成一 物質的組成 說明 : 各選項說明如下 : ( 改寫自 99 學年度指考 ) MnO (A) 題幹已說明此一反應為製氧的反應, KClO 3O + KCl 生 選項 (A) 正確 3(s) (g) (s), 故有氧產 (B) 此反應中會產生氯氣, 氯氣的來源是由於不穩定的 ClO, ClO 分解會產生 Cl ClO Cl + O 氯氣溶於水會產生氯離子, 與硝酸銀作用, 產生白色沉澱, 反應如下 : + + Cl + HO Cl + H + ClO ; Cl +Ag AgCl 選項 (B) 正確 (C) 臭氧的生成, 在題幹所給予的條件不會生成, 必須是氧氣在高壓放電, 或是在紫外 線的照射下, 才可能生成臭氧, 本實驗並未提供相關的反應條件, 故不會有臭氧的 產生 選項 (C) 錯誤 (D) KCl 為固體, 不會以氣體狀態逸出 選項 (D) 錯誤 (E) 氯的同位素有 35 Cl 與 37 Cl, 因此, ClO 的分子量也有兩種, 分別是 : = 67 與 = 69 ; 此外, 35 Cl 與 37 Cl 的存量比為 75%:5%, 符合質譜儀分析的尖峰強 度 3:1 且 ClO 具氧化力, 可使潤濕的碘化鉀 - 澱粉試紙變色 選項 (E) 正確 9
14 四 測驗考生應用化學知識的能力例 9. 下列分子, 哪一個屬於多氯聯苯化合物? (A) (B) (C) (D) (E) (99 學年度指考 ) 參考答案 :C 測驗目標 :1a. 基本的化學名詞 定義及現象 4a. 瞭解化學與生活之關係測驗內容 : 基礎化學 ( 二 ) 含碳元素的物質二 有機化合物說明 : 此題評量考生對多環芳香族化合物名稱的了解, 聯苯 - 為二個苯環與角 - 角方式連接而成, 並非以邊 - 邊方式聯結 ( 此為稠聯 ) 各選項說明如下: (A) 為苯的衍生物 ; (B) 為萘的衍生物 ( 一種稠聯 ); (C) 為聯苯的衍生物 ; (D) 為菲的衍生物 ; (E) 為蔥的衍生物 例 10. 國內媒體曾報導, 有些新裝潢的房間或新購買的玩具, 其所用的聚合物材料會逸 出有害健康的物質 試問下列哪一物質, 最有可能從聚合物逸出? (A) 甲醇 (B) 甲醛 (C) 乙醇 (D) 乙酸 (E) 塑化劑 ( 改寫自 98 學年度指考 ) 參考答案 :BE 測驗目標 :c. 化學實驗的安全 衛生及環保的認識及執行 4a. 瞭解化學與生活之關係 測驗內容 : 基礎化學 ( 二 ) 含碳元素的物質二 有機化合物 10
15 說明 : 各選項說明如下 : (A) 甲醇, 雖然甲醇具毒性但並非常見聚合物的單體 (B) 甲醛, 為尿素甲醛聚合物的單體, 可從新的塑料中釋放出, 而甲醛亦具毒性 (C) 乙醇, 並非常見聚合物的單體 (D) 乙酸, 並非常見聚合物的單體 (E) 塑化劑, 可能會出現於一般塑膠製成的玩具, 並有害人體健康 例 11. 實驗桌上有五支標明 1-5 的試管, 含有未知成分的溶液, 只知其可能為氯化鈉溶 液 溴化鈉溶液 碘化鈉溶液 乙醇的正己烷溶液 乙炔的正己烷溶液 某生進 行實驗測試, 以 + 表示有反應發生, - 表示沒有反應, 空白為未測試, 得到 的結果歸納如下表 測試 試管 AgNO3( aq ) MnO( s ) Cl( aq ) Br / CCl KMnO 4 / OH 下列有關測試結果的敘述, 哪些正確? (A) 試管 1 3 與 4 中, 可能含有鹵素鹽類 (B) 試管 3 最可能是氯化鈉溶液 (C) 試管 最可能是乙炔溶液 (D) 試管 4 與 AgNO aq 作用會生成白色的沉澱 3( ) (E) 試管 5 的化合物可使 KMnO / OH 的溶液褪色 參考答案 :AE 測驗目標 :4c. 應用化學原理解決問題的能力 測驗內容 : 選修化學物質性質三 有機化合物七 無機化合物 說明 : 4 (100 學年度指考 ) 從硝酸銀測試中, 可以判斷出試管 含有鹵素離子 再從氯水及溴的四氯化 碳溶液兩個測試中, 可以判斷出試管 1 為氯化鈉溶液 試管 3 為溴化鈉溶液 試管 4 為 碘化鈉溶液 11
16 各試管的反應如下 : NaBr + Cl NaCl + Br... 試管 3 NaI + Cl NaCl + I... 試管 4 NaI + Br NaBr + I... 試管 4 從溴的四氯化碳溶液測試中, 即可判斷出試管 為乙醇的正己烷溶液 試管 5 為乙炔 的正己烷溶液 Br + C H 有反應... 試管 5 Br + C H 5OH 沒有反應... 試管 依據題意,(A) (E) 為正確選項 例 1. 下列哪一個聚合物以加成聚合的方式合成得到? (A) 達克倫 (B) 天然橡膠 (C) 蛋白質 (D) 耐綸 (E) 纖維素 (100 年度研究用試卷 ) 參考答案 :B 測驗目標 :4c. 應用化學原理解決問題的能力測驗內容 : 選修化學化學應用八 化學的應用與發展說明 : 各選項說明如下 : (A) 達克倫是由單體乙二醇及對苯二甲酸反應, 形成的酯類化合物, 屬於縮合聚合反應 (B) 天然橡膠是由單體異戊二烯加成反應, 形成的烯類化合物, 屬於加成聚合反應 (C) 蛋白質是由單體胺 ( R NH ) 與酸 ( R' COOH ) 反應, 形成的醯胺類化合物, 屬於縮合聚合反應 (D) 耐綸是由單體 1 6 一己二酸與 1 6 一己二胺反應, 形成的醯胺類化合物, 屬於縮合聚合反應 (E) 纖維素是由單醣間經脫水反應聚合而成, 屬於縮合聚合反應 1
17 附件一 指定科目考試測驗內容 壹 教材綱要本測驗內容由普通高級中學必修科目 基礎化學 與 選修科目化學 教材綱要重新排列而成, 分主題 主題內容 應修內容 說明 備註 參考節數等六部分 高級中學基礎化學 ( 一 ) 基礎化學( 二 ) 基礎化學( 三 ) 選修化學 主題 主題內容 應修內容 說 明 備 註 基礎化學 ( 一 ) 1. 物質的分類 純物質與混合物 一 物質的組成 元素與化合物 物質的分離與純化. 原子與分子 定比定律及倍比定律 物 道耳頓原子說 質 分子的概念 基 3. 原子量與分子量 原子質量單位 原子量 本 分子量 組 莫耳與亞佛加厥常數 莫 成 耳質量 4. 溶液 溶液的組成 溶解度 濃度的概念 重量百分濃 度 體積莫耳濃度 百萬 分之一濃度 基礎化學 ( 一 ) 1. 原子結構 拉塞福原子模型 原子與 二 原子構造與元 原子核的相對大小 素週期表 原子核的組成與原子序物 能階的概念質. 原子中電子的 原子序 1~18 元素之原子基排列的電子排列 價殼層及價本電子構 3. 元素性質的規 原子的價電子與元素性造律性質規律性的關係 4. 元素週期表 元素週期表 元素的分類 參考節數
18 高級中學基礎化學 ( 一 ) 基礎化學( 二 ) 基礎化學( 三 ) 選修化學主題主題內容應修內容說明備註 選修化學一 原子構造物質構造基礎化學 ( 一 ) 三 化學反應物質變化 1. 氫原子光譜 電磁波與能量 氫原子放射光譜與芮得 柏方程式. 波耳氫原子模 波耳氫原子模型 型 3. 原子軌域 氫原子能階 量子數與原子軌域 不涉及量子力學 4. 電子組態 遞建原理 洪德法則 包立不相容原理 多電子原子的電子組態 5. 原子性質的趨 元素的原子半徑 游離 勢 能 電負度的週期性 1. 化學式 化學式的意義 實驗式 分子式 示性式 結構式 分子模型. 化學反應式與 化學反應表示法均衡 觀察法與代數法均衡化學反應式 3. 化學計量 化學反應中質量的關係 限量試劑的概念 4. 化學反應中的 放熱反應與吸熱反應 化能量變化學反應熱 熱化學反應式 赫斯定律及能量守恆 參考節數 1 7 物質構造 基礎化學 ( 二 ) 1. 八隅體與路易 八隅體規則 一 物質的構造與 斯結構 以電子點表示分子結構 特性. 離子鍵與離子 以八隅體規則說明離子不涉及晶格 晶體 鍵的形成 形狀及晶格 離子晶體的特性 能 3. 共價鍵與分子 以八隅體規則說明共價 化合物 鍵的形成 分子化合物的特性 4. 網狀固體 網狀固體的特性 5. 金屬固體 金屬固體的特性及電子不涉及晶格 海模型 堆積 14 10
19 高級中學基礎化學 ( 一 ) 基礎化學( 二 ) 基礎化學( 三 ) 選修化學主題主題內容應修內容說明備註 選修化學 1. 化學鍵的種類二 化學鍵結. 價鍵理論物質構造 3. 分子間作用力 離子鍵 共價鍵 金屬鍵 鍵極性 鍵偶極與極性分不涉及鍵偶子極矩的計算 分子極性與分子形狀 σ 鍵 π 鍵 共振結構 混成軌域 價殼層電子對互斥理論以第二週期 與分子形狀元素的化合物為例, 不涉及含 d 軌域的混成軌域 氫鍵與凡得瓦力 參考 節數 1 物質變化物質性質 基礎化學 ( 一 ) 1. 結合反應與分 結合反應 沉澱反應 用常見的化 四 常見的化學反應 解反應. 酸鹼反應 3. 氧化還原反應 分解反應 電解質與非電解質 水的解離與 ph 值 阿瑞尼斯酸鹼定義 強酸與強鹼的中和反應 酸鹼指示劑 氧化還原的概念 常見的氧化劑與還原劑及其應用 學反應型態, 尤其是大氣或水溶液中的主要反應為實例 選修化學 1. 布 洛酸鹼理論 布 洛酸鹼定義 水溶液 四 水溶液中酸 中質子轉移的概念鹼 鹽的平衡 共軛酸鹼對. 酸鹼度 酸鹼強度 酸鹼滴定 滴定曲線圖 弱酸 弱鹼水溶液的平衡 弱酸 弱鹼的解離常數 (K a K b ) 雙質子酸 3. 緩衝溶液 緩衝溶液的形成與應用
20 高級中學基礎化學 ( 一 ) 基礎化學( 二 ) 基礎化學( 三 ) 選修化學主題主題內容應修內容說明備註 4. 鹽 鹽的種類與簡易命名不涉及弱酸與弱鹼反應形成的鹽, 在水溶液中的酸鹼平衡計算 選修化學 1. 氧化數五 氧化還原反應物. 氧化還原滴定質 3. 電池電動勢性質 4. 電解基礎化學 ( 三 ) 1. 氣體性質一 氣體. 氣體的定律物質狀 3. 理想氣體態 4. 分壓選修化學 1. 水的相變化六 液態與溶液物. 汽化與蒸氣壓質狀 3. 溶液的性質態 氧化數的定義 反應式的均衡 氧化還原滴定與計量 電池半反應式 標準還原電位與電池電壓 法拉第電解定律 電解 電鍍及其應用 大氣 氣體的通性 氣體粒子的運動與溫度 波以耳定律 查理定律 亞佛加厥定律 絕對溫度 理想氣體 理想氣體方程不涉及氣體 式及其應用動力論 莫耳分率 道耳頓分壓定律 粒子的運動模型與物質狀態變化 水的相變與相圖 相態變化的能量關係 汽化 蒸氣壓 沸點 熔點 相對溼度 重量莫耳濃度 拉午耳定律 亨利定律 溶液的沸點上升與凝固點下降 滲透 逆滲透 滲透壓 膠體溶液 16 參考節數
21 高級中學基礎化學 ( 一 ) 基礎化學( 二 ) 基礎化學( 三 ) 選修化學主題主題內容應修內容說明備註 基礎化學 ( 三 ) 二 化學反應速率物質變化基礎化學 ( 三 ) 三 化學平衡物質變化選修化學七 無機化合物物質性質 基礎化學 ( 二 ) 含二 有機化合物碳元素的物質 1. 反應速率定律 反應速率 反應速率定律式 反應速率常數 一級 二級反應 半生期的意義與應用. 碰撞學說 化學反應的碰撞理論 活化能 活化複合體 反應能量圖 3. 影響反應速率 濃度 壓力 接觸面積 的因素溫度對反應速率的影響 催化反應與催化劑 1. 化學平衡 可逆反應及動態平衡. 平衡常數 平衡定律式 平衡常數 反應商與反應進行的方向 3. 影響平衡的因素 溫度 濃度 壓力對平衡的影響 勒沙特列原理 4. 溶解平衡 溶度積 同離子效應 1. 非金屬元素. 主族金屬元素 3. 過渡金屬元素 氫 碳 氮 氧 矽 氯重要化合物 及其在生活及環境中常的內容應著 見的重要化合物重生活中常 第三週期金屬及其在生見的範例 活中常見的重要化合物含化合物的 過渡金屬的性質 配位化立體結構 合物配位化合物不涉及鍵結理論 1. 烷 烯 炔與環 烷 烯 炔 環烷與其結環烷至多為 烷 構 六圓環, 環烷上有取 代基的碳不 超過兩個. 異構物 結構異構物 幾何異構物 參考節數
22 高級中學基礎化學 ( 一 ) 基礎化學( 二 ) 基礎化學( 三 ) 選修化學 主題 主題內容 應修內容 說 明 備 註 參考節數 3. 有機化合物的 簡易國際純粹與應用化 命名 學聯盟 (IUPAC) 系統命 4. 芳香族化合物 名法 苯 甲苯 萘 含化合物的 5. 官能基與常見 醇 醚 醛 酮 酸 酯 立體結構 的有機化合物 胺與醯胺的官能基 常見有機化合物的基本 性質與用途 6. 生物體中的有 單醣 雙醣 多醣 機物質 : 醣類 胺基酸及其結構 蛋白質 蛋白質 脂肪 脂肪酸 三酸甘油酯 核苷酸 核苷酸及核酸 選修化學三 有機化合物物質性質 1. 有機化合物的 元素分析與有機化合物組成的組成. 碳氫化合物 有 以通性簡介其結構 特有機化合物機鹵化物 醇 性 重要反應以代表各官酚 醛 有機 烯 : 加成反應如氫化 鹵能基之常見 酸 酯 油脂 胺 醯胺 化 ( 檢驗 ) HX 與 H O, 化合物為例 聚合反應, 僅以乙烯 氯烯加成反應 乙烯 苯乙烯為例僅以乙烯為 炔 : 電石製備乙炔, 加成例, 不涉及位反應, 氧化與鹵化向選擇 苯 : 磺化 芳香族與烯類 (C=C) 的差異 ( 不與 1 Br 作用 ) 醇 : 發酵製備 ( 介紹其用途, 未來能源 ) 及工業製備 ( 水煤氣 ), 甲 乙醇氧化成醛 ; 醇氧化成醛 酮 酸 醛 : 氧化反應 銀鏡 ( 與葡萄糖, 還原醣單元連結 ) 酸與酯 : 酯化 皂化 胺 : 酸鹼反應 18
23 高級中學基礎化學 ( 一 ) 基礎化學( 二 ) 基礎化學( 三 ) 選修化學 主題 主題內容 應修內容 說 明 備 註 選修化學 1. 聚合物 聚合物的性質 八 化學的應用與 加成與縮合聚合反應 發展 常見的加成聚合物與縮 合聚合物 橡膠化 澱粉與纖維素學. 生物體中的大 醯胺基 肽鍵與蛋白質 應分子酵素用 核酸 3. 先進材料 先進材料如半導體 液 晶 導電聚乙炔 奈米尺度 基礎化學 ( 二 ) 1. 化石燃料 煤 石油 天然氣 三 化學與能源 石油分餾及其主要產物 烴的燃燒與汽油辛烷值. 電池 化學電池原理 化 常見的電池 : 乾電池 鉛 學 蓄電池 鋰電池 燃料電 能 池 源 3. 能源 化學能的轉換 常用能源及替代能源, 包 括簡介臺灣的再生能源 及附近海域能源的蘊藏 與開發 基礎化學 ( 二 ) 1. 生活中的化學 簡介化學 化工與日常生 化 四 化學與化工 活的關係 學. 化學與永續發展 簡介化學 化工對環境永 應 續發展的重要 用 3. 化學與先進科技 簡介化學 化工對先進科 技發展的重要 參考節數
24 貳 實驗內容 高中基礎化學實驗 實驗名稱 ( 建議節數 ) 說 明 技 能 試 藥 1. 示範實驗 : 利用 ph 值及控制酸鹼觀察 提問 討鹽酸 氫氧化鈉 常見化學反應的型態 度與指示劑, 使至少七論 論述 報酚酞 溴瑞香草個杯子顯出不同的顏告 資料檢索藍 酚紅 硝酸鉛 ( 一節 ) 色 碘化鉀 硝酸鉛與碘化鉀的反應. 物質的分離 學習基本分離技術 : 如傾析 過濾 濾 基礎 ( 一節 ) 傾析 過濾 濾紙層紙層析 集氣析 集氣法 或蒸餾的法 蒸餾 ( 集氣 化學 條件與技能 及蒸餾可採現場或影片示範 ) ( 一 ) 3. 硝酸鉀的溶 測量硝酸鉀之溶解度溶解度的測硝酸鉀 解與結晶 與溫度的關係 定 圖形與數 ( 一 ~ 二節 ) 固態物質的結晶 據 結晶 4. 化學反應熱 測量強酸 強鹼中和反反應熱的測量氫氧化鈉溶液 鹽 ( 一節 ) 應的反應熱 ( 不考慮系統熱容量概念 ) 硝酸鉀溶於水的熱量變化 酸 硝酸鉀固體 ( 反應容器可用保麗龍杯 ) 5. 示範實驗 : 以電腦軟體或模型製作觀察 提問 討 分子在三度空間的模型 ( 一節 ) 簡單分子的三度空間模論 論述 報型 ( 以簡單的化合物為範告 資料檢索例, 使用模型或 3D 立體 基礎化學 ( 二 ) 結構作為建立圖像之輔助工具以認識分子結構 ) 可參考的分子: 二氧化碳 水 氨 甲烷 乙烷 乙烯 乙炔 順或 反式丁烯二酸 苯 甲 醇 乙醚 丙酮 甲醛 乙酸及基本生物物質等 0
25 高中基礎化學實驗 實驗名稱 ( 建議節數 ) 說 明 技 能 試 藥 6. 有機物質的 葡萄糖 碘 硫酸銅在滴管的使用 葡萄糖 碘 ( 微 一般物性 ( 一節 ) 一般有機溶劑中的溶溶液配製解度 一般有機溶劑的互溶性 有機化合物的揮發性及氣味 量 ) 硫酸銅 甲苯 乙醇 乙醚 丙酮 己烷 乙酸 乙酸乙酯 ( 上述溶劑可選擇使用 ) 紅色石蕊試紙 7. 化學電池 簡易化學電池組三用電表的使硫酸鋅 硫酸銅 ( 一節 ) 用 硫酸鎳 硝酸銀 鋅片 銅片 鎳片 碳棒 硝酸鉀 ( 鹽橋 ) 8. 界面活性劑 界面活性劑幫助油溶溶解 萃取 油溶性染劑 十二 的效應 ( 一節 ) 性染劑溶入水中 鎂離子可破壞脂肪酸界面活性劑的效應 烷基磺酸鈉 C 1 ~ C 16 脂肪酸鈉 ( 肥皂 ) 可溶性鈣或鎂鹽 9. 秒錶反應 碘酸鉀與亞硫酸氫鈉秒錶的使用 化碘酸鉀溶液 焦亞 ( 一節 ) 的反應速率 學反應速率的硫酸鈉溶液 可溶 測量 性澱粉 硫酸溶液 10. 平衡常數與 平衡常數的測量 : 比色溶液濃度的稀硫氰化鉀溶液 酸 勒沙特列法求硫氰化鐵生成反釋法 分度吸量化的硝酸鐵溶液 基原理應的平衡常數管與安全吸球二氧化氮礎 ( 一 ~ 二節 ) Fe 3+ +SCN FeSCN + 的使用 利用化 勒沙特列原理 : 二氧化比色法求物質學氮雙聚反應的平衡的的濃度 ( 三 ) 影響 ( 現場或影片示 範 ) 11. 溶度積測定 測定 MgC O 4 的溶度精密秤量 ( 或可 MgC O 4 ( 硫酸 過 ( 一節 ) 積 選擇滴定分析錳酸鉀 ) 法 ) 1
26 高中選修化學實驗實驗名稱說明技能試藥烴的性質 : 裝置反應設備 簡電石 過錳酸鉀溶液 溴 乙炔的製備 ( 可視實驗易氣體測漏 熔點水 己烷 環己烯 甲苯 室通風設備選擇現場或測定酒精影片示範 ) 順丁烯二酸 反丁烯二烴類化合物的性 1 區別飽和烴與不飽和烴酸 橙 IV 指示劑 鎂帶 質順反異構物的鑑定 : 矽光油或沙拉油 酚酞溶 由熔點測定及昇華現象液 標準氫氧化鈉溶液分辨順反丁烯二酸異構物 標定標準鹼液標定 滴定標準鄰苯二甲酸氫鉀溶 測定未知濃度酸液的濃液 氫氧化鈉溶液 鹽 酸鹼滴定度酸 酚酞溶液 未知酸或鹼溶液 電解法電鍍電解銅片 鋅片 酒精 丙酮 電解電鍍 非電 3 銀鏡反應硫酸鋅 硫酸銅 硝酸解電鍍銀 葡萄糖 濃氨水 利用草酸鈉測定過錳酸滴定 有效數字 過錳酸鉀溶液 硫酸 草鉀的濃度精密度及準確度酸鈉溶液 硫酸亞鐵溶液 4 氧化還原滴定 利用過錳酸鉀分析物質的檢驗中亞鐵離子的含量 凝固點下降的測 水的凝固點凝固點的測定尿素 食鹽 冰塊 ( 冷劑 ) 定 尿素水溶液的凝固點 釩 (V) 的橙紅色硫酸溶觀察 提問 討五氧化二釩 硫酸 鹽 液被氫還原成各種顏色論 論述 報告 酸 鋅粉 硫酸鎳或氯化的釩 (IV) 釩 (III) 釩 (II) 資料檢索鎳 乙二胺示範實驗 : 離子溶液錯合物的形成 綠色鎳 (II) 離子水溶液與乙二胺結合成藍 靛 紫色 用硫代硫酸鈉與鹽酸反硫代硫酸鈉 鹽酸 清潔應製造奈米硫粒劑奈米硫粒的合成 以廷得耳效應檢驗奈米硫粒的生成
27 8 9 高中選修化學實驗 實驗名稱 說 明 技 能 試 藥 軟水與硬水的檢驗 硬水的定性檢硫酸鈣 硫酸鎂 飽和碳 暫時硬水與永久硬水的測 離子交換法 酸鈉溶液 陽離子交換樹 硬水的檢測軟化 區別 脂 ( 如安柏銳 IR10, 法 利用離子交換法軟化硬 50~100 篩目 ) 大理石碎 水 塊 稀鹽酸 石灰 蒸餾 水 肥皂水 醇 醛 酮在水中溶解定性有機分析技甲醇 甲醛 丙醛 丙酮 度的比較 術 1- 丙醇 - 丙醇 丁酮 醇 醛 酮的性 醇 醛 酮與斐林試液 硝酸銀溶液 過錳酸鉀溶 質 的反應 液 斐林試液 硫酸 濃 以銀鏡反應區別一級醇 氨水 二鉻酸鉀 鈉 和二級醇 以柳酸與乙酐反應製備簡單合成技術 產丙酮 柳酸 乙酐 濃硫阿斯匹靈物鑑定與產率酸 飽和碳酸氫鈉溶液 耐綸的製備濾紙 濃鹽酸 酒精 氯 10 化學合成化鐵溶液 己二胺的氫氧化鈉溶液 己二醯氯的正己烷溶液 3
28 附件二 化學化學科 99 課綱與 95 暫綱的綱的差異 99 課綱與 95 暫綱的差異, 就化學科而言, 主要有三點, 分別是修習學分的不同 課綱實質內容的不同以及內容順序的不同 以下分別就這幾點作說明 : 一 學分學分數的差異表一 99 課綱與 95 暫綱修習學分的差異 年級 課綱 高一 高二 高三 (3~4)+(3~4) 4+4 就表一來看,99 課綱化學科的修習學分數為 1~14 學分, 比 95 暫綱 16 學分, 至少減 少 學分, 減少的學分是屬於高二的化學, 上學期與下學期各減少 1 學分 二 課綱內容的差異就表二來看,99 課綱化學科的內容與 95 暫綱差異不大, 比較明顯的刪減內容, 包括 : 高一的土壤 高二化學反應速率的零級反應 高三的金屬固體的晶格堆積等單元 至於增加的內容部分, 包括 : 海洋能源 定比與倍比定律 核苷酸及核酸 生物體的大分子 去氧核糖核酸與核糖核酸 常見的先進材料, 如 : 半導體 液晶 導電聚乙炔 奈米尺度, 以及化學的應用與發展 化學工業等 這些增加的內容, 大都與台灣的環境 ( 如海洋能源 ), 或是近代生物化學與材料化學的重大發展相關, 嘗試用各種新的角度, 來引起學生對此一學門的興趣 4
29 表二 99 課綱與 95 暫綱實質內容的差異 99 課綱比 95 暫綱減少的部分 年級 (95) 內容 高一 土壤 ( 主要成分及其應用 ) 高二 化學反應速率 - 零級反應的反應速率 高三 金屬固體 - 晶格堆積 99 課綱比 95 暫綱增加的部分 年級 (99) 內容 高一 化學與先進科技 ( 簡介化學對先進科技發展的重要 ) 高一 海洋能源 ( 簡介臺灣的再生能源及附近海域能源的蘊藏與開發 ) 高一 原子與分子 - 定比與倍比定律 高二 核苷酸及核酸 高三 生物體中的大分子 - 去氧核糖核酸與核糖核酸 高三 化學的應用與發展 - 常見的先進材料 ( 常見的先進材料如半導體 液晶 導電聚乙炔 奈米尺度 ) 高三 化學的應用與發展 - 化學工業 ( 化學與化工產業 化學 化工與環境保護及永續發展 ) 不限定 附錄 : 物質的測量 ( 誤差 準確度 精密度及有效數字 ) 三 課綱順序的差異就 95 與 99 課綱而言, 兩者的內容與順序的關係, 是所謂 內容微調 結構大動 95 暫綱中, 部分原屬於高二或高三的內容, 因著課程結構的調整, 而列為高一或高二的內容 舉例來說 :95 暫綱中高二的化學反應的係數平衡移至 99 課綱的高一內容, 並加入限量試劑的概念 ; 晶體結構原先在 95 暫綱是屬於高三 ( 上 ) 的內容, 在 99 課綱則調整為高二 ( 上 ) 這些內容結構的變化, 對指考的影響較小, 因指考是包括高中三年所學的內容 ; 但對學測的影響較大, 因學測只包括高一 高二的必修課程, 若是屬高三的內容, 則不屬於學測的測驗範圍 5
30 表三 99 課綱與 95 暫綱順序的差異 年級 99 課程綱要 年級 95 課程暫行暫行綱要 高一 物質變化 - 化學反應 - 化學式的意義 化學反應式與均衡 限量試劑的概念 高二 ( 上 ) 物質的變化 - 化學反應 - 化學式的意義 化學反應的係數平衡 高一 物質變化 - 熱化學反應式 赫斯定律及能量守恆 高二 ( 上 ) 物質的變化 - 能量的變化 赫斯定律 高二 物質構造 - 物質的構造與特性 ( 網狀固 高三 物質的構造 - 晶體的結構 ( 共價網狀晶 ( 上 ) 體 ) ( 上 ) 體及其結構與特性的關係 ) 高二 含碳元素的物質 - 官能基與常見的有 高三 物質的性質 - 有機化合物 - 官能基的探 ( 上 ) 機化合物 ( 下 ) 討 高二 含碳元素的物質 - 生物體中的物質 ( 醣 高三 物質的性質 - 有機化合物 - 聚合物 ( 上 ) 類 蛋白質 脂肪 ) ( 下 ) 高二 物質變化 - 化學平衡 高三 物質的變化 - 化學平衡 ( 下 ) ( 上 ) 高二 ( 下 ) 物質變化 - 水溶液中酸 鹼 鹽的平衡 ( 弱酸 弱鹼的解離常數 Ka Kb) ( 緩衝溶液 鹽的種類 ) 高三 ( 上 ) 物質的變化 - 水溶液中的平衡 ( 弱酸 弱鹼的解離常數 Ka Kb) ( 緩衝溶液 鹽的水解 ) 高三 物質構造 - 原子構造 ( 波耳的氫原子模 高二 物質的構造 - 原子的結構 ( 波耳的氫原 ( 上 ) 型 )( 原子軌域與電子組態 ) ( 上 ) 子模型 )( 原子軌域與電子組態 ) 高三 ( 上 ) 物質變化 - 氧化還原反應 ( 氧化數的定義 )( 反應式的均衡 ) ( 氧化還原滴定 ) 高二 ( 上 ) 物質的變化 - 氧化與還原 ( 氧化還原滴定 ) ( 氧化數的規則及其應用 ) 高三 物質性質 - 無機化合物 高二 物質的性質 - 非金屬與金屬元素 ( 下 ) ( 下 ) 高三 物質狀態 - 液態與溶液 - 水的相變化 高二 物質的狀態 - 粒子的運動模型及三態變 ( 下 ) ( 粒子的運動模型與物質狀態變化 ) ( 上 ) 化 高三 物質狀態 - 液態與溶液 ( 亨利定律 ) 高二 物質的狀態 - 溶液的性質 ( 亨利定律 ) ( 下 ) ( 上 ) 高三 物質狀態 - 液態與溶液 ( 重量莫耳濃 高二 物質的狀態 - 溶液的性質 ( 常用濃度的 ( 下 ) 度 ) ( 上 ) 表示法 ) 整體來說,99 課綱與 95 暫綱有三項主要的差異, 就指考而言, 第二項內容 的增刪影響最大, 希望上述說明, 有助於命題 教學以及學生考試的準備 6
<4D F736F F D D313036ABFCA6D2A4C6BEC7A6D2B8D5BBA1A9FA28ADD7AD71292DBDD2BAF5B74CBDD528B1C6AAA9BD5A292D A457BAF4A5CE2
 大學入學考試中心 指定科目考試 考試說明 ( 適用於 99 課綱微調 ) 中華民國 104 年 9 月 版權所有 指定科目考試化學考試說明 ( 適用於 99 課綱微調 ) 目 錄 壹 測驗目標... 1 貳 測驗內容... 參 試題舉例... 附件一 指定科目考試測驗內容... 14 指定科目考試考試化學考試說明 ( 適用於 99 課綱微調 ) 民國 106 年開始, 指定科目考試 將依據 103
大學入學考試中心 指定科目考試 考試說明 ( 適用於 99 課綱微調 ) 中華民國 104 年 9 月 版權所有 指定科目考試化學考試說明 ( 適用於 99 課綱微調 ) 目 錄 壹 測驗目標... 1 貳 測驗內容... 參 試題舉例... 附件一 指定科目考試測驗內容... 14 指定科目考試考試化學考試說明 ( 適用於 99 課綱微調 ) 民國 106 年開始, 指定科目考試 將依據 103
Unit_18(C)N.indd
 重點 第 18 節 日 常 使 用 的 化 學 電 池 不同種類的化學電池 如何選擇適合的化學電池 使用化學電池對環境造成的影響 第 19 節 簡 單 化 學 電 池 簡單化學電池內的反應 金屬的電化序 簡單化學電池內的鹽橋 丹聶爾電池 第 20 節 氧 化 作 用 和 還 原 作 用 氧化作用和還原作用的定義 常見的氧化劑和還原劑 物種的氧化能力和還原能力 氧化數 第 21 節 化 學 電 池 內
重點 第 18 節 日 常 使 用 的 化 學 電 池 不同種類的化學電池 如何選擇適合的化學電池 使用化學電池對環境造成的影響 第 19 節 簡 單 化 學 電 池 簡單化學電池內的反應 金屬的電化序 簡單化學電池內的鹽橋 丹聶爾電池 第 20 節 氧 化 作 用 和 還 原 作 用 氧化作用和還原作用的定義 常見的氧化劑和還原劑 物種的氧化能力和還原能力 氧化數 第 21 節 化 學 電 池 內
化工群 專業科目 ( 一 ) 普通化學 普通化學實驗 分析化學 分析化學實驗 普通化學 單元教材綱要 1. 緒論 1. 化學簡史 2. 化學對人類文明的貢獻 3. 物質的種類與性質 4. 物質的狀態與變化 5. 物質的分離 6. 有效數字 2. 計量化學 1. 原子量與分子量 2. 莫耳 3. 化學
 化工群 專業科目 ( 一 ) 普通化學 普通化學實驗 分析化學 分析化學實驗 普通化學 單元教材綱要 1. 緒論 1. 化學簡史 2. 化學對人類文明的貢獻 3. 物質的種類與性質 4. 物質的狀態與變化 5. 物質的分離 6. 有效數字 2. 計量化學 1. 原子量與分子量 2. 莫耳 3. 化學式 4. 化合物的百分組成 5. 定比定律與倍比定律 6. 反應的種類 7. 化學反應式的意義與平衡
化工群 專業科目 ( 一 ) 普通化學 普通化學實驗 分析化學 分析化學實驗 普通化學 單元教材綱要 1. 緒論 1. 化學簡史 2. 化學對人類文明的貢獻 3. 物質的種類與性質 4. 物質的狀態與變化 5. 物質的分離 6. 有效數字 2. 計量化學 1. 原子量與分子量 2. 莫耳 3. 化學式 4. 化合物的百分組成 5. 定比定律與倍比定律 6. 反應的種類 7. 化學反應式的意義與平衡
中國的煤
 課內活動及課後練習的建議答案 課內活動 討論區 ( 3 頁 ) 1 2 網上追蹤 ( 5 頁 ) 2008 年末世界各地煤的蘊藏量地區 蘊藏量 ( 百萬公噸 ) 佔全球的百分比 097 29.8% 15 00 1.8% 272 33.0% 1 38 0.2% 32 013 3.9% 259 253 114 500 31.4% 13.9% 82 001 100.0% 272.2.1 15.0 32.0
課內活動及課後練習的建議答案 課內活動 討論區 ( 3 頁 ) 1 2 網上追蹤 ( 5 頁 ) 2008 年末世界各地煤的蘊藏量地區 蘊藏量 ( 百萬公噸 ) 佔全球的百分比 097 29.8% 15 00 1.8% 272 33.0% 1 38 0.2% 32 013 3.9% 259 253 114 500 31.4% 13.9% 82 001 100.0% 272.2.1 15.0 32.0
指定科目考試考試說明 目 錄 壹測驗目標...1 貳測驗內容... 參試題舉例... 附錄一高中化學新舊課程綱要的比較...1 附錄二之測驗內容...13 附錄三 88 年與 95 年實驗課程的比較...
 大學入學考試中心 指定科目考試 考試說明 中華民國九十六年九月 版權所有 指定科目考試考試說明 目 錄 壹測驗目標...1 貳測驗內容... 參試題舉例... 附錄一高中化學新舊課程綱要的比較...1 附錄二之測驗內容...13 附錄三 88 年與 95 年實驗課程的比較... 指定科目考試 考試說明 本次指定科目考試的考試說明, 主要是為因應民國九十五年正式實施的 普通高級中學課程暫行綱要 ( 民國九十三年八月三十一日發布
大學入學考試中心 指定科目考試 考試說明 中華民國九十六年九月 版權所有 指定科目考試考試說明 目 錄 壹測驗目標...1 貳測驗內容... 參試題舉例... 附錄一高中化學新舊課程綱要的比較...1 附錄二之測驗內容...13 附錄三 88 年與 95 年實驗課程的比較... 指定科目考試 考試說明 本次指定科目考試的考試說明, 主要是為因應民國九十五年正式實施的 普通高級中學課程暫行綱要 ( 民國九十三年八月三十一日發布
cm CO Na CO HC NaO H CO SO
 cm CO Na CO HC NaO H CO SO C H Na CO CaCO Na CO CaCO ml mm mm cm cm b a b c d K CO A B C D E F G H F C A D B H G C F A KC O MnO MnO KC O MnO KClO MH NO H SO N H N O H SO NaO H Na O ml Na O O NaO
cm CO Na CO HC NaO H CO SO C H Na CO CaCO Na CO CaCO ml mm mm cm cm b a b c d K CO A B C D E F G H F C A D B H G C F A KC O MnO MnO KC O MnO KClO MH NO H SO N H N O H SO NaO H Na O ml Na O O NaO
生物考科 3 A B C D 答案 A 命題出處 7 12 測驗目標 評 析 2 AB C D 析 4 A B C D 答案 B 命題出處 2 測驗目標 析 A C H O N S B C D 21
 指定科目考試生物試題詳 臺南一中 郭人仲老師 第壹部分 : 選擇題 ( 占 71 分 ) 1 p 1 1/3 1 A B B C RNA D 答案 B 命題出處 4 2 11 測驗目標 析 A T C RNA D 2 A B C D T 20 答案 D 命題出處 6 11 測驗目標 析 A B C 生物考科 3 A B C D 答案 A 命題出處 7 12 測驗目標 評 析 2 AB C D 析 4
指定科目考試生物試題詳 臺南一中 郭人仲老師 第壹部分 : 選擇題 ( 占 71 分 ) 1 p 1 1/3 1 A B B C RNA D 答案 B 命題出處 4 2 11 測驗目標 析 A T C RNA D 2 A B C D T 20 答案 D 命題出處 6 11 測驗目標 析 A B C 生物考科 3 A B C D 答案 A 命題出處 7 12 測驗目標 評 析 2 AB C D 析 4
課綱實驗與綠色化學
 104 年綠色化學教育種子教師培訓課程研習營 課綱實驗與綠色化學 國立臺灣師範大學 葉名倉教授 2015 年 9 月 24 日 三 物質的構造與功能 1. 物質的分離與鑑定 CCa-Ⅴc-1 混合物的分離過程與純化方法, 包括蒸餾 萃取 色層分析 硬水軟化 海水純化等 CCa- Ⅴ c-2 化合物特性的鑑定 1.1 墨水蒸餾可分離墨水中的色素與水 1.2 以丙酮可以萃取花或葉中的色素 1.3 以色層分析分離花或葉萃取液中的色
104 年綠色化學教育種子教師培訓課程研習營 課綱實驗與綠色化學 國立臺灣師範大學 葉名倉教授 2015 年 9 月 24 日 三 物質的構造與功能 1. 物質的分離與鑑定 CCa-Ⅴc-1 混合物的分離過程與純化方法, 包括蒸餾 萃取 色層分析 硬水軟化 海水純化等 CCa- Ⅴ c-2 化合物特性的鑑定 1.1 墨水蒸餾可分離墨水中的色素與水 1.2 以丙酮可以萃取花或葉中的色素 1.3 以色層分析分離花或葉萃取液中的色
生物科 左營高中 / 許惠紋 一 前言 二 試題特色 號稱五年來最難題目 2. 高二 高三課程出題比例高 康熹 97 指考科目. 生物科
 97 指定科目考試生物趨勢分析 2 97 指定科目考試生物解析大揭密 5 康熹生物科 試題 答案依據大考中心公布內容 本刊物內容同步刊載於 http://www.knsi.com.tw 970038 248 30 (02) 2299-9006 (02) 2299-9110 0800-313-688 97 7 16 生物科 左營高中 / 許惠紋 一 前言 二 試題特色 10.5 1 6 2 1.5 3
97 指定科目考試生物趨勢分析 2 97 指定科目考試生物解析大揭密 5 康熹生物科 試題 答案依據大考中心公布內容 本刊物內容同步刊載於 http://www.knsi.com.tw 970038 248 30 (02) 2299-9006 (02) 2299-9110 0800-313-688 97 7 16 生物科 左營高中 / 許惠紋 一 前言 二 試題特色 10.5 1 6 2 1.5 3
(Microsoft PowerPoint - B14 \273\304\252\272\272w\251w [\254\333\256e\274\322\246\241])
![(Microsoft PowerPoint - B14 \273\304\252\272\272w\251w [\254\333\256e\274\322\246\241]) (Microsoft PowerPoint - B14 \273\304\252\272\272w\251w [\254\333\256e\274\322\246\241])](/thumbs/103/157927719.jpg) LOGO http://www2.thu.edu.tw/~orlab 原 理 標定 NaOH: 得 NaOH 的正確濃度 NaOH + KHC 8 H 4 O 4 H 2 O + NaKC 8 H 4 O 4 公式 : V = W KHP:KHC 8 H 4 O 4 (s)( = 204.22 /mol) V() NaOH = 1000( ) L W KHP () 204.22( ) mol www.themeallery.com
LOGO http://www2.thu.edu.tw/~orlab 原 理 標定 NaOH: 得 NaOH 的正確濃度 NaOH + KHC 8 H 4 O 4 H 2 O + NaKC 8 H 4 O 4 公式 : V = W KHP:KHC 8 H 4 O 4 (s)( = 204.22 /mol) V() NaOH = 1000( ) L W KHP () 204.22( ) mol www.themeallery.com
<4D F736F F D DB0AAA4A4BDD2B57BB0F2C2A6A4C6BEC7ACECBAF5AD6E >
 必修 - 自然領域 - 基礎化學課程綱要 普通高級中學必修科目 基礎化學 課程綱要 壹 課程目標一 本課綱延續九年一貫課程的精神, 掌握普通高中的教育目標, 以中小學一貫課程體系參考指引為依據, 兼顧人文 社會與自然領域學生的科學學習目標 二 教材內容著重在基礎的化學原理及應用與實驗活動學習, 認識並瞭解物質的組成 結構 性質及其中的能量變化, 並藉認識科學發展史學習科學知識的產生及發展 三 教材應能加強科學基本素養,
必修 - 自然領域 - 基礎化學課程綱要 普通高級中學必修科目 基礎化學 課程綱要 壹 課程目標一 本課綱延續九年一貫課程的精神, 掌握普通高中的教育目標, 以中小學一貫課程體系參考指引為依據, 兼顧人文 社會與自然領域學生的科學學習目標 二 教材內容著重在基礎的化學原理及應用與實驗活動學習, 認識並瞭解物質的組成 結構 性質及其中的能量變化, 並藉認識科學發展史學習科學知識的產生及發展 三 教材應能加強科學基本素養,
á à
 á à + 2- NH 4 SO4 1 1 2 1 3 1 14 12 6 13 6 6 12 6 2 1 3 1 235 92 18 8 131 53 12 6 1 16 8 12 1 12 6 1 1 2 1 1 1 2 1 6 1 1 6 10 14 p d f 3 5 7 p d f 0 0 0 p d f NH + 4 A werner 1866 1919
á à + 2- NH 4 SO4 1 1 2 1 3 1 14 12 6 13 6 6 12 6 2 1 3 1 235 92 18 8 131 53 12 6 1 16 8 12 1 12 6 1 1 2 1 1 1 2 1 6 1 1 6 10 14 p d f 3 5 7 p d f 0 0 0 p d f NH + 4 A werner 1866 1919
1-1 人住在地球上和活在宇宙中
 附錄四 1 σ 鍵 (σ bond) 58,69,75,76,102,104 π 鍵 (π bond) 58,75,76,79,102,104 八隅體規則 (octect rule) 58 三相點 (triple point) 123,124,154 凡得瓦 (J. D. van der Waals) 58,90,101 凡得瓦力 (van der Waals force) 58,90,95~97,101,102,104,127
附錄四 1 σ 鍵 (σ bond) 58,69,75,76,102,104 π 鍵 (π bond) 58,75,76,79,102,104 八隅體規則 (octect rule) 58 三相點 (triple point) 123,124,154 凡得瓦 (J. D. van der Waals) 58,90,101 凡得瓦力 (van der Waals force) 58,90,95~97,101,102,104,127
FeS 2 在 晶 體 中 為 Fe 2+ S 22ˉ 故 選 (A) 4. 下 圖 代 表 某 反 應 座 標 圖, 下 列 敘 述 何 者 錯 誤? (A) B - A 為 活 化 能 (B) A - C 為 反 應 熱 (C) B 代 表 活 化 錯 合 物 的 相 對 能 量 (D) B -
 1. 在 含 有 0.050 M MgCl 2 及 1.0 M 氨 的 1.00 升 水 溶 液 中, 頇 加 入 多 少 克 的 氯 化 銨, 才 能 使 鎂 的 鹽 類 不 沉 澱? Mg(OH) 2 的 K sp 為 1.5 10-11,NH 3 的 K b 為 1.8 10-5 (A) 50 g (B) 56 g (C) 5.0 g (D) 4.3 g 答 案 :(B) [Mg 2+ ] =
1. 在 含 有 0.050 M MgCl 2 及 1.0 M 氨 的 1.00 升 水 溶 液 中, 頇 加 入 多 少 克 的 氯 化 銨, 才 能 使 鎂 的 鹽 類 不 沉 澱? Mg(OH) 2 的 K sp 為 1.5 10-11,NH 3 的 K b 為 1.8 10-5 (A) 50 g (B) 56 g (C) 5.0 g (D) 4.3 g 答 案 :(B) [Mg 2+ ] =
廢液桶之標示
 吳 鳳 科 技 大 學 實 驗 室 廢 棄 物 貯 存 容 器 標 示 及 存 放 須 知 一 材 質 : ( 一 ) 廢 棄 物 貯 存 容 器 應 使 用 HDPE, 容 積 為 20 公 升 之 方 型 容 器 ( 二 ) 存 放 時, 下 方 應 有 防 漏 盤 ( 材 質 與 尺 寸 法 令 並 無 規 定, 但 應 為 耐 腐 蝕 材 質 可 供 承 接 之 容 器, 例 如 : 不 鏽
吳 鳳 科 技 大 學 實 驗 室 廢 棄 物 貯 存 容 器 標 示 及 存 放 須 知 一 材 質 : ( 一 ) 廢 棄 物 貯 存 容 器 應 使 用 HDPE, 容 積 為 20 公 升 之 方 型 容 器 ( 二 ) 存 放 時, 下 方 應 有 防 漏 盤 ( 材 質 與 尺 寸 法 令 並 無 規 定, 但 應 為 耐 腐 蝕 材 質 可 供 承 接 之 容 器, 例 如 : 不 鏽
員林高中 陳品誌老師化學考科 壹前言 自高中教科書 88 年開放一綱多本以來, 歷經 88 課綱 95 暫綱 99 課綱與 99 微調課綱等四個變革, 經過僅 17 年而已, 改變算是多了些 因應課綱的改變與調整, 為協助同學準備 105 年的指考化學考科, 以下先就化學考科的測驗目標 試卷內容及歷
 化學考科 / / 105 / / 7 0 2 4 8 76 / / 7 0 2 5 2 8-1 / / 06 2619621 #311 / E-mail / periodical @ hanlin.com.tw / http://www.worldone.com.tw http://www.worldone.com.tw NO.00847 ZXCV 員林高中 陳品誌老師化學考科 壹前言 自高中教科書
化學考科 / / 105 / / 7 0 2 4 8 76 / / 7 0 2 5 2 8-1 / / 06 2619621 #311 / E-mail / periodical @ hanlin.com.tw / http://www.worldone.com.tw http://www.worldone.com.tw NO.00847 ZXCV 員林高中 陳品誌老師化學考科 壹前言 自高中教科書
3-3 蒸氣壓 103 飽和蒸氣壓之計算 nc 時 ca B 兩種液體之蒸氣壓分別為 48.0 及 80.0 mmhgc 今於一內容積為 10 升之密閉容器中 c 充入 0.02 莫耳 A 氣體及 0.05 莫耳 B 氣體 c 溫度仍維持 27 ncc 當物系達平衡時 c 容器內氣體之
 102 互動式教學講義 選修化學 ( 上 ) 3-3 蒸氣壓 一 液體的蒸氣壓 ( 配合翰版課本 P.100 ~ P.102) 1 c c c. 1 吸熱 c. 2 c 放熱. 2 1 c c c c. c. 課 P.100 2 備 P.185 1 c 一定 c 無關. 2 溫度升高時 c 液體分子的平均動能增加 c 造成液體的飽和蒸氣壓也漸增. 3 沸點較高的液體 c 分子間的引力較大 c 在同
102 互動式教學講義 選修化學 ( 上 ) 3-3 蒸氣壓 一 液體的蒸氣壓 ( 配合翰版課本 P.100 ~ P.102) 1 c c c. 1 吸熱 c. 2 c 放熱. 2 1 c c c c. c. 課 P.100 2 備 P.185 1 c 一定 c 無關. 2 溫度升高時 c 液體分子的平均動能增加 c 造成液體的飽和蒸氣壓也漸增. 3 沸點較高的液體 c 分子間的引力較大 c 在同
f n kg 1 J 1 2 A 5 B 0.05 C D E A B C D E ppb ppb parts per billion ppb A 1 µg 1
 自然101 學年度全國公私立高級中學 學科能力測驗模擬考試 自然考科 作答注意事項 考試範圍 : 高一 ~ 高二考試時間 :100 分鐘題型題數 : 第壹部分共 40 題 第貳部分共 28 題作答方式 : 用 2B 鉛筆在 答案卡 上作答, 修正時應以橡皮擦擦拭, 切勿使用修正液 ( 帶 ) 參考資料 : 重力加速度 g=10 m s 2 克卜勒行星第三定律 : R3 = 定值 T 2 正面彈性碰撞公式
自然101 學年度全國公私立高級中學 學科能力測驗模擬考試 自然考科 作答注意事項 考試範圍 : 高一 ~ 高二考試時間 :100 分鐘題型題數 : 第壹部分共 40 題 第貳部分共 28 題作答方式 : 用 2B 鉛筆在 答案卡 上作答, 修正時應以橡皮擦擦拭, 切勿使用修正液 ( 帶 ) 參考資料 : 重力加速度 g=10 m s 2 克卜勒行星第三定律 : R3 = 定值 T 2 正面彈性碰撞公式
縣 94 學年度 上 學期 區 國民中學 Q 年級 R 領域教學計畫表 設計者:
 高雄市立茄萣國中國中 103 學年度第一學期八年級 英文補救教學彈性學習課程計畫表 一 教材來源 : 二 教學節數 : 每週 (1) 節, 學期共 ( 20 ) 節 三 各單元內涵分析 : 週次 第一週 第二週 第三週 第四週 9/1 9/5 9/8 9/12 9/15 9/19 9/22 9/26 Lesson1 ( 一 ) Lesson1 ( 一 ) Lesson2 ( 二 ) Lesson2
高雄市立茄萣國中國中 103 學年度第一學期八年級 英文補救教學彈性學習課程計畫表 一 教材來源 : 二 教學節數 : 每週 (1) 節, 學期共 ( 20 ) 節 三 各單元內涵分析 : 週次 第一週 第二週 第三週 第四週 9/1 9/5 9/8 9/12 9/15 9/19 9/22 9/26 Lesson1 ( 一 ) Lesson1 ( 一 ) Lesson2 ( 二 ) Lesson2
 1 cal = 4.18 J N 0 = 6.02 10 : 1.00 : 12.0 : 14.0 : 16.0 : 32.0 23 1 40 2 1. (A) (B) (C) (D) (E) (C) (A) ( ) (B) ( ) (D) (NaI KIO 3 ) (E) ( Ca 2+ Mg 2+ Fe 2+ ) (C) 1 2 3 75 6 (Ga 29.8 2403 ) 310 K 1.3
1 cal = 4.18 J N 0 = 6.02 10 : 1.00 : 12.0 : 14.0 : 16.0 : 32.0 23 1 40 2 1. (A) (B) (C) (D) (E) (C) (A) ( ) (B) ( ) (D) (NaI KIO 3 ) (E) ( Ca 2+ Mg 2+ Fe 2+ ) (C) 1 2 3 75 6 (Ga 29.8 2403 ) 310 K 1.3
zyk00124zw.PDF
 A B=AB( ) AB=AB( ) 4P 50 2 === 2P 2 O 5 2KClO 3 2KCl 3O 2 NH 3 H 2 O CO 2 =NH 4 HCO 3 2KMnO 4 K 2 MnO 4 MnO 2 O 2 CO CO 2 ( ) 1.250 / 1.977 / 1 1 1 0.02 2CO O2 2CO 2 CO CuO Cu CO 2 CO 2 C 2CO Ca(OH) 2
A B=AB( ) AB=AB( ) 4P 50 2 === 2P 2 O 5 2KClO 3 2KCl 3O 2 NH 3 H 2 O CO 2 =NH 4 HCO 3 2KMnO 4 K 2 MnO 4 MnO 2 O 2 CO CO 2 ( ) 1.250 / 1.977 / 1 1 1 0.02 2CO O2 2CO 2 CO CuO Cu CO 2 CO 2 C 2CO Ca(OH) 2
 3 3 4 4 3 3 3 1 6 ( n) 85 U 0 9 85 1 90 1 U + n + Kr + 3 n 9 36 0 =1 sp sp 3 sp 14. H + 1 O = H O( ) + 68 NH + 3 O = 3 1 N + 3H O( ) +18 N + 3 H = NH 3 CO( ) + 1 O ( ) = CO ( ) + 67. 6 (1) () (3) (4)
3 3 4 4 3 3 3 1 6 ( n) 85 U 0 9 85 1 90 1 U + n + Kr + 3 n 9 36 0 =1 sp sp 3 sp 14. H + 1 O = H O( ) + 68 NH + 3 O = 3 1 N + 3H O( ) +18 N + 3 H = NH 3 CO( ) + 1 O ( ) = CO ( ) + 67. 6 (1) () (3) (4)
( )1. 關於氫氣的燃燒反應 :2H 2(g) +O 2(g) 2H 2 O (L) 的敘述, 下列何者正確? (A)ΔH 為正值 (B)1 atm 25 時, 此反應可以自然發生 (C) 生成物的熱含量總和較反應物的熱含量總和低 (D) 在 1 atm 100 時所放的熱量為標準反應熱 答案 :
 ( )1. 關於氫氣的燃燒反應 :2H 2(g) +O 2(g) 2H 2 O (L) 的敘述, 下列何者正確? (A)ΔH 為正值 (B)1 atm 25 時, 此反應可以自然發生 (C) 生成物的熱含量總和較反應物的熱含量總和低 (D) 在 1 atm 100 時所放的熱量為標準反應熱 答案 :(C) 解析 :(A) 燃燒為放熱反應,ΔH 必為負值 (B) 燃燒需點火, 溫度達到燃點, 才能發生燃燒反應,
( )1. 關於氫氣的燃燒反應 :2H 2(g) +O 2(g) 2H 2 O (L) 的敘述, 下列何者正確? (A)ΔH 為正值 (B)1 atm 25 時, 此反應可以自然發生 (C) 生成物的熱含量總和較反應物的熱含量總和低 (D) 在 1 atm 100 時所放的熱量為標準反應熱 答案 :(C) 解析 :(A) 燃燒為放熱反應,ΔH 必為負值 (B) 燃燒需點火, 溫度達到燃點, 才能發生燃燒反應,
【中文名称】盐酸;氢氯酸
 1 ... 1... 9... 9... 10... 11... 11... 12... 13... 13... 14... 14... 15 1357-1357-3.3.1.1.3.7 HMTA... 16... 16... 17... 17... 18... 19... 19... 20... 20 33-4--13H-... 21 33-4--13H-... 21... 22 EDTA...
1 ... 1... 9... 9... 10... 11... 11... 12... 13... 13... 14... 14... 15 1357-1357-3.3.1.1.3.7 HMTA... 16... 16... 17... 17... 18... 19... 19... 20... 20 33-4--13H-... 21 33-4--13H-... 21... 22 EDTA...
http://ckweb.ck.tp.edu.tw/stuconf/nature/chem/C3Kweb/exam/Colle
 90 學 年 大 學 聯 考 試 題 第 一 部 份 : 單 一 選 擇 題 ( 共 佔 31 分 ) 說 明 : 下 列 第 1 題 至 第 5 題, 每 題 2 分 ; 第 6 題 至 第 12 題, 每 題 3 分 每 題 各 有 4 個 備 選 答 案 答 錯 倒 扣 題 分 之 1/3; 整 題 不 作 答, 則 該 題 得 零 分 答 案 請 在 選 擇 題 答 案 卡 上 標 出 1.
90 學 年 大 學 聯 考 試 題 第 一 部 份 : 單 一 選 擇 題 ( 共 佔 31 分 ) 說 明 : 下 列 第 1 題 至 第 5 題, 每 題 2 分 ; 第 6 題 至 第 12 題, 每 題 3 分 每 題 各 有 4 個 備 選 答 案 答 錯 倒 扣 題 分 之 1/3; 整 題 不 作 答, 則 該 題 得 零 分 答 案 請 在 選 擇 題 答 案 卡 上 標 出 1.
(Microsoft PowerPoint - Chapter 12 [\254\333\256e\274\322\246\241])
![(Microsoft PowerPoint - Chapter 12 [\254\333\256e\274\322\246\241]) (Microsoft PowerPoint - Chapter 12 [\254\333\256e\274\322\246\241])](/thumbs/77/75538188.jpg) Chapter 12 Physical Properties of solutions Chemistry English 99-2 Semester 12.1 Type of Solutions 溶液的形態 Vocabulary and Phrase 字與詞 Saturated solutions Unsaturated solution Supersaturated solutions Crystallization
Chapter 12 Physical Properties of solutions Chemistry English 99-2 Semester 12.1 Type of Solutions 溶液的形態 Vocabulary and Phrase 字與詞 Saturated solutions Unsaturated solution Supersaturated solutions Crystallization
 70 1999 4 f x = Msinω x + ϕ ω 0 [a b] f a = -M f b = M g x = Mcos ω x + ϕ [a b] [ ] A B C M D - M ωα + ϕ = kπ π ωb + ϕ = kπ + π k Z ωx + ϕ [ kπ π kπ]( k Z) g π (x) ωx + ϕ [ kπ kπ + ]( k Z) g x ωx +
70 1999 4 f x = Msinω x + ϕ ω 0 [a b] f a = -M f b = M g x = Mcos ω x + ϕ [a b] [ ] A B C M D - M ωα + ϕ = kπ π ωb + ϕ = kπ + π k Z ωx + ϕ [ kπ π kπ]( k Z) g π (x) ωx + ϕ [ kπ kπ + ]( k Z) g x ωx +
 + 7 1 5, Cl Cl + 4 + 6 HSO4 S S S + 6 + 6 HSO4 S S S 0 + 6 + 4 + S S S S + 7 + KMnO 4 Mn Mn + + + [I ] 0 1M 0 I E Fe3+ / Fe+ ( 0771. ) E 1 /1 ( 0536. ) 3+ 3+ + 3+ Fe I I Fe + I = Fe + I [ Fe ] = [ I ]
+ 7 1 5, Cl Cl + 4 + 6 HSO4 S S S + 6 + 6 HSO4 S S S 0 + 6 + 4 + S S S S + 7 + KMnO 4 Mn Mn + + + [I ] 0 1M 0 I E Fe3+ / Fe+ ( 0771. ) E 1 /1 ( 0536. ) 3+ 3+ + 3+ Fe I I Fe + I = Fe + I [ Fe ] = [ I ]
( )1. 已知 H 2 O (l) H 2(g) O 2(g) ΔH=285 kj C (s) +O 2(g) CO 2(g) ΔH=-394 kj C (s) +2H 2(g) CH 4(g) ΔH=-76 kj 則甲烷 (CH 4 ) 的莫耳燃燒熱為多少 kj? (A) 888 (
 ( )1. 已知 H 2 O (l) H 2(g) + 1 2 O 2(g) ΔH=285 kj C (s) +O 2(g) CO 2(g) ΔH=-394 kj C (s) +2H 2(g) CH 4(g) ΔH=-76 kj 則甲烷 (CH 4 ) 的莫耳燃燒熱為多少 kj? (A) 888 (B) 750 (C)-750 (D)-888 kj 答案 :(D) 解析 :H 2 O (L) H 2(g)
( )1. 已知 H 2 O (l) H 2(g) + 1 2 O 2(g) ΔH=285 kj C (s) +O 2(g) CO 2(g) ΔH=-394 kj C (s) +2H 2(g) CH 4(g) ΔH=-76 kj 則甲烷 (CH 4 ) 的莫耳燃燒熱為多少 kj? (A) 888 (B) 750 (C)-750 (D)-888 kj 答案 :(D) 解析 :H 2 O (L) H 2(g)
基 礎 化 學 ( 一 ) 講 義 目 次 第 1 章 物 質 的 組 成 1 1 物 質 的 分 類 1 1 2 原 子 與 分 子 16 1 3 原 子 量 與 分 子 量 31 1 4 溶 液 48 實 驗 二 硝 酸 鉀 的 溶 解 與 結 晶 74 國 戰 大 考 試 題 78 實 驗 相
 內 容 由 蔡 明 倫 老 師 和 李 雅 婷 老 師 編 纂 基 礎 化 學 ( 一 ) 講 義 第 1 章 物 質 的 組 成 班 級 : 拉 瓦 節 和 其 使 用 的 實 驗 儀 器 座 號 : 姓 名 : 基 礎 化 學 ( 一 ) 講 義 目 次 第 1 章 物 質 的 組 成 1 1 物 質 的 分 類 1 1 2 原 子 與 分 子 16 1 3 原 子 量 與 分 子 量 31 1
內 容 由 蔡 明 倫 老 師 和 李 雅 婷 老 師 編 纂 基 礎 化 學 ( 一 ) 講 義 第 1 章 物 質 的 組 成 班 級 : 拉 瓦 節 和 其 使 用 的 實 驗 儀 器 座 號 : 姓 名 : 基 礎 化 學 ( 一 ) 講 義 目 次 第 1 章 物 質 的 組 成 1 1 物 質 的 分 類 1 1 2 原 子 與 分 子 16 1 3 原 子 量 與 分 子 量 31 1
35 C 58 B 1 :
 1 2 1. 0625522. 050061 120 120 46 60 40 20 2012 2011 2012 1 2 3 4 5 6 8 9 11 12 14 28 30 36 7 13 29 31 35 144 35 C 58 B 1 : 3 4 5 40 84 9 11 2 6 27 9 29 13 28 31 31 35 35 36 7 3 12 27 6 7 29 30 31 29 30
1 2 1. 0625522. 050061 120 120 46 60 40 20 2012 2011 2012 1 2 3 4 5 6 8 9 11 12 14 28 30 36 7 13 29 31 35 144 35 C 58 B 1 : 3 4 5 40 84 9 11 2 6 27 9 29 13 28 31 31 35 35 36 7 3 12 27 6 7 29 30 31 29 30
( )6. 水在 45 C 時, 其 K w , 則 ph 7 的溶液酸鹼性為何? (A) 強酸性 (B) 弱酸性 (C) 弱鹼性 (D) 強鹼性 答案 :(C) 解析 : 水的離子積 =[H + ][OH - ]=10-14 M 2, 但是 [H + ]=[OH - ], 因此溶
![( )6. 水在 45 C 時, 其 K w , 則 ph 7 的溶液酸鹼性為何? (A) 強酸性 (B) 弱酸性 (C) 弱鹼性 (D) 強鹼性 答案 :(C) 解析 : 水的離子積 =[H + ][OH - ]=10-14 M 2, 但是 [H + ]=[OH - ], 因此溶 ( )6. 水在 45 C 時, 其 K w , 則 ph 7 的溶液酸鹼性為何? (A) 強酸性 (B) 弱酸性 (C) 弱鹼性 (D) 強鹼性 答案 :(C) 解析 : 水的離子積 =[H + ][OH - ]=10-14 M 2, 但是 [H + ]=[OH - ], 因此溶](/thumbs/71/64761329.jpg) ( )1. 在 25 C 時有關純水的下列敘述中, 何者錯誤? (A)[H ] [OH ] 10 7 M (B) 水解離常數 10 14 M 2 (D)pH poh 答案 :(B) (C) 水可視為極弱的酸也是極弱的鹼 解析 :1 公升的水質量 1000 克, 水的莫耳數 = 1000 55.5 18 = 莫耳, 水的莫耳濃度 = 55.5 55.5M 1 = 1 公升的水能解離出 10-7 莫耳的
( )1. 在 25 C 時有關純水的下列敘述中, 何者錯誤? (A)[H ] [OH ] 10 7 M (B) 水解離常數 10 14 M 2 (D)pH poh 答案 :(B) (C) 水可視為極弱的酸也是極弱的鹼 解析 :1 公升的水質量 1000 克, 水的莫耳數 = 1000 55.5 18 = 莫耳, 水的莫耳濃度 = 55.5 55.5M 1 = 1 公升的水能解離出 10-7 莫耳的
29(C).indd
 重點 第 29 節 碳 化 合 物 的 化 學 導 論 特定同系列的簡介 碳化合物的系統命名 官能基及碳鏈的長度對碳化合物的物理性質的影響 第 30 節 同 分 異 構 結 構 異 構 鏈 異 構 位 置 異 構 及 官 能 基 異 構 立體異構 幾何異構及對映異構 第 31 節 各 種 官 能 基 的 典 型 化 學 反 應 一 些 烷 烯 鹵 烷 醇 醛 酮 羧 酸 酯 和 酰 胺 的 反 應
重點 第 29 節 碳 化 合 物 的 化 學 導 論 特定同系列的簡介 碳化合物的系統命名 官能基及碳鏈的長度對碳化合物的物理性質的影響 第 30 節 同 分 異 構 結 構 異 構 鏈 異 構 位 置 異 構 及 官 能 基 異 構 立體異構 幾何異構及對映異構 第 31 節 各 種 官 能 基 的 典 型 化 學 反 應 一 些 烷 烯 鹵 烷 醇 醛 酮 羧 酸 酯 和 酰 胺 的 反 應
1 { ph
 !!!!!!!!!!!!!!!!!!!!!!!!!!! 1 1!!!!!!!!!!!!!!!!!!!!!! 1 2!!!!!!!!!!!!!!!!!!!!!!!!!! 7 3!!!!!!!!!!!!!!!!!!!!!!!!! 15 4!!!!!!!!!!!!!!!!!!!!!!!!!!! 21!!!!!!!!!!!!!!!!!!!!!!!!!!!! 30!!!!!!!!!!!!!!!!!!!!!!!
!!!!!!!!!!!!!!!!!!!!!!!!!!! 1 1!!!!!!!!!!!!!!!!!!!!!! 1 2!!!!!!!!!!!!!!!!!!!!!!!!!! 7 3!!!!!!!!!!!!!!!!!!!!!!!!! 15 4!!!!!!!!!!!!!!!!!!!!!!!!!!! 21!!!!!!!!!!!!!!!!!!!!!!!!!!!! 30!!!!!!!!!!!!!!!!!!!!!!!
答案 :(D) 解析 :C H 4 +3O CO +H O C H 6 O+3O CO +3H O C 3 H 8 O+(9/)O 3CO +4H O C 3 H 4 +4O 3CO +H O C 3 H 8 +5O 3CO +4H O 所以需要的 O, 以 C 3 H 8 最多 ( )7. 肼和四
 ( )1. 在下列反應中, axo4 by ch dx ey 8HO, 方程式係數 b d 分別為 (A)5,6 (B)10, (C)6, (D)10,5 答案 :(B) 解析 : 先平衡 O( 右邊 8 個 O), 再平衡 X( 左邊 個 X) d= 再平衡 H( 右邊 16 個 H) 得 XO 4 - +by - +16H + X + +ey +8H O 再平衡電荷 :--b+16=x=4 b=10,
( )1. 在下列反應中, axo4 by ch dx ey 8HO, 方程式係數 b d 分別為 (A)5,6 (B)10, (C)6, (D)10,5 答案 :(B) 解析 : 先平衡 O( 右邊 8 個 O), 再平衡 X( 左邊 個 X) d= 再平衡 H( 右邊 16 個 H) 得 XO 4 - +by - +16H + X + +ey +8H O 再平衡電荷 :--b+16=x=4 b=10,
的 浓 度 为 0.1125 mol/ L. 7. 痕 量 Au 3+ 的 溶 液 在 盐 酸 介 质 中 能 被 阴 离 子 交 换 树 脂 交 换 而 得 到 富 集, 这 时 Au 3+ 是 以 AuCl 4 - 形 式 被 交 换 到 树 脂 上 去 的 8. 将 Fe 3+ 和 Al 3+
 二 填 空 题 原 子 吸 收 1. 空 心 阴 极 灯 是 一 种 ( 锐 性 ) 光 源, 它 的 发 射 光 谱 具 有 ( 谱 线 窄 强 度 大 ) 特 点 当 灯 电 流 升 高 时, 由 于 ( 自 吸 变 宽 热 变 宽 ) 的 影 响, 导 致 谱 线 轮 廓 ( 变 宽 ), 测 量 灵 敏 度 ( 下 降 ), 工 作 曲 线 ( 线 性 关 系 变 差 ), 灯 寿 命 (
二 填 空 题 原 子 吸 收 1. 空 心 阴 极 灯 是 一 种 ( 锐 性 ) 光 源, 它 的 发 射 光 谱 具 有 ( 谱 线 窄 强 度 大 ) 特 点 当 灯 电 流 升 高 时, 由 于 ( 自 吸 变 宽 热 变 宽 ) 的 影 响, 导 致 谱 线 轮 廓 ( 变 宽 ), 测 量 灵 敏 度 ( 下 降 ), 工 作 曲 线 ( 线 性 关 系 变 差 ), 灯 寿 命 (
 6 2012 8476你猜得到它是什麼嗎 它就是 高分子! 生活中的高分子 有種物質的重要性不亞於我們所呼吸的空氣, 不管身在何處, 都有它的存在, 它甚至就隱藏在人體裡面! 人類若失去了它, 就得回到遠古時代, 甚至可能終止生命 高分子是什麼 高分子是由千個 甚至萬個以上的原子所組成, 呈現柔軟的特性 日常生活中使用的塑膠袋就是由高分子製造的, 人體組成中的 DNA 也是一種高分子 2012 8476
6 2012 8476你猜得到它是什麼嗎 它就是 高分子! 生活中的高分子 有種物質的重要性不亞於我們所呼吸的空氣, 不管身在何處, 都有它的存在, 它甚至就隱藏在人體裡面! 人類若失去了它, 就得回到遠古時代, 甚至可能終止生命 高分子是什麼 高分子是由千個 甚至萬個以上的原子所組成, 呈現柔軟的特性 日常生活中使用的塑膠袋就是由高分子製造的, 人體組成中的 DNA 也是一種高分子 2012 8476
Unit_6(C).indd
 第2章 第 微觀世界 I 6 節 週期表 6.1 如何把元素分組 在 超 級 市 場 購 物 時 你 會 發 現 同 類 貨 品 都 會 擺 放 在 一 起 圖 6.1 元 素 的 數 目 雖 然 比 超 級 市 場 裏 的 貨 品 種 類 為 少 但 若 能 把 元 素 分 成 若 干 組 對 研 究 它 們 的 性 質 會 有 極 大 幫 助 究 竟 化 學 家 用 甚 麼 原 則 把 元 素
第2章 第 微觀世界 I 6 節 週期表 6.1 如何把元素分組 在 超 級 市 場 購 物 時 你 會 發 現 同 類 貨 品 都 會 擺 放 在 一 起 圖 6.1 元 素 的 數 目 雖 然 比 超 級 市 場 裏 的 貨 品 種 類 為 少 但 若 能 把 元 素 分 成 若 干 組 對 研 究 它 們 的 性 質 會 有 極 大 幫 助 究 竟 化 學 家 用 甚 麼 原 則 把 元 素
 2013~2015 保健食品產業專業人才 供需調查 2011 5 2011529 2012 2013~2015 2012 44.67% 2011 11.96% 2013~2015 ... 1... 1... 5... 10... 12... 13... 14... 19... 20... 22... 24... 12... 19... 21... 22 III IV 1... 1 2... 3
2013~2015 保健食品產業專業人才 供需調查 2011 5 2011529 2012 2013~2015 2012 44.67% 2011 11.96% 2013~2015 ... 1... 1... 5... 10... 12... 13... 14... 19... 20... 22... 24... 12... 19... 21... 22 III IV 1... 1 2... 3
教师招聘中学化学1-11.FIT)
 教 师 招 聘 考 试 中 学 化 学 历 年 真 题 汇 编 试 卷 渊 一 冤 渊 时 间 院 员 圆 园 分 钟 满 分 院 员 缘 园 分 冤 一 尧 单 项 选 择 题 渊 每 小 题 圆 分 袁 共 缘 园 分 冤 员 援 石 墨 烯 是 由 碳 原 子 构 成 的 单 层 片 状 结 构 的 新 材 料 渊 结 构 示 意 图 如 图 所 示 冤 袁 可 由 石 墨 剥 离 而 成 袁
教 师 招 聘 考 试 中 学 化 学 历 年 真 题 汇 编 试 卷 渊 一 冤 渊 时 间 院 员 圆 园 分 钟 满 分 院 员 缘 园 分 冤 一 尧 单 项 选 择 题 渊 每 小 题 圆 分 袁 共 缘 园 分 冤 员 援 石 墨 烯 是 由 碳 原 子 构 成 的 单 层 片 状 结 构 的 新 材 料 渊 结 构 示 意 图 如 图 所 示 冤 袁 可 由 石 墨 剥 离 而 成 袁
第 1 頁 95 學 年 度 共 15 頁 第 壹 部 分 ( 佔 96 分 ) 一 單 選 題 ( 佔 72 分 ) 說 明 : 第 1 至 36 題 為 單 選 題, 每 題 均 計 分 每 題 選 出 一 個 最 適 當 的 選 項, 標 示 在 答 案 卡 之 選 擇 題 答 案 區 每 題
 大 學 入 學 考 試 中 心 九 十 五 學 年 度 學 科 能 力 測 驗 試 題 - 作 答 注 意 事 項 - 考 試 時 間 : 100 分 鐘 題 型 題 數 第 壹 部 分 共 48 題 第 貳 部 分 共 20 題 作 答 方 式 用 2B 鉛 筆 在 答 案 卡 上 作 答, 修 正 時 應 以 橡 皮 擦 拭, 切 勿 使 用 修 正 液 選 擇 題 答 錯 不 倒 扣 參 考
大 學 入 學 考 試 中 心 九 十 五 學 年 度 學 科 能 力 測 驗 試 題 - 作 答 注 意 事 項 - 考 試 時 間 : 100 分 鐘 題 型 題 數 第 壹 部 分 共 48 題 第 貳 部 分 共 20 題 作 答 方 式 用 2B 鉛 筆 在 答 案 卡 上 作 答, 修 正 時 應 以 橡 皮 擦 拭, 切 勿 使 用 修 正 液 選 擇 題 答 錯 不 倒 扣 參 考
無投影片標題
 Organic Chemistry II 11.1 醇 類 硫 醇 和 醚 類 11.2 醇 類 和 醚 類 之 性 質 11.3 醛 類 和 酮 類 11.4 醛 類 和 酮 類 之 性 質 11.5 對 掌 分 子 11.6 羧 酸 類 11.7 酯 類 11.8 胺 類 11.9 醯 胺 類 11.1 醇 類 硫 醇 類 和 醚 類 ALCOHOLS, THIOLS AND ETHERS 將
Organic Chemistry II 11.1 醇 類 硫 醇 和 醚 類 11.2 醇 類 和 醚 類 之 性 質 11.3 醛 類 和 酮 類 11.4 醛 類 和 酮 類 之 性 質 11.5 對 掌 分 子 11.6 羧 酸 類 11.7 酯 類 11.8 胺 類 11.9 醯 胺 類 11.1 醇 類 硫 醇 類 和 醚 類 ALCOHOLS, THIOLS AND ETHERS 將
2 (Diffraction) 400nm 700nm Young
 990026 Physics 248 30 (02)2299-9006 (02)2299-9110 99 4 2000 Wave 2 (Diffraction) 400nm 700nm Young 2008 8 16 3 mm 4 LED 5 注意 : 噴灑過硫酸銅水溶液的酒精燈一定要清洗乾淨, 否則沒有燃燒到的銅離子附著在酒精燈外, 必定會使酒精燈的金屬外殼逐漸氧化 LED 6 7 8 CQ 提示
990026 Physics 248 30 (02)2299-9006 (02)2299-9110 99 4 2000 Wave 2 (Diffraction) 400nm 700nm Young 2008 8 16 3 mm 4 LED 5 注意 : 噴灑過硫酸銅水溶液的酒精燈一定要清洗乾淨, 否則沒有燃燒到的銅離子附著在酒精燈外, 必定會使酒精燈的金屬外殼逐漸氧化 LED 6 7 8 CQ 提示
99600936zw.PDF
 附 录 相对原子质量表 按照元素符号的字母次序排列 ( ) ( ) ( ) [ 1 1] ( 1 1) ( ) [ 1 2] ( ) [ 1 3] ( 1 3) [ 1 4] ( ) 4 1 2 3 4 [ ] 1 2 (1) (2) (3) (4) (5) (6) 3 0 1535 232 ( ) 101.325 101.325 100 357 2750 / 3 / 3 7.8 / 3 2.7
附 录 相对原子质量表 按照元素符号的字母次序排列 ( ) ( ) ( ) [ 1 1] ( 1 1) ( ) [ 1 2] ( ) [ 1 3] ( 1 3) [ 1 4] ( ) 4 1 2 3 4 [ ] 1 2 (1) (2) (3) (4) (5) (6) 3 0 1535 232 ( ) 101.325 101.325 100 357 2750 / 3 / 3 7.8 / 3 2.7
物質科學_化學篇
 物 質 科 學 化 學 篇 ( 上 ) 講 義 編 者 : 陳 義 忠 55 物 質 科 學 _ 化 學 篇 ( 上 ) 第 四 章 溶 液 4-1 溶 液 的 性 質 : 1. 溶 液 : (1) 由 兩 種 或 兩 種 以 上 的 純 物 質 混 合 而 成 的 均 勻 混 合 物, 稱 為 溶 液 包 含 固 態 液 態 及 氣 態 () 溶 液 由 溶 質 和 溶 劑 所 組 成 在 形 成
物 質 科 學 化 學 篇 ( 上 ) 講 義 編 者 : 陳 義 忠 55 物 質 科 學 _ 化 學 篇 ( 上 ) 第 四 章 溶 液 4-1 溶 液 的 性 質 : 1. 溶 液 : (1) 由 兩 種 或 兩 種 以 上 的 純 物 質 混 合 而 成 的 均 勻 混 合 物, 稱 為 溶 液 包 含 固 態 液 態 及 氣 態 () 溶 液 由 溶 質 和 溶 劑 所 組 成 在 形 成
在配位化學中, 配位基 EDTA 是屬於下列何者? 本試題共 5 頁 : 第 2 頁 (A) 單牙基 (Mono-dantate ligand) () 六牙基 (exa-dantate ligand) (B) 雙牙基 (Bi-dantate ligand) (D) 四牙基 (Tetra-dantat
 本試題共 5 頁 : 第 頁 注意事項 一 本試題共 50 題, 皆為單選題, 請選擇最適當選項, 每題 2 分, 共計 00 分, 每題答錯倒扣 07 分 ; 不作答不計分 二 答題依題號順序劃記在答案卡上, 寫在試題紙上無效 ; 答案卡限用 2B 鉛筆劃記, 若未按規定劃記, 致電腦無法讀取者, 考生自行負責 三 本試題必須與電腦答案卡一併繳回, 不得攜出試場 將 6 g 的尿素 (Urea,
本試題共 5 頁 : 第 頁 注意事項 一 本試題共 50 題, 皆為單選題, 請選擇最適當選項, 每題 2 分, 共計 00 分, 每題答錯倒扣 07 分 ; 不作答不計分 二 答題依題號順序劃記在答案卡上, 寫在試題紙上無效 ; 答案卡限用 2B 鉛筆劃記, 若未按規定劃記, 致電腦無法讀取者, 考生自行負責 三 本試題必須與電腦答案卡一併繳回, 不得攜出試場 將 6 g 的尿素 (Urea,
 - 2-2- HCO HPO SO 3 4 4 P P R P QR Q R Q + - - H HCO3 - HCO 3 - - Cl HCO 3 HCO - 3 - HCO - 3 - HCO 3 - = 100 2- SO 4 - H 2 PO 4 HPO 4 - HPO 4 2- Na
- 2-2- HCO HPO SO 3 4 4 P P R P QR Q R Q + - - H HCO3 - HCO 3 - - Cl HCO 3 HCO - 3 - HCO - 3 - HCO 3 - = 100 2- SO 4 - H 2 PO 4 HPO 4 - HPO 4 2- Na
(Microsoft Word \253\374\246\322\244\306\276\307\270\325\250\367\251w\275Z.doc)
 大學入學考試中心 九十九學年度指定科目考試試題 化學考科 - 作答注意事項 - 考試時間 :80 分鐘作答方式 : 選擇題用 B 鉛筆在 答案卡 上作答, 修正時應以橡皮擦拭, 切勿使用修正液 ( 帶 ) 非選擇題請在 答案卷 上作答, 務必使用筆尖較粗之黑色墨水的筆書寫, 且不得使用鉛筆 更正時, 可以使用修正液 ( 帶 ) 說明 : 下列資料, 可供回答問題之參考 一 元素週期表 (1~6 號元素
大學入學考試中心 九十九學年度指定科目考試試題 化學考科 - 作答注意事項 - 考試時間 :80 分鐘作答方式 : 選擇題用 B 鉛筆在 答案卡 上作答, 修正時應以橡皮擦拭, 切勿使用修正液 ( 帶 ) 非選擇題請在 答案卷 上作答, 務必使用筆尖較粗之黑色墨水的筆書寫, 且不得使用鉛筆 更正時, 可以使用修正液 ( 帶 ) 說明 : 下列資料, 可供回答問題之參考 一 元素週期表 (1~6 號元素
包 裝 維 生 素 礦 物 質 類 之 錠 狀 膠 囊 狀 食 品 營 養 標 示 應 遵 行 事 項 一 本 規 定 依 食 品 安 全 衛 生 管 理 法 第 二 十 二 條 第 三 項 規 定 訂 定 之 二 本 規 定 所 稱 維 生 素 礦 物 質 類 之 錠 狀 膠 囊 狀 食 品, 指
 包 裝 維 生 素 礦 物 質 類 之 錠 狀 膠 囊 狀 食 品 營 養 標 示 應 遵 行 事 項 一 本 規 定 依 食 品 安 全 衛 生 管 理 法 第 二 十 二 條 第 三 項 規 定 訂 定 之 二 本 規 定 所 稱 維 生 素 礦 物 質 類 之 錠 狀 膠 囊 狀 食 品, 指 以 營 養 添 加 劑 作 為 維 生 素 礦 物 質 來 源 之 錠 狀 膠 囊 狀 食 品 三
包 裝 維 生 素 礦 物 質 類 之 錠 狀 膠 囊 狀 食 品 營 養 標 示 應 遵 行 事 項 一 本 規 定 依 食 品 安 全 衛 生 管 理 法 第 二 十 二 條 第 三 項 規 定 訂 定 之 二 本 規 定 所 稱 維 生 素 礦 物 質 類 之 錠 狀 膠 囊 狀 食 品, 指 以 營 養 添 加 劑 作 為 維 生 素 礦 物 質 來 源 之 錠 狀 膠 囊 狀 食 品 三
 Fe O + 3CO = 2Fe + 3CO 2 3 2 160 256 1500 x 160 1500 = 2 56 x 2 = 56 1500 x 160 = 1050 x x 100 12 38 12 100 38 316 = = =. x x 1000 37 2 137 2 37 2 1000 137 2 271 = = =.... 36 100 40 100 40 36
Fe O + 3CO = 2Fe + 3CO 2 3 2 160 256 1500 x 160 1500 = 2 56 x 2 = 56 1500 x 160 = 1050 x x 100 12 38 12 100 38 316 = = =. x x 1000 37 2 137 2 37 2 1000 137 2 271 = = =.... 36 100 40 100 40 36
EXAMINATION RULES
 考 試 規 則 : 1. 競 賽 者 必 須 在 考 試 前 10 分 鐘 到 達 考 場 2. 競 賽 者 不 可 以 攜 帶 任 何 工 具, 但 是 個 人 所 需 要 的 醫 藥 用 品 及 器 具 不 在 此 限 3. 競 賽 者 必 須 坐 在 指 定 的 位 置 4. 在 考 試 開 始 前, 競 賽 者 必 須 檢 查 大 會 提 供 的 文 具 及 任 何 工 具 ( 筆 尺 計
考 試 規 則 : 1. 競 賽 者 必 須 在 考 試 前 10 分 鐘 到 達 考 場 2. 競 賽 者 不 可 以 攜 帶 任 何 工 具, 但 是 個 人 所 需 要 的 醫 藥 用 品 及 器 具 不 在 此 限 3. 競 賽 者 必 須 坐 在 指 定 的 位 置 4. 在 考 試 開 始 前, 競 賽 者 必 須 檢 查 大 會 提 供 的 文 具 及 任 何 工 具 ( 筆 尺 計
( )1. 已知 A 溶液 ph 值為 4.0, 若 B 溶液的氫離子濃度為 A 之 4 倍, 則 B 溶液 ph 值為多少? (A)8.0 (B)6.0 (C)4.4 (D)3.4 (E)3.2 答案 :(D) 解析 :A 液 :PH=4 [H + ]=10-4 M B 液 : [H + ]=4x
![( )1. 已知 A 溶液 ph 值為 4.0, 若 B 溶液的氫離子濃度為 A 之 4 倍, 則 B 溶液 ph 值為多少? (A)8.0 (B)6.0 (C)4.4 (D)3.4 (E)3.2 答案 :(D) 解析 :A 液 :PH=4 [H + ]=10-4 M B 液 : [H + ]=4x ( )1. 已知 A 溶液 ph 值為 4.0, 若 B 溶液的氫離子濃度為 A 之 4 倍, 則 B 溶液 ph 值為多少? (A)8.0 (B)6.0 (C)4.4 (D)3.4 (E)3.2 答案 :(D) 解析 :A 液 :PH=4 [H + ]=10-4 M B 液 : [H + ]=4x](/thumbs/95/122916627.jpg) ( )1. 已知 A 溶液 ph 值為 4.0, 若 B 溶液的氫離子濃度為 A 之 4 倍, 則 B 溶液 ph 值為多少? (A)8.0 (B)6.0 (C)4.4 (D).4 (E).2 答案 :(D) 解析 :A 液 :PH=4 [H + ]=10-4 M B 液 : [H + ]=4x10-4 M, 又 10-4
( )1. 已知 A 溶液 ph 值為 4.0, 若 B 溶液的氫離子濃度為 A 之 4 倍, 則 B 溶液 ph 值為多少? (A)8.0 (B)6.0 (C)4.4 (D).4 (E).2 答案 :(D) 解析 :A 液 :PH=4 [H + ]=10-4 M B 液 : [H + ]=4x10-4 M, 又 10-4
9-2
 第九章遺傳 第一節孟德爾的遺傳 豌豆 9-1 9-2 立人高中專用生物教材遺傳 9- 1 1 1 1 1 1 = 2 2 2 1 2 9- 9-5 立人高中專用生物教材遺傳 9-6 立人高中專用生物教材遺傳 9-7 立人高中專用生物教材遺傳 第二節半顯性與複對偶基因遺傳 ( 1 1 1 1 2 2 2 2 1 2 1 ( 9-8 立人高中專用生物教材遺傳 ( 9-9 立人高中專用生物教材遺傳 第三節二項式定理與多基因遺傳
第九章遺傳 第一節孟德爾的遺傳 豌豆 9-1 9-2 立人高中專用生物教材遺傳 9- 1 1 1 1 1 1 = 2 2 2 1 2 9- 9-5 立人高中專用生物教材遺傳 9-6 立人高中專用生物教材遺傳 9-7 立人高中專用生物教材遺傳 第二節半顯性與複對偶基因遺傳 ( 1 1 1 1 2 2 2 2 1 2 1 ( 9-8 立人高中專用生物教材遺傳 ( 9-9 立人高中專用生物教材遺傳 第三節二項式定理與多基因遺傳
一、
 中華民國第四十五屆中小學科學展覽會作品說明書 高中組生物 ( 生命科學 ) 科 040715 微在蛋隙 探討蛋殼奈米孔隙的通透性質 國立新竹女子高級中學 作者姓名 : 高二鄭涵 高二陳可萱 高二朱婉君 指導老師 : 張淳琤 何家齊 H2OCO2O2 1 O2 CO2 DDT O2CO2 H2O SO2 CO2 NO2 () () H2O 1. H2O 2. H2O 3. H2O () CO2 1.
中華民國第四十五屆中小學科學展覽會作品說明書 高中組生物 ( 生命科學 ) 科 040715 微在蛋隙 探討蛋殼奈米孔隙的通透性質 國立新竹女子高級中學 作者姓名 : 高二鄭涵 高二陳可萱 高二朱婉君 指導老師 : 張淳琤 何家齊 H2OCO2O2 1 O2 CO2 DDT O2CO2 H2O SO2 CO2 NO2 () () H2O 1. H2O 2. H2O 3. H2O () CO2 1.
Microsoft Word 指考化學試卷定稿.docx
 考試時間 :80 分鐘 作答方式 : 大學入學考試中心 106 學年度指定科目考試試題化學考科 - 作答注意事項 - 選擇題用 B 鉛筆在 答案卡 上作答 ; 更正時, 應以橡皮擦擦拭, 切勿使用修正液 ( 帶 ) 非選擇題用筆尖較粗之黑色墨水的筆在 答案卷 上作答 ; 更正時, 可以使用修正液 ( 帶 ) 未依規定畫記答案卡, 致機器掃描無法辨識答案 ; 或未使用黑色墨水的筆書寫答案卷, 致評閱人員無法辨認機器掃描後之答案者,
考試時間 :80 分鐘 作答方式 : 大學入學考試中心 106 學年度指定科目考試試題化學考科 - 作答注意事項 - 選擇題用 B 鉛筆在 答案卡 上作答 ; 更正時, 應以橡皮擦擦拭, 切勿使用修正液 ( 帶 ) 非選擇題用筆尖較粗之黑色墨水的筆在 答案卷 上作答 ; 更正時, 可以使用修正液 ( 帶 ) 未依規定畫記答案卡, 致機器掃描無法辨識答案 ; 或未使用黑色墨水的筆書寫答案卷, 致評閱人員無法辨認機器掃描後之答案者,
0 0 = 1 0 = 0 1 = = 1 1 = 0 0 = 1
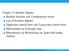 0 0 = 1 0 = 0 1 = 0 1 1 = 1 1 = 0 0 = 1 : = {0, 1} : 3 (,, ) = + (,, ) = + + (, ) = + (,,, ) = ( + )( + ) + ( + )( + ) + = + = = + + = + = ( + ) + = + ( + ) () = () ( + ) = + + = ( + )( + ) + = = + 0
0 0 = 1 0 = 0 1 = 0 1 1 = 1 1 = 0 0 = 1 : = {0, 1} : 3 (,, ) = + (,, ) = + + (, ) = + (,,, ) = ( + )( + ) + ( + )( + ) + = + = = + + = + = ( + ) + = + ( + ) () = () ( + ) = + + = ( + )( + ) + = = + 0
tbjxD219zw.PDF
 nm 1nm=10-9m CO 2 CO 2 1 1 A+B=AB 2H + O 2H O 2 2 2 AB=A+B A+BC=AC+B MnO 2 2KClO3 2KCl3O2 Zn+2HCl==ZnCl +H AB+CD=AD+CB NaOH+HC==NaCl+H O 1-2 S + O2 SO2 CuO + H Cu + H O 2 2 2 3 2Fe + 3CO 2 Fe O +
nm 1nm=10-9m CO 2 CO 2 1 1 A+B=AB 2H + O 2H O 2 2 2 AB=A+B A+BC=AC+B MnO 2 2KClO3 2KCl3O2 Zn+2HCl==ZnCl +H AB+CD=AD+CB NaOH+HC==NaCl+H O 1-2 S + O2 SO2 CuO + H Cu + H O 2 2 2 3 2Fe + 3CO 2 Fe O +
6-1-1極限的概念
 選 修 數 學 (I-4 多 項 式 函 數 的 極 限 與 導 數 - 導 數 與 切 線 斜 率 定 義. f ( 在 的 導 數 : f ( h 對 實 函 數 f ( 若 極 限 存 在 h h 則 稱 f ( 在 點 可 微 分 而 此 極 限 值 稱 為 f ( 在 的 導 數 以 f ( 表 示 f ( f ( 函 數 f ( 在 的 導 數 也 可 以 表 成 f ( 註 : 為 了
選 修 數 學 (I-4 多 項 式 函 數 的 極 限 與 導 數 - 導 數 與 切 線 斜 率 定 義. f ( 在 的 導 數 : f ( h 對 實 函 數 f ( 若 極 限 存 在 h h 則 稱 f ( 在 點 可 微 分 而 此 極 限 值 稱 為 f ( 在 的 導 數 以 f ( 表 示 f ( f ( 函 數 f ( 在 的 導 數 也 可 以 表 成 f ( 註 : 為 了
Microsoft Word - Z8I11A0-102.doc
 自 然 考 科 學 測 試 題 關 鍵 解 析 前 言 物 理 科 今 年 自 然 科 考 題 共 68 題, 其 中 物 理 科 占 了 17 題, 今 年 的 題 目 難 度 屬 中 偏 易, 考 題 分 配 十 分 平 均 由 於 是 新 課 綱 第 一 次 學 測, 所 以 新 的 內 容 大 致 上 均 入 題, 大 都 為 物 理 科 普 知 識 就 算 是 第 二 部 分 的 考 題,
自 然 考 科 學 測 試 題 關 鍵 解 析 前 言 物 理 科 今 年 自 然 科 考 題 共 68 題, 其 中 物 理 科 占 了 17 題, 今 年 的 題 目 難 度 屬 中 偏 易, 考 題 分 配 十 分 平 均 由 於 是 新 課 綱 第 一 次 學 測, 所 以 新 的 內 容 大 致 上 均 入 題, 大 都 為 物 理 科 普 知 識 就 算 是 第 二 部 分 的 考 題,
¦ÛµM¬ì²Ä3¦¸²Õ¨÷-¾Ç´ú¤ºŁ¶«ÊŁ±.prn, page Normalize ( <4D F736F F D20A6DBB54DACECB2C433A6B8B2D5A8F72DBEC7B4FAA4BAADB6ABCAADB12E646F63> )
 100 40 28 2B c 3 10 8 m s h 6.63 10 34 J s e 1.6 10 19 C hc 1240 E hf ev λ λ nm 1 ev 1.6 10-19 J 1 mol 6.02 10 23 ph 8 10 N 14 O 16 Fe 56 Ag 108 NO.99341003 103-E3 第壹部分 ( 占 80 分 ) 56 1 說明 : 第 1 題至第 k
100 40 28 2B c 3 10 8 m s h 6.63 10 34 J s e 1.6 10 19 C hc 1240 E hf ev λ λ nm 1 ev 1.6 10-19 J 1 mol 6.02 10 23 ph 8 10 N 14 O 16 Fe 56 Ag 108 NO.99341003 103-E3 第壹部分 ( 占 80 分 ) 56 1 說明 : 第 1 題至第 k
7-2 水溶液的酸鹼性與pH值 補充題目
 一 單選題 7- 水溶液的酸鹼性與 ph 值補充題目 (D). 對中性水溶液而言, 溫度升高時, 下列正確敘述為 (A)pH 變大 (B)pOH 變大 (C) 變小 (D) 水的解離度 增加 (E). 均為 ph=3 的甲 乙水溶液, 甲液溫度 0C, 乙液為 60C, 則 (A) 甲乙之 [H + ][OH - ] 值相等 (B) 甲的 較大 (C) 甲乙之 poh 相等 (D) 乙的酸性比甲弱
一 單選題 7- 水溶液的酸鹼性與 ph 值補充題目 (D). 對中性水溶液而言, 溫度升高時, 下列正確敘述為 (A)pH 變大 (B)pOH 變大 (C) 變小 (D) 水的解離度 增加 (E). 均為 ph=3 的甲 乙水溶液, 甲液溫度 0C, 乙液為 60C, 則 (A) 甲乙之 [H + ][OH - ] 值相等 (B) 甲的 較大 (C) 甲乙之 poh 相等 (D) 乙的酸性比甲弱
PowerPoint 簡報
 氧化還原滴定教學 013,4 化學科劉獻文師 1 大綱 氧化還原反應與方程式平衡 氧化還原滴定實驗操作 氧化還原滴定的電位計算 常見的氧化還原滴定法 : 高錳酸鉀法 二鉻酸鉀法 碘量法 氧化還原反應 氧化還原反應 : 當物質相遇時, 電子從甲物質傳遞至乙物質的現象或反應 氧化 : 物質失去電子的反應 還原 : 物質得到電子的反應 還原劑 : 氧化還原反應中提供 ( 或失去 ) 電子者 氧化劑 : 氧化還原反應中得到
氧化還原滴定教學 013,4 化學科劉獻文師 1 大綱 氧化還原反應與方程式平衡 氧化還原滴定實驗操作 氧化還原滴定的電位計算 常見的氧化還原滴定法 : 高錳酸鉀法 二鉻酸鉀法 碘量法 氧化還原反應 氧化還原反應 : 當物質相遇時, 電子從甲物質傳遞至乙物質的現象或反應 氧化 : 物質失去電子的反應 還原 : 物質得到電子的反應 還原劑 : 氧化還原反應中提供 ( 或失去 ) 電子者 氧化劑 : 氧化還原反應中得到
电 化 电 化 学 学 第 2 讲 原 电 池 一 教 学 目 标 理 解 原 电 池 的 工 作 原 理 并 正 确 书 写 电 极 反 应 和 总 反 应 方 程 式 知 识 导 航 构 造 条 件 构 造 及 工 作 原 理 工 作 原 理 燃 料 电 池 原 电 池 电 极 反 应 及 现
 www.xdf.cn 1 电 化 电 化 学 学 第 2 讲 原 电 池 一 教 学 目 标 理 解 原 电 池 的 工 作 原 理 并 正 确 书 写 电 极 反 应 和 总 反 应 方 程 式 知 识 导 航 构 造 条 件 构 造 及 工 作 原 理 工 作 原 理 燃 料 电 池 原 电 池 电 极 反 应 及 现 象 常 规 电 池 新 型 电 池 综 合 训 练 二 教 学 重 点 和
www.xdf.cn 1 电 化 电 化 学 学 第 2 讲 原 电 池 一 教 学 目 标 理 解 原 电 池 的 工 作 原 理 并 正 确 书 写 电 极 反 应 和 总 反 应 方 程 式 知 识 导 航 构 造 条 件 构 造 及 工 作 原 理 工 作 原 理 燃 料 电 池 原 电 池 电 极 反 应 及 现 象 常 规 电 池 新 型 电 池 综 合 训 练 二 教 学 重 点 和
市立臺中一中 106 學年度第一學期第一次期中考高二化學科試題 單選題及多重選擇題請將答案填入答案卡, 劃記不清不予計分 非選擇題請將答案填寫於答案卷上, 與答案卡一併繳回電腦卡代號 :05 一 單選題 (15 題每題 3 分共 45 分 ) ( )01. 某溶液加入 Na 2 SO 4(aq) 不
 市立臺中一中 106 學年度第一學期第一次期中考高二化學科試題 單選題及多重選擇題請將答案填入答案卡, 劃記不清不予計分 非選擇題請將答案填寫於答案卷上, 與答案卡一併繳回電腦卡代號 :05 一 單選題 (15 題每題 3 分共 45 分 ) ( )01. 某溶液加入 Na 2 SO 4(aq) 不沉澱, 但加入 AgNO 3(aq) 會產生黑褐色沉澱, 則該溶液最有可能是以下何者? (A)KNO
市立臺中一中 106 學年度第一學期第一次期中考高二化學科試題 單選題及多重選擇題請將答案填入答案卡, 劃記不清不予計分 非選擇題請將答案填寫於答案卷上, 與答案卡一併繳回電腦卡代號 :05 一 單選題 (15 題每題 3 分共 45 分 ) ( )01. 某溶液加入 Na 2 SO 4(aq) 不沉澱, 但加入 AgNO 3(aq) 會產生黑褐色沉澱, 則該溶液最有可能是以下何者? (A)KNO
08分析實驗二 莫耳法測定氯含量.doc
 一 目的 實驗二 莫耳法測定氯含量 學習莫耳 (Mohr method) 沉澱滴定法, 利用氯化銀沉澱的產生, 測 定未知物樣品中氯離子的含量, 並熟悉重量滴定法 (weight titration method) 圖 2-1 重量滴定分析 圖 2-2 以碳酸氫鈉控制酸鹼度 - 1 - 二 原理 沉澱滴定法 (Precipitation titrimetry) 是利用滴定劑與待分析物形成難溶的離子性沉澱物
一 目的 實驗二 莫耳法測定氯含量 學習莫耳 (Mohr method) 沉澱滴定法, 利用氯化銀沉澱的產生, 測 定未知物樣品中氯離子的含量, 並熟悉重量滴定法 (weight titration method) 圖 2-1 重量滴定分析 圖 2-2 以碳酸氫鈉控制酸鹼度 - 1 - 二 原理 沉澱滴定法 (Precipitation titrimetry) 是利用滴定劑與待分析物形成難溶的離子性沉澱物
2817.00.10.00.7 氧 化 鋅 2820.90.00.00.5-A 氧 化 亞 錳 2820.90.00.00.5-Y 其 他 氧 化 錳 ( 食 品 添 加 物 ) 2821.10.11.00.8-A 氧 化 鐵 2 / 23 2821.10.11.00.8-Y 氧 化 鐵, 三 氧
 1301.90.40.00.7 蟲 膠 1302.39.10.00.6 鹿 角 菜 膠 1515.30.00.00.0-A 蓖 麻 油 1515.30.00.00.0-Y 篦 麻 油 及 其 餾 分 物 ( 食 品 添 加 物 ) 1521.10.00.00.6-A 米 糠 蠟 1521.10.00.00.6-Y 植 物 蠟, 不 論 已 否 精 製 或 著 色 ( 食 品 添 加 物 ) 2102.30.00.00.7
1301.90.40.00.7 蟲 膠 1302.39.10.00.6 鹿 角 菜 膠 1515.30.00.00.0-A 蓖 麻 油 1515.30.00.00.0-Y 篦 麻 油 及 其 餾 分 物 ( 食 品 添 加 物 ) 1521.10.00.00.6-A 米 糠 蠟 1521.10.00.00.6-Y 植 物 蠟, 不 論 已 否 精 製 或 著 色 ( 食 品 添 加 物 ) 2102.30.00.00.7
彰化縣第51屆中小學科學展覽會
 彰 化 縣 101 年 第 52 屆 中 小 學 科 學 展 覽 會 作 品 說 明 書 科 別 : 化 學 科 組 別 : 國 中 組 作 品 名 稱 : 關 鍵 詞 : 晶 寶 寶 氫 鍵 聚 合 物 - 以 分 子 觀 點 探 討 晶 寶 寶 吸 現 象 編 號 : - I - 目 錄 摘 要 --------------------------------------------------------------------------------------------------
彰 化 縣 101 年 第 52 屆 中 小 學 科 學 展 覽 會 作 品 說 明 書 科 別 : 化 學 科 組 別 : 國 中 組 作 品 名 稱 : 關 鍵 詞 : 晶 寶 寶 氫 鍵 聚 合 物 - 以 分 子 觀 點 探 討 晶 寶 寶 吸 現 象 編 號 : - I - 目 錄 摘 要 --------------------------------------------------------------------------------------------------
大學甄選入學委員會
 14 學 年 度 大 學 繁 星 推 薦 入 學 - 第 一 類 學 群 至 第 七 類 學 群 各 校 系 一 覽 表 21 中 學 系 16 16 22 外 國 語 文 學 系 23 劇 場 藝 術 學 系 2 2 24 企 業 管 理 學 系 1 11 2 資 訊 管 理 學 系 學 測 術 科 考 試 分 發 比 序 科 目 檢 定 及 級 分 項 目 檢 定 及 分 數 項 目 4 4 學
14 學 年 度 大 學 繁 星 推 薦 入 學 - 第 一 類 學 群 至 第 七 類 學 群 各 校 系 一 覽 表 21 中 學 系 16 16 22 外 國 語 文 學 系 23 劇 場 藝 術 學 系 2 2 24 企 業 管 理 學 系 1 11 2 資 訊 管 理 學 系 學 測 術 科 考 試 分 發 比 序 科 目 檢 定 及 級 分 項 目 檢 定 及 分 數 項 目 4 4 學
分 的 理 解 和 把 握, 对 基 础 知 识 多 回 顾 多 记 忆 北 京 新 东 方 学 校 优 能 中 学 高 中 理 综 项 目 3. 流 式 细 胞 仪 可 根 据 细 胞 中 DNA 含 量 的 不 同 对 细 胞 分 别 计 数 研 究 者 用 某 抗 癌 药 物 处 理 体 外
 北 京 市 2015 年 高 考 理 综 试 题 逐 题 解 析 北 京 新 东 方 优 能 中 学 高 中 理 综 项 目 1. 乙 肝 疫 苗 的 有 效 成 分 是 乙 肝 病 毒 的 一 种 抗 原, 接 种 该 疫 苗 后, 人 体 会 产 生 相 应 抗 体 该 抗 体 A. 由 T 淋 巴 细 胞 产 生 B. 可 与 多 种 抗 原 结 合 C. 可 裂 解 乙 肝 病 毒 D. 可
北 京 市 2015 年 高 考 理 综 试 题 逐 题 解 析 北 京 新 东 方 优 能 中 学 高 中 理 综 项 目 1. 乙 肝 疫 苗 的 有 效 成 分 是 乙 肝 病 毒 的 一 种 抗 原, 接 种 该 疫 苗 后, 人 体 会 产 生 相 应 抗 体 该 抗 体 A. 由 T 淋 巴 细 胞 产 生 B. 可 与 多 种 抗 原 结 合 C. 可 裂 解 乙 肝 病 毒 D. 可
1970 新技術的應用 X = 20 + B 13B δ13c X 1 X
 凡發生過的必留下痕跡 同位素分析的考古應用? 如何考古 06 2013 9 489 經由人骨中碳和氮同位素的分析, 提供考古學家另一個探討古代攝食系統的途徑 另外, 可以藉由鍶同位素分析了解人群的來源與遷移過程 1970 新技術的應用 13 15 13 12 15 14 13 15 13 12 15 13 15 13 X = 20 + B 13B δ13c X 1 X 2013 9 489 07 δ
凡發生過的必留下痕跡 同位素分析的考古應用? 如何考古 06 2013 9 489 經由人骨中碳和氮同位素的分析, 提供考古學家另一個探討古代攝食系統的途徑 另外, 可以藉由鍶同位素分析了解人群的來源與遷移過程 1970 新技術的應用 13 15 13 12 15 14 13 15 13 12 15 13 15 13 X = 20 + B 13B δ13c X 1 X 2013 9 489 07 δ
zyk00217zw.PDF
 NH NO N 2H O 4 2 2 2 1 1 N2 + O2 === NO 2 2 /K 1000 1500 1811 2033 8.86 10 5 3.30 10 3 1.14 10 2 2.21 10 2 CaC2 N 2 CaCN 2C 1000 Na 2CO 34CN 2 2NaCN3CO /Pa NH / 1.01 5.05 1.01 3.03 6.06 10 6 10 6 10 7
NH NO N 2H O 4 2 2 2 1 1 N2 + O2 === NO 2 2 /K 1000 1500 1811 2033 8.86 10 5 3.30 10 3 1.14 10 2 2.21 10 2 CaC2 N 2 CaCN 2C 1000 Na 2CO 34CN 2 2NaCN3CO /Pa NH / 1.01 5.05 1.01 3.03 6.06 10 6 10 6 10 7
Microsoft PowerPoint - ch04
 第四章 化學反應的型態與溶液的計量化學 (Solution Stoichiometry) 水 生命之必需是一種常用的溶劑 (solvent) 形成水溶液 (aqueous solution) 常以 (aq) 的下標表示例如 : Na + (aq) 結構 H δ H δ + δ + 105 o 高度極化的 H 鍵 氫帶部分正電荷 δ 帶部分負電荷 δ + 帶部分正電荷 整體而言 : 為一極性分子 (polar
第四章 化學反應的型態與溶液的計量化學 (Solution Stoichiometry) 水 生命之必需是一種常用的溶劑 (solvent) 形成水溶液 (aqueous solution) 常以 (aq) 的下標表示例如 : Na + (aq) 結構 H δ H δ + δ + 105 o 高度極化的 H 鍵 氫帶部分正電荷 δ 帶部分負電荷 δ + 帶部分正電荷 整體而言 : 為一極性分子 (polar
碳石墨產品 特種石墨 (1) 單晶矽製造設備 (2) 臨界電漿測試設備 (JT-60) * 照片由日本原子力研究開發機構提供 (1) (2)
 碳石墨產品 特種石墨 (1) 單晶矽製造設備 (2) 臨界電漿測試設備 (JT-6) * 照片由日本原子力研究開發機構提供 (1) (2) 特種石墨產品特性 (CIP) 等方性石墨 等方性石墨和異方性石墨 1 µm 可靠性高 超強耐熱性 2, 2,5 卓越的導電性 出色的耐化學性 輕量且便於加工 1 µm 5 1 15 2 [Mg/m 3 ] 5 製程 / 6 用途 LED EDM 環境和能源 *
碳石墨產品 特種石墨 (1) 單晶矽製造設備 (2) 臨界電漿測試設備 (JT-6) * 照片由日本原子力研究開發機構提供 (1) (2) 特種石墨產品特性 (CIP) 等方性石墨 等方性石墨和異方性石墨 1 µm 可靠性高 超強耐熱性 2, 2,5 卓越的導電性 出色的耐化學性 輕量且便於加工 1 µm 5 1 15 2 [Mg/m 3 ] 5 製程 / 6 用途 LED EDM 環境和能源 *
Gaussian Reflection
 第 七 章 芳 香 胺 类 药 物 的 分 析 芳 胺 类 药 物 芳 烃 胺 类 药 物 : 苯 乙 胺 类 药 物 芳 氧 丙 醇 胺 类 药 物 第 一 节 芳 胺 类 药 物 的 分 析 对 氨 基 苯 甲 酸 酯 类 芳 酰 胺 类 一. 基 本 结 构 和 典 型 药 物 ( 一 ) 对 氨 基 苯 甲 酸 酯 类 药 物 基 本 结 构 : O R 1 NH C OR 2 典 型 药
第 七 章 芳 香 胺 类 药 物 的 分 析 芳 胺 类 药 物 芳 烃 胺 类 药 物 : 苯 乙 胺 类 药 物 芳 氧 丙 醇 胺 类 药 物 第 一 节 芳 胺 类 药 物 的 分 析 对 氨 基 苯 甲 酸 酯 类 芳 酰 胺 类 一. 基 本 结 构 和 典 型 药 物 ( 一 ) 对 氨 基 苯 甲 酸 酯 类 药 物 基 本 结 构 : O R 1 NH C OR 2 典 型 药
 é SI 12g C = 6 12 = 1 H2( g) + O2( g) H2O( l) + 286kJ ( 1) 2 1 1 H 2( g) + O2( g) H2O( l) H = 286kJ mol ( 2) 2 1 N 2 ( g) + O2( g) NO 2 ( g) 34kJ 2 1 1 N 2 ( g) + O2( g) NO 2 ( g) H = + 34kJ mol 2 1 N
é SI 12g C = 6 12 = 1 H2( g) + O2( g) H2O( l) + 286kJ ( 1) 2 1 1 H 2( g) + O2( g) H2O( l) H = 286kJ mol ( 2) 2 1 N 2 ( g) + O2( g) NO 2 ( g) 34kJ 2 1 1 N 2 ( g) + O2( g) NO 2 ( g) H = + 34kJ mol 2 1 N
食 品 添 加 物 規 格 檢 驗 方 法 清 單 編 號 品 名 公 告 日 期 第 ( 八 ) 類 營 養 添 加 劑 08001 食 品 添 加 物 規 格 檢 驗 方 法 - 維 生 素 A 粉 末 80 年 9 月 10 日 衛 署 食 字 第 971766 號 08002 食 品 添 加
 附 表 防 疫 物 資 安 全 儲 備 品 項 表 分 類 防 疫 藥 品 防 疫 器 材 防 護 裝 備 品 項 一 藥 品 : ( 一 ) 用 於 預 防 性 投 藥 之 抗 生 素 ( 二 ) 流 感 抗 病 毒 藥 物 二 病 媒 防 治 用 藥 : 行 政 院 環 境 保 護 署 許 可 輸 入 製 造 之 環 境 用 藥 殺 蟲 劑 昆 蟲 生 長 調 節 劑 及 微 生 物 製 劑 三
附 表 防 疫 物 資 安 全 儲 備 品 項 表 分 類 防 疫 藥 品 防 疫 器 材 防 護 裝 備 品 項 一 藥 品 : ( 一 ) 用 於 預 防 性 投 藥 之 抗 生 素 ( 二 ) 流 感 抗 病 毒 藥 物 二 病 媒 防 治 用 藥 : 行 政 院 環 境 保 護 署 許 可 輸 入 製 造 之 環 境 用 藥 殺 蟲 劑 昆 蟲 生 長 調 節 劑 及 微 生 物 製 劑 三
<4D6963726F736F667420576F7264202D20C2C8BBAFB0B1BBF9B9AFA1AAA1AAECEEB0DFCBAAD6D0B5C4D2FED0CEC9B1CAD62E646F63>
 氯 化 氨 基 汞 祛 斑 霜 中 的 隐 形 杀 手 北 京 大 学 经 济 学 院 陆 雨 薇 摘 要 : 氯 化 氨 基 汞 是 劣 质 祛 斑 霜 中 经 常 使 用 的 添 加 剂 本 文 首 先 分 析 了 氯 化 氨 基 汞 的 结 构 性 质 制 备, 并 进 而 设 计 和 比 较 了 几 种 简 易 且 可 行 性 较 好 的 氯 化 氨 基 汞 检 测 方 法 应 用 这 些
氯 化 氨 基 汞 祛 斑 霜 中 的 隐 形 杀 手 北 京 大 学 经 济 学 院 陆 雨 薇 摘 要 : 氯 化 氨 基 汞 是 劣 质 祛 斑 霜 中 经 常 使 用 的 添 加 剂 本 文 首 先 分 析 了 氯 化 氨 基 汞 的 结 构 性 质 制 备, 并 进 而 设 计 和 比 较 了 几 种 简 易 且 可 行 性 较 好 的 氯 化 氨 基 汞 检 测 方 法 应 用 这 些
试卷
 江 西 省 三 校 2016 届 高 三 联 考 化 学 试 题 可 能 用 到 的 相 对 原 子 质 量 :H=1 O=16 C=12 N=14 S=32 Na=23 Fe=56 Cu=64 一 选 择 题 ( 每 小 题 只 有 一 个 正 确 答 案, 每 小 题 3 分, 共 计 48 分 ) 1. 下 列 有 关 化 学 用 语 表 示 正 确 的 是 ( ) A. 水 分 子 的 球
江 西 省 三 校 2016 届 高 三 联 考 化 学 试 题 可 能 用 到 的 相 对 原 子 质 量 :H=1 O=16 C=12 N=14 S=32 Na=23 Fe=56 Cu=64 一 选 择 题 ( 每 小 题 只 有 一 个 正 确 答 案, 每 小 题 3 分, 共 计 48 分 ) 1. 下 列 有 关 化 学 用 语 表 示 正 确 的 是 ( ) A. 水 分 子 的 球
 ( )C:H:O = 40.0 12 : 6.7 1 :53.3 = 3.33:6.7:3.33 = 1:2:1(10 ) 16 4.C + H O CO + H (3 ) 2 2 11.2 5.6 = 0.5 O 2 ; = 0.25) H 2 (3 22.4 22.4 0.322.41000 x = = 60 (4 ) 256 + + (1) K NH PO, 4 (, ): 4 (,
( )C:H:O = 40.0 12 : 6.7 1 :53.3 = 3.33:6.7:3.33 = 1:2:1(10 ) 16 4.C + H O CO + H (3 ) 2 2 11.2 5.6 = 0.5 O 2 ; = 0.25) H 2 (3 22.4 22.4 0.322.41000 x = = 60 (4 ) 256 + + (1) K NH PO, 4 (, ): 4 (,
(1) (2) (3) 1. (1) 2
 0386 71.32% 14A 1 (1) (2) (3) 1. (1) 2 (a) (b) (i) (ii) (iii) 3 (iv) (a) (b) (c) (d) 6% 4 2013 3 26 [2013]624 10 5 2013 6 28 [2013]1246 2015 3 [2015]351 0.2 6 [2015]748 180C 7 * * 8 14A (2) 417,800,000
0386 71.32% 14A 1 (1) (2) (3) 1. (1) 2 (a) (b) (i) (ii) (iii) 3 (iv) (a) (b) (c) (d) 6% 4 2013 3 26 [2013]624 10 5 2013 6 28 [2013]1246 2015 3 [2015]351 0.2 6 [2015]748 180C 7 * * 8 14A (2) 417,800,000
(Microsoft Word - 98\244\306\276\307.doc)
 中國醫藥大學九十八學年度學士後中醫學系招生考試試題 科目 : 化學 注意事項 1. 本試題共計 5 頁, 如有缺頁應立即舉手, 請監試人員補發 2. 選擇題答案請以 2B 鉛筆作答於電腦答案卡, 如寫在本試題紙上不予計分 3. 本試題必須隨同電腦答案卡一併繳交 選擇題 ( 單選題, 共 50 題, 每題 2 分, 共 100 分, 請選擇最合適的答案 ) 考試時間 : 八十分鐘 1. 下列哪一個物質的鹼性最強
中國醫藥大學九十八學年度學士後中醫學系招生考試試題 科目 : 化學 注意事項 1. 本試題共計 5 頁, 如有缺頁應立即舉手, 請監試人員補發 2. 選擇題答案請以 2B 鉛筆作答於電腦答案卡, 如寫在本試題紙上不予計分 3. 本試題必須隨同電腦答案卡一併繳交 選擇題 ( 單選題, 共 50 題, 每題 2 分, 共 100 分, 請選擇最合適的答案 ) 考試時間 : 八十分鐘 1. 下列哪一個物質的鹼性最強
《化學》試題評析
 103 年 學 士 後 中 全 套 詳 解 化 學 選 擇 題 ( 單 選 題, 共 50 題, 每 題 2 分, 共 100 分, 請 選 擇 最 合 適 的 答 案 ) (D) 1. 下 列 反 應 中, 下 列 反 應 中, 3.0 莫 耳 的 甲 與 2.0 莫 耳 的 乙 反 應 生 成 4.0 莫 耳 的 丙, 請 問 此 反 應 的 產 率 是 多 少? 2 甲 + 乙 3 丙 + 丁
103 年 學 士 後 中 全 套 詳 解 化 學 選 擇 題 ( 單 選 題, 共 50 題, 每 題 2 分, 共 100 分, 請 選 擇 最 合 適 的 答 案 ) (D) 1. 下 列 反 應 中, 下 列 反 應 中, 3.0 莫 耳 的 甲 與 2.0 莫 耳 的 乙 反 應 生 成 4.0 莫 耳 的 丙, 請 問 此 反 應 的 產 率 是 多 少? 2 甲 + 乙 3 丙 + 丁
实 验 结 果 选 用 多 种 晶 体 盐 在 不 同 磷 酸 三 钠 溶 液 中 进 行 生 长 快 慢 探 究, 最 后 确 定 磷 酸 三 钠 溶 液 的 最 佳 浓 度 为 5% 左 右 本 实 验 方 案 提 供 了 多 种 实 验 装 置 供 大 家 选 用, 让 师 生 有 更 多 的
 设 计 编 号 01-173 题 目 奇 妙 的 化 学 溶 洞 原 料 磷 酸 三 钠 ( 晶 体 ) 三 氯 化 铁 ( 晶 体 ) 氯 化 铜 ( 晶 体 ) 胆 矾 ( 晶 体 ) 明 矾 ( 晶 体 ) 硫 酸 镁 ( 晶 体 ) 蒸 馏 水 等 仪 器 设 备 标 本 瓶 或 一 次 性 透 明 水 杯 或 烧 杯 EPE 珍 珠 棉 泡 沫 粗 铜 丝 塑 料 吸 管 美 工 刀 直
设 计 编 号 01-173 题 目 奇 妙 的 化 学 溶 洞 原 料 磷 酸 三 钠 ( 晶 体 ) 三 氯 化 铁 ( 晶 体 ) 氯 化 铜 ( 晶 体 ) 胆 矾 ( 晶 体 ) 明 矾 ( 晶 体 ) 硫 酸 镁 ( 晶 体 ) 蒸 馏 水 等 仪 器 设 备 标 本 瓶 或 一 次 性 透 明 水 杯 或 烧 杯 EPE 珍 珠 棉 泡 沫 粗 铜 丝 塑 料 吸 管 美 工 刀 直
1
 1 () () 2 () () 1987 1988 () () 2010 來 理 3 () () () () () 4 () ( ) ( ) 來 理 () 1 5 高中生對手搖杯飲料之成癮度探討 高中生對手搖杯飲料之成癮度探討 以東港海事為例 價格便 宜 14% 離家近 12% 特色茶 飲 店面 19% 設計 3% 品牌 10% 促銷活 動 8% 品質 14% 碳酸 咖啡 6% 2% 服 務 態 度
1 () () 2 () () 1987 1988 () () 2010 來 理 3 () () () () () 4 () ( ) ( ) 來 理 () 1 5 高中生對手搖杯飲料之成癮度探討 高中生對手搖杯飲料之成癮度探討 以東港海事為例 價格便 宜 14% 離家近 12% 特色茶 飲 店面 19% 設計 3% 品牌 10% 促銷活 動 8% 品質 14% 碳酸 咖啡 6% 2% 服 務 態 度
学 而 思 老 师 们 の 嘱 托 集 数 学 詹 昊 凯 老 师 の 嘱 托 丨 从 近 年 高 考 命 题 看 解 析 几 何 复 习 方 向...2 问 老 师 の 嘱 托 丨 一 点 高 等 数 学 知 识 就 能 够 秒 杀 函 数 导 数 题?!...5 杨 老 师 の 嘱 托 丨 1
 咨 询 电 话 1010899 2016 高 考 命 题 方 向 预 测 大 型 讲 座 在 考 后 填 报 志 愿 的 今 天, 每 1 分 都 变 得 更 加 珍 贵 知 己 知 彼 方 能 百 战 不 殆, 对 高 考 的 熟 悉 程 度 将 在 一 定 程 度 上 影 响 你 的 实 力 发 挥, 而 近 年 高 考 和 一 模 二 模 都 会 潜 移 默 化 的 影 响 着 今 年 高 考,
咨 询 电 话 1010899 2016 高 考 命 题 方 向 预 测 大 型 讲 座 在 考 后 填 报 志 愿 的 今 天, 每 1 分 都 变 得 更 加 珍 贵 知 己 知 彼 方 能 百 战 不 殆, 对 高 考 的 熟 悉 程 度 将 在 一 定 程 度 上 影 响 你 的 实 力 发 挥, 而 近 年 高 考 和 一 模 二 模 都 会 潜 移 默 化 的 影 响 着 今 年 高 考,
ZX 102 國 文 科 大 甲 高 中 朱 碧 霞 老 師 壹 前 言 102 99.07.29 1. 2. 3. 4. 99 101 38 2 76 1 24 102 1. 20 2. 6 18 1 貳 試 題 分 析 99 101 102 一 選 擇 題 1 99~101 年 試 卷 架 構
 102 四技二專 統一入學測驗 大甲高中 朱碧霞 老師 共同科目 國文 發行人 陳炳亨 總召集 周耀琨 總編輯 蔣海燕 主 編 陳俊龍 校 對 黃筱閔 美 編 林靖雨.本書內容同步刊載於翰林我的網 出 版 民國一 二年一月 發行所 7 0 2 4 8 臺南市新樂路 76 號 編輯部 7 0 2 5 2 臺南市新忠路 8-1 號 電 話 (06)2619621#314 E-mail periodical@hanlin.com.tw
102 四技二專 統一入學測驗 大甲高中 朱碧霞 老師 共同科目 國文 發行人 陳炳亨 總召集 周耀琨 總編輯 蔣海燕 主 編 陳俊龍 校 對 黃筱閔 美 編 林靖雨.本書內容同步刊載於翰林我的網 出 版 民國一 二年一月 發行所 7 0 2 4 8 臺南市新樂路 76 號 編輯部 7 0 2 5 2 臺南市新忠路 8-1 號 電 話 (06)2619621#314 E-mail periodical@hanlin.com.tw
< B2C438B4C1A4C6BEC7ABFCA6D2B4C1A55A2E696E6464>
 2016 第8期 獨家發行 CHEMISTRY 電子檔索取QR 專刊 http://www.facebook.com/chwachemistry https://goo.gl/6js7dx ፓ ᒙᡡ ᾦ ፍᚯ 員林高中 陳品誌老師 筆者曾對本校學生針對 105 指考化學考科的準備作一些趨勢分析 其中 杕只要有計算的部分 一定涉及 化學計量 的觀念 包含莫耳數 氣體化合體積定律 結合理想氣體 的相關定律等
2016 第8期 獨家發行 CHEMISTRY 電子檔索取QR 專刊 http://www.facebook.com/chwachemistry https://goo.gl/6js7dx ፓ ᒙᡡ ᾦ ፍᚯ 員林高中 陳品誌老師 筆者曾對本校學生針對 105 指考化學考科的準備作一些趨勢分析 其中 杕只要有計算的部分 一定涉及 化學計量 的觀念 包含莫耳數 氣體化合體積定律 結合理想氣體 的相關定律等
99學年度康熹版本指考模擬卷解答.doc
 九十九學年度指定科目考試模擬試卷 化學考科 教師解答卷 - 作答注意事項 - 考試時間 :80 分鐘 作答方式 : 請使用較粗的黑色原子筆 鋼珠筆或中性筆, 在 答案卷 上作答 命題老師 : 中和高中 / 周裕明老師 說明 : 下列資料, 可供回答問題之參考一 元素週期表 (1~36 號元素 ) 1 H 1.0 3 Li 6.9 4 Be 9.0 11 12 Na Mg 23.0 24.3 19 K
九十九學年度指定科目考試模擬試卷 化學考科 教師解答卷 - 作答注意事項 - 考試時間 :80 分鐘 作答方式 : 請使用較粗的黑色原子筆 鋼珠筆或中性筆, 在 答案卷 上作答 命題老師 : 中和高中 / 周裕明老師 說明 : 下列資料, 可供回答問題之參考一 元素週期表 (1~36 號元素 ) 1 H 1.0 3 Li 6.9 4 Be 9.0 11 12 Na Mg 23.0 24.3 19 K
试卷
 玉 溪 一 中 高 2015 届 高 三 上 学 期 期 中 考 化 学 试 题 相 对 原 子 质 量 : N-14,Na-23,Cl-35.5, Cu-64 说 明 : 测 试 时 间 120 分 钟, 满 分 100 分 第 I 卷 ( 选 择 题 共 46 分 ) 一 选 择 题 ( 本 题 包 括 23 小 题, 每 小 题 2 分, 共 46 分 每 小 题 只 有 一 个... 选 项
玉 溪 一 中 高 2015 届 高 三 上 学 期 期 中 考 化 学 试 题 相 对 原 子 质 量 : N-14,Na-23,Cl-35.5, Cu-64 说 明 : 测 试 时 间 120 分 钟, 满 分 100 分 第 I 卷 ( 选 择 题 共 46 分 ) 一 选 择 题 ( 本 题 包 括 23 小 题, 每 小 题 2 分, 共 46 分 每 小 题 只 有 一 个... 选 项
目錄 單元一 : 化學計量 P.1 單元二 : 氣體 P.8 單元三 : 溶液 P.15 單元四 : 反應速率與平衡 P. 單元五 : 酸鹼鹽 P.3 單元六 : 氧化還原 P.40 單元七 : 原子結構與週期表 P.49 單元八 : 化學鍵 P.54 單元九 : 金屬與非金屬 P.63 單元十 :
 忠明高中總複習叢書 化學總複習精華 解答本 說明 : 下列資料, 可供回答問題之參考 一 元素週期表 (1~36 號元素 ) 1 H 1.0 3 Li 6.9 4 Be 9.0 5 B 10.8 6 C 1.0 7 N 14.0 8 O 16.0 9 F 19.0 He 4.0 10 Ne 0. 11 Na 3.0 1 Mg 4.3 13 Al 7.0 14 Si 8.1 15 P 31.0 16
忠明高中總複習叢書 化學總複習精華 解答本 說明 : 下列資料, 可供回答問題之參考 一 元素週期表 (1~36 號元素 ) 1 H 1.0 3 Li 6.9 4 Be 9.0 5 B 10.8 6 C 1.0 7 N 14.0 8 O 16.0 9 F 19.0 He 4.0 10 Ne 0. 11 Na 3.0 1 Mg 4.3 13 Al 7.0 14 Si 8.1 15 P 31.0 16
高雄市光華國民中學九十二學年度第一學期一年級
 05 三年級彈性課程教學計畫表 高雄市立壽山國民中學 05 學年度第 2 學期三年級 彈性課程 補救英語 教學計畫 壹 各單元教學目標 ( 一 ) 培養學生基本的英語溝通能力 ( 二 ) 培養學生學習英語的興趣與方法 ( 三 ) 增進學生對本國與外國文化習俗之認識 貳 各單元內涵分析 週次 2/3-2/9 日期單元名稱對應之能力指標節數評量方式 L Martin and Henry 2 2/20-2/26
05 三年級彈性課程教學計畫表 高雄市立壽山國民中學 05 學年度第 2 學期三年級 彈性課程 補救英語 教學計畫 壹 各單元教學目標 ( 一 ) 培養學生基本的英語溝通能力 ( 二 ) 培養學生學習英語的興趣與方法 ( 三 ) 增進學生對本國與外國文化習俗之認識 貳 各單元內涵分析 週次 2/3-2/9 日期單元名稱對應之能力指標節數評量方式 L Martin and Henry 2 2/20-2/26
12 25 12 25 6 12.5 s 3 A B C D E 3 D 4 1 26.5C 2 5 3 4 37
 ZX p A B C D E B 3 7 B a A 24 50 B 24 C 12 25 D 12 E 6 12.5 E 3 36 12 25 12 25 6 12.5 s 3 A B C D E 3 D 4 1 26.5C 2 5 3 4 37 ZX d 1 1 A B C D E E 3 38 26 fn n 2 k n2k n f 3 A B C D E BCE 3 5 A 1 1 B C
ZX p A B C D E B 3 7 B a A 24 50 B 24 C 12 25 D 12 E 6 12.5 E 3 36 12 25 12 25 6 12.5 s 3 A B C D E 3 D 4 1 26.5C 2 5 3 4 37 ZX d 1 1 A B C D E E 3 38 26 fn n 2 k n2k n f 3 A B C D E BCE 3 5 A 1 1 B C
8-2(PART-1)原子量、分子量、莫耳數
 ( 一 ) 莫耳濃度 A 定義 : 平均每 1 公升的溶液中含有溶質的莫耳數, 即稱為 莫耳濃度 B 公式 : 莫耳濃度 (M)= 莫耳數 公升 溶質的莫耳數 (mole)= M L C 單位 : M ( mole/l ) 註 : 溶液的體積需用 公升 為單位 說明 : 溶液的配置 : (1) 直接秤取定量的溶質 (2) 將溶質加入適量的水先行溶解 (3) 將溶液稀釋配置, 成為需要的體積 配置 2M
( 一 ) 莫耳濃度 A 定義 : 平均每 1 公升的溶液中含有溶質的莫耳數, 即稱為 莫耳濃度 B 公式 : 莫耳濃度 (M)= 莫耳數 公升 溶質的莫耳數 (mole)= M L C 單位 : M ( mole/l ) 註 : 溶液的體積需用 公升 為單位 說明 : 溶液的配置 : (1) 直接秤取定量的溶質 (2) 將溶質加入適量的水先行溶解 (3) 將溶液稀釋配置, 成為需要的體積 配置 2M
現在人類獲取地球內部訊息的方法, 是從可能影響我們身家性命安全的地震, 用數學模型把地震資料轉換成地震波速度, 進而獲得地底物質密度與深度的關係 地下世界知多少 km/s g/cm 3 P Gpa km S P S 3,000 3,000 ak K 透視地底 Percy Bridgma
 透視地球深處 的窗戶? extreme condition extreme environment 94.5 1 270 21 3.9 12.3 6,400 300 4,000 1864 Jules Gabriel Verne 1959 2008 1990 Paul Preuss 2003 24 2013 2 482 現在人類獲取地球內部訊息的方法, 是從可能影響我們身家性命安全的地震, 用數學模型把地震資料轉換成地震波速度,
透視地球深處 的窗戶? extreme condition extreme environment 94.5 1 270 21 3.9 12.3 6,400 300 4,000 1864 Jules Gabriel Verne 1959 2008 1990 Paul Preuss 2003 24 2013 2 482 現在人類獲取地球內部訊息的方法, 是從可能影響我們身家性命安全的地震, 用數學模型把地震資料轉換成地震波速度,
(CIP) : / :,, :,2000.5 ISBN 7-04 - 008822-3 - - N - 42 CIP (2000)60397 55 100009 010-64054588 010-64014048 / 8501168 1/ 32 7.875
 ( ) (CIP) : / :,, :,2000.5 ISBN 7-04 - 008822-3 - - N - 42 CIP (2000)60397 55 100009 010-64054588 010-64014048 http:/ / www.hep.edu.cn 8501168 1/ 32 7.875 190 000 8.40, ( ) 1 16 16 16 18 21 22 24 24 24
( ) (CIP) : / :,, :,2000.5 ISBN 7-04 - 008822-3 - - N - 42 CIP (2000)60397 55 100009 010-64054588 010-64014048 http:/ / www.hep.edu.cn 8501168 1/ 32 7.875 190 000 8.40, ( ) 1 16 16 16 18 21 22 24 24 24
本章綱要 -1 節點電壓法 -2 迴路電流法 -3 重疊定理 - 戴維寧定理 -5 諾頓定理 -6 戴維寧與諾頓等效電路之轉換 -7 最大功率轉移定理 Chapter 直流網路分析 0626-0.indd 125 2009/11/10 下午 0:58:09
 ELECTRICITY ELECTRICITY BASIC BASIC 本章學習目標 1. 利用節點電壓法分析各支路的電流 2. 利用迴路電流法分析各迴路的電流 3. 瞭解重疊定理在多電源電路的應用. 利用戴維寧與諾頓定理化簡電路 5. 瞭解戴維寧與諾頓等效電路的轉換 6. 學習負載如何在電路中獲得最大的功率轉移 0626-0.indd 12 2009/11/10 下午 0:58:02 本章綱要 -1
ELECTRICITY ELECTRICITY BASIC BASIC 本章學習目標 1. 利用節點電壓法分析各支路的電流 2. 利用迴路電流法分析各迴路的電流 3. 瞭解重疊定理在多電源電路的應用. 利用戴維寧與諾頓定理化簡電路 5. 瞭解戴維寧與諾頓等效電路的轉換 6. 學習負載如何在電路中獲得最大的功率轉移 0626-0.indd 12 2009/11/10 下午 0:58:02 本章綱要 -1
※※※※※
 ... 1 (030-910301)... 2... 3... 5... 7... 8 (030-910302)... 9... 10... 11... 13... 14 (030-910303)... 15... 16... 18... 20... 21 (030-910304)... 22 ... 23... 24... 26... 27 (030-910305)... 28... 29...
... 1 (030-910301)... 2... 3... 5... 7... 8 (030-910302)... 9... 10... 11... 13... 14 (030-910303)... 15... 16... 18... 20... 21 (030-910304)... 22 ... 23... 24... 26... 27 (030-910305)... 28... 29...
(1) 64 15 2062 50 8 818 60 41606 63 8305 53 3 11201 38 10 216C 2012815 2012815 2012815 2012815 2012815 201464 200211 20128 20128 20128 20128 20146 4 2
 (1) 51 41 49 6 6 7 161 4 27 338 2012815 2012815 2012815 200712 20093 20086 211 (1) 64 15 2062 50 8 818 60 41606 63 8305 53 3 11201 38 10 216C 2012815 2012815 2012815 2012815 2012815 201464 200211 20128
(1) 51 41 49 6 6 7 161 4 27 338 2012815 2012815 2012815 200712 20093 20086 211 (1) 64 15 2062 50 8 818 60 41606 63 8305 53 3 11201 38 10 216C 2012815 2012815 2012815 2012815 2012815 201464 200211 20128
1810塗料、染料及顏料製造業
 行 業 細 項 代 碼 公 告 類 別 ( 三 ) 登 記 資 本 額 新 臺 幣 一 百 萬 元 以 上 事 業 行 業 中 項 代 碼 20 藥 品 及 醫 用 化 學 製 品 製 造 業 事 業 廢 棄 物 清 理 計 畫 書 關 聯 表 行 業 細 項 名 稱 行 業 細 項 代 碼 行 業 細 項 名 稱 2001 原 料 藥 品 及 醫 用 化 學 製 品 製 造 業 2004 中 藥
行 業 細 項 代 碼 公 告 類 別 ( 三 ) 登 記 資 本 額 新 臺 幣 一 百 萬 元 以 上 事 業 行 業 中 項 代 碼 20 藥 品 及 醫 用 化 學 製 品 製 造 業 事 業 廢 棄 物 清 理 計 畫 書 關 聯 表 行 業 細 項 名 稱 行 業 細 項 代 碼 行 業 細 項 名 稱 2001 原 料 藥 品 及 醫 用 化 學 製 品 製 造 業 2004 中 藥

