¿ï�ת«²z¤W_½Ò¥»_²Ä1³¹
|
|
|
- 块阴 易
- 7 years ago
- Views:
Transcription
1 熱學 1-1 溫度與熱 1-2 熱容量與比熱 1-3 熱膨脹 1-4 物質的三態變化與潛熱 1-5 理想氣體方程式 1-6 氣體動力論
2 熱氣球發展的年代正是熱學研究興起的年代, 隨著熱學研究的推進, 氣球也愈飛愈高愈遠 你知道理想氣體方程式的奠基者查爾斯, 除了對氣體熱學性質的研究外, 其實也是一位氣球飛行家嗎? Imagination is more important than knowledge. 想像力比知識更重要 - 愛因斯坦 (Albert Einstein, )
3 火的發現與使用在人類文明的演進上占有相當重要的地位, 人們用火提供的熱 (heat) 來烹煮食物, 也在寒冬中用火來製造一個溫暖的環境, 但早期人們始終不清楚熱到底是什麼? 而冷熱又是一種什麼樣的概念? 一直要到十七世紀溫度計發明, 人們可以客觀的對冷熱加以測量與量化, 才正式開啟了熱學的研究 熱會對物質造成各種影響, 例如加熱可以使物體的溫度上升, 可以讓物體受熱膨脹, 甚至可以讓物體產生狀態變化 ( 如冰塊融化成水 ) 等 熱學研究除了探索這些物質受熱現象及其規律, 也深入追尋熱的本質為何 巨觀世界中的熱學現象又和微觀世界的粒子運動有何關聯? 由於人類的好奇與努力, 對熱學的探索終於陸續開花結果, 不論是十八世紀熱氣球的發明與蒸汽機的改進, 抑或是十九 二十世紀利用氣體分子模型及物質微觀結構來解釋物體的熱學性質, 均引領人類文明進入一個新的境界 ( 圖 1-1) 圖 1-1 人類文明的演進與熱學的發展息息相關
4 1-1 溫度與熱 溫度與熱是熱學中兩個重要的概念, 不只是日常生活中不易區辨, 在物理學的發展史上, 這兩個概念也曾經混淆不清 但是一經釐清, 熱學便得以快速地發展, 可見概念的清楚明確對科學發展有相當的重要性 想一想將兩壺質量不同的水放在瓦斯爐上 ( 圖 1-2), 以同樣的火力加熱, 從室溫到沸騰, 所需的加熱時間是否相同? 試著從這個問題判斷溫度與熱量這兩個概念是否相同? 圖 溫度與熱平衡 天氣冷的時候我們會多穿件衣服, 而天氣熱的時候我們會穿得較涼快一點, 冷熱不同的環境我們會有不同的穿著, 然而每個人對冷熱的感受並不相同 做一做準備一盆溫熱的水 一盆室溫的水以及一盆冰水, 將左右兩手分別放入溫水及冰水中一小段時間, 接著同時將兩手放到室溫的水中, 你有什麼樣的感覺呢? 親自嘗試以上實驗更能體會其中的困惑 : 同一盆水的冷熱程度應該相同, 但我們竟有截然不同的感覺! 顯然僅憑感覺來表達物體的冷熱程度, 似乎過於主觀, 不僅會因人而異, 而且受限於人體感官的限制 然而客觀的冷熱衡量標準是否存在呢?
5 科學家從許多實驗的結果中歸納出一個結論 : 當和外界隔離的兩個 物體可以彼此傳熱時, 只要經過足夠的時間, 兩物體的巨觀物理量 ( 即 可經由實驗直接測得的物理量, 例如壓力 表 1-1 不同溫度計與其所利用的測溫物質與性質 溫度計 水銀溫度計 酒精溫度計 電阻溫度計 定容氣體溫度計 定壓氣體溫度計 指針式溫度計 熱電偶溫度計 液晶溫度計 輻射溫度計 體積或其他等 ) 將各自不再 變化, 此時我們說這兩物體達到熱平衡 (thermal equilibrium) 狀態 對於 兩個處於熱平衡狀態的物體, 我們認定其有相同的客觀冷熱程度, 並以 溫度 (temperature) 來表示物體的冷熱程度 亦即達熱平衡的物體會有相 同的溫度 2. 溫度計 由經驗可知, 當物體溫 度變動時, 有些性質會隨之 變化 這些會反映物體溫 度的物理量稱為測溫性質 (thermometric property), 利用這些性質可以設計一測 量物體溫度的工具 溫度 計 (thermometer), 如表 1-1 所列 而測量溫度的基本原 測溫物質與性質 水銀的體積 酒精的體積 導體的電阻 氣體的壓力 氣體的體積 雙金屬片的長度差 熱電偶的電動勢 液晶的顏色 熱輻射電磁波的強度 理, 正是利用前面的說法 : 當溫度計和待測物達成熱平衡時, 兩者的溫 度相同 製作溫度計時, 必然會牽涉到溫度如何標示的問題 用於表示溫度 數值的標尺稱為溫標 (temperature scale) 常見的攝氏溫標( ) 將一 大氣壓下純水的冰點 ( 即冰和水共存時的溫度 ) 定為 0, 而將一大氣 壓下純水的沸點定為 100 兩定點溫度間等分成 100 等分 壓力 (pressure) 反映單位面積的正向力, 日常生活中常以大氣壓 (atm) 或帕 (Pa) 為單位 更詳細的介紹將留待 1-5 節
6 溫標的演變 十七世紀, 英國科學家虎克 (Robert Hooke, ) 首先注意到, 將溫度計放入冰和水共存的環境時, 溫度計內的液面始終會維持在同一高度, 這表示水變成冰或冰熔化成水的過程, 是在固定溫度下進行的 1712 年左右, 德國物理學家華倫海特 (Daniel Fahrenheit, ) 以虎克的研究為基礎, 將冰與鹽相混合後, 所能達到的最低溫度定為 0, 而概略地將人體溫度定為 100, 兩者間等分成 100 個刻度 在此刻畫下, 一大氣壓下水的冰點是 32, 而沸點則是 212 這種溫標稱為 華氏溫標, 至今只有美國等少數國家仍在使用 1742 年, 瑞典天文學家攝氏 (Anders Celsius, ) 將一大氣壓下水的冰點定為 100, 沸點定為 0, 兩者間均分成 100 個刻度, 和現行攝氏溫標恰好相反 1743 年, 才被修改成現行使用中的攝溫氏標 此溫標在使用上非常方便, 因此在採用公制單位系統的國家甚受歡迎 1954 年, 第十屆國際度量衡大會為表彰攝氏的貢獻, 特別將此溫標命名為 攝氏溫標 華氏溫標度數 F 和攝氏溫標度數 C 的換算關係可利用圖 1-3 的 比例關係 C = F 化簡為 F= 9 5 C 年, 愛爾蘭人克耳文爵士 (Lord Kelvin, 原名為 William Thomson, ) 根據法國物理學家卡諾 (Nicolas Leonard Sadi Carnot, ) 的熱力學理論, 創立了克氏溫標 其優點是不受使用物質的影響, 在各溫度範圍下均能適用 1927 年, 第七屆國際度量衡大會, 採用其作為最基本的溫標 1960 年, 第十一屆國際度量衡大會, 將冰 水和水蒸氣三相共存時的溫度定為 K 克氏溫標又稱絕對溫標, 克氏溫標度數 K 和攝氏溫標度數 C 的換算關係為 K=C 關於克氏標將於本章稍後有更詳細的介紹 3. 熱的本質 圖 1-3 華氏溫標度數 F 和攝氏溫標度數 C 的對應關係示意圖 對於溫度的概念獲得釐清之後, 我們回頭想想最開始的問題 : 要讓 一杯室溫的水沸騰必須要加熱提供熱量, 那麼熱的本質又是什麼呢? 歷史上關於熱的本質的看法, 大抵可歸納成兩類 : 一為熱質說, 二 為熱動說 在熱質說中, 認為熱是無色 無味 又沒有質量的流質, 稱 為熱質 (caloric) 熱質不能產生, 也不能消失, 總量維持守恆 有一處 的熱質增加時, 溫度會升高, 而另一處的熱質便會減少, 使溫度降低 這種說法對於解釋熱傳導及熱量測定的問題頗為成功, 在十九世紀初以
7 前, 獲得多數科學家的支持
8 但在 1797 年, 英國科學家侖福特伯爵 (Count Rumford, 原名為 Benjamin Thompson, ) 在慕尼黑監製大砲時, 發現大砲僅鑽磨 一段短時間, 砲管和鑽頭就變得很熱, 而且若不斷鑽磨, 熱可以源源不 絕地產生, 依照熱質說這裡觀察到的溫度上升是因為獲得熱質, 但過程 中卻似乎沒有觀察到有任何其他地方因熱質減少而溫度下降, 顯然與熱 質總量維持守恆的說法不合 1799 年, 英國化學家戴維 (Humphry Davy, ) 也提出將兩塊冰互相摩擦, 結果兩塊冰均發生熔化的現象, 同樣僅觀察到熱質的獲得造成冰塊熔化, 卻沒有觀察到其他地方因熱質 減少而溫度下降的現象 熱質說顯然無法解釋以上這些熱質憑空不斷產 生, 卻沒有地方熱質減少變冷的怪異現象, 於是他們主張熱可以由運動 而產生, 並大膽指出, 熱可以和力學能互相轉換 他們認為熱是組成物 質的微小粒子的運動表現, 可由物體的力學運動轉化而來, 這種學說稱 為熱動說 侖福特與戴維的實驗和論述雖然已經相當充分, 但並未說服當時多 數科學家放棄熱質說 四十年後, 英國物理學家焦耳 (James Prescott Joule, ) 發表他在多次測量所得精確的數據, 指出熱是能量的 一種形式, 熱質說才正式被推翻 溫標的演變 熱 與 溫度 這兩個概念, 在物理學發展史上, 曾混淆了很長一段時間 在十八世紀中葉以前, 溫度有時被視為 熱的強度, 有時又被視為是 熱的數量 若持溫度是 熱的數量 觀點, 則 熱的數量 愈多便表示溫度愈高 依照此種看法, 將一杯冷水與一杯熱水混合, 所含 熱的數量 增加, 混合後水的溫度應較原本的熱水更高, 這顯然與日常經驗不合, 因此並不是一個好的解釋 荷蘭學者布爾哈夫 (Hermann Boerhaave, ), 在其著作中曾描述 : 等量的冷熱水混合後, 其末是冷熱水度的平均值, 但對於不同物質混合後的末卻非平均值感到不解, 即使將等量的含意從等質量改成等體積, 仍是如此, 此問題稱為 布爾哈夫疑難 蘇格蘭科學家布萊克 (Joseph Black, ) 仔細研究前人留下的資料後, 明確指出 溫度 應是反映 熱的強度, 而 熱量 才是反映 熱的數量, 如此才可解釋冷熱水混合後, 末溫介於冷熱水溫之間的事實 同時他也斷言, 不同物質作相同溫度變化時, 會吸收或釋放不同量的熱, 並以此解釋了布爾哈夫疑難
9 4. 焦耳實驗與熱功當量 在熱質說盛行的年代, 熱量單位 卡 ( 記作 cal) 的定義是 : 在標準大氣壓下, 使 1 克純水升高 1 ( 更準確的說法是從 14.5 升到 15.5 ) 所需的熱 熱動說指出熱是能量的一種形式, 並且將物體發生溫度變化或相變時進出的能量稱為熱 熱功當量實驗的目的在於找出需對物體作多少功, 才可使物質的升溫效果 可以和 1 卡熱量相當 1840 年至 1878 年間, 焦耳以各種方法作 圖 1-4 焦耳的熱功當量實驗 槳葉攪拌法 了數百次的作功生熱實驗, 取得大量的熱功當量數據 圖 1-4 便是其中的一種實驗裝置 在他 1849 年的報告中所記載的熱功當量相當於 4.15 焦耳 / 卡, 和今日公認的熱功當量 焦耳 / 卡接近 焦耳的熱功當量實驗, 顯示熱可以由位能或動能轉換而得, 因此熱是能量的一種形式 1948 年, 國際度量衡大會為了表明熱是代表物體間因溫差而轉移的能量, 熱的單位應和能量的單位相同, 因此將 1 卡直接定義為 焦耳 熱功當量的實驗, 確認了熱是能量的一種形式, 而且可以和力學能互相轉換 焦耳小傳 焦耳於 1818 年出生於英國曼徹斯特附近的索爾福德, 父親是啤酒釀造商 焦耳自幼聰明好學, 對家中的動力設備產生極大的興趣 他曾向英國化學家道耳頓 (John Dalton, ) 學習, 並在他的鼓勵下從事科學研究工作 1837 年, 他發表了電學與磁學方面的研究心得 1840 年, 在英國皇家學會上發表了關於電流生熱的論文 此後, 他在自己家中進行實驗研究, 花了約四十年的時間, 用盡各種方法, 才找出精確的熱功當量關係, 成為能量守恆律的主要貢獻者 1852 年, 他和克耳文發現氣體自由膨脹時, 溫度不會下降的現象 終其一生, 焦耳對熱學方面作了許多非常有價值的貢獻, 為紀念其功績, 人們將能量 功及熱的單位命名為焦耳
10 1-2 熱容量與比熱 在前一節中我們已經了解熱與溫度這兩個概念的內涵及其差異, 而當兩個溫度不一樣的物體彼此之間可以交換熱量時, 熱會由高溫的物體流向低溫的物體 高溫物體因為熱的流失, 使其溫度逐漸降低 ; 低溫物體因有熱的流入, 使其溫度逐漸上升, 直到兩者的溫度相同達成熱平衡 接著我們想要了解的是物體獲得或者失去熱與其溫度變化之間有何關聯呢? 1. 熱容量 布萊克最早提出同質量的不同物質, 在發生相同溫度變化時, 會吸收或釋放不同數量的熱, 因而解釋了 布爾哈夫疑難 他的學生與後人正式提出熱容量 (heat capacity) 與比熱 (specific heat) 的概念來進一步說明此一解釋 當一物體吸收或放出熱且其溫度發生變化時, 定義物體的熱容量為 : 物體每升高或降低 1 時, 所吸收或放出的熱即其熱容量 一般以符號 C 表示熱容量, 其單位為 cal/ 設某物質溫度升高 Δt 時, 共吸收 ΔQ 的熱, 則依上述定義, 其熱容量 C 可寫成 C= ΔQ Δt 1-1 式 亦即 Q=CΔt 1-2 式 物體溫度升高時所吸收的總熱為其熱容量與溫度變化的乘積 關於布爾哈夫疑難可參考第 10 頁科學短文
11 2. 比熱 雖然熱容量已經可以簡單說明物質得失熱及其溫度變化間的關係, 但由進一步的實驗得知,10 克的水與 100 克的水同樣上升 1 時, 所吸收的熱有 1:10 的關係, 因此熱容量與物質質量有正比關係 為了方便比較, 我們進一步定義 : 單位質量的熱容量稱為比熱, 並以符號 s 表示, 其單位為 cal/g 設某物體的質量為 m, 共吸收 ΔQ 的熱, 結果使其溫度升高 Δt, 則依上述的定義, 其比熱 s 為 s= ΔQ mδt 1-3 式 亦即 ΔQ=msΔt 1-4 式 上式顯示溫度上升 Δt 時所吸收的熱 ΔQ 亦為正, 反之當 Δt 為負時 ΔQ 亦為負, 代表放熱 另外, 比較 (1-1) 式與 (1-3) 式, 可得知物體熱容量與其比熱的關係為 C=ms 1-5 式 一般來說, 在通常的溫度範圍內, 比熱會隨溫度而有些微改變 例如同樣是 1 克純水, 從 10 上升至 11 和從 50 上升至 51 時, 所需的熱稍有差異 將純水在 0 至 100 的比熱加以平均後, 恰等於水在 15 附近的比熱 因此, 早期將一卡定義為 1 克純水從 14.5 上升至 15.5 所吸收的熱 雖然如此, 在通常的溫度範圍內, 同一物質的比熱仍可視為常數
12 比熱是與材料有關的 表 1-2 在一大氣壓下 25 時常見物質的比熱 物理量, 不同物質的比 物質 比熱 s (cal/g ) 物質比熱 s (cal/g ) 熱並不相同, 其數值常 鋁 酒精 可作為分辨物質的參考 鐵 醋酸 銅 氫 從表 1-2 中可發現, 銀 氮 各物質的比熱沒有一定鉛 氧 的關係, 但水的比熱相 汞 氦 較於這些常見的固體與 水 氖 液體大多了, 你是否注意到其中的特殊意義呢? 當我們提供相同的熱給 相同質量的水以及其他常見的固體或液體, 由於水的比熱較大, 因此其 溫度變化較小, 而這正是造成大陸性氣候與海洋性氣候差別的一個重要 原因 想一想 1. 將兩壺質量不同的水放在瓦斯爐上, 以同樣的火力加熱, 從室溫到沸騰有相同的溫度變化, 並且已知兩壺水的比熱是相同的, 試說明為何兩壺水所需的加熱時間 ( 即所需提供的熱 ) 並不相同 2. 夏天到海水浴場戲水時, 沙灘上的沙在陽光照射下非常的燙, 但同樣在太陽長時間照射下的海水, 溫度並沒有明顯地升高, 這和海水的熱容量有何關係? 1-1 英制的熱量單位稱為 英制熱單位 (British thermal unit), 簡寫為 BTU, 其定義為使 1 磅 (lb) 水上升 1 所需的熱, 則 1 BTU 相當於多少卡? [ 解答 ] 英制質量單位 1 lb= kg=453.6 g, 水的比熱為 1 cal/g, 而上升 1 相當於上升 5 9, 由 ΔQ=m sδt 知 1 BTU=(453.6 g)(1 cal/g )( 5 9 )=252.0 cal
13 1-2 有 A 和 B 兩種液體, 其質量 比熱 初溫分別為 m 1 s 1 t 1 與 m 2 s 2 t 2, 今將 兩者混合均勻, 假設不發生化學變化, 也無熱散失, 則 (1) 混合液體的末溫為何? (2) 混合液體的熱容量為何? (3) 混合液體的比熱為何? [ 解答 ] (1) 設末溫為 t, 則混合後 A 液體熱的變化為 ΔQ 1 =m 1 s 1 (t-t 1 ), 而 B 液體熱的變化為 ΔQ 2 =m 2 s 2 (t-t 2 ) 由於熱變化為正表示吸 熱, 熱變化為負表示放熱 根據題目敘述混合後不發生化學變化, 也無熱散失, 表示 A 和 B 的總熱變化為零 即 ΔQ=ΔQ 1 +ΔQ 2 =m 1 s 1 (t-t 1 )+m 2 s 2 (t-t 2 )=0 解得末溫 t= m 1 s 1 t 1 +m 2 s 2 t 2 m 1 s 1 +m 2 s 2 (2) 設混合液體溫度升高 Δt, 則 A 液體熱的變化 ΔQ 1 =m 1 s 1 Δt,B 液體 熱的變化 ΔQ 2 =m 2 s 2 Δt 因此混合液體的總吸收熱為 ΔQ=ΔQ 1 +ΔQ 2 =m 1 s 1 Δt+m 2 s 2 Δt 根據熱容量的定義, 混合液體的熱容量為 C= ΔQ Δt =m 1 s 1 +m 2 s 2 相當於在混合液體中, 每一種成分液體之熱容量的總和 (3) 承 (2), 根據 (1-3) 式, 混合液體的比熱為 s= ΔQ mδt = m 1 s 1 +m 2 s 2 m 1 +m 2 等於混合液體每單位質量的熱容量
14 1-3 熱膨脹 在日常生活中, 我們知道大多數物體具有熱脹冷縮的現象, 其原因是物體溫度升高時, 組成物體的分子其平均間距變大, 造成外觀上的膨脹 以下將定量描述物體的熱脹冷縮與溫度變化間的關聯, 並進而注意 到氣體熱脹冷縮的一些特殊現象 1. 熱膨脹係數 熱脹冷縮使得固態物體的長度隨溫度上升 而增加 如圖 1-5 所示, 若物體在初溫時的起 始長度為 L 0, 溫度升高 Δt 時的物體長度為 L, 則其長度增加量 ΔL=L-L 0, 由實驗的結果得 知, 在溫度變化不太大時, 物體長度增加的 比例與上升的溫度成正比, 可寫為 ΔL L 0 =α t 圖 1-5 物體長度的增加量 ΔL 與上升溫度 Δt 及起始長度 L 0 成正比 1-6 式 式中 α 是與材質有關的常數, 稱為線膨脹係數 (coefficient of linear expansion) 此係數的單位為 -1, 其意義為當溫度上升 1 時, 物體長度的增加量與起始長度的比值 在一般的溫度範圍內,α 值都很小, 且幾乎為定值 表 1-3 列出常見物質在室溫範圍時的線膨脹係數 將 ΔL=L-L 0 代入 (1-6) 式, 整理可得 L=L 0 ( 1+αΔt ) 1-7 式 此式不但方便我們直接計算出物體熱膨脹後的長度 L, 也說明後來的長度除了與上升的溫度 Δt 有關外, 也與物體起始長度 L 0 有關 稍加注意便可發現,(1-7) 式不只可以用來描述物體的熱膨脹, 當物體溫度下降 ( 即溫度變化 Δt<0) 時, 物體後來的長度 L 會較原本的長度 L 0 來得短, 此即物體遇冷收縮的現象 事實上, 只要溫度變
15 化範圍不太大, 不管是膨脹或收縮, 固態物體長度變化的比例, 均會與 其溫度變化成正比, 並且熱脹與冷縮有相同的線膨脹係數, 因此熱膨脹 較明顯的物體遇冷收縮也較明顯 物質 表 1-3 常見固態物質在室溫範圍時之線膨脹係數 線膨脹係數 α( ) 物質線膨脹係數 α( ) 鋅 30.2 鎳 13.4 鉛 28.9 鐵 11.8 鋁 23.1 鋼 11.7 錫 22.0 普通玻璃 9.0 銀 18.9 耐熱玻璃 1.2 銅 16.5 低膨脹鋼 0.7 金 14.2 合成石英 0.5 在一般的溫度變化下, 物體的 熱膨脹效應並不明顯, 但其影響 卻不能忽視, 否則建築物 橋樑 鐵軌等, 都可能因熱膨脹而產生 變形 圖 1-6 所示的橋樑伸縮縫, 便是為了預防橋樑因熱膨脹而引 起變形之用 然而鐵軌的伸縮縫 雖然具有避免鐵軌因熱膨脹彎曲 圖 1-6 橋樑之伸縮縫是為了預防橋樑因熱膨脹而引起變形之用 而影響行車安全的目的, 但伸縮縫本身也影響行車的穩定及舒適度, 因 此目前各國的新式高速鐵路多半利用溫度預力工法的技術 : 先將長鋼軌 拉緊再焊接在一起, 則即使溫度上升鋼軌亦只是減少彼此之間拉伸的張 力, 而不致伸長變形 此一技術亦應用在臺灣高鐵的建設上 想一想請利用表 1-3 查出玻璃和鐵的線膨脹係數, 並藉此說明何以冰箱中的果醬罐 ( 玻璃瓶身及鐵蓋 ) 打不開時, 稍微利用溫熱的水浸泡便可以輕易地打開
16 1-3 利用傳統方法鋪設鐵軌, 如果鋪設鋼製鐵軌時的溫度為 0.0, 每一段鐵軌的長度為 25.0 m, 欲使其在溫度 40.0 時不致於彎曲變形, 則每一節鐵軌之間應留有多大的伸縮縫? [ 解答 ] 根據表 1-3 可得鋼的線膨脹係數為 由圖 1-7 可看出每一節鐵軌在 40.0 時的長度 L 40 會比在 0.0 時的長度 L 0 多出 ΔL=L 40 -L 0 =L 0 αδt 圖 1-7 =(25.0 m)( )( ) = m=11.7 mm 因此, 每一節鐵軌間的伸縮縫至少須為 11.7 mm 如果鋪設時預留的伸縮縫不足, 則當溫度過高時, 會因熱膨脹而使鐵軌彎曲變形 1-4 利用一把在 0.00 時經過校正的鋼尺, 在溫度 時測量一根鉛棒的長 度, 得其讀數為 m 若考慮熱膨脹效應, 則 (1) 鉛棒在 時的真正長度為何? (2) 鉛棒在 0.00 時的真正長度為何? [ 解答 ] 由表 1-3 得知, 鋼與鉛的線膨脹係數分別為 與 (1) 一把在 0.00 時校正過的鋼尺, 表示在 0.00 時其刻度 0 與刻度 1 之間的 距離應為 m 長, 但由於熱膨脹效應, 在 時, 鋼尺的 刻度 0 與刻度 1 之間的距離增加了 ΔL=( m)( )(30.00 )= m 同時鉛棒恰能對齊鋼尺的刻度, 代表鉛棒在 時的真正長度為 m m= m
17 (2) 由於鉛棒在 時的真正長度為 m 則在溫度 0.00 時鉛棒的長度減少了 ( m)( )(30.00 ) = m, 故鉛棒在 0.00 時的真正長度為 m m= m 可見在不同溫度下的測量結果會有些微出入, 對於要求精確的實驗而言, 溫度變化是一項不可忽視的重要因素 2. 面膨脹 溫度變化對固態物體的長度有影響, 同樣也會表現在其面積和體積上 如圖 1-8 所示, 考慮一平板, 在初溫時的長 寬分別為 a 0 b 0, 其對應的面積為 A 0 =a 0 b 0 若此平板的線膨脹係數為 α, 當溫度升高 Δt 時, 其長度變為 a=a 0 (1+αΔt) 寬度變為 b=b 0 (1+αΔt), 因此其面積 A 變為 A=a b=a 0 b 0 (1+αΔt) 2 =A 0 (1+αΔt) 式 從表 1-3 知, 一般物質在溫度變化不大的情況下, 線膨脹係數與溫度變化的乘積 α Δt <<1, 所以上式可近似為 A=A 0 (1+2αΔt+α 2 Δt 2 ) A 0 (1+2αΔt) 圖 1-8 平板的長度 寬度受熱 增長後, 其面積也會變大 仿照先前定義線膨脹係數的方式, 可將此平板後來的面積 A 表示為 1-9 式 A=A 0 (1+βΔt) 1-10 式
18 式中 β 稱為面膨脹係數, 單位亦為 -1, 其意義為當溫度上升 1 時, 物體面積的增加量與起始面積的比值, 亦即與 (1-10) 式可看出 β 2α 即面膨脹係數約為線膨脹係數的 2 倍 ΔA A 0 =βδt 比較 (1-9) 式 1-11 式 多項式 (1+x) n 在 x 很小時的近似 (1+x) 2 =1+2x+x 2, 當 x 很小時可近似為 (1+x) 2 1+2x (1+x) 3 =1+3x+3x 2 +x 3, 當 x 很小時可近似為 (1+x) 3 1+3x 依此類推 (1+x) n =1+nx+, 當 x 很小時可近似為 (1+x) n 1+nx 你可以利用計算機按按看 1.2 2, 1.1 2, ,, 甚至是表 1-3 中那些很小的線膨脹係數的平方, 看看上面的近似是否正確 1-5 如圖 1-9 所示, 在溫度 10.0 時, 將一鋼板挖出一半徑 為 5.00 cm 的圓洞 則當溫度升高為 30.0 時, 請利用 表 3-1 所提供的數據, 求出此圓洞面積的增加量為何? [ 解答 ] 鋼板的面膨脹係數為其線膨脹係數的 2 倍, 根據表 1-3 可得 β 2α= 當溫度升高時, 鋼板上的各部分都必須做同樣比例的膨脹, 因此 圓洞的熱膨脹情形和鋼板的其他部分一樣, 也就是說, 圓洞的膨 脹就如同被挖去的圓板仍留在原處時一樣 由 (1-11) 式知, 溫 度上升至 30.0 時圓洞所增加的面積為 ΔA=π(5.00 cm) 2 ( )( ) = cm 2 圖 1-9 圓洞的膨脹情形和被挖去的圓板相同
19 想一想在範例 1-5 中, 若是將鋼板四周固定, 則因熱膨脹而增加出來的面積將增至何處? 3. 體膨脹 同樣地, 如圖 1-10 所示, 物體的體膨脹亦可依照前文面膨脹 的推導方式, 將長方體後來的體 積 V 表示為 圖 1-10 長方體的長 寬 高受熱增長後, 其體積也變大 V=V 0 (1+γΔt) 1-12 式 式中 γ 稱為體膨脹係數, 單位亦為 -1, 其意義為當溫度上升 1 時, 物 體體積的增加量與起始體積之比值, 亦即 為線膨脹係數的 3 倍, 即 γ 3α ΔV V 0 =γδt, 且體膨脹係數約 1-13 式 液體和氣體屬於流體, 其形狀會隨所盛容器而改變, 因此並無所謂的線膨脹及面膨脹, 但即便是氣體, 只要在壓力固定的情況下, 其體積可以明確測定, 因此可定義其體膨脹係數 表 1-4 列出一般常見液體在室溫範圍時的體膨脹係數, 與表 1-3 相比可知, 液體的體膨脹係數較固體的體膨脹係數大 表 1-4 常見液體在室溫範圍時之體膨脹係數 物質 體膨脹係數 γ( ) 物質體膨脹係數 γ( ) 丙酮 汽油 9.50 苯 甘油 5.05 乙醇 水 2.07 松節油 9.73 水銀 1.82
20 由於水的熱膨脹在 0 至 4 的範圍內有異常的行為 : 當溫度由 0 升高時, 其體積反而減少, 即其體膨脹係數是負值 但在 4 以上的溫度, 水的體積隨溫度的升高而增大, 即其體膨脹係數為正值 此現象使得水在 4 時的體積最小, 而密度最大 在寒冬時節, 當湖面自 0 開始結冰時, 而冰層下則仍保有密度較大接近 4 相對較溫暖的水, 此一特殊現象使水中生物得以存活 想一想請依照面膨脹的推導過程, 自行推導物體的體膨脹係數約為線膨脹係數的 3 倍 做一做 如圖 1-11 的實驗裝置, 一燒瓶的瓶口以插有玻璃管的橡皮塞塞緊 事先在玻璃管內滴入一滴紅墨水, 使紅墨水的位置稍高於橡皮塞, 以便觀察 雙手握住燒瓶, 以手溫加熱瓶內的空氣 不久可見管中的紅墨水逐漸上移至較高的位置 雙手移開後, 則見紅墨水逐漸下移, 最後回降到原來的位置 想想看如何利用熱膨脹來說明這個現象呢? 圖 1-11 手握瓶子, 手溫使瓶內的氣體受熱膨脹, 驅使細管中的紅墨水向上移動 1787 年, 法國人查爾 斯 (Jacques Alexander Cesar Charles, ) 從實 驗中發現 : 在密閉容器內的定量低密度氣體, 若氣體壓力維持不變, 則其體積與攝氏溫度有線性關係, 圖 1-12 在密閉容器內的低密度氣體, 若氣體壓力維持不變, 則其體積與攝氏溫度成線性關係
21 此一結果稱為定壓的查爾斯 - 給呂薩克定律 ( Charles'andGay- Lussac's law) 如圖 1-12 所示, 若在相同壓力下, 以 V 0 和 V 分別代表 氣體在攝氏溫度 0 和 t 時的體積, 則由實驗結果知 V=V 0 ( t ) 1-14 式 亦即在密閉容器中壓力固定的定量低密度氣體,0 時的體膨 脹係數 γ= , 此一體膨脹係數較液 體或固體之體膨脹係數大多了 值得一提的是只要在密閉容器 中固定壓力且維持低密度, 則此一體膨脹係數與氣體種類以及 氣體分子數均無關, 其間的奧秘我們將在本章稍後做更詳細的 說明 利用定壓下氣體體積會膨脹的特性, 可作成定壓氣體溫 度計, 如圖 1-13 所示 想一想 普通玻璃製成的厚玻璃杯, 在急速加滿熱水時, 常易發生破裂的情況, 請討論其原因及改進方法 圖 1-13 伽利略很早就利用定量氣體受熱膨脹的原理, 製成溫度計 圖中玻璃瓶中空腔部分的氣體受熱膨脹會擠壓使細管中的液體上升 在密閉容器內的定量低密度氣體, 當壓力保持固定時, 其體積與溫度遵循 (1-14) 式的線性關係, 則在 100 時其體膨脹係數為何? [ 解答 ] 令 0 時氣體體積為 V 0,100 時氣體體積為 V 100, 攝氏溫度 t 時氣體體積為 V, 則當溫度自 100 上升至 t, 其體積 V=V 100 [ 1+γ 100 (t-100 )] 將 V=V 0 ( t) 及 V 100 =V 0 [ (100 )] 代入化簡可得氣體在 100 時的體膨脹係數 γ 100 = 相較於 0 時的體膨脹係數, 可知氣體的體膨脹係數隨溫度升高而變小, 不可視為定值
22
23 物質的三態變化與潛熱 從日常生活經驗中, 我們知道物體受熱後溫度升高, 或冷卻後溫度降低, 至某一程度時, 其形態會發生變化, 例如固態 (solid state) 的冰受熱後, 熔化成液態 (liquid state) 的水 ; 若再繼續加熱, 則水經由蒸發或沸騰的過程, 轉變為氣態 (gaseous state) 的水蒸汽 這些形態的改變稱為物態變化 均勻的 固體 液體 氣體分別為不同的相 (phase), 因此其間的變化也稱為相變 (phase transition) 圖 1-14 顯示物質三態變化的關係 事實上物態的變化不只是受到溫度的影響, 壓力亦會造成物態的改變, 例如日常生活中使用的桶裝瓦斯就是利用高壓將瓦斯液化成液態瓦斯 1. 物質三態變化的粒子模型 圖 1-14 物質三態與相變 物質的三態變化, 可以利用物質的粒子模型 (particle model) 予以解釋 組成物質的眾多分子或原子之間, 彼此有互相作用的力, 統稱為分子力 (molecular force) 分子力的量值和方向與兩分子間的距離有關, 當分子間的距離夠大時其作用是互相吸引, 且分子力的量值會隨距離的增加而迅速地減弱 固體內的分子由於彼此互相吸引牽制, 呈現有規則的排列 但更仔細觀察會發現各分子並不是在該位置固定不動, 而是在附近做凌亂無序的微小振動 由於分子力的強力束縛, 使固體不易變形, 因此固體具有一定的形狀與體積 ( 圖 1-15(c)) 當固體受熱時, 外界提供的能量使其溫度升高, 分子振動的速度與幅度都會變大 如果溫度夠高, 分子間的劇烈振動使得其間的距離增加, 因此分子力的束縛相對地減弱, 有些分子將無法再被拘束於固定位
24 置, 而有較為自由的運動, 轉變成液體 固體轉變成液體的過程稱為熔化 (fusion) 相對於固體, 液體中的分子可以更容易地移動, 但減弱的分子力仍足以使它們牽連在一起, 因此液體雖無固定的形狀, 但仍具有一定的體積 ( 圖 1-15(b)) 圖 1-15 物質的粒子模型示意圖 :(a) 固體 ;(b) 液體 ;(c) 氣體 繼續對此液體加熱, 分子運動的速度更快, 並且分子距離的增加將 使分子力更形減弱 當分子可完全掙脫分子力束縛時, 液體就轉變成氣 體, 此一過程稱為汽化 (vaporization) 此時在液體內部將形成許多氣 泡翻湧而出, 這種現象稱為沸騰 (boiling) 由於氣體分子間的距離甚 大, 分子間的束縛力較弱, 因此氣體分子可以自由地移動, 這使得氣體 在任意容器中可以充滿整個空間, 其形狀與體積會隨著容器而改變, 這 是氣體與固體或液體很明顯的一個差別 ( 圖 1-15(c)) 有時某些固態物質在特定壓力範 圍下受熱可以直接變成氣體, 此種過 程稱為昇華 (sublimation) 乾冰( 即 固態二氧化碳, 圖 1-16) 和碘的昇華 現象是最常見的例子 氣體在特定壓 力範圍下降溫直接變成固體的過程則 稱為凝華 (deposition) 圖 1-16 乾冰是固態二氧化碳, 在常溫下會直接昇華成氣體
25 以上一般性的敘述可以用水為例做具體的說明 圖 1-17 顯示水在一大氣壓下, 以穩定熱源加熱的三態變化過程 起先為 -50 固態的冰塊受熱而溫度升高, 到達 0 時, 冰塊開始熔化, 在冰和水共存的期間, 雖然繼續加熱, 但溫度卻保持不變, 這時的溫度稱為冰在一大氣壓下的熔點 (fusion point) 當冰完全熔化成水後, 溫度才再繼續升高 到達 100 時, 水開始沸騰, 在水和水蒸汽共存期間, 溫度也保持不變, 這時的溫度稱為水在一大氣壓下的沸點 (boiling point) 當水完全汽化成水蒸汽後, 溫度才會再升高 冰塊或水受熱溫度升高期間, 外界所提供的熱主要用於增加水分子的動能, 而在冰塊熔化或水汽化的期間, 物質溫度卻沒有升高, 這時外界所提供的能量跑到哪裡去了呢? 這個問題將在稍後再做進一步的說明 除水外, 其他的純物質也有同樣的現象, 各有其特定的熔點和沸點 表 1-5 列出一大氣壓下常見物質的熔點與沸點 根據實驗測出的熔點或沸點, 有助於我們判斷物質的種類 圖 1-17 水在一大氣壓下, 以穩定熱源加熱的三態變化過程 表 1-5 一大氣壓下常見物質的熔點與沸點 物質熔點 ( ) 沸點 ( ) 物質熔點 ( ) 沸點 ( ) 鐵 水 銅 水銀 金 酒精 銀 氮 鋁 氧 鉛 氦 -269
26 低熔點的金屬 鎵 (Gallium) 大部分金屬熔點都很高, 但也有少數幾種金屬熔點很不一樣, 例如常見的水銀熔點是 -39, 常溫下即呈液態 另一種特別的金屬元素 鎵, 它的熔點僅 29.6, 較低的室溫下呈固態, 但放在手上就會熔化 ( 圖 1-18) 圖 1-18 鎵的熔點很低, 放在手上就會熔化 水或其他的純物質在冷卻降溫時, 從氣態轉變為液態再轉變為固態的過程, 仍如圖 1-17 所示, 只是進行的方向相反而已 氣體轉變成液體的過程, 稱為凝結 (condensation) 或液化 (liquefaction) 凝結期間, 氣態和液態共存, 溫度保持不變 這時的溫度稱為凝點 (condensation point) 在一定的壓力下, 同一物質的凝點和沸點相同, 例如水蒸汽在一大氣壓下, 當溫度降至 100 時, 開始凝結成水 同樣地, 液體轉變成固體的凝固 (freezing) 過程, 溫度保持不變, 直至液體全部轉變成固體時為止, 期間固定不變的溫度稱為凝固點 (freezing point) 在通常的狀況下, 同一物質的凝固點和熔點相同, 例如在一大氣壓下, 水在 0 時會開始凝固 2. 潛熱 早在十八世紀中葉, 布萊克便從眾多實驗中發現, 當物態發生變化時, 物質所吸收的熱並不顯示在溫度上升的效應 布萊克因此提出潛熱 (latent heat) 的概念, 即物態變化時所吸收或放出的熱, 稱為潛熱 此一概念的提出使得討論物態變化時, 對能量變化的來龍去脈有更加完整而清楚的了解, 大大有助於能量守恆律的確立 以水為例, 在冰的熔化期間, 由熱源處所輸入的熱主要用於瓦解固體分子間的鍵結, 而不是在增加分子運動的能量, 因此溫度保持不變 當物態變化時, 其溫度保持不變, 所吸收或放出的熱, 主要用於改變分
27 子間的位能 每一克物質在熔化時, 從固態轉變為同溫度的液態, 所需吸收的熱稱為該物質的熔化熱 (heat of fusion) 由實驗可測知冰的熔化熱約為 80 卡 / 克 同理, 在水的沸騰期間, 由熱源處所輸入的熱主要用於掙脫液體內分子間的束縛, 使其分子間的位能增加, 但平均而言分子運動的速度量值並沒有增加, 因此氣態的水蒸汽和液態的水共存時, 溫度不變 每一克物質在汽化時, 從液態轉變為同溫度的氣態, 所需吸收的熱稱為該物質的汽化熱 (heat of vaporization) 由實驗可測知水在沸點時的汽化熱約為 540 卡 / 克 由於純物質在冷卻降溫的過程, 與加熱升溫的過程相同, 只是變化的方向相反而已, 因此每一克物質在液化時, 從氣態轉變為同溫度的液態, 所需放出的熱量稱為該物質的凝結熱 (heat of condensation), 此凝結熱和該物質的汽化熱相等, 同理凝固凝固熱 (heat of solidification) 會和該物質的熔化熱相等 以上提到的熔化熱 凝固熱 汽化熱和凝結熱, 就是單位質量的潛熱 表 1-6 顯示常見物質在一大氣壓下的熔化熱與汽化熱, 請注意表中數值以 SI 制的單位 焦耳 / 公斤 (J/kg) 表示 表 1-6 一大氣壓下常見物質的熔化熱與汽化熱熔化熱汽化熱熔化熱汽化熱物質 ( 10 3 J/kg) ( 10 3 物質 J/kg) ( 10 3 J/kg) ( 10 3 J/kg) 鐵 247 水 銅 204 水銀 金 酒精 銀 105 氮 鋁 氧 鉛 氦 20
28 1-7 對一質量為 500 g 比熱為 0.60 cal/g 的某固態物質穩定加熱, 其加熱時間與溫 度的關係如圖 1-19 所示, 則 (1) 此物質的熔化熱為何? (2) 此物質在液態時的比熱為何? (3) 此物質的汽化熱為何? [ 解答 ] (1) 由 ΔQ=msΔt 可知該物質在最初 10 分鐘內所吸收的熱量為 (500 g)(0.60 cal/g )[ 20 -(-20 )]=12000 cal 因此熔化階段 20 分鐘內, 共吸熱 cal cal 故其熔化熱為 500 g =48 cal/g (2) 在 30 分鐘至 50 分鐘的加熱時間內, 液體溫度從 20 上升至 60, 故此液體的比熱為 s= cal ( 500 g ) ( ) 圖 1-19 =1.2 cal/g (3) 在 50 分鐘至 90 分鐘的加熱時間內, 此液體共吸熱 cal, 4800 cal 故其汽化熱為 =96 cal/g 500 g 蒸發 當液體尚未發生沸騰時, 在液體表面上有些運動速度較快的分子, 也可以掙脫分子力的束縛而逸出變成氣體, 這種僅在液體表面發生的汽化現象, 稱為蒸發 (evaporation) 地面上的一灘水, 經過一段時間後便不見了, 就是蒸發所造成的 平常晾衣服可使衣服乾燥, 如圖 1-20, 也是蒸發的結果 液體蒸發時, 由於失去能量較大的分子, 因此溫度會降低, 造成冷卻的效果 打針前, 塗上酒精的手臂感覺涼快, 便是因為酒精容易揮發, 蒸發時從手臂上帶走熱而使溫度降低 圖 1-20 平常晾衣服也是利用蒸發使衣服乾燥
29 1-8 小健在製作涼拌苦瓜時需要用到冰水, 因此他取了 300 g 0 的冰, 加入 1000 g 20 的冷水中, 均勻混和後末溫為何? [ 解答 ] 冰的熔化熱是 80 cal/g, 因此 300 g 0 的冰全部熔化需要吸收熱 (300 g)(80 cal/g)=24000 cal 相較之下,1000 g 20 的水降至 0 的過程中, 僅會釋放出熱 (1000 g)(1 cal/g )(20 )=20000 cal 水所放出的熱只能使 化, 故末溫為冰水共存的 cal 80 cal/g =250 g 的冰塊熔化, 仍有 50 g 冰未熔 水的三態變化和所伴隨熱的進 出, 幾乎是處處可見 廚房內作菜 時, 只要鍋內有足夠的水, 不管鍋 底下的火有多猛, 就不必擔心菜會 燒焦, 因為水沸騰時, 溫度保持不 變 裝熱水杯子內側水的上方與裝 冰水杯子的外側常見有小水珠, 以 及清晨時葉子上的小露珠 ( 圖 1-21), 都是水蒸氣遇冷凝結成水的現象 圖 1-21 清晨時葉子上的小水珠, 是空氣中的水蒸氣遇冷凝結而來 想一想為何在降霜之前, 在果樹上噴水, 可防止水果凍傷?
30 3. 三相圖 為了進一步了解物質三態變化所涉及的壓力 溫度和體積之間的關係, 我們將氣態的純物質放在密閉的容器內, 如圖 1-22 所示 容器開口由一個緊密不漏氣, 且無摩擦的活塞所封閉 活塞可上下自由移動, 用以調節容器的體積 有一與容器壁熱接觸的恆溫器用於控制容器內的物質溫度, 而施於活塞上的力則用於控制容器內的壓力 圖 1-22 研究物質三態變化的實驗裝置示意圖 由實驗的結果得知, 影響物質狀態的三個變量, 即壓力 P 溫度 T 和體積 V 並非完全獨立 例如若溫度維持不變, 則增加壓力會導致體積的減小 ; 若壓力維持不變, 則增加溫度會使體積增大 換句話說, 就定量的氣體而言, 三個變量之間只能有兩個是獨立的, 另一個會隨其餘兩個的變化而改變 為便於說明物態的變化, 我們選取壓力和溫度作為改變物態的兩個因素 圖 1-23 所示為一般物質的 P-T 三相圖, 用於描述溫度和壓力對物態變化的影響 圖中的三條曲線分別是熔化曲線 汽化曲線和昇華曲線, 各為固態 液態和氣態三相之間的分界線, 該圖又簡稱為三相圖 圖 1-24 所示則為少數物質, 例如水 生鐵 銻 鉍等的三相圖, 其和 圖 1-23 一般物質物態變化的三相圖示意 圖 1-24 水 生鐵等少數物質物態變化的三相圖示意
31 前圖的主要差異在熔化曲線的傾斜方向 在這三條曲線交點處的特定壓力和溫度下, 三態可共存而達成熱平衡, 稱為此物質的三相點 (triple point), 例如水在約 大氣壓 0.01 時, 固態的冰 液態的水和氣態的水蒸汽三者可穩定共存, 此即水的三相點 在三相圖中, 若將壓力維持在一大氣壓, 當溫度從低溫開始升高時, 則物質從固態開始先變成液態, 再轉為氣態 等壓線與熔化曲線交點所對應的溫度稱為熔點, 而與汽化曲線交點所對應的溫度稱為沸點, 如圖 1-25 所示 從圖中熔化曲線和汽化曲線的傾斜趨勢可看出, 若將壓力增大, 則物質的熔點與沸點均會隨之升高 但是像水 生鐵 銻 鉍等少數物質, 由於從固態熔化成液態時, 體積反而減小, 即壓力的增加有助於熔化, 因此這些物質的熔點會隨壓力的增大而降低, 不過其效應並不顯著 以水而言, 壓力每增加一大氣壓, 冰的熔點才降低約 此外, 雖然此類物質的熔點隨壓力的增加而降低, 但其沸點仍隨壓力的增大而升高 ( 表 1-7), 從圖 1-26 中即可看出此一趨勢 圖 1-25 當壓力增大時, 大多數物質的熔點和沸點皆隨之升高 圖 1-25 當壓力增大時, 大多數物質的熔點和沸點皆隨之升高 表 1-7 水在不同壓力的沸點 壓力 (hpa) 註 沸點 ( ) hpa 即百帕,1 hpa=100 Pa, 為氣象預報常用的氣壓單位
32 在三相圖中, 除了可以透過以上討論了解在固定壓力的條件下, 改變溫度對物態及相變的影響外, 亦可以在圖中畫一條垂直於 T 軸的直線, 討論當溫度維持不變時, 壓力變化對物質相變的影響過程, 請你自己試著練習分析說明 想一想 1. 何以使用壓力鍋可以更快把飯煮熟? 又為何在高山上不易把飯煮熟? 2. 在製造奶粉 即溶咖啡 藥品等的過程中需要脫水, 但不希望因高溫而發生變質, 應如何處理? 為何冰面如此滑溜? 花式溜冰表演者穿著銳利的冰刀, 在堅硬的冰面上快速地溜來溜去, 輕快自在如圖 1-27, 但是何以能夠如此, 卻困擾著科學家們將近百年的時間! 有許多種想法曾試圖解釋此現象, 最具代表性的有以下兩種 : 一為人體重量在冰刀上造成的壓力, 使冰的熔點降低, 因而使表面的冰層熔化成水 ; 另一種想法為冰刀與冰的摩擦, 所產生的熱使表面的冰層熔化成水 然而這兩種想法, 都經不起數量的考驗, 如正文中所述壓力每增加一大氣壓時, 冰的熔點才降低約 以人體重量作用在冰刀上的壓力, 最大不過 200 大氣壓, 頂多使冰熔點降低約 1.5, 但是在攝氏零下數十度的溫度下, 照樣可以自在地溜冰, 顯然無法用以上理論解釋 直到最近幾年, 科學家才了解真正的原因 原來冰和空氣接觸的界面, 厚度約在數個分子距離內的表面層, 其結構和內部規則排列的情形大不相同 這個薄層裡的分子排列凌亂, 鬆軟而具有相當的流動性, 兼有固體和液體的性質, 而這也就是為什麼即使穿著鞋子踩在冰上也甚滑溜的原因 將多數物質粉末抓在手中並無法成團, 但是將雪花或碎冰捏在手中便可成雪球或冰球, 其原因也是由於冰具有這個性質特殊的表面層 ( 本文參考 Scientific American, February 2000) 圖 1-27 花式溜冰表演者在光滑的冰面上滑溜
33 1-5 理想氣體方程式 前文曾經提及氣體分子可以自由地移動, 乃是因為氣體分子間的距離甚大, 分子間的束縛力較弱, 使得氣體在任意容器中可以充滿整個空間, 其形狀與體積會隨著容器而改變, 因此氣體容易膨脹也容易被壓縮 事實上, 當氣體受熱膨脹時, 除了溫度的上升與體積的膨脹以外, 壓力也可能會發生變化, 因此必須同時考慮壓力 體積與溫度, 才能對定量氣體的狀態做較完整的描述 1. 壓力與大氣壓力 氣體和液體一樣具有流動性, 沒有一定的形狀, 因此合稱為流體 (fluid) 這兩種流體的主要差異在於液體很難壓縮, 因此當溫度不變時, 其密度可視為定值 ; 氣體容易被壓縮, 也容易膨脹, 即使在定溫時, 其密度亦會隨壓力與體積條件而改變 不論是哪一種流體, 均會對接觸的容器壁產生壓力, 以下我們將透過較易觀察的液體來了解流體的壓力性質, 進而推廣到氣體的壓力性質 當液體靜止時, 外界 ( 例如容器壁 ) 對液體的作用力必定垂直於液體的表面 因為任何平行於液體表面的作用力, 都將使液體產生流動 反過來說, 液體本身也對外界施有同大的反作用力, 其方向垂直於和液體接觸的界面 做一做 如圖 1-28 所示, 將一裝滿水的寶特瓶 側面鑽孔, 使水自小孔中噴出, 仔細觀察 噴出的水柱方向是否與寶特瓶表面垂直? 這是什麼原因呢? 圖 1-28 從寶特瓶側面的小孔中所噴出的水柱, 其射出方向是否垂直於容器壁?
34 讓我們回顧國中時所學過關於壓力的概念 : 物體表面上, 每單位面積所受的正向力稱為壓力, 其 SI 單位為牛頓 / 公尺 2, 亦記為帕 (pascal, 符號為 Pa) 若垂直作用在物體表面上的力為 F, 受力面積為 A, 則該面積所受的平均壓力 P 可寫成 P= F A 1-15 式 較為特別的是, 在靜止液體內部任一處取一小塊液體, 則在這一小塊液體各個方向的表面所量測到的壓力皆相等 亦即作用在液體中任一點的壓力, 沒有一定的方向, 所以壓力不是一個向量 雖然壓力不是一個向量, 但若我們將 (1-15) 式改寫如下 F =P A 1-16 式 則可以利用壓力與面積求出垂直作用在此一表面上的作用力量值 氣體壓力的性質與液體相似, 因此如同可以用液體的重量來解釋對容器底部所造成的壓力一般, 我們也可以利用大氣層的重量來解釋大氣壓力 (atmospheric pressure) 假想從地面上沿鉛直向上的方向畫出一空氣柱, 則在地面上每單位面積所承受的空氣柱重量, 就是地面大氣壓力的量值 不同高度處所承受的空氣柱重量不同, 因此大氣壓力會隨高度而改變, 如圖 1-29 所示 但是由於大氣的密度愈往上就愈稀薄, 所 圖 1-29 海拔愈高處大氣壓力愈小,P 0 為地表大氣壓力
35 謂 空氣柱 的高度, 實際上很難定出 要想從空氣柱的重量來計算地面上所承受的大氣壓力, 並不是一件容易的事 1644 年, 義大利科學家托里切利 (Evangelista Torricelli, ) 設計了一個簡單的實驗, 可以測量大氣壓力, 稱為托里切利實驗 他在一根約一公尺長的玻璃試管中注滿水銀, 然後封住管口使水銀不致流出, 接著將玻璃試管倒置在事先準備好的水銀槽內 結果管內的水銀面下降至約離槽內水銀面的鉛直高度為 76 公分處, 此高度和玻璃試管的傾斜角度無關, 但若管頂離水銀槽液面的鉛直高度小於 76 公分, 則玻璃管內將充滿水銀, 如圖 1-30 所示 管內水銀柱下降後, 在頂部所空出來的空間僅含有少量的水銀蒸汽, 可視為真空, 一般稱為托里切利真空 圖 1-30 利用托里切利實驗測定大氣壓力 穩定後由於水銀槽中的液體靜止不流動, 因此在同一水平面的壓力勢必相等, 如圖 1-30 紅色虛線處, 亦即管外水銀面上所受的大氣壓力等於管內水銀柱所施的壓力 因此之故大氣壓力亦可用水銀柱的高度來表示, 例如一般將一大氣壓 ( 記為 1 atm) 視為與 76 公分高水銀柱 ( 記為 76 cmhg) 所造成的壓力相當, 可記為 1 atm=76 cmhg 但實際上由於大氣壓力會隨各種因素而改變, 水銀柱的重量亦會隨所處位置而不同, 因此 SI 制更精確地將一大氣壓的值定義為 1 atm= Pa Pa
36 想一想 1. 正文中提及 1 atm 相當於 76 cmhg 的壓力, 又說約等於 Pa, 你知道這是怎樣估算出來的嗎? 請利用 (1-15) 式 水銀的密度為 kg/m 3 以及重力加速度量值為 9.8 m/s 2 來做估算 2. 大氣壓力時時刻刻存在於日常生活周遭, 但我們卻似乎毫無所覺, 試依據以下步驟估算人體承受大氣壓力所形成的作用力量值 (1) 請將正文中 1atm 的量值換算成日常生活中較孰悉的單位, 估計體表每平方公尺約承受幾公斤重的作用力 (2) 以一般成年人頭頂截面積約 0.03m 2 來估算, 頭頂所承受的大氣壓力總作用力量值約為多少公斤重? (3) 你有沒有被估算出來的作用力量值嚇到呢? 人體承受這麼大的作用力卻沒有被壓垮, 也沒有什麼受到壓力的感覺, 想想看這是什麼原因呢? 做一做取一個空的飲料鋁罐, 裝入少量的水, 放置於酒精燈上加熱, 直到冒出水蒸氣 ( 圖 1-31(a)), 此時罐內原有的空氣被水蒸氣排出 接著用坩鍋鉗迅速將鋁罐倒扣入一旁裝水的水槽中, 會看到由於罐內的水蒸氣凝結成水, 造成鋁罐內壓力驟降, 罐外的大氣壓力會把鋁罐壓扁 ( 圖 1-31(b)) ( 實驗時須注意噴出的水蒸氣, 並且留意在壓扁鋁罐時發出的聲音 ) (a) (b) 圖 1-31 利用大氣壓力將鋁罐壓扁
37 2. 克氏溫標 1802 年法國科學家給呂薩克 (Joseph Louis Gay-Lussac, ) 基於查爾斯的研究, 從實驗中發現 : 在密閉容器內的定量低密度氣體, 若氣體體積維持不 變, 則其壓力 P 與攝氏溫度 t 有一線性關係 ( 圖 1-32) 如下 圖 1-32 定量的低密度氣體, 若氣體體積維持不變, 其壓力與攝氏溫度成線性關係 P=P 0 ( t) 1-17 式 式中 P 0 代表氣體在 0 時的壓力, 此一結果稱為定容的查爾斯 - 給呂薩克 定律 奇妙的是即使改變氣體種類或質量, 定容的查爾斯 - 給呂薩克定律依 然成立, 並且各直線外插之延長線, 在橫軸竟相交於同一點, 該點溫度 為 你有沒有注意到這個結果和第三節熱膨脹一節中所提到 的定壓的查爾斯 - 給呂薩克定律 (1-14) 式一樣? 兩者相同的形式是否有 什麼奧妙之處呢? 其實早在 1699 年, 法國物理學家阿蒙頓 (Guillaume Amontons, ) 就已經利用自製的儀器注意到此一現象, 並推測 當溫度低到某個程度 ( 即圖中的 ) 時, 對應的氣體壓力或氣 體體積均為零, 不過實際上氣體在到達此低溫之前, 早已成為液體或固 體了 是理論中的最低溫度,1848 年克耳文建議將此溫度定為 絕對零度 (absolute zero), 記為 0 K, 並且規定克氏溫標溫度變化一度 與攝氏溫標溫度變化一度相同, 若以 T 代表克氏溫度,t 代表攝氏溫度, 則兩溫標的關係為 T=t 根據此一關係可知 0 = K 1-18 式
38 如圖 1-33 所示, 若是改以克氏溫標描述定容的查爾斯 - 給呂薩克定律, 則可得到以下較簡潔的描述 : 在密閉容器內的定量低密度氣體, 若氣體體積維持不變, 則其壓力 P 和克氏溫度 T 成正比, 即 P=P 0 ( t ) =P 0 ( T ) T 同樣的道理, 如圖 1-34 所示, 若是改以克氏溫標描述 第三節的定壓的查爾斯 - 給呂 薩克定律, 則可得到以下較簡潔的描述 : 在密閉容器內的定量低密度氣 體, 若氣體壓力維持不變, 則其體積 V 和克氏溫度 T 成正比, 即 圖 1-34 密閉容器中壓力固定的低密度氣體, 其體積 V 和克氏溫度 T 成正比 圖 1-33 密閉容器體積固定時, 低密度氣體的壓力 P 和克氏溫度 T 成正比 V=V 0 ( t ) =V 0 ( T ) T 由於水的冰點和沸點容易受到大氣 壓力變動的影響, 在精密度要求漸高的 趨勢下, 已不適合作為溫標訂定的標 準, 因此 1954 年國際度量衡大會中決 議改以冰 水和水蒸汽三者共存而達成 熱平衡時的三相點為溫度標準, 並定義 該點的溫度為 K, 由此來定義克 氏溫標
39 1-9 將一個內部充填定量氣體的球泡與氣壓計緊密相連如 圖 1-35, 若是可忽略球泡本身的熱漲冷縮, 則可利用 此球泡內壓力的變化來量測溫度 在室溫 20.0 時, 球泡內的壓力為 80.0 cmhg, 接著將球泡改放置在某 待測液體中使其達成熱平衡, 此時球泡內壓力變為 cmhg, 則此待測液體的溫度為何? 圖 1-35 利用固定體積球泡內壓力的變化來量測溫度 [ 解答 ] 設待測液體攝氏溫度為 t, 由於定容氣體的壓力與克氏溫度成正比, 故 80.0 = t 即待測液體的溫度為 波以耳定律 氣體異於液體和固體的主要差別, 就是容易壓縮以致沒有固定的體 積 早在 1662 年, 英國科學家波以耳 (Robert Boyle, ) 就從 實驗研究中發現 : 在密閉容器內的定量低密度氣體, 若氣體溫度維持不 變, 則其壓力 P 與其體積 V 成反比, 即 P 1 V 此關係式稱為波以耳定律 (Boyle's law) 對密閉容器內的定量氣體, 當溫度維持一定時, 其壓力 P 與體 積 V 的關係曲線如圖 1-36 所示, 而 狀態 A 與狀態 B 遵守以下關係式 P A V A =P B V B = 定值 1-19 式 圖 1-36 密閉容器中溫度固定的低密度氣體, 其壓力 P 和體積 V 成反比 波以耳當年並未提及溫度維持不變, 此一條件是法國物理學家馬若特 (Edme Mariotte, ) 稍晚在 1676 年獨立提出, 所以此定律亦稱波以耳 - 馬若特定律
40 1-10 如圖 1-37(a) 所示, 將一針筒接上氣壓計以測量不同體積時的壓力變化 起初當針筒中空腔部分的高度為 30cm 時, 氣壓計所顯示的壓力為 1.0atm 在溫度維持不變, 且無氣體進出針筒的條件下, 將活塞向上推使針筒中空腔部分高度變為 20cm( 如圖 1-37(b)) 時, 針筒內的氣體壓力為何? [ 解答 ] 設針筒之截面積為 A, 根據波以耳定律 (1.0 atm)(30 cm)a=p'(20 cm)a 解得後來針筒內的氣體壓力 P'=1.5 atm 圖 亞佛加厥定律 前面我們學了許多關於在密閉容器內的定量低密度氣體, 描述其狀 態的物理量之間的關係, 現在讓我們將這些定律依年代排序如下 波以耳定律 :P V= 定值在固定溫度的條件下 定壓的查爾斯 給呂薩克定律 : V T 在固定壓力的條件下 定容的查爾斯 給呂薩克定律 : P T 在固定體積的條件下 綜合以上敘述可得 或者亦可寫成 P V T PV T = 常數 1-20 式 (1-20) 式顯示了一個相當有趣的結果 : 我們在分隔成體積相同的兩個氣室中, 裝有溫度 壓力與分子數皆相同的某種定量低密度氣體 當抽掉中間的隔板使兩邊的氣體混合達成平衡後, 溫度與壓力均未發生變化, 但我們注意到此時不論是氣體分子數抑或是體積均加倍了,
41 ( 如圖 1-38 示 ) 亦即 (1-20) 式中的常數應與氣體分子數 N 有關 PV T N 1-21 式 然而對不同氣體, 上式中的比例常數是否相同呢? 圖 1-38 固定氣體的壓力與溫度, 當氣體分子數加倍時氣體體積亦加倍 1811 年, 義大利人亞佛加厥 (Amedeo Avogadro, ) 發表了亞佛加厥假說 (Avogadro's hypothesis) 他認為氣體是由為數眾多的微小分子所組成, 並且指出在相同的溫度和壓力下, 任何同體積的氣體都含有相同數目的分子 此說法後來為實驗所證實, 改稱亞佛加厥定律 (Avogadro's law) 亞佛加厥定律說明了不管是何種氣體,(1-21) 式中的比例常數均相同, 亦即我們可以得到一個一般性的結果描述氣體性質另一方面, 由於一般狀況下, 氣體所擁有的分子數目非常大, 因此常用莫耳 (mole, 記作 mol) 這個單位來描述很大的數量 實驗顯示在 0 一大氣壓的條件下, 一莫耳的任何氣體, 皆占有約 22.4 升 (liter, 符號為 L) 的體積 而我們將一莫耳所含的粒子數目, 稱為亞佛加厥數 (Avogadro's number), 通常以 N A 表示 經過多年的實驗測量後, 亞佛加厥數最終被確認約為 N A = mol -1 若以 n 表示氣體分子的莫耳數, 則其所含的分子數目 N 為 N=n N A 因此我們亦可以氣體分子莫耳數 n 改寫 (1-21) 式如下 PV T n 1-22 式
42 5. 理想氣體方程式 在前面的敘述中, 不管是波以耳定律 定壓的查爾斯 - 給呂薩克定律或定容的查爾斯 - 給呂薩克定律, 所討論均是定量且溫度不太低的低密度氣體, 我們將滿足以上定律的氣體稱為理想氣體 (ideal gas) 接著讓我們將波以耳定律 定壓的查爾斯 - 給呂薩克定律 定容的查爾斯 - 給呂薩克定律與亞佛加厥定律結合後, 可改寫 (1-22) 式為 PV T =nr 1-23 式 上式中的 R 是與氣體種類無關之常數, 稱為理想氣體常數 (ideal gas constant) 其值約為 R=0.082 atm L/mol K=8.31 J/mol K 一般習慣將 (1-23) 式寫成 PV=nRT 1-24 式 此方程式是由波以耳定律 定壓的查爾斯 - 給呂薩克定律 定容的查爾斯 - 給呂薩克定律以及亞佛加厥定律等經驗定律歸納而得, 唯有當討論的是理想氣體時, 才滿足此一關係式, 因此稱 (1-24) 式為理想氣體方程式 (equation for ideal gas), 或稱為理想氣體定律 (ideal gas law) 想一想 試利用正文中的敘述 : 實驗顯示在 0 1 atm 的條件下,1 mol 的理想氣體, 占有約 22.4 L 的體積 並配合理想氣體方程式估算理想氣體常數 R 的值 實驗顯示, 若利用現代科技將低密度氣體降到極低的溫度, 此時氣體分子因為能量相當小而會展現出一些古典物理所未曾預期到的量子效應, 這使得以上的氣體方程式不再適用, 因此正文中才會另外要求須在溫度不太低的情況下 不過一般室溫下教室內的空氣 ( 甚至是極地區的低溫空氣 ) 都可視為理想氣體
43 1-11 如圖 1-39 所示, 當閥門關閉時,A B 兩空腔內分別封有 1 mol 的理想氣體並以裝有閥門的細管相連 已知兩空腔的容積比為 1:2, 溫度分別維持在 300 K 與 400 K 今將閥門打開, 則在達成穩定狀態時,A 空腔內的氣體分子莫耳數為何?( 設 A B 空腔的溫度與容積在閥門打開後仍然分別維持不變 ) [ 解答 ] 如圖 1-40 所示, 閥門關閉時, 設 A B 兩空腔內氣體壓力分別為 P A 及 P B, 由理想氣體方程式 P V=n R T 可得 圖 1-39 閥門打開後, 氣體會流動, 直到兩空腔內的氣體壓力相等, 達成穩定狀態 P A V=(1 mol)r(300 K) 1 P B (2V)=(1 mol)r(400 K) 2 將 1 式除以 2 式可得壓力比 P A :P B =3:2 因此一旦閥門打開, 空腔 A 內的氣體分子 圖 1-40 莫耳數會減少至 n A, 而空腔 B 內的氣體分子 莫耳數會增加至 n B, 直到空腔內氣體壓力均 為 P 達成穩定, 如圖 1-41 所示 由理想氣體 方程式 P=n R T 可得 P V=n A R(300 K) P(2V)=n B R(400 K) 將 3 式除以 4 式可得莫耳數比 n A :n B =2:3 又因為 n A +n B =2 mol, 所以 3 4 n A = 2 (2 mol)=0.8 mol 2+3 即 A 空腔內的氣體分子莫耳數變為 0.8 mol 圖 1-41
44 1-6 氣體動力論 十七世紀時, 隨著熱學研究的進展, 科學家們開始探究熱現象的本質, 分子運動理論因之興起 1678 年, 虎克首先以組成氣體的分子不斷撞擊容器壁, 來解釋氣體壓力的產生 這是最早從氣體分子運動的觀點, 來說明氣體壓力起因的嘗試 1738 年, 瑞士科學家白努利 (Daniel Bernoulli, ) 從虎克的假設出發, 以微觀方式導出波以耳定律 這些有關分子運動的想法, 在當時未能持續發展, 一個原因是當時熱質說正居於主流想法的地位, 更重要的是分子運動理論, 尚無法以量化的方式來解釋熱現象 直到十九世紀中葉, 焦耳的熱功當量實驗推翻熱質說, 確立熱是能量的一種形式後, 分子運動理論才又快速發展起來 這些處理氣體分子運動的理論稱為氣體動力論氣體動力論 (kinetict heory of gases) 1. 理想氣體的基本假設 氣體動力論指出, 氣體是由數量極大的微小氣體分子所組成, 而且這些分子持續地進行無規則的運動 當分子碰撞容器壁時, 由於動量的變化, 便產生了力以及壓力 前一節中我們已經學會如何以理想氣體方程式描述氣體的狀態, 要利用氣體動力論定量地解釋壓力的成因, 必須先了解氣體動力論對理想氣體分子的基本假設 : 1. 理想氣體是由數量極大且隨機運動的分子所組成, 因此適合使用統計性質來分析處理 2. 由於氣體分子的體積遠小於容器的體積, 可將氣體分子視為質點, 並且由於氣體分子間的距離相當大, 因此未接觸時可以忽略其間的交互作用 3. 氣體分子彼此之間及其與容器壁的交互作用, 僅考慮極短接觸時間內的彈性碰撞, 其他時間均視為作等速運動 以下將從理想氣體的假設開始, 來定量地瞭解氣體壓力產生的原因
45 理想氣體分子的統計性質 當理想氣體分子的數量 N 很大時, 這些個別看似隨機運動的氣體分子, 會表現出一些整體的統計性質, 我們來看看其中幾點 : 1. 先僅考慮在 x 方向上的運動, 由於氣體分子有些往右 有些往左 有些快 有些慢, 直觀上我們預期這些分子在 x 方向上的平均速度會為零, 即 v x,av =0 同理 v y,av =0, v z,av =0 因此平均速度 v av =0 2. 但速率僅反映快慢不含方向性, 因此平均速率 v s,av 0 3. 另一方面, 各方向速度分量平方的平均亦不為零, 即 v 2 x,av= v 2 1x+v 2 2x+ +v 2 Nx 0,v N 2 y,av 0,v 2 z,av 0 但特別的是這些不同方向的速度分量平方之平均會相等, 並且恰為速度量值平方之 1 平均的 3, 即 v 2 x,av=v 2 y,av=v 2 z,av= 1 3 v2 av 2. 分子運動與氣體壓力 此處我們僅將簡略說明在熱平衡時分子運動與氣體壓力之間的關 係, 較詳細的推導證明補充於第 53 頁延伸閱讀, 供有興趣的同學參考 如圖 1-42 所示, 考慮在一個邊長為 L 容積為 V=L 3 的正立方體密閉容器 內, 含有 N 個相同的理想氣體分子, 每個分子的質量均為 m, 並且均為 隨機運動 設想將所有氣體分子逐個加以編號, 並且將其運動速度分解 成 x y z 三個方向的分量 現在我們先單純地考慮編號 1 號的 (a) 圖 1-42 氣體分子以 v 1x 的 x 方向速度分量朝 A x 面入射如圖 (a) 由於與容器壁的碰撞是彈性碰撞, 因此即便接下來與上壁碰撞如圖 (b), 碰撞前後 x 方向的速度分量不變 (b)
46 氣體分子在 x 方向上的運動 當此分子以 v 1x 的 x 方向速度分量入射右側 A x 面, 由於與容器壁的碰撞是彈性碰撞, 因此在該分子與 A x 面碰撞後,x 方向的速度分量會變成 - v 1x, 即該分子的動量變化量值為 Δp 1x =2m v 1x 1-25 式 此一動量變化乃是因為該分子受容器壁作用力影響之故 另一方面根據牛頓第二運動定律 F= Δp Δt, 我們可以將 (1-25) 式 的動量變化量值, 乘以此分子與 A x 面的碰撞頻率 1 Δt, 求出該分子受容 器壁的平均作用力量值 考慮左右容器壁相距 L, 因此該分子連續兩次撞 擊 A x 面所經歷的時間 Δt= 2L v 1x, 即此分子與 A x 面的碰撞頻率為 1 Δt = v 1x 2L 1-26 式 利用 (1-25) 式與 (1-26) 式可知此氣體分子受到 A x 面的平均作用力量 值為 f 1x = Δp 1x Δt = mv2 1x L 1-27 式 此一作用力與容器右側 A x 面受到該氣體分子的反作用力量值相等而方向 相反 細心的你是否從 (1-27) 式中出現的 mv 2 1x 聯想到我們學過的動能型 式 1 2 mv2 呢? 事實上在更詳細的分析過程中, 當我們將此一結果推廣到 全部 N 個氣體分子, 並且這些氣體分子在各方向做隨機運動時, 我們不但可以確定 A x 面受到所有氣體分子撞擊的總作用力量值 F x 會與所有氣體分子的總平移動能 (translation energy) 成正比, 而且還可以
47 推知其比例常數, 一般寫成 F x = 1 3 ( mv 2 1 L + mv 2 2 L + + mv N 2 L ) 更進一步我們知道壓力是單位面積的垂直作用力, 因此對 A x 面而 言, 壓力 P 可寫成 P= F x L 2 = 1 3V ( mv 1 2 +mv mv N 2 ) 1-28 式 此一壓力不僅僅是描述 A x 面所受的壓力, 同時由於各方向壓力相同, (1-28) 式也反映容器中各處的壓力 還記得剛才曾經提到過總作用力量值會與總平移動能成正比嗎? 我們可以定義平均平移動能 K av 如下 K av = 1 N ( 1 2 mv mv mv N 2 )= 1 2 mv rms 式 式中 v rms 稱為方均根速率 (root-mean-square speed), 是一個較簡單方便的選擇可以用來反映平均的分子運動快慢 則利用 (1-29) 式可以將 (1-28) 式改寫成以下較簡潔的型式 P= 2 3V ( 1 2 mv mv mv N 2 )= 2 3V ( N K av ) 方均根速率 方均根速率 v rms 的定義為 v rms = v 1 2 +v v 2 N, 將各個分子的運動速 N 率平方之後取平均再開平方根, 其值與平均速率並不相同, 而是一個方便的選擇, 可以在概念上反映平均的運動快慢及平移動能 此處比例常數的推得可參考第 46 頁科學短文的第 3 點, 或是第 53 頁起延伸閱讀第五點及第六點亦有詳細說明
48 一般寫成 PV= 2 3 NK av 1-30 式 式中的 N K av 正是氣體分子平移動能的總和, 而透過以上簡略的推導過 程已經顯示容器內的氣體壓力正是由氣體分子碰撞容器壁產生, 並且其 值會與每單位體積的分子平移動能成正比 這是多麼神奇的一件事啊! 科學家們利用氣體動力論的幾個簡單假 設, 已成功地將微觀粒子的碰撞運動, 與巨觀世界中的氣體壓力與體積 等物理量建立關係如 (1-30) 式 這些關係一旦建立, 我們僅需利用壓力 計 尺和天平等工具, 分別測量容器內的氣體壓力 體積和質量 ( 用以 推知氣體分子數 ), 便可以推算微觀世界的物理量, 例如氣體分子的總 動能和方均根速率等 換句話說, 容器內氣體的壓力等巨觀可測量的物 理量, 是微觀世界中眾多分子運動的統計結果, 這難道不是一件令人嘖 嘖稱奇的事嗎? 1-12 你知道一顆普通氣球內部氣體分子的總動能是多少嗎? 請利用氣體動力論估算一 顆內部裝填 1.0 g 氦氣, 體積為 m 3, 壓力為 1.2 atm 的氣球, 試求此氣 球內氦氣分子的總動能為何? [ 解答 ] 根據 (1-30) 式, 氦氣分子的總動能 K 為 K=N K av = 3 2 P V = 3 2 ( Pa)( m 3 )= J 這些氦氣分子的總動能約與 100 瓦的燈泡點亮 9 秒鐘所消耗的能量差 不多
49 3. 分子平均動能與溫度 在瞭解容器內的氣體壓力可由氣體分子碰撞容器壁來解釋後, 我們將進一步探討另一個熱學中相當重要的巨觀物理量 溫度, 和微觀世界中的物理量之間的關係 對照理想氣體方程式 (1-24) 式和 (1-30) 式, 可以看出氣體分子的平均平移動能為 K av = 3 2 R N A T 式中理想氣體常數 R 和亞佛加厥數 N A 的比值, 稱為波茲曼常數 (Boltzmann constant)k, 其值為 k= R N A = 8.31 J/mol.K mol -1 = J/K 因此一個氣體分子的平均平移動能可表示為 K av = 1 2 mv2 rms= 3 2 kt 1-31 式 由上式中可知, 氣體分子的平均平移動能 K av 和克氏溫度 T 成正比, 與氣 體的種類 壓力 體積等因素無關 只要溫度相同, 各種氣體分子的平 均平移動能皆會相等 你是否注意到此中的奧妙之處呢? 原來溫度是分 子平均平移動能的量度, 溫度的高低反映出氣體分子運動的劇烈程度! 氣體動力論再一次神奇的連結巨觀與微觀世界不同的觀點 因此, 我們 亦可以利用 (1-31) 式從巨觀的溫度推知微觀氣體分子運動的方均根速率 如下 v rms = 3kT m = 3RT M 1-32 式 式中 M 為一莫耳氣體分子的質量 由 (1-32) 式可知分子的方均根速 率, 只與溫度和分子質量有關, 與壓力 分子數目及體積等因素都無 關
50 對相同的分子而言, 溫度愈高, 其方均根速率便愈大 而在溫度相同時, 質量愈大的分子, 其方均根速率則愈小 另一方面, 利用波茲曼常數的定義, 我們不一定要以氣體分子莫耳數 n 來表示理想氣體方程式, 也可以用氣體分子數 N 改寫理想氣體方程式如下 P V=n R T=n(k N A )T=(n N A )k T=N k T 亦即理想氣體方程式也可以寫成 P V=N k T 1-33 式 這讓我們在處理問題時有更大的彈性 舉例來說,(1-31) 式指出一個氣 體分子的平均平移動能為 K av = 3 2 kt, 因此若氣體分子總數為 N( 莫耳數 為 n), 則該氣體系統總動能 K 可寫成 或者亦可以寫成 甚至可以寫成 K= 3 2 N k T 1-34 式 K= 3 2 n R T 1-35 式 K= 3 2 PV 1-36 式 請你自己動手驗證這些結果 此處的 (1-34) 式與 (1-35) 式, 似乎可以 很簡單地由巨觀的溫度來計算氣體系統總動能, 但由於我們沒有辦法一 一細數氣體分子的數目, 因此還必須透過其他條件找到氣體系統的分子 數或莫耳數, 才有辦法求得總動能 相較於此,(1-36) 式則可以更加直 接的利用兩個巨觀的物理量 : 壓力與體積, 來求出氣體系統的總動能
51 科學家們以微觀的分子運動的觀點, 成功地解釋許多與氣體有關的巨觀現象, 例如對壓力成因的探究以及指出溫度是分子運動快慢的量度等 氣體動力論的成就又引領科學家們將分子運動的理論, 應用在解釋液體與固體的性質, 例如物質的比熱等, 也都得到相當不錯的結果 至十九世紀末, 一個定量且完整的分子運動理論便已建構完成 1-13 日常生活中, 我們可能很難想像微小的氣體分子是以多快的速率在運動, 請你利用氣體動力論估算, 在室溫 20.0 時, 空氣中的氦氣分子方均根速率為何?( 已知氦的分子量為 ) [ 解答 ] 根據 (1-32) 式, 在室溫 20.0 ( 相當於 K) 時, 氦氣分子的方均根速率為 v rms = 3 RT M = 3 ( 8.31 J/mol.K ) ( K ) kg/mol = m/s 換算後此一速率將近時速五千公里! 不過空氣中組成成分較多的氮氣 或氧氣等, 由於質量均較氦氣大, 因此同樣在室溫 20.0 時, 方均根 速率均較氦氣小, 其值約為 500 m/s, 與空氣中的聲速 343 m/s 相當 想一想 1997 年諾貝爾物理獎得主朱棣文 (1948-, 華裔美籍科學家, 圖 1-43) 的主要貢獻是發展以雷射冷卻原子的方法 某實驗室以此方法將鈉原子 ( 23 Na) 冷卻後, 測得這些氣態鈉原子的方均根速率為 0.20 m/s, 若將此系統視為理想氣體, 則這些鈉原子的絕對溫度為多少? 圖 1-43 朱棣文
52 分子運動與氣體壓力的詳細推導 考慮如圖 1-44 所示, 在一個邊長為 L 容積為 V=L 3 的正立方體密閉容器內, 含有 N 個相同的理想氣體分子, 每個分子的質量均為 m, 並且均為隨機運動 我們透過以下幾個步驟的討論, 來瞭解分子運動與氣體壓力的關係 一 先考慮一個分子在 x 方向的運動考慮某個氣體分子在 x 方向上的速度分量為 v x, 並且如圖 1-45 所示入射右側 A x 面 由於氣體分子與容器壁的碰撞是彈性碰撞, 在該分子與 A x 面碰撞後, 其 y 方向和 z 方向的速度分量將不會改變, 僅有 x 方向的速度分量在碰撞後變成 - v x, 即該分子的動量變化 Δ p x 為 Δ p x =m(- v x )-m v x =-2m v x (1) 此一動量變化乃是因為該分子受容器壁作用力影響之故, 欲找此一作用力, 需先找出作用時間 Δt, 再利用牛頓第二運動定律找出作用力 二 考慮氣體分子與 A x 面的作用時間由於將氣體分子視為質點且做彈性碰撞, 乍想之下因為接觸時間甚小, 會得到瞬時作用力甚大的怪異結果 實際上與 A x 面發生碰撞的並不是只有這一個分子, 在此一分子與容器壁發生碰撞的期間之外仍有許多其他分子與容器壁發生碰撞, 因此要考慮的是平均作用力而非瞬時作用力 ( 圖 1-46), 亦即要找的時間是平均碰撞時間, 也就是此一分子每隔多久會碰撞一次 A x 面 當此分子從 A x 面反彈後, 也有可能撞擊上下前後的其他容器壁面, 但由於皆為彈性碰撞, 類似之前的分析, 此種碰撞僅會改變 y 方向和 z 方向的速度分量, 而平行於 x 軸的速度分量則要在撞擊到左側的 A' x 面時才會再一次被改變方向, 但其量值仍維持 v x 圖 1-44 密閉容器中有許多氣體分子隨機運動 圖 1-45 分子撞擊容器壁前後, 其速度變化的情形 圖 1-46 圖中藍色實線描述氣體分子與容器壁碰撞的瞬時作用力變化, 而紅色虛線代表平均作用力
53 不變 考慮左右容器壁相距 L, 因此再度返回撞擊 A x 面所經歷的時間 Δt 為 Δt= 2L v x 此即氣體分子與 A x 面間的平均作用時間 三 考慮 A x 面受到一個分子碰撞的平均作用力 綜合 (1) 式與 (2) 式, 此氣體分子受到 A x 面的平均作用力 f x, 其量值為 f x = Δp x Δt = 2mv x = mv x 2 2L L v x 再根據作用力與反作用力定律, 可知容器右側 A x 面受到該體分子的作用力 f x ' 與 f x 雖 然方向相反, 但量值相同均為 四 接著考慮 N 個分子的運動 f ' x =f x = mv x 2 L 設想將全部 N 個氣體分子逐個加以編號, 則全部氣體分子撞擊 A x 面的總作用力 F x 為各分子對此面的作用力 f 1x ' f 2x ' f Nx ' 之和, 其量值為 N F x = f ix '= m L (v 1x 2 +v 2 2x + +v 2 Nx ) (3) i=1 由此可知, 與 x 軸垂直的 A x 面所受的總力, 會與各分子沿此方向的速度分量的平方和 有關 五 考慮 N 個分子的統計性質 當我們完整考慮氣體分子在各方向的運動時, 首先會注意到各分子運動速度量值的 平方會等於各方向分量的平方和, 即 v 1 2 =v 1x 2 +v 1y 2 +v 1z 2 v 2 2 =v 2 2x +v 2 2 2y +v 2z v 2 N =v 2 Nx +v 2 2 Ny +v Nz 另一方面, 根據氣體動力論的假設, 由於分子朝各方向運動的機率相等, 因此雖然各個分子的運動有快有慢, 並且在各方向的分量也不盡相同, 但平均而言, 所有分子的 x 方向速度分量平方之和, 會與 y 方向或 z 方向速度分量平方之和相等, 也就是上面紅色方框框起來的部分會相等, 即 v 2 1x +v 2 2x + +v 2 Nx =v 2 1y +v 2 2y + +v 2 Ny =v 2 1z +v 2 2 2z + +v Nz (2)
54 綜合以上敘述可得 或者可以寫成 v 1 2 +v v N 2 =(v 1x 2 +v 1y 2 +v 1z 2 )+(v 2x 2 +v 2y 2 +v 2z 2 )+ +(v Nx 2 +v Ny 2 + +v Nz 2 ) =(v 1x 2 +v 2x 2 + +v Nx 2 )+(v 1y 2 +v 2y 2 + +v Ny 2 )+(v 1z 2 +v 2z 2 + +v Nz 2 ) =3(v 1x 2 +v 2x 2 + +v Nx 2 ) (v 1x 2 +v 2x 2 + +v Nx 2 )= 1 3 (v 1 2 +v v N 2 ) (4) 1 3, 1 3, 2 例如 v 1x 並不一 此處請特別留意是所有分子某方向的速度分量平方之和才會等於速度平方之和的 至於個別分子某方向的速度分量平方並不一定會等於其速度平方的 定會等於 1 3 v 1 2 六 考慮 N 個分子造成的力與壓力 綜合以上所述, 將 (4) 式代入 (3) 式, 可得 N 個氣體分子撞擊 A x 面的總作用力量值為 F x = m 3L (v 1 2 +v v N 2 ) 亦即容器右側 A x 面所受的壓力 P 為 P= F x L 2 = m 3V (v 1 2 +v v N 2 ) (5) 事實上 (5) 式所得到的壓力 P 不只是反映 A x 面所受的壓力, 也由於各方向的速度分量平 方和均相同, 亦可看出正文提到的各方向壓力會相同的結果, 因此由式同時也反映容器 中各處的壓力 七 最後考慮方均根速率與平均動能 此外, 在由式中可看出壓力 P 與各個分子的運動快慢有關, 我們可以很方便地選擇 方均根速率 v rms 來反映平均的分子運動快慢, 其定義為 v 2 rms= v 1 2 +v v N 2 N 利用方均根速率可以進一步簡化 (5) 式如下 P= m 3V (N v2 rms) (7) (6)
55 另一方面, 由於分子平移動能的平均值為 K av = 1 N ( 1 2 mv mv mv N 2 )= 1 2 mv2 rms (8) 恰可利用方均根速率反映平均平移動能, 這也說明了之前選擇方均根速率的方便性 最 後, 我們稍加改寫 (7) 式並將 (8) 式代入可得 一般寫成 P= 2N 3V ( 1 2 mv2 rms)= 2N 3V K av P V= 2 3 N K av (9) 式中的 N K av 正是各氣體分子平移動能的總和, 而推導過程顯示容器內的氣體壓力是由 氣體分子碰撞容器壁產生, 其值與每單位體積的分子平移動能成正比 八 補充考慮與其他分子間的碰撞 以上討論雖未考慮到分子間碰撞的情況, 但即使加以考慮也不會影響到最後的結 果 因為分子之間的碰撞為彈性碰撞, 故分子碰撞後, 其總動能並不改變 因此所產生 的壓力, 也不會因為考慮到分子間的碰撞而有所不同 另外以上推導雖是針對正立方體 容器, 但其結果對任意形狀的容器仍然成立
56 布朗運動 氣體動力論對分子的若干假設, 可定量地解釋氣體壓力的成因與度的含意 同樣地將該理論應用在液體與固體中, 也相當成功 依據氣體動力論的假設, 分子的運動是混亂無規的, 但是直到十九世紀末, 分子存在的真實性仍沒有直接的實驗證據 1827 年, 英國植物學家布朗 (Robert Brown, ) 在研究植物授粉的過程中, 意外發現顯微鏡下懸浮水中的花粉微粒, 竟然不停地作不規則的折線運動, 如圖 1-47 所示 他進一步發現任何物質只要碾成微粒, 並使其懸浮在液體中, 都能看到如花粉般的不規則運動, 而且顆粒愈小, 運動便愈活躍 這種懸浮在液體中微小顆粒的運動, 稱為布朗運動 (Brownian motion) 在布朗運動發表之後的五十年間, 科學家們都未能 圖 1-47 布朗運動對布朗運動提出合理正確的解釋 直到分子運動論再次興起, 英國的拉姆賽 (William Ramsay, ) 才於 1876 年提出, 布朗運動是由於懸浮在水中的微粒, 受到水分子不均勻的碰撞所引起 此後三十年間, 企圖用分子運動論來解釋布朗運動的種種嘗試層出不窮, 但始終未能建立起可用實驗檢驗的定量理論 直到 1905 年, 愛因斯坦從分子碰撞的觀點, 以統計方法分析布朗運動的現象, 這是第一篇可用實驗檢驗的定量理論 在此理論中, 他預言了微粒平均運動路徑長度, 與度 微粒大小 微粒濃度及液體黏稠度等因素的關係, 為後來的實驗驗證工作指引了具體的方向 如溫度愈高, 水分子運動的速度愈快, 撞擊微粒的作用愈強, 布朗運動便愈明顯 另一方面, 若微粒愈小, 在某瞬間與其相撞的分子數愈少, 則撞擊作用的不均勻性就愈明顯, 而布朗運動便愈活躍 法國物理學家佩蘭 (Jean Baptiste Perrin, ), 注意到愛因斯坦關於布朗運動的論文後, 便於 1908 年著手進行一系列的實驗, 到 1910 年完全成功地驗證了愛因斯坦的布朗運動理論 佩蘭的實驗為原子與分子的存在, 提供了直接的證據, 終結了一場歷時約半世紀, 關於原子或分子是否存在的爭論 此後, 人們普遍接受原子論的觀點, 而不再視其為假說 為此, 佩蘭獲得了 1926 年的諾貝爾物理獎的殊榮 布朗運動證實了分子不停地在運動, 而且溫度愈高其運動便愈劇烈, 這種運動常稱為熱運動 原子 分子的熱運動, 會影響到實驗測量的精密度, 即使再精密的儀器仍無法避免粒子熱運動所造成的誤差, 此種誤差屬於隨機誤差 不過對於要求精密的實驗而言, 可適度降低測量時的溫度, 以減少粒子的熱運動, 使測量的精密度提高
57 1-1 溫度與熱 1. 和外界隔離的兩個物體可以彼此傳熱, 並且經過足夠的時間, 使兩物體的巨觀物理 量各自不再變化, 則稱這兩物體達到熱平衡狀態 2. 處於熱平衡狀態的物體, 具有相同的客觀冷熱程度, 亦即會有相同的溫度 3. 焦耳熱功當量的實驗, 確認了熱是能量的一種形式, 而且可以和力學能互相轉換 1 cal 相當於 J 1-2 熱容量與比熱 4. 物體每升高或降低 1, 所吸收或放出的熱即其熱容量, 其單位為 cal/ 5. 單位質量的熱容量稱為比熱, 其單位為 cal/g 熱容量 C 與比熱 s 滿足 C=m s 的關係 6. 若物體的質量為 m 比熱為 s, 當有 ΔQ 的熱變化, 使其溫度變化 Δt 時, 滿足 ΔQ=msΔt 並且溫度上升時熱變化為正代表吸熱, 反之溫度下降時熱變化為負代 表放熱 1-3 熱膨脹 7. 若物體在初溫時的起始長度為 L 0, 溫度升高 Δt 時的長度為 L, 兩者間因熱膨脹而有 L=L 0 (1+αΔt) 的關係 式中 α 是與材質有關的線膨脹係數, 其單位為 -1, 代表當溫度上升 1 時, 物體長度的增加量與起始長度的比值 8. 物體的面膨脹與體膨脹亦有類似線膨脹的關係, 並且面膨脹係數 β 2α, 體膨脹係 數 γ 3α, 單位均為 一般物質在室溫範圍時, 氣體的體膨脹係數比液體大, 液體的體膨脹係數又比固體 大 10. 定壓的查爾斯 - 給呂薩克定律指出, 在密閉容器內的定量低密度氣體, 若氣體壓力維 1 持不變, 則其體積 V 與攝氏溫度 t 滿足 V=V 0 ( t) 11. 在密閉容器中壓力固定的定量低密度氣體,0 時的體膨脹係數 γ= 一體膨脹係數與氣體種類以及氣體分子數無關 此
58 1-4 物質的三態變化與潛熱 12. 當物質的溫度或壓力發生變化時, 其物態會發生改變, 稱為物態變化或相變 13. 物態變化時所吸收或放出的熱, 稱為潛熱 主要用於改變分子間的位能, 而不 是在增加分子的動能, 因此在相變期間溫度保持不變 14. 三相圖中三條曲線的交點稱為三相點 在此特定壓力和溫度下, 三態可共存而 達成熱平衡 15. 一般物質壓力增大時, 其熔點與沸點均會隨之升高 但是像水 生鐵 銻 鉍 等少數物質, 其熔點會隨壓力的增大而降低, 沸點則仍隨壓力增大而升高 1-5 理想氣體方程式 16. 物體表面上, 每單位面積所受的正向力稱為壓力, 單位為 Pa( 即 N/m 2 ) 17. 一般將 1 atm 視為與 76 cmhg 所造成的壓力相當, 其值約 Pa 18. 定容的查爾斯 - 給呂薩克定律指出, 在密閉容器內的定量低密度氣體, 若氣體體積維 1 持不變, 則其壓力 P 與攝氏溫度 t 滿足 P=P 0 ( t) 19. 理論中的最低溫度為 , 稱為絕對零度, 記為 0K 水的三相點溫度 定義為 K 20. 波以耳定律指出, 在密閉容器內的定量低密度氣體, 若保持氣體溫度維持不 變, 則其壓力 P 與其體積 V 反比 21. 亞佛加厥定律指出, 在相同的溫度和壓力下, 任何同體積的氣體都含有相同數 目的分子 22. 理想氣體方程式 P V=n R T 中,R 是與氣體種類無關的常數, 其值約為 R=0.082 atm L/mol K=8.31 J/mol K 1-6 氣體動力論 23. 對定量的低密度氣體而言, 氣體分子的體積遠小於容器的體積, 可將氣體分子 視為質點, 彼此之間的碰撞及其與容器壁之間的碰撞均視為彈性碰撞 且由於 氣體分子間的距離相當大, 除了碰撞外可以忽略其他的交互作用 此外, 一般 氣體均是由數量極大的氣體分子所組成, 因此適用統計性質 滿足以上條件的 氣體稱為理想氣體
59 24. 容器內氣體壓力是由氣體分子碰撞容器壁產生, 其值與每單位體積的分子平移動能成正比, 即 P V= 2 3 N K av 25. 容器內氣體的壓力 溫度等宏觀可測量的物理量, 是微觀世界中眾多分子運動 的統計結果 26. 一個氣體分子的平均平移動能可表示為 K av = 1 2 mv2 rms= 3 2 k T, 和克氏溫度 T 成正比, 與氣體的種類 壓力 體積等因素無關 27. 溫度是分子平均平移動能的量度, 溫度的高低反映出氣體分子運動的劇烈程 度 28. 氣體分子運動的方均根速率為 v rms = 3kT = 3RT, 只與溫度和分子質 m M 量有關, 與壓力 分子數目及體積等因素都無關 29. 理想氣體方程式亦可寫成 P V=N k T, 式中 N 為氣體分子的個數, 且波茲曼常數 k= R N = J/K A 30. 氣體系統總動能可寫成 K= 3 2 N k T= 3 2 n R T= 3 2 P V
60 ( 題號有 者為難題 ) 一 問答題 1. 測量體溫時, 為何酒精溫度計須與身體保持接觸一段時間? 2. 將 400 g 50 的鐵塊 ( 比熱為 cal/g ) 與 500 g 40 的銅塊 ( 比熱為 cal/g ) 接觸時, 熱的流動方向為何? 3. 不同物體吸收相同熱時, 比熱大的物質, 其溫度變化一定比較小嗎? 4. 同一物質自不同的初始溫度, 上升相同的溫度, 其長度的增加量是否必定相同? 5. 古老的擺鐘 ( 圖 1-48) 由於擺長會受到溫度變化的影響而熱脹冷縮, 進而影響週期, 若將鐘擺視為單擺, 請問夏天溫度較高時應該如何調整擺長, 使其維持原本的週期呢? 6. 若是不考慮熱的散失, 對某一物質以相同的穩定熱源加熱時間愈長, 其溫度一定愈高嗎? 7. 根據水的三相圖, 固態的冰也可以直接昇華成氣態的水蒸汽, 請問冰昇華的條件為何? 8. 根據調查, 臺灣東部海域深度為 200 m 的海水溫度約為 15, 若有一小氣泡自該處上升至溫度約為 27 的海平面附近, 且假 圖 1-48 設氣泡溫度和周圍之水溫相同, 請根據理想氣體方程式判斷氣泡在海平面附近的體積較深度 200 m 處大或小 9. 依據氣體動力論, 密閉容器內全部氣體分子的總動量為何? 10. 當容器內所裝的氣體很稀薄時, 其總動能很小, 故其溫度必然很低, 以上敘述正確嗎? 二 計算題 1-1 溫度與熱 11. 用一根質量為 0.50 kg 的鐵鎚, 以 20 m/s 的水平速度, 敲擊靠在牆角質量為 1.0 kg 的鐵塊 若鐵鎚有一半的力學能轉變成鐵塊的熱, 並且這些熱不再散失, 則敲擊幾次後, 鐵塊溫度可上升 1.0?( 已知鐵的比熱為 cal/g )
61 1-2 熱容量與比熱 12. 以加熱器加熱質量為 200 g 的純水, 升高 10.0 需費時 100 s, 但以之加熱 400 g 的另一液體時, 升高 5.0 僅需費時 25 s 若加熱器供熱穩定且不計熱的散失, 則該液體的比熱與熱容量分別為何? 13. 已知金的比熱為 cal/g, 銀的比熱為 cal/g 今將這兩種金屬作成合金, 且測得此合金的比熱為 0.041cal/g, 則其中金與銀的質量比為何? 14. 一量熱器中裝有 130 g 的水, 靜置一段時間後水溫為 20 今將質量為 200 g 初溫為 100 的熱水倒入量熱器中, 達熱平衡時水的末溫為 60, 則 (1) 量熱器熱容量的測量值為何? (2) 若操作過程有熱的散逸, 則測量值較真值大或小? 1-3 熱膨脹 15. 一單擺的擺線由線膨脹係數為 的材料製成 在 0 時, 其週期為 T 0 ; 在 30 時, 其週期為 T, 則週期變化的百分誤差為何? 16. 已知鋼的線膨脹係數為 , 當一鋼球的溫度從 0 上升到 50 時, 其密度減少的百分比為何? 17. 在 20 時, 將厚度均為 1.0 mm 長度均為 10.0 cm 的銅片與鋁片, 接合成一雙金屬片, 並保持平直狀態 已知銅與鋁的線膨脹係數分別為 與 , 當溫度升至 30 時, 此雙金屬片會往哪一側彎曲? 其平均曲率半徑為何? 1-4 物質的三態變化與潛熱 18. 已知冰的熔化熱為 80 cal/g, 水的汽化熱為 540 cal/g 質量為 m 1 溫度為 0 的冰與質量為 m 2 溫度為 100 的水蒸汽混合, 則 (1) 平衡時末溫為 100 的條件為何? (2) 平衡時末溫為 0 的條件為何? 19. 已知冰的比熱為 0.50 cal/g. 熔化熱為 80 cal/g, 水的汽化熱為 540 cal/g 今將 54.0 g -40 的冰與 5.4 g 100 的水蒸汽混合, 若過程中無熱的進出, 則達成熱平衡時會有多少液態的水?
62 1-5 理想氣體方程式 20. 如圖 1-49 所示, 將一粗細均勻 長度為 40 cm 的量筒, 筒口朝下, 鉛直壓入水銀槽中 若大氣壓力為 76 cmhg, 當量筒口距離筒外水銀面 6.0 cm 時, 量筒內外水銀面的高度差為何? 21. 上課鐘響後,40 名同學進入教室內, 並將與這群同學相同體 積的空氣擠出教室外 若平均每人的體積為 m 3, 則在室溫 atm 的條件下, 請估算 圖 1-49 (1) 有多少個空氣分子流失到教室外? (2) 已知空氣的平均分子量為 28.8, 則流失空氣的質量為何? 22. 如圖 1-50 所示, 將一容器內裝入理想氣體後, 以一能自由滑動之活塞隔成 A B 兩室 在 27 時,A B 兩室體積和壓力均為 V 和 P 今將 A 室緩慢加熱至 127,B 室則保持 27, 則平衡時 (1) A 室體積增加多少? 圖 1-50 (2) 兩室壓力為何? 23. 一氦氣鋼瓶容積為 35.0 L, 內部充填氦氣的壓力為 105 atm 今欲用此鋼瓶對氣球充氣, 且要求將每一個氣球充至體積為 3.00 L 壓力為 1.05 atm, 則此鋼瓶最多可充幾個氣球? 1-6 氣體動力論 24. 請利用氣體動力論與理想氣體方程式的結果, 證明氣體運動的方均根速率可寫 成 v rms = 3P ρ, 其中 P 為氣體壓力,ρ 為氣體密度 25. 某密閉容器中裝有氦氣, 當其絕對溫度增為原來的 4 倍, 並且容積維持不變 時, 氦氣分子每秒撞擊單位面積容器壁之次數變為原來的若干倍? 26. 如圖 1-51 所示, 有兩個體積固定的絕熱容器分別 裝有 A B 兩種單原子理想氣體, 其壓力 體積 與溫度分別為 P 1 V 1 T 1 及 P 2 V 2 T 2 今用 一細管連通此兩容器, 則平衡時 : (1) 壓力為何? (2) 溫度為何? 圖 1-51
10 6, 地球的熱循環
 52 2013 4 484 人類活動與 地球熱循環 46 不斷追求進步的我們, 殊不知在迅猛發展的同時, 已經陸續對地球的整個環境生態引爆一顆顆不定時炸彈, 所造成的傷害正逐漸擴大並增強中 10 6,000 500 地球的熱循環 3 2013 4 484 53 54 2013 4 484 工業革命後, 人類活動產生的熱迅速增加, 使地球原本趨於最適合人類活動的熱平衡必須重新調整 環境變遷 18 280
52 2013 4 484 人類活動與 地球熱循環 46 不斷追求進步的我們, 殊不知在迅猛發展的同時, 已經陸續對地球的整個環境生態引爆一顆顆不定時炸彈, 所造成的傷害正逐漸擴大並增強中 10 6,000 500 地球的熱循環 3 2013 4 484 53 54 2013 4 484 工業革命後, 人類活動產生的熱迅速增加, 使地球原本趨於最適合人類活動的熱平衡必須重新調整 環境變遷 18 280
0 0 = 1 0 = 0 1 = = 1 1 = 0 0 = 1
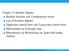 0 0 = 1 0 = 0 1 = 0 1 1 = 1 1 = 0 0 = 1 : = {0, 1} : 3 (,, ) = + (,, ) = + + (, ) = + (,,, ) = ( + )( + ) + ( + )( + ) + = + = = + + = + = ( + ) + = + ( + ) () = () ( + ) = + + = ( + )( + ) + = = + 0
0 0 = 1 0 = 0 1 = 0 1 1 = 1 1 = 0 0 = 1 : = {0, 1} : 3 (,, ) = + (,, ) = + + (, ) = + (,,, ) = ( + )( + ) + ( + )( + ) + = + = = + + = + = ( + ) + = + ( + ) () = () ( + ) = + + = ( + )( + ) + = = + 0
 6 2012 8476你猜得到它是什麼嗎 它就是 高分子! 生活中的高分子 有種物質的重要性不亞於我們所呼吸的空氣, 不管身在何處, 都有它的存在, 它甚至就隱藏在人體裡面! 人類若失去了它, 就得回到遠古時代, 甚至可能終止生命 高分子是什麼 高分子是由千個 甚至萬個以上的原子所組成, 呈現柔軟的特性 日常生活中使用的塑膠袋就是由高分子製造的, 人體組成中的 DNA 也是一種高分子 2012 8476
6 2012 8476你猜得到它是什麼嗎 它就是 高分子! 生活中的高分子 有種物質的重要性不亞於我們所呼吸的空氣, 不管身在何處, 都有它的存在, 它甚至就隱藏在人體裡面! 人類若失去了它, 就得回到遠古時代, 甚至可能終止生命 高分子是什麼 高分子是由千個 甚至萬個以上的原子所組成, 呈現柔軟的特性 日常生活中使用的塑膠袋就是由高分子製造的, 人體組成中的 DNA 也是一種高分子 2012 8476
Microsoft PowerPoint - 热学002.pptx
 热 学 ( 求 是 科 学 班 ) 第 二 节 物 态 和 物 态 方 程 吴 建 澜 浙 江 大 学 物 理 系 2014 年 1) 物 体 的 基 本 宏 观 参 数 : 2) 理 想 气 体 物 态 方 程 理 想 气 体 微 观 模 型 3) 非 理 想 气 体 物 态 方 程 van der Waals 方 程 ; Viral (Onnes) 方 程 4) 相 与 相 变 的 初 步 概
热 学 ( 求 是 科 学 班 ) 第 二 节 物 态 和 物 态 方 程 吴 建 澜 浙 江 大 学 物 理 系 2014 年 1) 物 体 的 基 本 宏 观 参 数 : 2) 理 想 气 体 物 态 方 程 理 想 气 体 微 观 模 型 3) 非 理 想 气 体 物 态 方 程 van der Waals 方 程 ; Viral (Onnes) 方 程 4) 相 与 相 变 的 初 步 概
現在人類獲取地球內部訊息的方法, 是從可能影響我們身家性命安全的地震, 用數學模型把地震資料轉換成地震波速度, 進而獲得地底物質密度與深度的關係 地下世界知多少 km/s g/cm 3 P Gpa km S P S 3,000 3,000 ak K 透視地底 Percy Bridgma
 透視地球深處 的窗戶? extreme condition extreme environment 94.5 1 270 21 3.9 12.3 6,400 300 4,000 1864 Jules Gabriel Verne 1959 2008 1990 Paul Preuss 2003 24 2013 2 482 現在人類獲取地球內部訊息的方法, 是從可能影響我們身家性命安全的地震, 用數學模型把地震資料轉換成地震波速度,
透視地球深處 的窗戶? extreme condition extreme environment 94.5 1 270 21 3.9 12.3 6,400 300 4,000 1864 Jules Gabriel Verne 1959 2008 1990 Paul Preuss 2003 24 2013 2 482 現在人類獲取地球內部訊息的方法, 是從可能影響我們身家性命安全的地震, 用數學模型把地震資料轉換成地震波速度,
二次曲線 人們對於曲線的使用及欣賞 比曲線被視為一種數學題材來探討要早 得多 各種曲線中 在日常生活常接觸的 當然比較容易引起人們的興趣 比如 投擲籃球的路徑是拋物線 盤子的形狀有圓形或橢圓形 雙曲線 是較不常見的 然而根據科學家的研究 彗星的運行軌道是雙曲線的一部 分 我們將拋物線 圓與橢圓 雙曲
 -1 圓方程式 第 章 二次曲線 38 二次曲線 人們對於曲線的使用及欣賞 比曲線被視為一種數學題材來探討要早 得多 各種曲線中 在日常生活常接觸的 當然比較容易引起人們的興趣 比如 投擲籃球的路徑是拋物線 盤子的形狀有圓形或橢圓形 雙曲線 是較不常見的 然而根據科學家的研究 彗星的運行軌道是雙曲線的一部 分 我們將拋物線 圓與橢圓 雙曲線合稱為圓錐曲線 因為在平面坐標 系中 其對應的方程式均為二元二次式
-1 圓方程式 第 章 二次曲線 38 二次曲線 人們對於曲線的使用及欣賞 比曲線被視為一種數學題材來探討要早 得多 各種曲線中 在日常生活常接觸的 當然比較容易引起人們的興趣 比如 投擲籃球的路徑是拋物線 盤子的形狀有圓形或橢圓形 雙曲線 是較不常見的 然而根據科學家的研究 彗星的運行軌道是雙曲線的一部 分 我們將拋物線 圓與橢圓 雙曲線合稱為圓錐曲線 因為在平面坐標 系中 其對應的方程式均為二元二次式
SW cdr
 1~2 3 4 5~6 7~8 9~10 11 12 13 14 15 16~18 16 16 17 17 18 18 18 19 19 19 20 21 22 23~26 23 24 24 25 26 27 27 27 : 110V 1 110V 110V 15A 2 3 23 24 4 ( ) 5 6 1 2 26 20 l 1 7 3 4 5 15 17 18 12 7~13 6 ~ 8 ~
1~2 3 4 5~6 7~8 9~10 11 12 13 14 15 16~18 16 16 17 17 18 18 18 19 19 19 20 21 22 23~26 23 24 24 25 26 27 27 27 : 110V 1 110V 110V 15A 2 3 23 24 4 ( ) 5 6 1 2 26 20 l 1 7 3 4 5 15 17 18 12 7~13 6 ~ 8 ~
第四章 牛頓定律
 p. 1 熱力學與氣體動力學 Thermodynamics and Kinetic Theory of Gases p. 2 QUIZ 姓名學號 (1) The temperature of a gas in a closed container at 27 o C is raised to 327 o C. By what multiple has v RMS changed? p. 3 (2)
p. 1 熱力學與氣體動力學 Thermodynamics and Kinetic Theory of Gases p. 2 QUIZ 姓名學號 (1) The temperature of a gas in a closed container at 27 o C is raised to 327 o C. By what multiple has v RMS changed? p. 3 (2)
TH8-2.¼Æ¾Ç¦ÒÃDch14.3®Õ²M
 第 14 章溫度與熱量 14-1 1. 將質量不等而溫度分別為 50 0 與 10 的水混合後, 不考慮熱的散失, 其平衡溫度不可 能為 (A) 5 (B) 15 (C) 0 (D) 25 (E) 40 14-2 2. 攝氏溫度標與華氏溫度標的關係可以下列那一個函數關係表示之? (A) (B) (C) (D) (E). 有某個新溫標將水的冰點定為 80 度, 沸點定為 -80 度, 則 50 相當該溫標的
第 14 章溫度與熱量 14-1 1. 將質量不等而溫度分別為 50 0 與 10 的水混合後, 不考慮熱的散失, 其平衡溫度不可 能為 (A) 5 (B) 15 (C) 0 (D) 25 (E) 40 14-2 2. 攝氏溫度標與華氏溫度標的關係可以下列那一個函數關係表示之? (A) (B) (C) (D) (E). 有某個新溫標將水的冰點定為 80 度, 沸點定為 -80 度, 則 50 相當該溫標的
Chapter 1 藥理學的基本原理
 CHAPTER 13 溫度和熱量 大綱 圖片 表格 13-1 熱平衡與溫度 13-2 溫度計 13-3 固體的熱膨脹 13-4 液體的膨脹 13-5 理想氣體 13-6 熱量和比熱 13-7 熱功當量 13-8 物質的三態變化 13-9 熱的傳遞 CHAPTER 13 溫度和熱量 大綱 圖片 表格 圖 13-1 圖 13-2 圖 13-3 圖 13-4 圖 13-5 圖 13-6 圖 13-7 圖
CHAPTER 13 溫度和熱量 大綱 圖片 表格 13-1 熱平衡與溫度 13-2 溫度計 13-3 固體的熱膨脹 13-4 液體的膨脹 13-5 理想氣體 13-6 熱量和比熱 13-7 熱功當量 13-8 物質的三態變化 13-9 熱的傳遞 CHAPTER 13 溫度和熱量 大綱 圖片 表格 圖 13-1 圖 13-2 圖 13-3 圖 13-4 圖 13-5 圖 13-6 圖 13-7 圖
Microsoft Word - ACL chapter02-5ed.docx
 第 2 章神奇的質數 2.1.1 什麼是質數 1 1 1 打下好基礎 - 程式設計必修的數學思維與邏輯訓練 1 1 0 10 2 3 5 7 4 6 8 9 10 4 10000 1229 1000 168 2 3 5 7 11 13 17 19 23 29 31 37 41 43 47 53 59 61 67 71 73 79 83 89 97 101 103 107 109 113 127 131
第 2 章神奇的質數 2.1.1 什麼是質數 1 1 1 打下好基礎 - 程式設計必修的數學思維與邏輯訓練 1 1 0 10 2 3 5 7 4 6 8 9 10 4 10000 1229 1000 168 2 3 5 7 11 13 17 19 23 29 31 37 41 43 47 53 59 61 67 71 73 79 83 89 97 101 103 107 109 113 127 131
 第二節 研究方法 本論文第一章 緒論 說明研究動機與目的 研究方法及研究的範圍及限制 並對 飲食散文的義界 作一觀念的釐清 第二章 文獻探討 就將本研究的理 論建構中的概念作釐清 分別為 現代文學 飲食文學的重要論著 等兩個部 分來描述目前文獻的研究成果 並探討其不足待補述的地方 本研究以 文化研 究 為主要研究基礎 統攝整個研究架構 在不同章節裡 佐以相關研究方法進 行論述 茲圖示如下 研究方法
第二節 研究方法 本論文第一章 緒論 說明研究動機與目的 研究方法及研究的範圍及限制 並對 飲食散文的義界 作一觀念的釐清 第二章 文獻探討 就將本研究的理 論建構中的概念作釐清 分別為 現代文學 飲食文學的重要論著 等兩個部 分來描述目前文獻的研究成果 並探討其不足待補述的地方 本研究以 文化研 究 為主要研究基礎 統攝整個研究架構 在不同章節裡 佐以相關研究方法進 行論述 茲圖示如下 研究方法
4
 練習 9A ( 9. 特殊角的三角比 T ( 在本練習中, 不得使用計算機 如有需要, 答案以根式或分數表示. 試完成下表 三角比 θ 0 4 60 sin θ cos θ tan θ 求下列各數式的值 (. cos 60. sin 4 4. tan 4. cos0 4 tan 0 7. sin 4 cos 4 8. cos 60 tan 4 9. tan 60sin 0 0. sin 60 cos
練習 9A ( 9. 特殊角的三角比 T ( 在本練習中, 不得使用計算機 如有需要, 答案以根式或分數表示. 試完成下表 三角比 θ 0 4 60 sin θ cos θ tan θ 求下列各數式的值 (. cos 60. sin 4 4. tan 4. cos0 4 tan 0 7. sin 4 cos 4 8. cos 60 tan 4 9. tan 60sin 0 0. sin 60 cos
CU0594.pdf
 8 SOHO 1 3 003 SOHO SOHO Coder Programmer HTML CSS PHP JavaScrip 009 LECTURE 1-1 1 048 PART 2 LECTURE 1-1 1 049 SOHO Landing Page Landing 050 PART 2 LECTURE 1-1 1 SEO SEO P.093 SEO SEO SEO SEO SEO 051
8 SOHO 1 3 003 SOHO SOHO Coder Programmer HTML CSS PHP JavaScrip 009 LECTURE 1-1 1 048 PART 2 LECTURE 1-1 1 049 SOHO Landing Page Landing 050 PART 2 LECTURE 1-1 1 SEO SEO P.093 SEO SEO SEO SEO SEO 051
男人的大腦 女人的大腦
 46 2014 6 498 男女大乾坤 男女的戀愛行為 男人的大腦 女人的大腦 2014 6 498 47 48 2014 6 498 女人的戀愛行為 70 900 男人的戀愛行為 8 2014 6 498 49 50 2014 6 498 對於愛與性的混淆 男女所面臨的問題 和我一樣喜歡做愛除了我, 不可以看別人相信我, 沒有問題現在, 和我做愛知道如何引燃我從不傷害我 朋友關係和性 嫉妒和占有欲
46 2014 6 498 男女大乾坤 男女的戀愛行為 男人的大腦 女人的大腦 2014 6 498 47 48 2014 6 498 女人的戀愛行為 70 900 男人的戀愛行為 8 2014 6 498 49 50 2014 6 498 對於愛與性的混淆 男女所面臨的問題 和我一樣喜歡做愛除了我, 不可以看別人相信我, 沒有問題現在, 和我做愛知道如何引燃我從不傷害我 朋友關係和性 嫉妒和占有欲
Microsoft PowerPoint - 2 [相容模式]
![Microsoft PowerPoint - 2 [相容模式] Microsoft PowerPoint - 2 [相容模式]](/thumbs/102/156448396.jpg) . Fluid Statics 1. 流體靜力學 (Fluid Statics): 係探討流體處於靜止狀態或流體內彼此無相對運動情況下之流體受力狀況 因無相對速度, 故無 du 速度梯度, 亦即無剪力, 流體受力主要為 dy 壓力與重力. 流體靜壓力之等向性 (Isotropic) 取一個很小的 element d dy d 因靜止 F = 0 : ( 力平衡 ) ( ) F = 因 ds sinθ
. Fluid Statics 1. 流體靜力學 (Fluid Statics): 係探討流體處於靜止狀態或流體內彼此無相對運動情況下之流體受力狀況 因無相對速度, 故無 du 速度梯度, 亦即無剪力, 流體受力主要為 dy 壓力與重力. 流體靜壓力之等向性 (Isotropic) 取一個很小的 element d dy d 因靜止 F = 0 : ( 力平衡 ) ( ) F = 因 ds sinθ
家具使用說明書_實體版2016.9
 續上頁 居家甲醛對策 保持室內空氣流通 甲醛會緩慢地釋放於空氣中 因此平時就需保持室內空氣流通 尤其新居落成時 請盡量將窗子開到最大 以利通風透氣 由於室內溫度 溼度升高時 會大量釋放甲醛 在夏季或梅雨季節 室內經常長時間處於密閉狀態 請特別謹慎注意 此外 若屋內有數個窗戶時 建議保持至少2 扇窗的通風 收納家具用游離甲醛吸附紙/4入 160元 主成分為多孔天然礦石與紙漿 並添加具吸附 分解效果的胺基酸
續上頁 居家甲醛對策 保持室內空氣流通 甲醛會緩慢地釋放於空氣中 因此平時就需保持室內空氣流通 尤其新居落成時 請盡量將窗子開到最大 以利通風透氣 由於室內溫度 溼度升高時 會大量釋放甲醛 在夏季或梅雨季節 室內經常長時間處於密閉狀態 請特別謹慎注意 此外 若屋內有數個窗戶時 建議保持至少2 扇窗的通風 收納家具用游離甲醛吸附紙/4入 160元 主成分為多孔天然礦石與紙漿 並添加具吸附 分解效果的胺基酸
中國的煤
 課內活動及課後練習的建議答案 課內活動 討論區 ( 3 頁 ) 1 2 網上追蹤 ( 5 頁 ) 2008 年末世界各地煤的蘊藏量地區 蘊藏量 ( 百萬公噸 ) 佔全球的百分比 097 29.8% 15 00 1.8% 272 33.0% 1 38 0.2% 32 013 3.9% 259 253 114 500 31.4% 13.9% 82 001 100.0% 272.2.1 15.0 32.0
課內活動及課後練習的建議答案 課內活動 討論區 ( 3 頁 ) 1 2 網上追蹤 ( 5 頁 ) 2008 年末世界各地煤的蘊藏量地區 蘊藏量 ( 百萬公噸 ) 佔全球的百分比 097 29.8% 15 00 1.8% 272 33.0% 1 38 0.2% 32 013 3.9% 259 253 114 500 31.4% 13.9% 82 001 100.0% 272.2.1 15.0 32.0
 的友誼 而且無論外貌怎樣改變 自信心是自己給自己的 發自內心 的自我認同感是無法改變的 只要自我認同才能得真正的心靈富足 而不是單純的改變外表 不同的整容公司亦會利用現今社會的價值觀來作宣傳 誇大整容 後的效果 又用明星效應 令消費者認為整容真的能變成明星一樣 整容這個風氣是由人們的價值觀造成的 有人指出 我們要接納 整容後的人以及香港社會應對此持更開放的態度 但相反地 為什麼 不能接納那些我們認為不
的友誼 而且無論外貌怎樣改變 自信心是自己給自己的 發自內心 的自我認同感是無法改變的 只要自我認同才能得真正的心靈富足 而不是單純的改變外表 不同的整容公司亦會利用現今社會的價值觀來作宣傳 誇大整容 後的效果 又用明星效應 令消費者認為整容真的能變成明星一樣 整容這個風氣是由人們的價值觀造成的 有人指出 我們要接納 整容後的人以及香港社會應對此持更開放的態度 但相反地 為什麼 不能接納那些我們認為不
理性真的普遍嗎 注意力的爭奪戰 科學發展 2012 年 12 月,480 期 13
 12 科學發展 2012 年 12 月,480 期 你可能不知道的媒體影響 劉正山若用 選戰 的角度來看選舉和參與選舉, 你大腦裡情感的作用一定大過理性的作用, 便會很習慣地拿各種媒體或別人的觀點來使自己的選擇合理化 2012 理性真的普遍嗎 注意力的爭奪戰 科學發展 2012 年 12 月,480 期 13 14 科學發展 2012 年 12 月,480 期 agendasetting 報紙和網路新聞的頭版空間有限,
12 科學發展 2012 年 12 月,480 期 你可能不知道的媒體影響 劉正山若用 選戰 的角度來看選舉和參與選舉, 你大腦裡情感的作用一定大過理性的作用, 便會很習慣地拿各種媒體或別人的觀點來使自己的選擇合理化 2012 理性真的普遍嗎 注意力的爭奪戰 科學發展 2012 年 12 月,480 期 13 14 科學發展 2012 年 12 月,480 期 agendasetting 報紙和網路新聞的頭版空間有限,
1970 新技術的應用 X = 20 + B 13B δ13c X 1 X
 凡發生過的必留下痕跡 同位素分析的考古應用? 如何考古 06 2013 9 489 經由人骨中碳和氮同位素的分析, 提供考古學家另一個探討古代攝食系統的途徑 另外, 可以藉由鍶同位素分析了解人群的來源與遷移過程 1970 新技術的應用 13 15 13 12 15 14 13 15 13 12 15 13 15 13 X = 20 + B 13B δ13c X 1 X 2013 9 489 07 δ
凡發生過的必留下痕跡 同位素分析的考古應用? 如何考古 06 2013 9 489 經由人骨中碳和氮同位素的分析, 提供考古學家另一個探討古代攝食系統的途徑 另外, 可以藉由鍶同位素分析了解人群的來源與遷移過程 1970 新技術的應用 13 15 13 12 15 14 13 15 13 12 15 13 15 13 X = 20 + B 13B δ13c X 1 X 2013 9 489 07 δ
Chapter 3 Camera Raw Step negative clarity +25 ] P / Step 4 0 ( 下一頁 ) Camera Raw Chapter 3 089
![Chapter 3 Camera Raw Step negative clarity +25 ] P / Step 4 0 ( 下一頁 ) Camera Raw Chapter 3 089 Chapter 3 Camera Raw Step negative clarity +25 ] P / Step 4 0 ( 下一頁 ) Camera Raw Chapter 3 089](/thumbs/50/27027900.jpg) Photoshop CC Camera Raw Photoshop Camera Raw Step 1 3 1 2 3 SCOTT KELBY Step 2 B Camera Raw 088 Chapter 3 Camera Raw Chapter 3 Camera Raw Step 3-4 -100 negative clarity +25 ] P / -75-50 Step 4 0 ( 下一頁
Photoshop CC Camera Raw Photoshop Camera Raw Step 1 3 1 2 3 SCOTT KELBY Step 2 B Camera Raw 088 Chapter 3 Camera Raw Chapter 3 Camera Raw Step 3-4 -100 negative clarity +25 ] P / -75-50 Step 4 0 ( 下一頁
01 用 ActionScript 3.0 開始認識 Flash CS3 Flash 是應用在網路上非常流行且高互動性的多媒體技術, 由於擁有向量圖像體積小的優點, 而且 Flash Player 也很小巧精緻, 很快的有趣的 Flash 動畫透過設計師的創意紅遍了整個網際網路 雖然很多人都對 Fl
 01 用 ActionScript 3.0 開始認識 Flash CS3 Flash 是應用在網路上非常流行且高互動性的多媒體技術, 由於擁有向量圖像體積小的優點, 而且 Flash Player 也很小巧精緻, 很快的有趣的 Flash 動畫透過設計師的創意紅遍了整個網際網路 雖然很多人都對 Flash 可以做精美的網路動畫並不陌生, 但是實際上 Flash 不僅如此, 只要搭配 ActionScript
01 用 ActionScript 3.0 開始認識 Flash CS3 Flash 是應用在網路上非常流行且高互動性的多媒體技術, 由於擁有向量圖像體積小的優點, 而且 Flash Player 也很小巧精緻, 很快的有趣的 Flash 動畫透過設計師的創意紅遍了整個網際網路 雖然很多人都對 Flash 可以做精美的網路動畫並不陌生, 但是實際上 Flash 不僅如此, 只要搭配 ActionScript
碳石墨產品 特種石墨 (1) 單晶矽製造設備 (2) 臨界電漿測試設備 (JT-60) * 照片由日本原子力研究開發機構提供 (1) (2)
 碳石墨產品 特種石墨 (1) 單晶矽製造設備 (2) 臨界電漿測試設備 (JT-6) * 照片由日本原子力研究開發機構提供 (1) (2) 特種石墨產品特性 (CIP) 等方性石墨 等方性石墨和異方性石墨 1 µm 可靠性高 超強耐熱性 2, 2,5 卓越的導電性 出色的耐化學性 輕量且便於加工 1 µm 5 1 15 2 [Mg/m 3 ] 5 製程 / 6 用途 LED EDM 環境和能源 *
碳石墨產品 特種石墨 (1) 單晶矽製造設備 (2) 臨界電漿測試設備 (JT-6) * 照片由日本原子力研究開發機構提供 (1) (2) 特種石墨產品特性 (CIP) 等方性石墨 等方性石墨和異方性石墨 1 µm 可靠性高 超強耐熱性 2, 2,5 卓越的導電性 出色的耐化學性 輕量且便於加工 1 µm 5 1 15 2 [Mg/m 3 ] 5 製程 / 6 用途 LED EDM 環境和能源 *
 2013~2015 保健食品產業專業人才 供需調查 2011 5 2011529 2012 2013~2015 2012 44.67% 2011 11.96% 2013~2015 ... 1... 1... 5... 10... 12... 13... 14... 19... 20... 22... 24... 12... 19... 21... 22 III IV 1... 1 2... 3
2013~2015 保健食品產業專業人才 供需調查 2011 5 2011529 2012 2013~2015 2012 44.67% 2011 11.96% 2013~2015 ... 1... 1... 5... 10... 12... 13... 14... 19... 20... 22... 24... 12... 19... 21... 22 III IV 1... 1 2... 3
( )1. 關於氫氣的燃燒反應 :2H 2(g) +O 2(g) 2H 2 O (L) 的敘述, 下列何者正確? (A)ΔH 為正值 (B)1 atm 25 時, 此反應可以自然發生 (C) 生成物的熱含量總和較反應物的熱含量總和低 (D) 在 1 atm 100 時所放的熱量為標準反應熱 答案 :
 ( )1. 關於氫氣的燃燒反應 :2H 2(g) +O 2(g) 2H 2 O (L) 的敘述, 下列何者正確? (A)ΔH 為正值 (B)1 atm 25 時, 此反應可以自然發生 (C) 生成物的熱含量總和較反應物的熱含量總和低 (D) 在 1 atm 100 時所放的熱量為標準反應熱 答案 :(C) 解析 :(A) 燃燒為放熱反應,ΔH 必為負值 (B) 燃燒需點火, 溫度達到燃點, 才能發生燃燒反應,
( )1. 關於氫氣的燃燒反應 :2H 2(g) +O 2(g) 2H 2 O (L) 的敘述, 下列何者正確? (A)ΔH 為正值 (B)1 atm 25 時, 此反應可以自然發生 (C) 生成物的熱含量總和較反應物的熱含量總和低 (D) 在 1 atm 100 時所放的熱量為標準反應熱 答案 :(C) 解析 :(A) 燃燒為放熱反應,ΔH 必為負值 (B) 燃燒需點火, 溫度達到燃點, 才能發生燃燒反應,
戒菸實務個案自助手冊105年Ver.2
 本計劃經費來自 品健康福利捐支應 衛生福利部國民健康署 我 名字 為了 以下理由 1. 2. 3. 4. 5. 決定從 年 月 日起 簽署人 (簽章) 見證人 (簽章) 年 月 日 a 準備戒 V 環境的準備 排除讓自己想吸 自己戒 的環境 V 心理的準備 瞭解自己的吸 的環境 建立能提醒 行為 強化戒 決心 V 身體的準備 評估身體的尼古丁依賴度 必要時找尋 藥物降低戒 戒 的難度
本計劃經費來自 品健康福利捐支應 衛生福利部國民健康署 我 名字 為了 以下理由 1. 2. 3. 4. 5. 決定從 年 月 日起 簽署人 (簽章) 見證人 (簽章) 年 月 日 a 準備戒 V 環境的準備 排除讓自己想吸 自己戒 的環境 V 心理的準備 瞭解自己的吸 的環境 建立能提醒 行為 強化戒 決心 V 身體的準備 評估身體的尼古丁依賴度 必要時找尋 藥物降低戒 戒 的難度
在餐點設計時, 往往會運用不同的質地做搭配, 以達到食用者口感的最佳平衡與變化
 百變的 廚房世界 廚藝與感官的饗宴 5 26 2014 2 494 在餐點設計時, 往往會運用不同的質地做搭配, 以達到食用者口感的最佳平衡與變化 2014 2 494 27 28 2014 2 494 食物的物理變化 5 廚房好比是一個食物實驗室, 運作時, 都在進行無數的物理與化學變化, 才能把樸實的原料食材轉為一道道令人驚嘆的美味 食物的化學變化 C 2014 2 494 29 62 65 廚房的魔術秀
百變的 廚房世界 廚藝與感官的饗宴 5 26 2014 2 494 在餐點設計時, 往往會運用不同的質地做搭配, 以達到食用者口感的最佳平衡與變化 2014 2 494 27 28 2014 2 494 食物的物理變化 5 廚房好比是一個食物實驗室, 運作時, 都在進行無數的物理與化學變化, 才能把樸實的原料食材轉為一道道令人驚嘆的美味 食物的化學變化 C 2014 2 494 29 62 65 廚房的魔術秀
2 part 01 浴室 浴室收納原則 要在浴室用的東西一定要收在浴室 從內容物只剩一點的洗滌劑容器開始整理 減少相同物品的數量 多的物品只要 1~2 個就夠了 每天要用的東西別放在浴室櫃子裡
 101 KANG SI 1010091 1. Home Economics. 康熹家政報報 101 KANG SI 第三期 24830 (02)2299-9006 (02)2299-9110 好書推薦 一天一點無壓力收納 : 600 萬網友推薦的實用整理聖經 本書簡介 600157 2 part 01 浴室 浴室收納原則 要在浴室用的東西一定要收在浴室 從內容物只剩一點的洗滌劑容器開始整理 減少相同物品的數量
101 KANG SI 1010091 1. Home Economics. 康熹家政報報 101 KANG SI 第三期 24830 (02)2299-9006 (02)2299-9110 好書推薦 一天一點無壓力收納 : 600 萬網友推薦的實用整理聖經 本書簡介 600157 2 part 01 浴室 浴室收納原則 要在浴室用的東西一定要收在浴室 從內容物只剩一點的洗滌劑容器開始整理 減少相同物品的數量
從道德主體的興發論孔子的文學批評理論
 19997 197-210 從道德主體的興發論孔子的文學批評理論 197 從道德主體的興發論孔子的文學批評理論一 問題與方法 1 ---- ---- 2 3 1 2 3 ---- 198 ---- ---- 4 二 內聖人格的形成與文學理想之建構 ( 一 ) 道德主體的確立 ( 仁 ) 與文學理想之根據 ( 質 ) 4 199 5 ---- 6 ( 二 ) 道德主體的落實 ( 禮 ) 與文學質素之要求
19997 197-210 從道德主體的興發論孔子的文學批評理論 197 從道德主體的興發論孔子的文學批評理論一 問題與方法 1 ---- ---- 2 3 1 2 3 ---- 198 ---- ---- 4 二 內聖人格的形成與文學理想之建構 ( 一 ) 道德主體的確立 ( 仁 ) 與文學理想之根據 ( 質 ) 4 199 5 ---- 6 ( 二 ) 道德主體的落實 ( 禮 ) 與文學質素之要求
1
 1 (1) (ideal gas erfect gas) (gas) (vaor) 3 () - (-), - (T-s) 0 1a a 4a 3a n k T S a 5b 3b n S T T S 1b 4a 1b 5a 1a b 3b 4b k 4b 5b 5a 3a b 0 (3) 1 T 4 (4) T, 1, T, T 1, 0 Q W U 1 T T, 1, ( 1) Q W U, 1,
1 (1) (ideal gas erfect gas) (gas) (vaor) 3 () - (-), - (T-s) 0 1a a 4a 3a n k T S a 5b 3b n S T T S 1b 4a 1b 5a 1a b 3b 4b k 4b 5b 5a 3a b 0 (3) 1 T 4 (4) T, 1, T, T 1, 0 Q W U 1 T T, 1, ( 1) Q W U, 1,
retrieve Molecular Biology of THE CELL 5 Thomas Südhof 從突變的酵母菌看出控制基因 DNA DNA Roger David Kornberg 謝克曼利用酵母菌突變株篩選出可調控細胞不同情況傳輸系統的多種基因, 這一發現為
 34 2014 6 498 2013 年諾貝爾生理醫學獎 揭開細胞傳輸系統的奧祕 2013 3 囊泡傳輸系統的重要性 60 vesicle traffic endocytosisexocytosis 細胞傳輸分子的關鍵 3 Randy Schekman James Rothman 細胞會依據執行不同的生物功能而製造出不同的分子, 這些分子都必須在正確的時間製造, 運輸到正確的位置或釋放到細胞外, 產生特定的生理效應
34 2014 6 498 2013 年諾貝爾生理醫學獎 揭開細胞傳輸系統的奧祕 2013 3 囊泡傳輸系統的重要性 60 vesicle traffic endocytosisexocytosis 細胞傳輸分子的關鍵 3 Randy Schekman James Rothman 細胞會依據執行不同的生物功能而製造出不同的分子, 這些分子都必須在正確的時間製造, 運輸到正確的位置或釋放到細胞外, 產生特定的生理效應
Microsoft PowerPoint - Chap. 9 Notes
 p. 1 熱力學與氣體動力學 Thermodynamics and Kinetic Theory of Gases 簡介 p. 2 熱力學 ( Thermodynamics ): 討論巨觀系統中的一些巨觀性質 ( 如體積, 壓力, 溫度 ) 巨觀系統間的互動 ( 如熱交換 ) 氣體動力學 ( Kinetic Theory of Gases ): 有些在此導出的觀念也一樣可以用於液體或固體當中 將巨觀性質與微觀的原子或分子運動關連在一起
p. 1 熱力學與氣體動力學 Thermodynamics and Kinetic Theory of Gases 簡介 p. 2 熱力學 ( Thermodynamics ): 討論巨觀系統中的一些巨觀性質 ( 如體積, 壓力, 溫度 ) 巨觀系統間的互動 ( 如熱交換 ) 氣體動力學 ( Kinetic Theory of Gases ): 有些在此導出的觀念也一樣可以用於液體或固體當中 將巨觀性質與微觀的原子或分子運動關連在一起
Microsoft Word - ok翁志文、張佳音...doc
 1 壹 研究動機 一般而言 傳統大三弦琴碼的擺放位置 圖 1 大約在琴鼓下方 由下往 上三分之一的地方 約 8.5 公分 但是這種擺法 學生在初學大三弦時 左手 常伴隨著指距較大 音準較難以掌握的困擾 為解決這個技巧上的問題 必須不 斷練習將手指指距撐開 並在琴桿上做記號來加以輔助 圖 1 傳統琴碼三分之一的擺放位置 8.5 公分 目前 北京中央音樂學院談龍建教授 採取將琴碼位置 往上移至 五度音
1 壹 研究動機 一般而言 傳統大三弦琴碼的擺放位置 圖 1 大約在琴鼓下方 由下往 上三分之一的地方 約 8.5 公分 但是這種擺法 學生在初學大三弦時 左手 常伴隨著指距較大 音準較難以掌握的困擾 為解決這個技巧上的問題 必須不 斷練習將手指指距撐開 並在琴桿上做記號來加以輔助 圖 1 傳統琴碼三分之一的擺放位置 8.5 公分 目前 北京中央音樂學院談龍建教授 採取將琴碼位置 往上移至 五度音
老人憂鬱症的認識與老人自殺問題
 18-24 25-44 45-64 65 10 8 6 4 2 0 ( 40% 15% Affect Cognition : drive Behavior DSM-V major depressive episode 2 9 5 Electronic Convulsion Therapy; ECT Rabins65 1% Rabins, 1992 20%-30% Blazer, 1994 65 12.9
18-24 25-44 45-64 65 10 8 6 4 2 0 ( 40% 15% Affect Cognition : drive Behavior DSM-V major depressive episode 2 9 5 Electronic Convulsion Therapy; ECT Rabins65 1% Rabins, 1992 20%-30% Blazer, 1994 65 12.9
 2 3 13 17 22 26 1 2 8 100738 +86 (10) 8508 5000 +86 (10) 8518 5111 www.kpmg.com.cn 2006 4 2002 2006 1 28% 2006 17 8 500 2006 2006 2006 7 2.5 2 1 500 500 40% 500 10 16 14 12 10 8 6 4 2 2002-2006 5.1 5.9
2 3 13 17 22 26 1 2 8 100738 +86 (10) 8508 5000 +86 (10) 8518 5111 www.kpmg.com.cn 2006 4 2002 2006 1 28% 2006 17 8 500 2006 2006 2006 7 2.5 2 1 500 500 40% 500 10 16 14 12 10 8 6 4 2 2002-2006 5.1 5.9
ZT0102_Cb-00封面
 50Hz Your Peace of Mind is Our Top Priority Qwik Jon Ulitma Drain Pump 202 132, 133... 3 Qwik Jon 103... 7... 13... 17 1 : 2012 Zoeller Qwik Jon Ulitma 202 ----- 6 7 3 9.6 m /hr Qwik Jon 103 270 271 117
50Hz Your Peace of Mind is Our Top Priority Qwik Jon Ulitma Drain Pump 202 132, 133... 3 Qwik Jon 103... 7... 13... 17 1 : 2012 Zoeller Qwik Jon Ulitma 202 ----- 6 7 3 9.6 m /hr Qwik Jon 103 270 271 117
目次 CONTENTS 2 1 乘法公式與多項式 二次方根與畢氏定理 因式分解 一元二次方程式
 給同學的話 1 2 3 4 目次 CONTENTS 2 1 乘法公式與多項式 1-1 3 1-2 7 1-3 11 1 16 2 二次方根與畢氏定理 2-1 20 2-2 24 2-3 29 2 33 3 因式分解 3-1 37 3-2 41 3-3 45 3 49 4 一元二次方程式 4-1 53 4-2 57 4-3 61 4 65 3 1-1 乘法公式 本節性質與公式摘要 1 分配律 : ddd
給同學的話 1 2 3 4 目次 CONTENTS 2 1 乘法公式與多項式 1-1 3 1-2 7 1-3 11 1 16 2 二次方根與畢氏定理 2-1 20 2-2 24 2-3 29 2 33 3 因式分解 3-1 37 3-2 41 3-3 45 3 49 4 一元二次方程式 4-1 53 4-2 57 4-3 61 4 65 3 1-1 乘法公式 本節性質與公式摘要 1 分配律 : ddd
Microsoft Word - ACI chapter00-1ed.docx
 前言 Excel Excel - v - 財務管理與投資分析 -Excel 建模活用範例集 5 相關 平衡 敏感 - vi - 前言 模擬 If-Then 規劃 ERP BI - vii - 財務管理與投資分析 -Excel 建模活用範例集 ERP + BI + ERP BI Excel 88 Excel 1. Excel Excel 2. Excel 3. Excel - viii - 前言 1.
前言 Excel Excel - v - 財務管理與投資分析 -Excel 建模活用範例集 5 相關 平衡 敏感 - vi - 前言 模擬 If-Then 規劃 ERP BI - vii - 財務管理與投資分析 -Excel 建模活用範例集 ERP + BI + ERP BI Excel 88 Excel 1. Excel Excel 2. Excel 3. Excel - viii - 前言 1.
目次 3 ONTNTS 1 相似形 上 國民中學數學第五冊習作 表示為仿會考或特招題 1-1 比例線段 3 1- 相似多邊形 相似三角形的應用 圓形 -1 點 線 圓 4 - 圓心角 圓周角與弦切角 外心 內心與重心 3-1 推理證明 三角形與多
 給同學的話 1.. 內 3. 內 內 目次 3 ONTNTS 1 相似形 上 國民中學數學第五冊習作 表示為仿會考或特招題 1-1 比例線段 3 1- 相似多邊形 8 1-3 相似三角形的應用 13 1 18 圓形 -1 點 線 圓 4 - 圓心角 圓周角與弦切角 9 34 3 外心 內心與重心 3-1 推理證明 40 3- 三角形與多邊形的心 45 3 51 3 1-1 比例線段 本節性質與公式摘要
給同學的話 1.. 內 3. 內 內 目次 3 ONTNTS 1 相似形 上 國民中學數學第五冊習作 表示為仿會考或特招題 1-1 比例線段 3 1- 相似多邊形 8 1-3 相似三角形的應用 13 1 18 圓形 -1 點 線 圓 4 - 圓心角 圓周角與弦切角 9 34 3 外心 內心與重心 3-1 推理證明 40 3- 三角形與多邊形的心 45 3 51 3 1-1 比例線段 本節性質與公式摘要
當無人飛行器越做越小時, 拍翅型的飛行方式應該是人類要參考及學習的 MAV P V 2 b P V b 0.96 P V 2 b L b 4 L b 4 W b 3 W b 3 2 向自然學習 MAV 3 升力與推力共生的拍翅運動 拍翅頻率的尺度變化
 54 204 0 502 仿生飛行 從人類飛行器談起 unmanned aerial vehicle, UAV UAV micro aerial vehicle, MAV 5 cm 0.5 0 log 0.5 (P V 2 ).5 2.5 2 log (b) P V 2 b b 希望製作一架微型飛機像鳥類或蝴蝶那麼小, 就得向會飛的動物學習飛行技巧了 當無人飛行器越做越小時, 拍翅型的飛行方式應該是人類要參考及學習的
54 204 0 502 仿生飛行 從人類飛行器談起 unmanned aerial vehicle, UAV UAV micro aerial vehicle, MAV 5 cm 0.5 0 log 0.5 (P V 2 ).5 2.5 2 log (b) P V 2 b b 希望製作一架微型飛機像鳥類或蝴蝶那麼小, 就得向會飛的動物學習飛行技巧了 當無人飛行器越做越小時, 拍翅型的飛行方式應該是人類要參考及學習的
3-3 蒸氣壓 103 飽和蒸氣壓之計算 nc 時 ca B 兩種液體之蒸氣壓分別為 48.0 及 80.0 mmhgc 今於一內容積為 10 升之密閉容器中 c 充入 0.02 莫耳 A 氣體及 0.05 莫耳 B 氣體 c 溫度仍維持 27 ncc 當物系達平衡時 c 容器內氣體之
 102 互動式教學講義 選修化學 ( 上 ) 3-3 蒸氣壓 一 液體的蒸氣壓 ( 配合翰版課本 P.100 ~ P.102) 1 c c c. 1 吸熱 c. 2 c 放熱. 2 1 c c c c. c. 課 P.100 2 備 P.185 1 c 一定 c 無關. 2 溫度升高時 c 液體分子的平均動能增加 c 造成液體的飽和蒸氣壓也漸增. 3 沸點較高的液體 c 分子間的引力較大 c 在同
102 互動式教學講義 選修化學 ( 上 ) 3-3 蒸氣壓 一 液體的蒸氣壓 ( 配合翰版課本 P.100 ~ P.102) 1 c c c. 1 吸熱 c. 2 c 放熱. 2 1 c c c c. c. 課 P.100 2 備 P.185 1 c 一定 c 無關. 2 溫度升高時 c 液體分子的平均動能增加 c 造成液體的飽和蒸氣壓也漸增. 3 沸點較高的液體 c 分子間的引力較大 c 在同
Microsoft Word - _m30.doc
 1 2 3 4 5 6 7 8 公式 2 4 2 1 能 整除 因此後玩 者贏 且關鍵數 字為3 的倍數 3 0 3 1 不能整除 所 以先拿餘數 2 關鍵數字是 4的倍 數 2 先玩者贏 4 0 4 1 能整除 因此 後玩者贏 且 關鍵數字為 5 的倍數 5 0 5 1 不能整除 所 以先拿餘數 2 關鍵 數字是 6的倍 數 2 先玩者贏 7 0 6 1 能整除 因此 後玩者贏 且 關鍵數字為7
1 2 3 4 5 6 7 8 公式 2 4 2 1 能 整除 因此後玩 者贏 且關鍵數 字為3 的倍數 3 0 3 1 不能整除 所 以先拿餘數 2 關鍵數字是 4的倍 數 2 先玩者贏 4 0 4 1 能整除 因此 後玩者贏 且 關鍵數字為 5 的倍數 5 0 5 1 不能整除 所 以先拿餘數 2 關鍵 數字是 6的倍 數 2 先玩者贏 7 0 6 1 能整除 因此 後玩者贏 且 關鍵數字為7
01.dvi
 物理資優營微積分教材 1 y = f ( ) (, f ( ) ) 點的切線斜率 : =lim f ( + ) f () 若 f () = n,n 為自然數 =lim ( + ) n n 微分的基本性質 : (i) 線性 : 若 a, b 是常數 (ii) 萊布尼茲律 : n n 1 + O ( ) = n n 1 {af ()+bg ()} = a + bg {f () g ()} = g + f
物理資優營微積分教材 1 y = f ( ) (, f ( ) ) 點的切線斜率 : =lim f ( + ) f () 若 f () = n,n 為自然數 =lim ( + ) n n 微分的基本性質 : (i) 線性 : 若 a, b 是常數 (ii) 萊布尼茲律 : n n 1 + O ( ) = n n 1 {af ()+bg ()} = a + bg {f () g ()} = g + f
Microsoft PowerPoint - Temperature and the Kinetic Theory of Gases.ppt [相容模式]
![Microsoft PowerPoint - Temperature and the Kinetic Theory of Gases.ppt [相容模式] Microsoft PowerPoint - Temperature and the Kinetic Theory of Gases.ppt [相容模式]](/thumbs/86/94232382.jpg) Temperature & the Kinetic Theory of Gases 溫度與氣體動力理論 Temperature & Heat 溫度 熱 高溫 energy 能量 低溫 Heat 是一種可藉由 temperature 差異傳輸的 energy: 若無溫度差, 就沒有 heat 傳遞 The Zeroth Law of Thermodynamics 熱力學第零定律 無法以其他原理證明,
Temperature & the Kinetic Theory of Gases 溫度與氣體動力理論 Temperature & Heat 溫度 熱 高溫 energy 能量 低溫 Heat 是一種可藉由 temperature 差異傳輸的 energy: 若無溫度差, 就沒有 heat 傳遞 The Zeroth Law of Thermodynamics 熱力學第零定律 無法以其他原理證明,
1
 P.1 WWF - Hong Kong 第二部分 1.利用世界自然基金會所提供的網上碳足印計算器 讓學生計算個人的二氧化碳排放量 2.碳足印計算器 www.climateers.org/chi/contents/climateer_calculator.php 3.教師更可利用碳足印的報告與學生分析二氧化碳的不同來源及相關的減碳行動 總結 紓緩氣候變化的個人行動 第一步就是先認識個人生活對環境的影響
P.1 WWF - Hong Kong 第二部分 1.利用世界自然基金會所提供的網上碳足印計算器 讓學生計算個人的二氧化碳排放量 2.碳足印計算器 www.climateers.org/chi/contents/climateer_calculator.php 3.教師更可利用碳足印的報告與學生分析二氧化碳的不同來源及相關的減碳行動 總結 紓緩氣候變化的個人行動 第一步就是先認識個人生活對環境的影響
<4D F736F F D A455B4C131B0AAA447A15DA6DBB54DB2D5A15EA4C6BEC72E646F63>
 國立臺中一中 102 學年度第二學期第一次期中考二年級 ( 自然組 ) 化學科試題科目代碼 :05 一 單選題 :1~23 題, 每題 2 分, 共 46 分, 不倒扣 1. 下圖為三種氣體在定溫下的粒子數目對粒子分布速率的分布曲線 試問圖中, 甲 乙及丙三曲線依序代表何種氣體較為合理?(H=1,He =4,C=12,N=14,O=16) (A) 氧 水蒸氣 氦 (B) 二氧化碳 氮 一氧化氮 (C)
國立臺中一中 102 學年度第二學期第一次期中考二年級 ( 自然組 ) 化學科試題科目代碼 :05 一 單選題 :1~23 題, 每題 2 分, 共 46 分, 不倒扣 1. 下圖為三種氣體在定溫下的粒子數目對粒子分布速率的分布曲線 試問圖中, 甲 乙及丙三曲線依序代表何種氣體較為合理?(H=1,He =4,C=12,N=14,O=16) (A) 氧 水蒸氣 氦 (B) 二氧化碳 氮 一氧化氮 (C)
 99 1 20045377 45 Wocester Galileo Galilei Heinrich Schwabe 11 46 20045377 Motorola http://sohowww.nascom.nasa.gov/data/summary/gif/031030/smdi_igram_fd_20031030_0800.gif SOHO 47 20045377 150 Cuno HoffmeisterLudwig
99 1 20045377 45 Wocester Galileo Galilei Heinrich Schwabe 11 46 20045377 Motorola http://sohowww.nascom.nasa.gov/data/summary/gif/031030/smdi_igram_fd_20031030_0800.gif SOHO 47 20045377 150 Cuno HoffmeisterLudwig
實驗: 水的膨脹和收縮 錐形瓶中裝滿 20 的水, 並使上端細管水面高出瓶塞 2cm,: (1) 玻璃管內滴入紅墨水目的在 (2) 插玻璃管目的在增加, 管口徑愈小, 水位升降愈, 靈敏度愈 (3) 錐形瓶放入沸水中, 則 先受熱體積膨脹, 水位會, 隨後瓶內的水受熱, 體積膨脹, 但液體的體積膨脹
 ( 一 ) 溫度 : A 熱水溫度較高, 冷水溫度較低, 但此種僅屬於 定性 的敘述 B 溫度: 物體 冷熱 的程度, 稱為溫度 例 :60 的熱水 或 10 的冷水, 皆為 定量 的敘述 C 溫度測量: 溫度改變時, 物質某些性質跟隨改變, 利用此性質改變的特性, 測量溫度的高低 (1) 利用液體 ( 如水銀 酒精 ) 體積 受熱膨脹, 測量溫度 (2) 利用氣體 體積 受熱膨脹, 測量溫度 (3)
( 一 ) 溫度 : A 熱水溫度較高, 冷水溫度較低, 但此種僅屬於 定性 的敘述 B 溫度: 物體 冷熱 的程度, 稱為溫度 例 :60 的熱水 或 10 的冷水, 皆為 定量 的敘述 C 溫度測量: 溫度改變時, 物質某些性質跟隨改變, 利用此性質改變的特性, 測量溫度的高低 (1) 利用液體 ( 如水銀 酒精 ) 體積 受熱膨脹, 測量溫度 (2) 利用氣體 體積 受熱膨脹, 測量溫度 (3)
Hz 1 k ,186 Hz k 4 k 8 k 2 k
 樂音或噪音! 頻率與音高 6 215 2 56 44 16 25, Hz 2 2 K Hz 27.5 4,186 Hz 2196.16 47 13289.75 9397.27 77 8372.2 5587.65 4186.1 3729.31 44. 261.63 41.2 32.7 27.5 18.35 16.35 2 25 5 Hz 1 k 27.5 4,186 Hz 63 125 2 k 4 k
樂音或噪音! 頻率與音高 6 215 2 56 44 16 25, Hz 2 2 K Hz 27.5 4,186 Hz 2196.16 47 13289.75 9397.27 77 8372.2 5587.65 4186.1 3729.31 44. 261.63 41.2 32.7 27.5 18.35 16.35 2 25 5 Hz 1 k 27.5 4,186 Hz 63 125 2 k 4 k
6-1-1極限的概念
 選 修 數 學 (I-4 多 項 式 函 數 的 極 限 與 導 數 - 導 數 與 切 線 斜 率 定 義. f ( 在 的 導 數 : f ( h 對 實 函 數 f ( 若 極 限 存 在 h h 則 稱 f ( 在 點 可 微 分 而 此 極 限 值 稱 為 f ( 在 的 導 數 以 f ( 表 示 f ( f ( 函 數 f ( 在 的 導 數 也 可 以 表 成 f ( 註 : 為 了
選 修 數 學 (I-4 多 項 式 函 數 的 極 限 與 導 數 - 導 數 與 切 線 斜 率 定 義. f ( 在 的 導 數 : f ( h 對 實 函 數 f ( 若 極 限 存 在 h h 則 稱 f ( 在 點 可 微 分 而 此 極 限 值 稱 為 f ( 在 的 導 數 以 f ( 表 示 f ( f ( 函 數 f ( 在 的 導 數 也 可 以 表 成 f ( 註 : 為 了
 46 2011 11 467 數位遊戲式學習系統 7 2011 11 467 47 3 DBGameSys 48 2011 11 467 正規化資料模組 如何配置並儲存電子化資料 以 便減少資料被重覆儲存的程序 DBGameSys的主要功能模組包 學習者 審核評分模組 含 正規化資料模組 審核評分 模組 高分列表模組3大區塊 系統資料庫 在正規化資料模組的執行 高分列表模組 過程中 先要求學習者瀏覽遊戲
46 2011 11 467 數位遊戲式學習系統 7 2011 11 467 47 3 DBGameSys 48 2011 11 467 正規化資料模組 如何配置並儲存電子化資料 以 便減少資料被重覆儲存的程序 DBGameSys的主要功能模組包 學習者 審核評分模組 含 正規化資料模組 審核評分 模組 高分列表模組3大區塊 系統資料庫 在正規化資料模組的執行 高分列表模組 過程中 先要求學習者瀏覽遊戲
1
 1 2 3 4 5 6 1 2 3 4 5 6 7 8 9 10 11 12 13 14 7 8 15 9 10 11 12 13 16 14 17 18 19 20 21 22 15 23 2.3 不同的分析角度 以上種種對影響健康因素的分析 其實來自不同的學說和理論 它們從不同角度分析 健康 建立對健康及影響健康因素的不同理解 這些角度包括 1 生物 2 社 會 3 心理 4 靈性 5 生態及
1 2 3 4 5 6 1 2 3 4 5 6 7 8 9 10 11 12 13 14 7 8 15 9 10 11 12 13 16 14 17 18 19 20 21 22 15 23 2.3 不同的分析角度 以上種種對影響健康因素的分析 其實來自不同的學說和理論 它們從不同角度分析 健康 建立對健康及影響健康因素的不同理解 這些角度包括 1 生物 2 社 會 3 心理 4 靈性 5 生態及
投影片 1
 計算機程式及實習 期末報告 題目 : 六宿炒翻天 班級 : 奈米一乙姓名 : 陳洋翼學號 :4A514050 老師 : 謝慶存 程式說明 設計結帳系統, 選擇數量後, 在按下計算, 將會顯示總金額 若是老人或小孩, 將可享 8 折或 9 折的優惠 程式畫面 填選數量 在火腿蛋炒飯的數量選擇 1, 並按下計算, 可得總金額 50 元 程式畫面 打折 填選完後, 若客人是小孩或老人, 選擇欲打折項目,
計算機程式及實習 期末報告 題目 : 六宿炒翻天 班級 : 奈米一乙姓名 : 陳洋翼學號 :4A514050 老師 : 謝慶存 程式說明 設計結帳系統, 選擇數量後, 在按下計算, 將會顯示總金額 若是老人或小孩, 將可享 8 折或 9 折的優惠 程式畫面 填選數量 在火腿蛋炒飯的數量選擇 1, 並按下計算, 可得總金額 50 元 程式畫面 打折 填選完後, 若客人是小孩或老人, 選擇欲打折項目,
Microsoft PowerPoint - CH 05-氣體
 第五章氣體 楊啟榮博士 教授 國立 Department of Mechatronic Technology National Taiwan Normal University Tel: 02-7734-3506; 0955-052-392 E-mail: ycr@ntnu.edu.tw 本章大綱 5.1 氣體物質 5.2 氣體壓力 SI 制壓力單位 大氣壓力 例題 5.1 5.3 氣體定律 壓力
第五章氣體 楊啟榮博士 教授 國立 Department of Mechatronic Technology National Taiwan Normal University Tel: 02-7734-3506; 0955-052-392 E-mail: ycr@ntnu.edu.tw 本章大綱 5.1 氣體物質 5.2 氣體壓力 SI 制壓力單位 大氣壓力 例題 5.1 5.3 氣體定律 壓力
POINT 1 配合不同症狀或目的, 有效地攝取最需要的五種營養素! POINT 不須進行複雜的營養計算和熱量計算工作! 第一類穀類 第二類肉 魚 蛋 乳製品 第三類蔬菜 海藻 水果
 須崎動物醫院院長 須崎恭彥 著 高慧芳 譯 POINT 1 配合不同症狀或目的, 有效地攝取最需要的五種營養素! POINT 不須進行複雜的營養計算和熱量計算工作! 第一類穀類 第二類肉 魚 蛋 乳製品 第三類蔬菜 海藻 水果 五大有效營養素 BEST1 BEST BEST3 BEST4 BEST5 6 - BEST1 BEST BEST3 BEST4 BEST5 1 6 6 1-1 1 1 1 1
須崎動物醫院院長 須崎恭彥 著 高慧芳 譯 POINT 1 配合不同症狀或目的, 有效地攝取最需要的五種營養素! POINT 不須進行複雜的營養計算和熱量計算工作! 第一類穀類 第二類肉 魚 蛋 乳製品 第三類蔬菜 海藻 水果 五大有效營養素 BEST1 BEST BEST3 BEST4 BEST5 6 - BEST1 BEST BEST3 BEST4 BEST5 1 6 6 1-1 1 1 1 1
 第一篇文概說第七章公文的用語及標點符號公本篇內容 第一章 緒論 第二章 公文的意義 第三章 公文與高 普 特各類考試 第四章 公文程式之意義及演變 第五章 公文之分類及其行文系統 第六章 公文之結構與行款 第一篇 第一章緒論 003 第一章緒論 等 等 004 最新應用公文 第一篇 第二章公文的意義 005 第二章公文的意義 第一節 一 須為公務員製作之文書 二 須為公務員 職務上 製作之文書 006
第一篇文概說第七章公文的用語及標點符號公本篇內容 第一章 緒論 第二章 公文的意義 第三章 公文與高 普 特各類考試 第四章 公文程式之意義及演變 第五章 公文之分類及其行文系統 第六章 公文之結構與行款 第一篇 第一章緒論 003 第一章緒論 等 等 004 最新應用公文 第一篇 第二章公文的意義 005 第二章公文的意義 第一節 一 須為公務員製作之文書 二 須為公務員 職務上 製作之文書 006
生與死的尊嚴 生與死的尊嚴
 生與死的尊嚴 目錄 生與死的尊嚴 2 認識生命的實相 3 生從何處來? 死往何處去? 8 佛教徒的生死觀 10 如何面對死亡? 如何使得死亡有尊嚴? 20 生與死的尊嚴 生與死的尊嚴 認識生命的實相 認識生命的實相 ( 一 ) 由生命的無奈 無所依賴及無所適從, 轉變為生命的可愛 可貴與自我的肯定 ( 二 ) 生命的出生與死亡, 關係密切, 不可分割 出生之時已確定了死亡的必然到臨 生未必可喜, 死未必可哀,
生與死的尊嚴 目錄 生與死的尊嚴 2 認識生命的實相 3 生從何處來? 死往何處去? 8 佛教徒的生死觀 10 如何面對死亡? 如何使得死亡有尊嚴? 20 生與死的尊嚴 生與死的尊嚴 認識生命的實相 認識生命的實相 ( 一 ) 由生命的無奈 無所依賴及無所適從, 轉變為生命的可愛 可貴與自我的肯定 ( 二 ) 生命的出生與死亡, 關係密切, 不可分割 出生之時已確定了死亡的必然到臨 生未必可喜, 死未必可哀,
( )1. 已知 H 2 O (l) H 2(g) O 2(g) ΔH=285 kj C (s) +O 2(g) CO 2(g) ΔH=-394 kj C (s) +2H 2(g) CH 4(g) ΔH=-76 kj 則甲烷 (CH 4 ) 的莫耳燃燒熱為多少 kj? (A) 888 (
 ( )1. 已知 H 2 O (l) H 2(g) + 1 2 O 2(g) ΔH=285 kj C (s) +O 2(g) CO 2(g) ΔH=-394 kj C (s) +2H 2(g) CH 4(g) ΔH=-76 kj 則甲烷 (CH 4 ) 的莫耳燃燒熱為多少 kj? (A) 888 (B) 750 (C)-750 (D)-888 kj 答案 :(D) 解析 :H 2 O (L) H 2(g)
( )1. 已知 H 2 O (l) H 2(g) + 1 2 O 2(g) ΔH=285 kj C (s) +O 2(g) CO 2(g) ΔH=-394 kj C (s) +2H 2(g) CH 4(g) ΔH=-76 kj 則甲烷 (CH 4 ) 的莫耳燃燒熱為多少 kj? (A) 888 (B) 750 (C)-750 (D)-888 kj 答案 :(D) 解析 :H 2 O (L) H 2(g)
840 提示 Excel - Excel -- Excel (=) Excel ch0.xlsx H5 =D5+E5+F5+G5 (=) = - Excel 00
 Excel - - Excel - -4-5 840 提示 Excel - Excel -- Excel (=) Excel ch0.xlsx H5 =D5+E5+F5+G5 (=) = - Excel 00 ( 0 ) 智慧標籤 相關說明提示 -5 -- Excel 4 5 6 7 8 + - * / % ^ = < >= & 9 0 (:) (,) ( ) Chapter - :,
Excel - - Excel - -4-5 840 提示 Excel - Excel -- Excel (=) Excel ch0.xlsx H5 =D5+E5+F5+G5 (=) = - Excel 00 ( 0 ) 智慧標籤 相關說明提示 -5 -- Excel 4 5 6 7 8 + - * / % ^ = < >= & 9 0 (:) (,) ( ) Chapter - :,
Microsoft PowerPoint pptx
 Chapter 8 hermodynamics: he Second and hird Law 8-1 Entropy Which is Spontaneous Change? 在室溫下 298K he Second Law of hermodynamics No process is possible in which the sole result is the absorption of heat
Chapter 8 hermodynamics: he Second and hird Law 8-1 Entropy Which is Spontaneous Change? 在室溫下 298K he Second Law of hermodynamics No process is possible in which the sole result is the absorption of heat
X 傳統育種技術 分子育種技術 基因改良育種
 06 2015 7 511 72 92? 2010? X 傳統育種技術 1960 1980 30 60 20 分子育種技術 5 10 3 5 基因改良育種 2015 7 511 07 改良後的基因及其生產的蛋白質都需經過嚴格的動物及田間生物安全試驗才會上市, 程序就跟新藥一樣 20 基改產品禁得起考驗 12 2013 1.75 50 1 5 1996 80 2013 156 35 21 6 90 08
06 2015 7 511 72 92? 2010? X 傳統育種技術 1960 1980 30 60 20 分子育種技術 5 10 3 5 基因改良育種 2015 7 511 07 改良後的基因及其生產的蛋白質都需經過嚴格的動物及田間生物安全試驗才會上市, 程序就跟新藥一樣 20 基改產品禁得起考驗 12 2013 1.75 50 1 5 1996 80 2013 156 35 21 6 90 08
2 (Diffraction) 400nm 700nm Young
 990026 Physics 248 30 (02)2299-9006 (02)2299-9110 99 4 2000 Wave 2 (Diffraction) 400nm 700nm Young 2008 8 16 3 mm 4 LED 5 注意 : 噴灑過硫酸銅水溶液的酒精燈一定要清洗乾淨, 否則沒有燃燒到的銅離子附著在酒精燈外, 必定會使酒精燈的金屬外殼逐漸氧化 LED 6 7 8 CQ 提示
990026 Physics 248 30 (02)2299-9006 (02)2299-9110 99 4 2000 Wave 2 (Diffraction) 400nm 700nm Young 2008 8 16 3 mm 4 LED 5 注意 : 噴灑過硫酸銅水溶液的酒精燈一定要清洗乾淨, 否則沒有燃燒到的銅離子附著在酒精燈外, 必定會使酒精燈的金屬外殼逐漸氧化 LED 6 7 8 CQ 提示
CO 2 以鄰為壑的台灣建築產業
 6 20114460台灣綠建築政策的成就 台灣的建築產業消耗了大量的水泥, 也排放了很多的營建廢棄物, 建築物的壽命卻嚴重偏低 建築的環保時代已來臨 1992 199212United Nations Commission on Sustainable Development, UNCSD1998 1996 CO 2 以鄰為壑的台灣建築產業 27.22 34 1 6 20114460 7 8 201144604
6 20114460台灣綠建築政策的成就 台灣的建築產業消耗了大量的水泥, 也排放了很多的營建廢棄物, 建築物的壽命卻嚴重偏低 建築的環保時代已來臨 1992 199212United Nations Commission on Sustainable Development, UNCSD1998 1996 CO 2 以鄰為壑的台灣建築產業 27.22 34 1 6 20114460 7 8 201144604
 40/60 AM Cardio 40/60 ... 4 Cardio 40/60... 4... 5... 5 :... 5... 5... 6 : Cardio 40/60... 6 / (Cardio 40)... 6 / (Cardio 60)... 6 :... 6 : GPS... 7 : Brytonsport.com... 8... 9 :... 9 GPS... 10... 11
40/60 AM Cardio 40/60 ... 4 Cardio 40/60... 4... 5... 5 :... 5... 5... 6 : Cardio 40/60... 6 / (Cardio 40)... 6 / (Cardio 60)... 6 :... 6 : GPS... 7 : Brytonsport.com... 8... 9 :... 9 GPS... 10... 11
....V....VII.... VIII
 ....V....VII.... VIII................................. 002... 002... 004... 006... 012... 014... 019.... 022.... 023................................. 026... 026... 027... 039 XIII...043... 043... 045....
....V....VII.... VIII................................. 002... 002... 004... 006... 012... 014... 019.... 022.... 023................................. 026... 026... 027... 039 XIII...043... 043... 045....
Microsoft Word - CoordinatesTransform.doc
 Cateian Cylindial ˆ= xˆ o + yˆin ˆ = ˆ = xˆin+ yˆ o + = Cylindial to Cateian: ˆ ˆ x o in 0 y in o 0 = 0 0 Cateian to Cylindial: + = + xˆ yˆ o in 0 x = in o 0 y 0 0 Cylindial Spheial ˆ = ˆ + ˆ = ˆ = xˆ
Cateian Cylindial ˆ= xˆ o + yˆin ˆ = ˆ = xˆin+ yˆ o + = Cylindial to Cateian: ˆ ˆ x o in 0 y in o 0 = 0 0 Cateian to Cylindial: + = + xˆ yˆ o in 0 x = in o 0 y 0 0 Cylindial Spheial ˆ = ˆ + ˆ = ˆ = xˆ
1,000 kb 100 六方體鑽石形成 Km ,000 1,500 2, Kb 5 1, Kb a 0 a 0 = nm 4 : Steve Sque, com/ :
 54 2014 1 493 天然鑽石的誕生 3,500 10 2012 9 10 2 Popigaikimberlite 1960 鑽石的真面目及變形 1915 W.H. Bragg W.L. Bragg X unit cell 18 8 8 6 6 4 1,000 kb 100 六方體鑽石形成 200 150 Km 50 10 1 0 500 1,000 1,500 2,000 4 50 Kb 5
54 2014 1 493 天然鑽石的誕生 3,500 10 2012 9 10 2 Popigaikimberlite 1960 鑽石的真面目及變形 1915 W.H. Bragg W.L. Bragg X unit cell 18 8 8 6 6 4 1,000 kb 100 六方體鑽石形成 200 150 Km 50 10 1 0 500 1,000 1,500 2,000 4 50 Kb 5
Wire Wound Ceramic Chip Inductor 繞線式陶瓷晶片大电流電感 HPWS Series for High Frequency HPWS 系列適用於高頻 INTRODUCTION 產品介紹 The HPWS is the chip inductors of a wire w
 INTRODUCTION 產品介紹 The HPWS is the chip inductors of a wire wound type widely used in the communication applications, such as cellular phones, television tuners, radios, and other electronic devices. The
INTRODUCTION 產品介紹 The HPWS is the chip inductors of a wire wound type widely used in the communication applications, such as cellular phones, television tuners, radios, and other electronic devices. The
縣 94 學年度 上 學期 區 國民中學 Q 年級 R 領域教學計畫表 設計者:
 高雄市立茄萣國中國中 103 學年度第一學期八年級 英文補救教學彈性學習課程計畫表 一 教材來源 : 二 教學節數 : 每週 (1) 節, 學期共 ( 20 ) 節 三 各單元內涵分析 : 週次 第一週 第二週 第三週 第四週 9/1 9/5 9/8 9/12 9/15 9/19 9/22 9/26 Lesson1 ( 一 ) Lesson1 ( 一 ) Lesson2 ( 二 ) Lesson2
高雄市立茄萣國中國中 103 學年度第一學期八年級 英文補救教學彈性學習課程計畫表 一 教材來源 : 二 教學節數 : 每週 (1) 節, 學期共 ( 20 ) 節 三 各單元內涵分析 : 週次 第一週 第二週 第三週 第四週 9/1 9/5 9/8 9/12 9/15 9/19 9/22 9/26 Lesson1 ( 一 ) Lesson1 ( 一 ) Lesson2 ( 二 ) Lesson2
Microsoft PowerPoint - senior2-2 [相容模式]
![Microsoft PowerPoint - senior2-2 [相容模式] Microsoft PowerPoint - senior2-2 [相容模式]](/thumbs/96/129696069.jpg) Chapter2 氣體的性質 2-1 影響氣體狀態的因素 2-2 氣體體積和壓力的關係 2-3 氣體體積溫度的關係 2-4 理想氣體 2-5 混和氣體的壓力 2-6 氣體的擴散 氣體性質 氣體是由不斷在運動的分子所組成 任一氣體通入任何容器中, 則迅速擴散而充滿此容器, 稱為氣體的擴散性 氣體無一定的形狀 也無一定的體積 氣體分子間的距離很大, 可被壓縮 亦可以加入其他氣體, 稱為氣體的壓縮性及可加入性
Chapter2 氣體的性質 2-1 影響氣體狀態的因素 2-2 氣體體積和壓力的關係 2-3 氣體體積溫度的關係 2-4 理想氣體 2-5 混和氣體的壓力 2-6 氣體的擴散 氣體性質 氣體是由不斷在運動的分子所組成 任一氣體通入任何容器中, 則迅速擴散而充滿此容器, 稱為氣體的擴散性 氣體無一定的形狀 也無一定的體積 氣體分子間的距離很大, 可被壓縮 亦可以加入其他氣體, 稱為氣體的壓縮性及可加入性
untitled
 1 2.1 ΔP r n n r ΔV ΔS ΔF r V s r f lim ΔV 0 r ΔF ρδv m/s 2 2 2 ΔP r n n r ΔV ΔS ΔF r V s r n lim Δ S 0 r ΔP ΔS n Pa 3 lim ΔS 0 r ΔP ΔS B ΔS ΔP r s 4 2 r f 1 ρ δ δδ 6 δ n δ O δ B 1 δδ 2 1 δδ 2 A 5 3 1
1 2.1 ΔP r n n r ΔV ΔS ΔF r V s r f lim ΔV 0 r ΔF ρδv m/s 2 2 2 ΔP r n n r ΔV ΔS ΔF r V s r n lim Δ S 0 r ΔP ΔS n Pa 3 lim ΔS 0 r ΔP ΔS B ΔS ΔP r s 4 2 r f 1 ρ δ δδ 6 δ n δ O δ B 1 δδ 2 1 δδ 2 A 5 3 1
1 500 表 1: 各國平均分數
 2012 年多益測驗全球考生資料統計報告 A < 1> 2012 B < 2> 100% 500 2012 2012 / 21 25 (38%) 57% (58%) 25% / 20% 35% 53% 31% 17% / 31% 12% 6 45 1-10% 81% 6 2012 48 3 30% 1 編註 1: 請見 P.15 編註 2: 請見 P.17 1 500 表 1: 各國平均分數 466
2012 年多益測驗全球考生資料統計報告 A < 1> 2012 B < 2> 100% 500 2012 2012 / 21 25 (38%) 57% (58%) 25% / 20% 35% 53% 31% 17% / 31% 12% 6 45 1-10% 81% 6 2012 48 3 30% 1 編註 1: 請見 P.15 編註 2: 請見 P.17 1 500 表 1: 各國平均分數 466
RMF Shape/ 外觀 : Tubular Photo Fiber Photo Area Ultrasonic s Model / 型號 RMF-DU10 RMF-DU40 RMF-DU10 K RMF-DU40 K RMF-DU10 K1 RMF-DU40 K1 Diffuse reflect
 Shape/ 外觀 : Tubular Photo RMF Model / 型號 RMF-10KP2 RMF-10KP2K RMF-DU30KP2 RMF-DU30KP2K Through beam / 對照式 Diffuse reflection / 擴散反射式 10M 30 cm Infrared LED 850 nm Infrared LED 875 nm 45 ma Max./Each side
Shape/ 外觀 : Tubular Photo RMF Model / 型號 RMF-10KP2 RMF-10KP2K RMF-DU30KP2 RMF-DU30KP2K Through beam / 對照式 Diffuse reflection / 擴散反射式 10M 30 cm Infrared LED 850 nm Infrared LED 875 nm 45 ma Max./Each side
Microsoft Word - 熱力-第六章_99_.doc
 Chapter 6 hermodynamic roperties of Fluids 6-. roperty relations for homogeneous phases. he first law for a closed system of n moles is: du = dq + dw (For the special case of a reversible process, du =
Chapter 6 hermodynamic roperties of Fluids 6-. roperty relations for homogeneous phases. he first law for a closed system of n moles is: du = dq + dw (For the special case of a reversible process, du =
表二 105 年國中教育會考英語科閱讀與聽力答對題數對應整體能力等級加標示對照表 閱讀答 對題數 聽力答對題數 待加強待加強待加強待加強待加強待加強待加強待加強待加強待加強待加強待加強
 表一 105 年國中教育會考國文科 社會科與自然科能力等級加標示與答對題數對照表 國文社會自然 A++ 46-48 60-63 51-54 A+ 42-48 44-45 54-63 58-59 46-54 49-50 A 42-43 54-57 46-48 B++ 37-41 45-53 37-45 B+ 20-41 31-36 24-53 38-44 20-45 30-36 B 20-30 24-37
表一 105 年國中教育會考國文科 社會科與自然科能力等級加標示與答對題數對照表 國文社會自然 A++ 46-48 60-63 51-54 A+ 42-48 44-45 54-63 58-59 46-54 49-50 A 42-43 54-57 46-48 B++ 37-41 45-53 37-45 B+ 20-41 31-36 24-53 38-44 20-45 30-36 B 20-30 24-37
物質科學_化學篇
 物質科學化學篇 ( 上 ) 講義編者 : 陳義忠 33 物質科學 _ 化學篇 ( 上 ) 第三章 氣體 3- 物質的三態 :. 狀態變化 : () 一般物質常有固 液 氣三態, 隨著溫度或壓力的改變, 相也會跟著改變 () 變化的過程中必伴有能量的變化 這能量變化有些可能是因為相變化所產生的, 而有些可能是因為物質本身溫度變化所造成的 例如 : 相變化 固態液態氣態 + + (3) 同一物質的能量大小順序為
物質科學化學篇 ( 上 ) 講義編者 : 陳義忠 33 物質科學 _ 化學篇 ( 上 ) 第三章 氣體 3- 物質的三態 :. 狀態變化 : () 一般物質常有固 液 氣三態, 隨著溫度或壓力的改變, 相也會跟著改變 () 變化的過程中必伴有能量的變化 這能量變化有些可能是因為相變化所產生的, 而有些可能是因為物質本身溫度變化所造成的 例如 : 相變化 固態液態氣態 + + (3) 同一物質的能量大小順序為
第三章 理想气体的热力学能、
 845 3 A B u = f ( ) 3345 ( du) = ( δq) = c d V c V0 duc V0 d3 u u c V d 3a c V 0 V 0 V huvu R g hf 3 5 dh) (δq) c d c 0 dhc 0 d3 h h c d 3a c 0 0 Ku 0 0 Ku 0 0 J/kgh 0 u 0 0 v 0 u 0 R g 0 0 J/kg 0 q c
845 3 A B u = f ( ) 3345 ( du) = ( δq) = c d V c V0 duc V0 d3 u u c V d 3a c V 0 V 0 V huvu R g hf 3 5 dh) (δq) c d c 0 dhc 0 d3 h h c d 3a c 0 0 Ku 0 0 Ku 0 0 J/kgh 0 u 0 0 v 0 u 0 R g 0 0 J/kg 0 q c
人為疏失 人與人之間的溝通合作, 往往是事故的最終防線, 若能發揮團隊合作的功能, 則比較能克服其他因素所造成的危害
 人為因素與 飛航安全 人為因素 7 7 8 人為因素的類別 H 1972 E. Edward SHELL S S L E software, H handware, E environment, L liveware L SHELL 20 2014 3 495 人為疏失 人與人之間的溝通合作, 往往是事故的最終防線, 若能發揮團隊合作的功能, 則比較能克服其他因素所造成的危害 2014 3 495
人為因素與 飛航安全 人為因素 7 7 8 人為因素的類別 H 1972 E. Edward SHELL S S L E software, H handware, E environment, L liveware L SHELL 20 2014 3 495 人為疏失 人與人之間的溝通合作, 往往是事故的最終防線, 若能發揮團隊合作的功能, 則比較能克服其他因素所造成的危害 2014 3 495
John Dalton, 1766 1844 W.H. Henry E. Hodgkinson S. Clegg S.H. Ware R. Potter B. Woodcroft James Prescott Joule 1818 12 24 1834 Pine Salford Street 180
 54 2002 1 349 John Dalton, 1766 1844 W.H. Henry E. Hodgkinson S. Clegg S.H. Ware R. Potter B. Woodcroft James Prescott Joule 1818 12 24 1834 Pine Salford Street 1800 1837 2002 1 349 55 1835 University
54 2002 1 349 John Dalton, 1766 1844 W.H. Henry E. Hodgkinson S. Clegg S.H. Ware R. Potter B. Woodcroft James Prescott Joule 1818 12 24 1834 Pine Salford Street 1800 1837 2002 1 349 55 1835 University
17-72c-1
 台灣喜宴文化與陶瓷餐具設計開發 廖素慧 林長弘 林秀娟 摘 要 喜宴文化它包括了生活風俗習慣 禮教的 禁忌與料理 飲食的結合 可以看到民族的思 想行為以及社會的結構模式 是生活文化的濃 縮 它的過程對於一對新人在人生旅程開始 時 得到關愛與祝福也給予責任 所以喜宴的 禮教約束 是人生很重要的一個過程 好的飲 食禮教約束可以產生良性的人生觀 從喜宴的 食物料理與新開發餐具的造形與裝飾美感等的 結合來做一個開始
台灣喜宴文化與陶瓷餐具設計開發 廖素慧 林長弘 林秀娟 摘 要 喜宴文化它包括了生活風俗習慣 禮教的 禁忌與料理 飲食的結合 可以看到民族的思 想行為以及社會的結構模式 是生活文化的濃 縮 它的過程對於一對新人在人生旅程開始 時 得到關愛與祝福也給予責任 所以喜宴的 禮教約束 是人生很重要的一個過程 好的飲 食禮教約束可以產生良性的人生觀 從喜宴的 食物料理與新開發餐具的造形與裝飾美感等的 結合來做一個開始
Zytiga... Zytiga... Zytiga Zytiga Zytiga
 250 本資料僅提供醫護人員衛教使用 ............... Zytiga... Zytiga... Zytiga... 2 3 4 5 6 7 8 9 Zytiga... 10 Zytiga... 10...... 13 18 Zytiga Zytiga 2 25% 3 PSA PSA 3~4 ng/ml PSA bone scan CT scan MRI 4 5 攝護腺癌之治療 治療方面
250 本資料僅提供醫護人員衛教使用 ............... Zytiga... Zytiga... Zytiga... 2 3 4 5 6 7 8 9 Zytiga... 10 Zytiga... 10...... 13 18 Zytiga Zytiga 2 25% 3 PSA PSA 3~4 ng/ml PSA bone scan CT scan MRI 4 5 攝護腺癌之治療 治療方面
原子結構
 順序 1 2 3 4 5 比熱 內 容影 部聲 部 轉場投影片 標題投影片 : 背景音樂 內容摘要 開場白 老師影像 各位同學大家 好 這個單元要 跟大家介紹比 熱 在介紹之 前, 我們先回顧 我們在熱量上 學過那些內容 轉場投影片 標題投影片 : 背景音樂 先備知識 先備知識 : 投影片 老師依投影片 熱量可以使物體 : 內容解講 溫度改變 狀態改變 熱量單位 : 卡 使 1 公克的水溫度上升 1
順序 1 2 3 4 5 比熱 內 容影 部聲 部 轉場投影片 標題投影片 : 背景音樂 內容摘要 開場白 老師影像 各位同學大家 好 這個單元要 跟大家介紹比 熱 在介紹之 前, 我們先回顧 我們在熱量上 學過那些內容 轉場投影片 標題投影片 : 背景音樂 先備知識 先備知識 : 投影片 老師依投影片 熱量可以使物體 : 內容解講 溫度改變 狀態改變 熱量單位 : 卡 使 1 公克的水溫度上升 1
( )... 5 ( ) ( )
 2016 大學校院招收大陸地區學生聯合招生委員會 71005 臺南市永康區南臺街 1 號 E-mail:rusen@stust.edu.tw WEB:http://rusen.stust.edu.tw TEL:+886-6-2435163 FAX:+886-6-2435165 2 0 1 6 0 1 1 9 2016... 2... 3... 5 ( )... 5 ( )... 5 1... 6 2...
2016 大學校院招收大陸地區學生聯合招生委員會 71005 臺南市永康區南臺街 1 號 E-mail:rusen@stust.edu.tw WEB:http://rusen.stust.edu.tw TEL:+886-6-2435163 FAX:+886-6-2435165 2 0 1 6 0 1 1 9 2016... 2... 3... 5 ( )... 5 ( )... 5 1... 6 2...
中期 12 中期 % 報告期 報告 44 中期 報 年中期報告 中國鋁業股份有限公司
 2016 2016 6 30 6 2016 2016 www.hkex.com.hk www.chalco.com.cn 2 6 8 10 中期 12 中期 12 13 16 22 25 26 27 5% 28 29 29 報告期 29 30 31 31 31 32 35 35 36 38 報告 44 中期 報 46 1 2016 年中期報告 中國鋁業股份有限公司 1. ALUMINUM CORPORATION
2016 2016 6 30 6 2016 2016 www.hkex.com.hk www.chalco.com.cn 2 6 8 10 中期 12 中期 12 13 16 22 25 26 27 5% 28 29 29 報告期 29 30 31 31 31 32 35 35 36 38 報告 44 中期 報 46 1 2016 年中期報告 中國鋁業股份有限公司 1. ALUMINUM CORPORATION
Suggested answers to in-text activities and unit-end exercises
 課內活動及課後練習的建議答案 小測試 P35.1( 第 5 頁 ) a) b) ΔH x = 97 kj mol 1 ΔH y = 144 kj mol 1 P35.( 第 56 頁 ) 1 a) 斜方晶硫較為穩定 b) 已知以下的數據 :` (1) S( 斜方晶 ) + O (g) SO (g) ΔH = 96.0 kj mol 1 () S( 單斜晶 ) + O (g) SO (g) ΔH =
課內活動及課後練習的建議答案 小測試 P35.1( 第 5 頁 ) a) b) ΔH x = 97 kj mol 1 ΔH y = 144 kj mol 1 P35.( 第 56 頁 ) 1 a) 斜方晶硫較為穩定 b) 已知以下的數據 :` (1) S( 斜方晶 ) + O (g) SO (g) ΔH = 96.0 kj mol 1 () S( 單斜晶 ) + O (g) SO (g) ΔH =
Microsoft Word - Tridentine NL_C.docx
 聖人慶日及節日 五月十一日 聖斐理伯與聖雅各伯 宗徒 慶日 五月二十九日 耶穌升天 節日 五月三十一日 聖母天地元后 慶日 文章分享 淺談拉丁文在天主教會的重要性 緒論 一直以來 教會拉丁語被視為西方文化之基石和羅馬天主教會的官方語言 可是在 近四十年來 這種 天主教徒的特徵 (sensus catholicus) 已從教會禮儀 信友靈修生活 等逐漸褪色 這現象當然與人們 甚至神長和教會機構對拉丁語應用之誤解有關
聖人慶日及節日 五月十一日 聖斐理伯與聖雅各伯 宗徒 慶日 五月二十九日 耶穌升天 節日 五月三十一日 聖母天地元后 慶日 文章分享 淺談拉丁文在天主教會的重要性 緒論 一直以來 教會拉丁語被視為西方文化之基石和羅馬天主教會的官方語言 可是在 近四十年來 這種 天主教徒的特徵 (sensus catholicus) 已從教會禮儀 信友靈修生活 等逐漸褪色 這現象當然與人們 甚至神長和教會機構對拉丁語應用之誤解有關
TYPE AND PARTS SELECTION OF ALUMINUM FRAME TOLERANCE OF ALUMINUM FRAME 鋁擠型專用資訊頁容易搜尋! 刊載多項技術資訊與使用範例! MISUMI
 TYE ND RTS SEECTION OF UMINUM FRME TOERNCE OF UMINUM FRME 容易! 刊載多項技術資訊與使用範例! Q HFS HFS 6N01SST5 HFS84040 HFSB84040 CF84040 HFSY84040 HFS84040 6N01SST5 HFSB84040 NFS NEFS NFS 6063ST5 6063ST5 HFSEFS NEFS84040
TYE ND RTS SEECTION OF UMINUM FRME TOERNCE OF UMINUM FRME 容易! 刊載多項技術資訊與使用範例! Q HFS HFS 6N01SST5 HFS84040 HFSB84040 CF84040 HFSY84040 HFS84040 6N01SST5 HFSB84040 NFS NEFS NFS 6063ST5 6063ST5 HFSEFS NEFS84040
SAHTECH 安全衛生技術中心 財團法人 事故 2
 SAHTECH 03-5836885#102 cchuang@sahtech.org 1 SAHTECH 安全衛生技術中心 財團法人 事故 2 SAHTECH 11.20 2010 SAHTECH SAHTECH 发 开关 点 图 SAHTECH 点 SAHTECH SAHTECH (2009.03.04) 2009.7.29 2009.7.29 SAHTECH SAHTECH 6.29 2010
SAHTECH 03-5836885#102 cchuang@sahtech.org 1 SAHTECH 安全衛生技術中心 財團法人 事故 2 SAHTECH 11.20 2010 SAHTECH SAHTECH 发 开关 点 图 SAHTECH 点 SAHTECH SAHTECH (2009.03.04) 2009.7.29 2009.7.29 SAHTECH SAHTECH 6.29 2010
Microsoft PowerPoint - Energy in Thermal Process & The 1st Law of Thermodynamics.ppt [相容模式]
![Microsoft PowerPoint - Energy in Thermal Process & The 1st Law of Thermodynamics.ppt [相容模式] Microsoft PowerPoint - Energy in Thermal Process & The 1st Law of Thermodynamics.ppt [相容模式]](/thumbs/93/112845245.jpg) Energy in Thermal Process & The 1st Law of Thermodynamics. 熱能與熱力學第一定律 焦耳 試驗 Joule s Experiment h ΔU g =-mgh ΔE int = mcδt ΔU g + ΔE int = 0 焦耳 試驗 Joule s Experiment Joule s Experiment Work temperature
Energy in Thermal Process & The 1st Law of Thermodynamics. 熱能與熱力學第一定律 焦耳 試驗 Joule s Experiment h ΔU g =-mgh ΔE int = mcδt ΔU g + ΔE int = 0 焦耳 試驗 Joule s Experiment Joule s Experiment Work temperature
t14phip
 China Tower Corporation Limited (a) (b) (c) (d) (e) (f) (g) (h) (i) (j) (k) 1933 1933 32 China Tower Corporation Limited [ ] [ ] : [ ] [ ] [ ] : [ ] [ ] : [ ] [ ] [ ] : [ ] [ ] [ ] [ ] : [ ] 1.00 : [ ]
China Tower Corporation Limited (a) (b) (c) (d) (e) (f) (g) (h) (i) (j) (k) 1933 1933 32 China Tower Corporation Limited [ ] [ ] : [ ] [ ] [ ] : [ ] [ ] : [ ] [ ] [ ] : [ ] [ ] [ ] [ ] : [ ] 1.00 : [ ]
10 不住在水裡的淡水龜 超級大 宅龜 台灣難得仍能保留少數的食蛇龜穩定族群, 在保育研究上顯得重要與珍貴
 40 2014 2 494 台灣食蛇龜生存的挑戰 失落的龜樂園 20 台灣的食蛇龜 J. E. Gray 1863 R. Swinhoe J. Reeve 台灣原來還算普遍的食蛇龜, 也名列投機者高價競逐的少數物種之一, 前景令人擔憂 10 不住在水裡的淡水龜 超級大 宅龜 0.07 8.25 2 40 5 16 台灣難得仍能保留少數的食蛇龜穩定族群, 在保育研究上顯得重要與珍貴 2014 2 494
40 2014 2 494 台灣食蛇龜生存的挑戰 失落的龜樂園 20 台灣的食蛇龜 J. E. Gray 1863 R. Swinhoe J. Reeve 台灣原來還算普遍的食蛇龜, 也名列投機者高價競逐的少數物種之一, 前景令人擔憂 10 不住在水裡的淡水龜 超級大 宅龜 0.07 8.25 2 40 5 16 台灣難得仍能保留少數的食蛇龜穩定族群, 在保育研究上顯得重要與珍貴 2014 2 494
第三冊第五章理化補充習題
 [ 溫度與溫度計 ] 理化補充習題 有** 記號者, 請填寫計算過程到理化計算本中 1. 左 右兩手分別放入冰水 熱水中, 隔一會同時抽出, 再放入同一盆溫水中, 則 : 左手感覺 熱 ( 冷或熱 ), 因其進行 吸 熱 ( 吸或放 ) 反應 右手感覺 冷 ( 冷或熱 ), 因其進行 放 熱 ( 吸或放 ) 反應 2. 有甲 乙 丙三桶水, 伊伊將左手伸入甲桶水中, 將右手伸入丙桶水中, 五分鐘後,
[ 溫度與溫度計 ] 理化補充習題 有** 記號者, 請填寫計算過程到理化計算本中 1. 左 右兩手分別放入冰水 熱水中, 隔一會同時抽出, 再放入同一盆溫水中, 則 : 左手感覺 熱 ( 冷或熱 ), 因其進行 吸 熱 ( 吸或放 ) 反應 右手感覺 冷 ( 冷或熱 ), 因其進行 放 熱 ( 吸或放 ) 反應 2. 有甲 乙 丙三桶水, 伊伊將左手伸入甲桶水中, 將右手伸入丙桶水中, 五分鐘後,
Chinese Fonts Font Book 2012 Additions
 Chinese Fonts Font Book 2012 Additions Chinese Fonts Font Book 2012 Additions 繁體 HK Collection Traditional 4 正雅蘭 MEllanHK-SemiBold 5 特黑體 MHeiHK-Heavy 6 特粗楷二 MKai2HK-Black 7 岩流體 MLavaHK-UltraBold 8 毡筆體
Chinese Fonts Font Book 2012 Additions Chinese Fonts Font Book 2012 Additions 繁體 HK Collection Traditional 4 正雅蘭 MEllanHK-SemiBold 5 特黑體 MHeiHK-Heavy 6 特粗楷二 MKai2HK-Black 7 岩流體 MLavaHK-UltraBold 8 毡筆體
基礎化學 ( 三 ) 講義目次 第 章氣體 氣體性質 氣體定律 5 3 理想氣體 39 4 氣體分壓 59 5 氣體擴散與逸散 79 國戰 大考試題 9 參考解答 97
 內容由蔡明倫老師編纂 基礎化學 ( 三 ) 講義 第 章氣體 班級 : 座號 : 姓名 : 基礎化學 ( 三 ) 講義目次 第 章氣體 氣體性質 氣體定律 5 3 理想氣體 39 4 氣體分壓 59 5 氣體擴散與逸散 79 國戰 大考試題 9 參考解答 97 第 章 氣體 - 氣體性質一 大氣 : 定義: 地球上空大約一千公里的氣體受到地球引力吸引的作用而圍繞地球, 這些圍繞地球的氣體稱為大氣 大氣的功用:
內容由蔡明倫老師編纂 基礎化學 ( 三 ) 講義 第 章氣體 班級 : 座號 : 姓名 : 基礎化學 ( 三 ) 講義目次 第 章氣體 氣體性質 氣體定律 5 3 理想氣體 39 4 氣體分壓 59 5 氣體擴散與逸散 79 國戰 大考試題 9 參考解答 97 第 章 氣體 - 氣體性質一 大氣 : 定義: 地球上空大約一千公里的氣體受到地球引力吸引的作用而圍繞地球, 這些圍繞地球的氣體稱為大氣 大氣的功用:
一、乘法公式與多項式
 一 乘法公式與多項式 多項式的乘法公式除了用來簡化多項式的乘法運算外, 還可運用於因式 分解 在本章中, 我們首先來複習已經學過的平方公式, 然後再延伸到立方公式 1-1 平方公式 二項式相乘公式 我們可利用分配律來展開 ( a+ )( c+ d) 的乘積而得到下列的公式 : ( a + )( c + d) ac + ad + c + d 公式 1 a c ac d ad c d 另一方面, 也可利用幾何圖形來解釋這個公式
一 乘法公式與多項式 多項式的乘法公式除了用來簡化多項式的乘法運算外, 還可運用於因式 分解 在本章中, 我們首先來複習已經學過的平方公式, 然後再延伸到立方公式 1-1 平方公式 二項式相乘公式 我們可利用分配律來展開 ( a+ )( c+ d) 的乘積而得到下列的公式 : ( a + )( c + d) ac + ad + c + d 公式 1 a c ac d ad c d 另一方面, 也可利用幾何圖形來解釋這個公式
_BK07.ps, page Preflight ( _BK07.indd )
 1 2 3 4 5 6 7 8 9 10 11 12 7.3 家庭變遷對健康的影響 在經濟起伏時 家庭支持十分重要 在 兩地三岸社會政策 一書中 魏雁濱 曾群 在 社會排斥 一文提及一項研究發現 在北歐六國和蘇格蘭 家人支持對防止失業 青年陷入貧窮發揮重要作用 在福利制度相對比北歐較弱的南歐國家如意大利 家庭 和社會網絡對失業者起較大的支持和保護作用 在中國人社會 家庭支持也十分重要 根據本港社會服務聯會
1 2 3 4 5 6 7 8 9 10 11 12 7.3 家庭變遷對健康的影響 在經濟起伏時 家庭支持十分重要 在 兩地三岸社會政策 一書中 魏雁濱 曾群 在 社會排斥 一文提及一項研究發現 在北歐六國和蘇格蘭 家人支持對防止失業 青年陷入貧窮發揮重要作用 在福利制度相對比北歐較弱的南歐國家如意大利 家庭 和社會網絡對失業者起較大的支持和保護作用 在中國人社會 家庭支持也十分重要 根據本港社會服務聯會
~p8t24w1d0fm;
 第一章導論 Update: 2017/2/21 一 熱傳學的領域能量的利用為機械工程的重要內容之一 熱力學探討能量轉換基本規則 熱傳學探討能量轉換方式與速度 二 能量傳遞的方式原子或分子的直接碰撞 : 熱傳導傳遞熱量的介質沒有移動 : 熱傳導 (conduction) 傳遞熱量的介質有移動 : 熱對流 (convection) 電磁波遠距離非接觸式傳遞 : 熱輻射 (radiation) 高等熱傳學中興大學機械工程研究所頁
第一章導論 Update: 2017/2/21 一 熱傳學的領域能量的利用為機械工程的重要內容之一 熱力學探討能量轉換基本規則 熱傳學探討能量轉換方式與速度 二 能量傳遞的方式原子或分子的直接碰撞 : 熱傳導傳遞熱量的介質沒有移動 : 熱傳導 (conduction) 傳遞熱量的介質有移動 : 熱對流 (convection) 電磁波遠距離非接觸式傳遞 : 熱輻射 (radiation) 高等熱傳學中興大學機械工程研究所頁
期交所規則、規例及程序
 黃 金 期 貨 合 約 細 則 下 述 合 約 細 則 適 用 於 黃 金 期 貨 合 約 : 相 關 資 產 合 約 單 位 交 易 貨 幣 合 約 月 份 報 價 最 低 價 格 波 幅 立 約 成 價 立 約 價 值 持 倉 限 額 成 色 不 少 於 995 的 黃 金 100 金 衡 安 士 美 元 現 貨 月 及 下 兩 個 曆 月 集 團 行 政 總 裁 與 證 監 會 會 商 後 可
黃 金 期 貨 合 約 細 則 下 述 合 約 細 則 適 用 於 黃 金 期 貨 合 約 : 相 關 資 產 合 約 單 位 交 易 貨 幣 合 約 月 份 報 價 最 低 價 格 波 幅 立 約 成 價 立 約 價 值 持 倉 限 額 成 色 不 少 於 995 的 黃 金 100 金 衡 安 士 美 元 現 貨 月 及 下 兩 個 曆 月 集 團 行 政 總 裁 與 證 監 會 會 商 後 可
 侧 侧 侧 侧 侧 侧 滤 爲 侧 2-1 ρ 2-2 舉例說明 相關閥類與配件的阻抗係數 K 可參考圖[2.3]選取 代 入上式即可求得該部分之壓損 圖 2.3 不同閥及裝置的阻抗係數 K (3) 直管 配件 閥件 串聯成一條管線的阻力 壓降或頭損 2-3 2-4 2-5 敍 2-6 侧 2-7 2-8 侧 2-9 2-10 2-11 2-12 2-13 2-14 2-15 2-16
侧 侧 侧 侧 侧 侧 滤 爲 侧 2-1 ρ 2-2 舉例說明 相關閥類與配件的阻抗係數 K 可參考圖[2.3]選取 代 入上式即可求得該部分之壓損 圖 2.3 不同閥及裝置的阻抗係數 K (3) 直管 配件 閥件 串聯成一條管線的阻力 壓降或頭損 2-3 2-4 2-5 敍 2-6 侧 2-7 2-8 侧 2-9 2-10 2-11 2-12 2-13 2-14 2-15 2-16
