我的家教-高中化學學測複習講義
|
|
|
- 肴玦谭 韩
- 5 years ago
- Views:
Transcription
1 基礎化學 ( 一 ) 單元 物質的組成 單元 原子構造與元素週期表 單元 化學反應 9 單元 化學與能源 7 基礎化學 ( 二 ) 單元 5 常見的化學反應 9 單元 6 物質的構造與特性 0 單元 7 有機化合物 8 單元 8 化學與化工 78
2 化學反應 化學式的種類 包括實驗式 分子式 結構式 示性式 電子點式 化學式 化學式中元素重量百分組成 A 元素重量百分組成 (%)= A 原子量 化學式中 A 原子數分子量 00 % 實驗式 分子式的求法 利用燃燒法測元素重量組成利用重量組成與原子量, 求實驗式再測分子量, 並計算分子量與式量比值, 即可得分子式 化學反應式與平衡 化學反應式 反應式平衡 以化學式和一些簡單符號來表示化學反應進行的過程 原理 : 遵守原子不滅 電荷守恆方法 : 觀察法 代數法 計量原理 利用反應式係數比 = 莫耳數比 = 同狀況下氣體體積比來計量 化學計量 計量方法 莫耳數法 化學計量時的相關名詞 理論產量 實際產量 產率 分解率 原子使用效率 化學反應中的能量變化 反應熱 反應熱種類 反應有些為吸熱 (Δ > 0), 有些為放熱 (Δ < 0) 熱化學反應式表示法 : 附物質狀態及反應熱的反應式影響因素 : 反應量 狀態 狀況 ( 溫度 壓力 ) 標準反應熱 (Δ 0 ): 在標準狀況 (5 atm) 下測量的反應熱 莫耳生成熱 莫耳燃燒熱 反應熱的求法 赫士定律 : 反應熱加成性定律代公式法 :Δ = 生成物總生成熱 - 反應物總生成熱 = 反應物總燃燒熱 - 生成物總燃燒熱 第 單元 化學反應 9
3 壹 化學式 一 化學式的意義 命題指數 以元素符號和數字的組合來表示物質組成的式子, 稱為化學式 二 化學式的種類 命題指數 種類定義乙酸甲醛 實驗式僅表示物質中所含元素的種類及各原子的最簡整數比 C O C O 分子式表示物質中一分子所含原子的種類及確實的數目 C O C O O O 結構式表明物質中原子間結合排列的化學式 C C C O 示性式 電子點式 表明官能基特性的化學式, 適用於有機化合物 以電子點表明原子間結合排列的化學式 C COO 羧基 C C O O CO 醛基 嫎 娋 䊼皆由極大數目的原子 ( 或離子 ) 互相堆積 而成的巨大結構, 而無法確定其組成原子的確實個數, 故常以 表示, 如金屬元素 (Fe Al), 離子化合物 (NaCl KNO ), 網狀晶體 ( 石英 SiO 金剛石 C) 不同化合物, 可以有相同的實驗式, 但兩者具有 : 㜬相同 䭻相同 同重量所含 相同 由非金屬元素組成的物質, 多為分子物質, 可用分子式表示, 如 O C 結構式不能表示分子真正形狀, 如甲烷結構式 C 中, 個氫原子並非在同一平面上, 甲 烷分子形狀 C 為鎻 5 同分異構物 : 分子式相同而結構式不同的化合物, 其物性 化性不同 例如 : 乙醇 C C O 與甲醚 C O C, 兩者分子式皆為 C 6 O O C 50 基礎化學 ( 一 )
4 三 化學式與元素的重量百分組成 命題指數 利用化學式可以計算化合物中各成分元素的重量百分組成 (%), 其方法為 : 某元素原子量 化學式中該元素原子數某元素重量百分組成 (%)= 00 % 分子量 6 例如 : 葡萄糖 (C 6 O 6 ) 中, 碳的含量為 :C % = 00 % = 0 % 四 實驗式與分子式的求法 :( 假設化合物含碳 氫 氧三元素 ) 命題指數 利用鎸, 測出燃燒產物 CO 與 O 的重量, 進一步計算出 C O 的重量 W 試樣克有機化合物中含 W W = W C CO # = W O # 8 W = W W W O 試樣 C O A B CuO Mg(ClO ) NaO O CO Mg( ClO ) 為乾燥劑, 吸收水, Mg( ClO ) 管增加的重量等於燃燒後產生水的重量 NaO 吸收二氧化碳,NaO 管增加的重量等於燃燒後產生二氧化碳的重量 求出 C O 原子莫耳數的最簡比例, 即可得實驗式 C::O = W C : W : W 6 O 有機化合物之實驗式為 C x y O z = x:y:z, 再由實驗測該有機化合物之分子量, 即可得分子式 若 分子量實驗式量 = n, 則分子式 = ( 實驗式 ) n 式量 = 實驗式中所有原子量的總和如 C x y O z 之式量 = x+y+6z 分子量 = 實驗式量 n 範例 化學式下列有關物質化學式的敘述, 哪些錯誤? 䕷 C COO 為醋酸的示性式, 而非分子式 二氧化矽的分子式為 SiO, 而食鹽的化學式為 NaCl 乙醇與甲醚分子式相同, 結構式不同, 稱為同分異構物, 兩者性質不同 甲烷的結構式為 C, 顯示其為一平面分子 蛯實驗式與分子式可表示化合物所含原子種類及部分化性答虲蚲 解 第 單元 化學反應 5
5 類題下列關於化學式的敘述, 何者錯誤? 離子化合物通常以實驗式表示 示性式可表明化合物的官能基 分子式相同的化合物, 其實驗式必相同 網狀固體因沒有分子的單位, 所以無法以結構式表示答蚲鑽石 石英雖然沒有分子結構, 但仍可以結構式呈現 範例 同分異構物下列關於等重的甲醛 (CO) 乙酸 (C COO) 和甲酸甲酯 (COOC ) 之各項敘述, 何者不正確? 三者原子數相同 分子數最多者為甲醛 與足量氧燃燒生成等重的 CO 燃燒所消耗的氧重以甲醛最多 所含碳的重量百分組成均相等答蚲解三者實驗式皆為 C O, 故等重時, 含有相同的原子數 相同的重量百分組成 n 甲醛 :n 乙酸 :n 甲酸甲酯 燃燒時所消耗的氧等重, 其燃燒產物 CO 與 O 亦為等重 類題有關醋酸 (C COO) 和葡萄糖 (C 6 O 6 ) 的敘述, 哪些正確? 兩者皆為分子式 兩者實驗式相同 兩者所含元素重量百分組成相同 等重時, 所含碳原子數相同 等重時, 兩者所含分子數相同答 範例 燃燒法求實驗式維他命 C 含 C O 三種元素, 今取. 克維他命 C 置於純氧中完全燃燒, 產物通過甲管 ( 裝無水過氯酸鎂 ) 和乙管 ( 裝 NaO), 甲管重量增加 0.5 克, 乙管重量增加.98 克, 則下列有關. 克維他命 C 的敘述, 何者錯誤? 含碳 0.5 克 含氧 0.7g 含氫的重量百分率.55% 維他命 C 的實驗式為 C O 答 解 甲管吸收, 乙管吸收 ( 克 ), ( 克 ), ( 克 ) C::O 原子莫耳數比 實驗式為 C O 5 基礎化學 ( 一 )
6 類題某有機化合物僅含 C O 三種元素, 其重量組成為碳 0.0 % 氫 6.6 %, 其餘為氧, 則此有機化合物的實驗式為下列何者? C O C O C O C O 答 範例 元素重量百分組成 哺乳動物的紅血球中, 血紅素約含 0. % 的鐵, 如果血紅素的分子量約為 68000, 則一分子的血紅素中含有幾個鐵原子?( 原子量 :Fe = 56) 5 答 解血紅素中鐵元素的重量百分組成 (%) = 00 % n = 類題自然界的鐵礦有赤鐵礦 (Fe O ) 磁鐵礦 (Fe O ) 和黃鐵礦 (FeS ) 此三種鐵礦含鐵的重量百分率, 由高而低的順序何者正確?( 原子量 :S =,O = 6,Fe = 56) Fe O > Fe O > FeS Fe O > Fe O > FeS FeS > Fe O > Fe O Fe O > FeS > Fe O 答 範例 5 含結晶水的化學式 帶有結晶水的某化合物.6 克, 經加熱除去所有結晶水後, 其重量為 0.90 克 如無水物的分子量為 90, 則一莫耳的該化合物中, 結晶水的莫耳數應為多少? 答虲 解 X: O 莫耳數比 =:n = : n= 類題將碳酸鈉晶體 0.57 克加熱除去結晶水, 可得到 0. 克的無水碳酸鈉粉末 碳酸鈉晶體的化學式為 NaCO$ xo, 則 x 為下列何值?( =,C =,O = 6,Na = ) 6 8 蛯 0 答蛯 第 單元 化學反應 5
7 貳 化學反應式與反應式的平衡 一 化學反應式 命題指數 化學反應式是用化學式和一些簡單的符號來表示化學反應的式子, 又稱為化學方程式 化學反應式需根據事實, 不可憑臆測寫出, 各化學式右下角常附記相態 如 (s) 表固體,(l) 表液體,(g) 表氣體,(aq) 表水溶液, 並且在箭號上方或下方註記反應所需條件 鐵粉 化學反應式可用以表示反應物與生成物的下列關係 例如 : N N 由反應式可得知反應物與生成物的變化量為 : ( ) + g ( g ) 00atm, 500cC ( g ) N (g) (g) N (g) 分子數 莫耳數 質 量 8 = 8 = 6 7 = 體 積 反應條件 00atm,500, 以鐵粉為催化劑 由上可知反應式能顯示 : 係數比 = 反應時的 比 = 反應時的 比 二 化學反應式的平衡 命題指數 原理 : 遵守 葲 方法 : 觀察法 代數法 觀察法 : 以最複雜物質 ( 含元素種類最多者 ) 的係數定為, 然後依兩邊出現次數由少至多的順 序, 遵循上述原則平衡, 最後再將係數化為最簡整數 舉例說明如下 : Ca ( PO ) + C+ SiO CaSiO + CO+ P 先將 Ca( PO) 係數定為 : Ca ( PO ) + C+ SiO CaSiO + CO+ P 依原子在兩邊出現次數由少至多的順序, 遵循原子不滅平衡 : 由 Ca 可得 CaSiO ; 由 P 可得 P ; 由 Si 可得 SiO ; 由 O 可得 5CO; 由 C 可得 5C Ca ( PO ) 5C SiO CaSiO 5CO P 最後再將係數化為最簡整數 : Ca ( PO ) + 0C+ 6SiO 6CaSiO + 0CO+ P 代數法 : 先利用觀察法將可決定的係數先做決定, 再將不能確定的係數設立未知數 依原子守恆或電荷守恆建立數學方程式 ( 若設立 n 個未知數, 須建立 n 個數學方程式 ) 解聯立方程式, 得未知數, 最後再將係數化為最簡整數 舉例說明如下 : 銅片在稀硝酸中反應, 生成一氧化氮 硝酸銅和水, 其淨離子反應式可寫為 : + + Cu + + NO Cu + NO+ O 5 基礎化學 ( 一 )
8 + + 由 步驟知 :Cu + a + bno Cu + cno + d O 依原子守恆知 :N 原子 :b = c (Ⅰ) 原子 :a = d (Ⅱ) O 原子 :b = c + d (Ⅲ) 依電荷守恆知 : a+ ( b) = (Ⅳ) 聯立 (Ⅰ)~(Ⅳ) 方程式得 :a = 8,b =,c =,d 即反應式為 Cu NO Cu NO + + O + + 最後係數化為整數 :Cu NO Cu + NO+ O = BLOG 若要將淨離子反應式寫成分子反應式, 則在生成物一方的陽離子 ( 或陰離子 ) 需用反應物之陰離子 ( 或陽離子 ) 來中和電性, 使成中性的物質, 如 : Cu NO +g + 6NO Cu + 8NO + + Cu + 6NO Cu( NO ) + NO + O + NO + O 範例 6 化學反應式有一碳氫氧化合物 分子內有 個氧原子, 實驗證實其 分子完全燃燒時, 產生 分子二氧化碳與 分子水, 針對此化合物的敘述, 下列哪些錯誤? 實驗式為 C O 分子式為 C O 分子式 = ( 實驗式 ) n,n = 燃燒反應式的最簡係數和為 0 莫耳化合物燃燒需氧 莫耳 答 解由題意知, 依原子不滅定律知 x =,y =,z = 即化學反應式為 䕷實驗式為 CO 蛯 莫耳 類題化學反應式可用來描述化學反應發生時, 物質間的變化關係 下列關於化學反應式的敘述, 何者錯誤? 化學反應式兩邊的原子種類相同 反應物與生成物所含的原子總數相同 反應式兩邊的分子總數相同 反應物與生成物的總重量相同答反應式兩邊原子種類 數目皆不變, 但係數與分子數不一定相同 第 單元 化學反應 55
9 範例 7 觀察法平衡反應式 利用觀察法平衡下列反應式 :KCrO 7+ Cl KCl + CrCl+ Cl+ O, 則其最簡係數和為若干? 6 9 蛯 7 答蚒 解依原子不滅 電荷不滅, 由某元素在反應式兩邊僅出現一次且原子數目不相等者, 先平衡之, 元素出現次數 較多者, 後平衡之 嫎 K Cr O 7 化學式最複雜, 設其係數為 娋依下列順序平衡之 :K Cr O Cl, 得 類題 將下列反應式平衡後, 若平衡係數皆取最簡單整數, 則哪些反應式左邊的平衡係數總和比右邊的 平衡係數總和少?( 應選三項 ) 催化分解 (g) (g) (g) N N + FeO(s) + CO(g) Fe(s) + CO(g) C6(O) (aq) + O (aq) CO 6 (aq) + O(l) Ca(CO ) (s) + Cl(aq) CaCl(aq) + CO(g) + O (l) C / C + Ag(N)NO AgC / CAg + N NO + N 0 學測 答 䕷蚲蛯 (g) (aq) (s) (aq) (g) 範例 8 代數法平衡反應式銅在濃硫酸中會發生反應, 其反應式如下 : + + acu+ b + cso xcu + y O+ zso 針對此均衡反應式, 下列各項係數間的關係式哪些是正確的? 依據硫原子不滅 :c = z 依據氫原子不滅 :b = y 依據氧原子不滅 :c = y + z 依據電荷不滅 :b + c = x 最簡係數總和為 0 答䕷虲蚒蛯解依原子不滅知 :Cu 原子 :a = x 原子 :b = y O 原子 :c = y + z S 原子 :c = z 原子總數 :a + b + 5c = x + y + z 依電荷不滅知 : 6 個未知數, 須立 6 個數學式聯立, 解聯立方程式得 a =,b =,c =,x =,y =,z =, 即均衡反應式為 類題 將鋁金屬與氫氧化鈉反應會產生氫氣, 其反應式如下 : Al + O + O Al(O) + ( 未平衡 ), 若平衡其係數至最簡整數, 則其係數總和為何? 答 均衡反應式為 56 基礎化學 ( 一 )
10 化學計量的流程可簡示如下 : 參 化學計量 一 化學計量的意義 命題指數 化學反應前後, 針對反應物與生成物的質量和莫耳數, 進行定量的計算, 稱為化學計量 二 化學計量的解題步驟及要領 : 莫耳數法 命題指數 寫出平衡反應式 將已知物的量換算成莫耳數, 其方法為 : 莫耳數 (n)= 重量分子量 ( 原子量 ) 粒子個數 0 atm 氣體體積升數 = = = 莫耳濃度 溶液體積升數 若題目有多個已知物的莫耳數時, 需先尋找何者為, 其方法為 : 各反應物以 莫耳數係數 比值最小者為限量試劑 利用反應式的係數比等於反應時莫耳數比, 由已知物 ( 指限量試劑 ) 之莫耳數, 推求待測物的 莫耳數, 其方法為 : 待測物的莫耳數 = 已知物的莫耳數 待測物的係數已知物的係數 5 最後將待測物的莫耳數換算成題目所要求的量 化學反應中被完全用完的反應物可決定生成物的產量, 此種被完全用完的反應物稱為限量試劑 BLOG 三 化學計量的相關名詞 命題指數 理論產量 : 限量試劑完全作用後, 根據反應式係數計算所得產物的最大量 實際產量 : 化學反應完成後實際所得的產物的量 產率 (%) = 實際產量理論產量 00 % 原子使用效率 (%) = 目標產物的質量所有產物的總質量 00 % 範例 9 均衡反應式的意義完全燃燒 x 莫耳正丁烷得 y 莫耳二氧化碳時, 下列 x 與 y 間的關係, 何者為正確? x = y y = x x = y y = x 第 單元 化學反應 57
11 答蚲 解 正丁烷完全燃燒的平衡反應式為 平衡反應式的係數比 = 反應莫耳數比 = 反應分子數比 = 同溫 同壓下反應氣體體積比 正丁烷莫耳數 : 二氧化碳莫耳數 = x:y = :8 y = x 範例 0 反應式的係數與化學計量 在固定體積的密閉容器內, 置入 X 和 Y 兩種氣體反應物後, 會生 成一種 Z 氣體產物, 右圖表示反應物和產物的濃度隨反應時間的 變化關係 下列哪一項可表示 X 和 Y 的化學反應式? X + Y Z X + Y Z X + Y Z X + Y Z X + Y Z 95 學測 M X Y Z 答 解反應時的莫耳數比 = 係數比 0 ~ 80 秒時反應莫耳數比 X:Y:Z = ( ):( ):( ) = :: 化學反應式為 X + Y Z 類題 在一密閉容器內, 等莫耳數的 X 和 Y 進行下列反應 : X(g) + Y(g) XY(g) 達成平衡 下列哪一個圖最能代表在此過程中,X 和 XY 的濃度隨時間變化的情形? 9 學測補考 XY X 產生 O 之莫耳數 剩餘 S 之莫耳數 XY X X XY (mol)x XY 答 䕷 同一時間間隔,X 減少濃度 :XY 增加濃度 = : 範例 化學計量與限量試劑 銀器在硫化氫存在的空氣中發生右列反應 : Ag + S + O AgS + O, 則.6 克銀 6.8 克硫化氫和. 克氧的混合物完全反應, 下列敘述哪些正確?(Ag = 08) Ag 為限量試劑 可得 0. 莫耳之 Ag S O 為限量試劑 產生 0. 莫耳的 O S 殘留 0. 莫耳 答 蚲 解反應式 Ag + S + O Ag S + O 莫耳數 = 0.mol 0.mol 0.mol 蚒 ( 莫耳數 / 係數 ) 最小者為限量試劑 Ag 為限量試劑 虲產生 Ag S 之莫耳數 (mol) 58 基礎化學 ( 一 )
12 類題 已知醋酸與乙醇在濃硫酸的催化下可進行如下的反應 : CCOO + CO 5 CCOOC5+ O 今各取 0 克的醋酸及乙醇合成乙酸乙酯, 經蒸餾純化得 克的乙酸乙酯, 下列敘述何者錯誤? 醋酸為限量試劑 最多可生成 0.5 莫耳乙酸乙酯 乙酸乙酯的產率為 0 % 乙酸乙酯的產率為 5 % 答 範例 混合物反應的化學計量 BaCO 和 CaCO 的混合物 6.9 克, 經加熱使其放出 CO 後得 BaO 和 CaO 的混合物.7 克 則原混合物中含有 BaCO 多少克?(Ba = 7,Ca = 0) 答 解混合物的反應, 需列出個別反應式, 利用係數比等於莫耳數比, 依題意列出數學式而解之, 設 BaCO 有 x mol, CaCO 有 y mol; 式量 BaCO = 97,CaCO = 00,BaO = 5,CaO = 56, 則反應式為 : 類題使丙烷和丁烷的混合氣體完全燃燒時, 得二氧化碳.7 克和水.98 克 該混合氣體中丙烷與丁烷之莫耳數比約若干? 答 : 範例 化學計量在常溫常壓, 未知體積之氧氣與 0 公升的一氧化碳, 在催化劑的存在下進行反應 反應後氣體之組成為二氧化碳與氧氣, 總體積為 70 公升 若反應後, 溫度與壓力維持不變, 則氧氣在反應 前 反應後的體積分別是多少公升? 䕷 60 0 虲 50 0 蚒 0 0 蚲 0 50 蛯 0 60 答虲解 0 學測 反應前與反應後, 氧的體積分別為 50 與 0 第 單元 化學反應 59
13 類題 50 atm 下, 取 升之某有機化合物氣體, 燃燒耗去 O 升, 則該化合物之分子式為哪些? C C C 6 C 6 O C O 答虲蚲範例 多步驟反應從鐵礦煉鐵製鐵的過程中涉及下列兩個化學反應 : C + O CO ; Fe O + CO Fe + CO () s ( g) ( g) () s ( g) () s ( g) 若第一個反應式中所產生的一氧化碳全部用於第二個反應式, 則欲產生 00 公斤的鐵, 須氧若干公斤?( 原子量 :Fe = 56,O = 6,C = ) 答.86 公斤 解 Fe 與 O 之莫耳數比, 得 x =.86( 公斤 ) 肆 化學反應中的能量變化 一 反應熱 命題指數 化學反應所伴隨的能量變化 定義 : 定溫 定壓下, 化學反應前後熱含量的變化, 通常 以 Δ 表示 Δ = 的總熱含量 - 的總熱含量 化學反應有些是吸熱, 有些是放熱 吸熱反應 :Δ > 0 放熱反應 :Δ < 0 各物質生成時, 儲存於其中的能量, 稱 為熱含量, 以 表示 >0 熱化學反應式 放熱反應 : 將反應熱加在生成物一邊或 Δ 取負值, 寫在反應式後面 例如 :Mg + O MgO + 0 kj 或 Mg + O MgO T = 0 kj () s ( g) () s <0 () s ( g) () s 吸熱反應 : 將反應熱加在反應物一邊或 Δ 取正值, 寫在反應式後面 例如 : NaCO + 85 kj NaCO + CO + O 或 () s () s ( g) () l NaCO Na CO + CO + O T =+ 85 kj () s () s ( g) () l 60 基礎化學 ( 一 )
14 反應熱與溫度及壓力有關, 在標準狀態 (5 atm) 下測得的反應熱, 稱為 標準反應熱, 以 Δ 0 表示 二 反應熱的種類 命題指數 莫耳生成熱 : 在 5 atm 下, 莫耳化合物由其成分元素生成時之反應熱 例如 : ( g) + I() s I( g) T =+ 5.9 kj / mol C + C T = 7. 8 kj / mol () s ( g) ( g) 莫耳生成熱可為放熱或吸熱 在標準狀態 (5 atm) 下之莫耳生成熱規定為零 若有同素異形體, 則訂定存量最多或最穩定之同素異形體為零, 如碳取石墨, 硫取斜方硫 (S 8 ), 磷取白磷 (P ), 氧取氧 (O ) 為零 莫耳燃燒熱 : 在 5 atm, 莫耳物質完全燃燒的反應熱 例如 :C + O CO T = 9 kj / mol () s ( g) ( g) C + O CO + O T = 890 kj / mol ( g) ( g) ( g) () l 莫耳燃燒熱必為 之物質, 其莫耳燃燒熱訂為零, 如 CO O N O e Fe O 等 若元素的狀態並不是在 5 atm 下應有的狀態, 其莫耳生成熱不為零 例如 :O () l Br ( g) g () s 之莫耳生成熱不為零 燃燒一般指物質與氧化合產生光及熱的現象, 因此必為放熱反應, 且物質須完全燃燒放出的 熱量才能為燃燒熱 例如 :C () s + O( g) CO( g) Δ= -0 kj, 此 Δ 稱 CO 莫耳生成熱, 非 C 之莫耳燃燒熱 元素的燃燒熱也是其燃燒產物的生成熱 例如 :C + O CO Δ= -9 kj, 此 Δ 是碳的莫耳燃燒熱, 亦為二氧化碳莫耳 () s ( g) ( g) 生成熱 BLOG 範例 5 反應熱 右圖為 A + B C +D 反應之熱含量變化圖,Δ 表示該反應之 反應熱, 則此反應的反應熱值為多少? Δ = kj Δ = + 00 kj Δ = + 00 kj Δ = - 00 kj kj 500 A+B 00 C+D 答 解反應熱 (Δ)= 生成物熱含量 ( 生 )- 反應物熱含量 ( 反 ) Δ = = -00( kj) 第 單元 化學反應 6
15 範例 6 反應熱與物質狀態已知乙醇燃燒有下列幾種反應 : CO + O CO + O + QkJ ; C O + O CO + O + Q kj 5 ( g) ( g) ( g) ( g) 5 () l ( g) ( g) ( g) CO + O CO + O + QkJ ; C O + O CO + O + Q kj 5 ( g) ( g) ( g) () l 5 () l ( g) ( g) () l 其中 Q Q Q Q 為熱量, 試比較它們之間的大小關係 答 Q >Q >Q >Q 解嫎若反應式相同, 而相態不同之反應, 欲比較其反應熱大小, 常利用位能圖來解題, 娋 上述四反應的位能圖如右 : (x 為乙醇莫耳汽化熱 ) 化學變化 (y 為水莫耳汽化熱 ) 䊼水的沸點 00, 乙醇沸點 78, 沸點愈高, 莫耳汽化熱愈大 y > x,y > x 又化學變化比物理變化熱效應大, 故 Q > Q > Q > Q 類題 已知 :(g) + O(g) O (g), T = 8kJ 有關此熱化學反應式的敘述, 下列何者正確? O ( g ) 的莫耳生成熱為 8kJ 此反應的能量變化可使周遭的溫度上升 O ( g ) 所含的能量比 ( ( g ) + O ( g ) ) 所含的能量高出 8kJ 若此一反應的產物是 O ( l ), 則反應的能量變化小於 8kJ 使 莫耳 O ( l ) 分解成 莫耳 ( g ) 與 莫耳 O ( g ) 時會吸熱 8kJ 答 範例 7 反應熱的種類下列有關反應熱的敘述, 何者正確? ( g ) 的莫耳燃燒熱與 O ( l ) 的莫耳生成熱同值異號 石墨的標準莫耳生成熱為零 C (s) + O (g) CO (g),δ = - 0 kj 為 C ( s ) 的莫耳燃燒熱 CO (g) + O CO (g) (g), 則反應之反應熱可稱為 CO 的莫耳生成熱 CO O O 的標準莫耳燃燒熱均為零答虲解 ( g ) 的莫耳燃燒熱與 O ( l ) 的莫耳生成熱之反應式相同, 故兩者反應熱同值同號蚒 C ( s ) 的莫耳燃燒反應為 蚲, 該反應之反應熱稱為 CO 莫耳燃燒熱 蛯 CO 為可燃性氣體, 標準莫耳燃燒熱不為零 6 基礎化學 ( 一 )
16 類題 下列何者物質之標準莫耳生成熱為零? CO ( g ) O ( g ) Fe ( s ) O ( g ) Br ( g ) 答 三 反應熱的三大重要定律 命題指數 由反應熱與反應的莫耳數成正比, 即反應式係數為 n 倍,Δ 亦為 n 倍 例如 : O O 85.8kJ (g) + (g) (l) T = + O O T = ( 85.8 )kj (g) (g) (l) # 反應以反方向進行, 反應熱同值異號, 即反應式逆寫,Δ 值變號 例如 : C + O CO = 9kJ (s) (g) (g) T CO C + O =+ 9kJ (g) (s) (g) T 赫斯定律 ( 或稱反應熱加成性定律 ): 若一反應可由兩個以上反應式的代數和表示時, 則其反應 熱也等於此數個反應熱的代數和, 此稱赫斯定律 例如 :A D 進行有兩種途徑 路徑 Ⅰ: A D 路徑 Ⅱ: A B +) B C C D A D T T T T T = T + T + T B A C D由上知路徑 Ⅰ 與路徑 Ⅱ 雖然反應過程不同, 但兩者最初狀態與最後狀態相同, 故反應熱相同, 與反應進行的路徑無關 四 反應熱的計算 命題指數 由反應熱的三大定律 反應式相加相減逆寫乘 n 倍 反應熱 T + T T T T n T 代入公式法 反應熱 Δ = ( 生成熱總和 ) - ( 生成熱總和 ) Δ = ( 燃燒熱總和 ) - ( 燃燒熱總和 ) 範例 8 赫斯定律 已知 C + C Δ = -.8 千卡 ; C + O CO Δ = 千卡 () s ( g) 8( g) () s ( g) ( g) ( g) + O( g) O () l Δ = 千卡 則丙烷之燃燒熱放熱值為多少千卡 / 莫耳? 第 單元 化學反應 6
17 答 解 方法一 赫斯定律 方法二 代公式法 : 反應熱 = 生成物總生成熱 - 反應物總生成熱 莫耳生成熱 莫耳燃燒熱類題反應熱 Δ = 反應物總燃燒熱 - 生成物總燃燒熱 x = - (kcal), 題目問燃燒熱,Δ 中的負值可省略利用下列熱化學方程式 : ( g) + O( g) $ O () l + 68 kcal ; C() s + O( g) $ CO( g) + 9 kcal ; C() s + ( g) $ C( g) + 8 kcal 求得 莫耳甲烷完全燃燒的反應熱為多少 kcal? 0 80 答 範例 9 反應熱的計量氫氣的莫耳燃燒熱為 kJ 莫耳液態過氧化氫分解成氧氣與液態水時放出 96.kJ 能量 下列敘述何者錯誤? 當 克液態過氧化氫分解成氧氣和液態水時, 可放出.89kJ 能量 液態過氧化氫的莫耳生成熱為 kJ 當 莫耳氫完全燃燒時, 可放出 85.8kJ 能量 液態過氧化氫分解為水及氧氣的熱化學方程式中的 Δ 應為負值 86 日大 答 解依題意知 : 反應熱 Δ = 生成物總生成熱 - 反應物總生成熱 由式 ( 莫耳生成熱 ) O 莫耳生成熱 = (kJ) 由式 Δ = ( 莫耳生成熱 ) 放熱反應 Δ 為負值 6 基礎化學 ( 一 )
18 範例 0 反應熱的應用有一暖暖包內含 00 毫升的水, 暖暖包中另有一塑膠袋子, 內裝有 0 克氯化鈣 使用時稍微用力敲打暖暖包, 使其中之塑膠袋破裂, 讓水與氯化鈣混合 已知氯化鈣的溶解熱為 kj / mol, 而水的比熱為.0 Jg - K - 假設氯化鈣的比熱甚小可以忽略, 而氯化鈣溶解所釋放出的熱量, 完全由 00 毫升的水所吸收 若在阿里山上, 取出一個 5 的暖暖包打開使用, 試問該暖暖包的溫度最高可升到幾?( 原子量 :Ca = 0,Cl = 5.5) 指考 答 解嫎 0 克氯化鈣溶於水放出熱量 (J) 娋假設暖暖包最高溫度到 t, 則 00 毫升水吸收熱量 䊼溶解釋出的熱量 = 水溫升高吸收的熱量, 解得 t = 76 一 基礎試題 鋫含甲烷和乙烷的混合氣體, 完全燃燒後, 得二氧化碳 6. 克及水 8.0 克 則該混合氣體 中, 甲烷 乙烷的莫耳數比為若干?( 原子量 : =,C =,O = 6) : : : : 蛯 : 鋳取氮 8 克和氫 8 克充分反應後, 共得到氨重.8 克, 則此反應之產率為多少? 9% 70% 6% 5% 鋴 0. 克的化合物 (M ) 和水發生下列反應 : M + O MO ( ) +, 若 () s () l () s ( g) 在 0 一大氣壓時, 可產生乾燥氫氣 8 毫升, 則 M 的原子量應是多少? 7 0 鋽已知 Mg, (s) + O (g) MgO (s) T = 60kJ, 則下列敘述哪些正碓?(Mg =,O = 6) ( 應選三項 ) 此為放熱反應 生成 克氧化鎂時, 放出 5. kj 的熱量 蛯氧化鎂為白色粉末, 溶於水, 水溶液呈酸性 此為吸熱反應 欲放出 00 kj 能量需燃燒鎂 克 鍃下列哪一反應可用來表示 N Cl () s 之莫耳生成反應式? N ( g) + ( g) + Cl( g) NCl() s N + + Cl NCl N + Cl NCl N + Cl NCl ( g) ( g) () s 鎄下列哪些所含碳的重量百分率相等?( 應選三項 ) ( g) ( g) ( g) () s ( aq) ( aq) () s C COO C 6 O 6 C O C 5 O COOC 第 單元 化學反應 65
19 鎭某有機化合物含 C O, 取 0.8g 燃燒, 先通過灼熱的氧化銅, 再通過 Mg( ClO ) 管, 重量增加 7.g, 又通過 NaO 管時, 重量增加 0.8g, 另由實驗測出量該有機物之分子 量為 08 則下列敘述何者錯誤? 實驗式為 C 7 8 O 分子式為 C 7 8 O 氧化銅的功能是使有機物完全燃燒 Mg( ClO ) 的功能為吸收 CO NaO 可用 KO 取代 䥅下列何項物質的化學式是以示性式表示? 乙醇 (C 6 O) 乙酸 ( C C O O ) 乙醛 C CO 食鹽 (NaCl) 水 ( O ) 䥑在 000mL 的氧氣中進行放電, 以產生臭氧 (O O ) 反應後, 在同溫同壓下, 其體積變為 900mL, 則下列哪些正確?( 應選三項 ) 生成臭氧 00mL 生成臭氧 00mL 剩餘氧氣 800mL 剩餘氧氣 700mL 蛯反應後臭氧的莫耳數占混合氣體總莫耳數的 9 麿某氣態烴 C x y O 0mL 完全燃燒, 需消耗同溫同壓下 O 0mL, 則該烴的分子式為何? C O C 6 O C O C 8 O 蛯 C 6 O 鐗某脂肪酸之通式為 C n no, 分析得碳的重量百分率為 5.5 %, 求 n 值為何? 5 6 蛯 7 匁某固體試樣含碳酸鈣與硫酸鎂之混合物 9. 克, 加熱時 CaCO(s) CaO(s) + CO(g), 硫酸鎂不因加熱分解, 若其中 CaCO 完全分解後, 試樣固體重量剩下 6.0 克, 則原混合物中 CaCO 的重量百分率約為多少?( 原子量 :Ca = 0,C =,O = 6) 8% 5% 70% 77% 蛯 90% 鐝二氧化錳 (MnO ) 加熱分解, 僅產生氧氣與一種純物質固體 ; 現有.6 克的二氧化錳, 加熱後, 剩餘的固體重.9 克, 則產生的固體化學式為何?(Mn = 55) MnO Mn O Mn O Mn O 5 鐭關於反應熱的敘述, 下列何者正確? 正反應的反應熱和逆反應的反應熱大小相等, 符號相反 如果反應熱為正值, 則為吸熱反應, 該反應不可能發生 反應熱加成定律說 : 反應熱和起始狀態 最終狀態以及物質變化的途徑有關 反應熱為分子動能變化的表現 鐾碳化鈣 (CaC, 俗稱電石 )96 克加水 7 克生成乙炔 (C ) 氣體, 其化學方程式為 : CaC(s) + O(l) C(g) + Ca(O ) (aq) ( 尚未平衡 ), 下列敘述哪些正確?( 應選三項 ) ( 原子量 :Ca = 0,O = 6,C =, = ) 最簡整數平衡係數總和為 理論上至多可生成乙炔 mol 反應後, 理論上剩下 O 8 克 產生的乙炔在 S.T.P. 時的體積為.6 升 若產生的乙炔在 S.T.P. 時的體積僅為. 升, 則產率為 66.7 % 66 基礎化學 ( 一 )
20 二 歷屆試題 在實驗室中可藉氯酸鉀分解反應製氧, 藉碳酸鈣分解產生二氧化碳, 汽車的安全氣囊則利用汽車 遭強力撞擊時, 引發三氮化鈉 (NaN ) 瞬間分解, 產生氮氣充滿氣囊, 達到保護作用 三氮化鈉 的分解反應為 NaN Na + N, 請回答第鋫 ~ 鋳題 (Na =,N = ) () s () s ( g) 鋫在常溫 常壓下, 若氮氣的莫耳體積是.5 升 / 莫耳, 則.0 克的三氮化鈉 ( 其式量為 每莫耳 65.0 克 ), 最多可產生多少升的氮氣? 鋳在常溫 常壓下, 三氮化鈉分解會放出.7 千焦耳 / 莫耳的熱量, 若此反應熱以 Δ 表 示, 則下列敘述, 何者正確? 三氮化鈉分解的熱化學反應式為 NaN Na + N +. 千焦耳 () s () s ( g) 三氮化鈉分解的熱化學反應式為 NaN Na + N +.7 千焦耳 () s () s ( g) 三氮化鈉分解的熱化學反應式為 NaN () s +.7 千焦耳 Na s + N 三氮化鈉分解反應的反應熱 Δ =.7 千焦耳 / 莫耳 () ( g) 9 學測補考 鋴已知 C 8 ( g) CO ( g) 和 O () l 之標準莫耳生成熱分別為 及 - 68 千卡, 則下列敘述哪些正確?( 應選二項 ) 每莫耳丙烷完全燃燒需消耗 5 莫耳氧氣 石墨之標準莫耳燃燒熱為 + 9 千卡 氫氣之標準莫耳燃燒熱為 - 千卡 丙烷之標準莫耳燃燒熱為 - 5 千卡 鑽石與石墨之莫耳燃燒熱相同 鋽在標準狀況下, 已知 CO 之標準莫耳生成熱為 kj, 且已知 : C + FeO Fe + CO,Δ = 6.6 kj () s () s () s ( g) 試問 :Fe O 之標準莫耳生成熱應為多少? 70 kj - 70 kj - 8. kj 9 指考 kj - 6. kj 9 指考 鍃尿素 ( N) CO( 分子量 = 60) 是工業上重要的化學原料, 也可作為農作物的肥料成分 由氨與二氧化碳反應可得尿素和水, 若在高壓反應容器內加入 克氨 ( 分子量 = 7) 與 66 克二氧化碳 ( 分子量 = ), 假設氨與二氧化碳完全反應後, 則下列有關此反應化學計 量的敘述, 哪幾項是正確的?( 應選三項 ) 平衡的化學反應式是 N + CO ( N ) CO + O 剩餘 8.5 克的氨未反應 剩餘 克的二氧化碳未反應 生成 60 克的尿素 生成 8 克的水 ( g) ( g) ( aq) () l 95 學測 鎄物質 X 燃燒時的化學反應式為 X+ O CO + O( 注意 : 只有產物的係數尚未平衡 ), 試問下列哪一個選項最有可能是 X? CO C C O C 5 O 95 指考 第 單元 化學反應 67
21 鎭某碳氫化合物. 克, 經完全燃燒後產生 6.6 克二氧化碳, 則此化合物最可能之分子式為何? C C 6 C C 8 C 0 95 指考䥅某些只含 C O 三種元素的有機化合物, 當 莫耳的該化合物完全燃燒時, 所需氧的莫耳數及所產生水的莫耳數, 均與 莫耳的甲烷完全燃燒時相同 試問下列化合物中, 哪些能滿足上述條件?( 應選三項 ) COO COOC C COO C 5 COO C (COO ) 96 指考䥑含有碳 氫 氧的化合物進行元素分析時, 須先將分析物完全氧化後, 再以不同的吸收管吸收所生成的二氧化碳及水蒸氣 下列有關元素分析實驗的敘述, 哪些是正確的?( 應選二項 ) 可用含水的過氯酸鎂吸收水蒸氣 可用氫氧化鈉吸收二氧化碳 化合物的含氧量, 可由所生成的水蒸氣及二氧化碳中的含氧量, 相加求得 由元素分析實驗, 可直接求得化合物的分子式 若以無水氯化亞鈷試紙檢驗實驗中所產生的水蒸氣, 則試紙呈粉紅色 97 指考 麿食品中的蛋白質含量, 可由測定其氮元素的含量來間接推算 臺灣在 97 年 9 月間發生的 毒奶 風波, 係不肖廠商在奶粉中添加三聚氰胺 ( 分子式 C 6 N 6, 分子量 6 g / mol), 以造成蛋白質含量較高的假象所導致 假設正常奶粉中的蛋白質, 其平均含氮量約 6.6%, 則三聚氰胺的含氮量約為正常奶粉中蛋白質平均含氮量的幾倍? 學測鐗已知蔗糖的分子量為 g / mol, 而其水溶液的發酵可用下列反應式表示 : C O + O C O+ CO 5 今取蔗糖. 克, 溶於水後, 加酵母使其發酵 假設只考慮蔗糖變為酒精的發酵, 且蔗糖的發酵只完成 50%, 則在此發酵過程中, 所產生的二氧化碳總共有幾毫升?( 在標準狀態下 ) 學測 匁下列有關化學式的敘述, 哪些正確?( 應選三項 ) 結構式可以表示化合物中原子間的排列情形 網狀固體因為沒有分子的單位, 所以無法以結構式表示 使用示性式的主要目的是補足分子式未能表示的官能基結構特性 從分子式可以得知分子中組成原子的種類 數目與原子連結順序 分子化合物的簡式 ( 實驗式 ) 可以從其元素分析數據及組成原子的原子量求得 98 指考 鐝四氧化二氮與甲聯胺 (C NN ) 的反應為登月小艇脫離月球返回地球時所用的動力來源 此二化合物反應的生成物為水 氮氣與二氧化碳 試問 : 此反應的平衡化學反應式中, 水與氮氣的係數比為何? : : : : : 98 指考 68 基礎化學 ( 一 )
22 鐭在一個體積可變的密閉容器內, 裝入氨氣 升 若在溫度與壓力不變的條件下使氨分解 : N(g) N(g) + (g) (N 係數未平衡 ), 試問當容器內氣體的體積由原來的 公升變成 公升時, 有多少百分比 (%) 的氨分解? 指考 鐾家用的瓦斯有天然氣 ( 主成分 C ) 或液化石油氣 ( 主成分 C 8 ) 若在同溫 同壓, 分 別使同體積的 C 與 C 8 完全燃燒, 則 C 8 所需氧氣的量是 C 的幾倍? 指考 䥪硝酸銅受熱分解, 可用右列反應式表示 : Cu( NO ) CuO + nx + O 為係數 試推出 X 是什麼化合物? T () s () s ( g) ( g), 式中 n NO NO N O N O N O 5 99 學測 鑔將 00.0mL 0.0M 的 Cl 溶液加於.g 的 Na CO 固體, 會產生氣泡 下列關於此反 應的敘述, 哪些正確?( 應選二項 ) 䕷此反應的平衡反應式為 : NaCO+ Cl NaCl + O + CO 虲若反應完全, 則可產生 0.88 克的 CO 蚒反應後會剩餘 0.0 莫耳的 Na CO 蚲此反應的限量試劑為 Cl 蛯此反應為沉澱反應 0 學測 鑹右圖的分子模型, 僅含碳氫氧氮四種元素, 圖中一短線連 結代表單鍵,= 短線連結代表雙鍵 有關此分子模型的敘 述, 哪些正確?( 應選二項 ) 䕷碳與氫的原子個數總和為 虲碳與氧的原子個數總和為 蚒氮與氧的原子個數總和為 蚲氮與氫的原子個數總和為 蛯碳與氮的原子個數總和為 9 0 學測 锭在一個密閉的容器中, 含有甲烷.6 克和氧氣 8.0 克 燃燒反應完全後, 則容器中所含的 分子總莫耳數為何? 學測 関一氧化碳和 Fe O 的化學反應式如下 : CO + Fe O Fe + CO, (g) (s) (s) (g) 試由下列三個反應式與赫斯定律, 計算上述反應的 (kj) Ⅰ Fe O + CO FeO + CO T = 8.5kJ (s) (g) (s) (g) Ⅱ Fe(s) + CO(g) FeO(s) + CO(g) T =.0kJ Ⅲ Fe O + CO FeO + CO T =.0kJ (s) (g) (s) (g) 下列哪一數值最接近計算的結果? 學測 第 單元 化學反應 69
23 䦧已知在標準狀態下,CO 與 CO 的莫耳生成熱分別為 - 0.kJ/mol 及 - 9.5kJ/mol 今有.0 克的碳燃燒後得 7.0 克的 CO 與.0 克的 CO, 則在此過程中, 約有多少熱量 (kj) 釋出? 學測 二鉻酸鉀 (K Cr O 7 ) 可用於檢測呼氣中的酒精濃度 酒精與 K Cr O 7 的反應式如下 : + + C CO+ CrO + 6 CCOO+ Cr + O 7 反應後, 顏色由橘紅變為綠, 經由儀器測得的數據可換算成酒 精濃度 在常溫 常壓下, 目前公認的血液中與呼氣中的酒精 濃度比例為 00: 法令規定每升呼氣中的酒精濃度不得超 過 0.5 毫克 已知呼氣中的酒精濃度與儀器所測得的變化量之 關係如右圖所示 請回答间 ~ 阳題 : 05 學測 间當某人呼氣造成的儀器上變化量為 0.80 時, 血液中的酒精濃度, 若以 M 計, 則最接近下 列哪一數值? 阳承上題, 此人呼氣中的酒精濃度是否超標? 是 否 不能確定 䧥硝酸銨 (N NO ) 受熱超過 00 時, 會完全分解產生水蒸氣 氮氣和氧氣 若將 0.0 克的硝酸銨, 加熱至完全分解, 至多會產生多少莫耳的氣體? 䕷.75 虲.50 蚒 5.5 蚲 學測 枠某一含有結晶水的草酸鎂 (MgC O $ n O ) 樣品.00 克, 若加熱至完全失去結晶水, 所 得無水草酸鎂的質量為 0.76 克, 則 n 的數值為何?(MgC O 的莫耳質量為 g/mol) 䕷 虲 5 06 學測 䨤已知在 5, 一大氣壓下, 氫氣與氧氣化合產生 莫耳液態水和氣態水的熱化學反應式 分別如下 : ( g) + O( g) O() l T = 85.8 kj + O O T =.8 kj ( g) ( g) ( g) 若在相同溫度與壓力下, 將 l.0 克的水直接汽化為水蒸氣, 則所需的能量 (kj) 最接近下 列哪一數值? 䕷.8.0. 蚲 學測 靀銅金屬溶於硝酸溶液的反應式如下 : Cu + NO Cu( NO ) + NO + O ( s) ( aq) ( aq) ( g) () l 若將 6.5 克銅線, 完全溶解於.00 M 的硝酸溶液, 則至少需要硝酸溶液, 約多少毫升? 䕷 蚲 學測 70 基礎化學 ( 一 )
24 Na 88 6 Y O(,6) 8 6 O 6 8 n n n= n = n = n= abcd a c a a 8 ( a ) a ( a 8 ) 7 a 0 c 8 c ( c ) c (c 8 ) 7 c b b b 8 b ( b ) ( b 8 ) 7 b 6 d 8 d d 6 C 7N Si Na Be Mg d ( d 8 ) (d ) 7 d Na Be Mg A 6A 7A A A6A7A A Li 6 C 0 Ne Mg 7 Cl 6 C 0 Ne 7 Cl 7 Cl 8 6 X 6 C 0 Ne A n X 0 X Y 9 0 Z 0 Z 9 W XYZW 096 XYZ W Na 0 Ca 9 F 6 S F 7 Na KLM 8 M Ca Ca F F CaF YZ Ca Ca S S CaS YW Na Na S S Na S X W SiO C O n n n W : W : W : : CO O 0
25 C COO C 6 O 6 x x = x # + # + 6 # 60 mol x x = # 6 + # + 6 # 6 80 mol Mg( ClO ) O NaO CO W # W 98. C # 0. 5 WO = = 0. 7 CO C O % 0.06 # 00%.55%. CO = : 006. : 07. : : 6 : 66. : =. : 6.6 :. = : : 6 C O % 00 % 0.% n # 56 # 00% n Fe O Fe% # = 56 # 00% = 70% # 56+ # 6 Fe O Fe% # = 56 # 00% = 7.% # 56+ # 6 FeS Fe% # = 56 # 00% = 6.7% # 56+ # Fe O Fe O FeS $ X (s) n O (g) X n O (s) T.6g 0.9g g X O n Na CO $ x O (s) n Na CO (s) 0.57g 0.g g Na CO O x x 0 T x O COzO CO O x y z x y COO COO CO K Cr O 7 K Cr O Cl KCrO7Cl KCl CrClCl7O N(g) N(g) (g) Fe O CO Fe CO (s) (g) (s) (g) C(O) O CO O 6 (aq) (aq) 6 (aq) (l) Ca(CO ) (s) Cl(aq) CaCl(aq) CO(g) O(l) C / C Ag(N ) NO AgC / CAg (g) (aq) (s) N NO N (aq) (g) Cu a x b y O c y z S c z a b 5c x y z b( + ) + c( ) = x( + ) 6 6 a b c x y z + + Cu + + SO Cu + O + SO Al + O + 6 O Al(O) + C0O 8CO0O xy 8 y x
26 0 80 XYZ ( )( )( 0. 0 ) X Y Z X XY Ag S O Ag S O mol 0.mol 0.mol Ag Ag S 0. # 0. mol O 0. # 0. mol S = # = 0. mol C COO CO 5 C COOC 0 = = g 00% # # 00% 5% 5 O BaCO x molcaco y mol BaCO 97CaCO 00BaO 5CaO 56 BaCO BaO CO xmol xmol xmol CaCO CaO CO ymol ymol ymol 97x + 00y = 6.9 ) 5x + 56y =.7 x 0.0 BaCO C 8 + xmol C + ymol 0 * 5O O CO + x CO + y + O + x + 5O + 5y CO : x y 7. + = mol O: x 5y = mol 8 x 0.05y 0.0 xy O(g) CO(g) CO(g) a a 0 0 ( a 0) + 0 = 70 a y y CxyOzO xco O z+ 6 = x+ C ) FeO 6C Fe O.86 O CO O 0 CO Fe Fe CO 6CO g g 00 # 0 Fe O : x # 0 : 56 x kJ Q Q Q Q CO 5 ( g) O( g) x kj CO 5 () l O( g) Q Q Q Q CO( g) O( g) y kj CO O C O CO 5 () l 5 ( g) ( g) ( l) T = xkj> 0 x O O T = ykj> 0 y () l ( g) y xy x Q Q Q Q O ( g ) 8 = kj/mol O ( g ) ( g ) O ( g ) 8kJ # # (g) +O (g) T= 8kJ O (g) O (l)
27 (g) + O(g) O(l) T < 8kJ O O > 8kJ (l) (g) (g) T ( g ) O ( l ) C ( s ) C(s) O(g) CO(g) CO (g) O(g) CO(g) CO CO 5atm (g) Fe (s) I (s) g () l O (g) Br ( l ) O C 8( g) C() s O( g) ) g O C 5O ( ) ( g) 8( g) ( g) C CO () s ( g) ( g) O () l CO O ( g) ( l) ) T = (. 8 ) T = 9. 0 T = 68. kcal # kcal # kcal # T = ( 8. ) + ( 90. ) # + ( 68. ) # = 50. kcal C 8 g + 5O g CO g + O l ( ) ( ) ( ) ( ) T = [ #( 9) + #( 68. )] [(. 8) # + 0 # 5 ] = 50. kcal C + C ( s) ( g) ( g) T 9 68 x 8 = [ ( 9) # + ( 68) # ] [ ( x) # ] x kcal ( g) + O( g) O( l) O O + O () l () l ( g) # # # = 8kJ T = kj T = 96. kj 96. #.89 kj 96. = ( 85.8) # O # O 87.6kJ O () l # = ( 85. 8) # = kj 0 # # J t 00 = 00 #. #( t 5 ) 0 # # # # = 00. ( t 5 ) t 76 C + O CO + O ; 7 C + O CO + O 6 xmol 0 0 y mol 0 0 x + x + x y y y x+ y = 6. x + y = 8 8 x0.y0. N + N 8 = 8 = %. 8 # # 00% 70% M x M 0. 8 # 0 = x 0 x+. 60 ] 5.kJ/g 00 # ] MgO O Mg(O) N () g () g Cl() g NCl() s C O C W W # C CO 0.8 # 8. W W # O 7. #
28 W = O W W C W = =.6 CO C 7 8 O n 08 ( ) C O Mg( ClO ) O ( g) O O 000 x 0 + x 000 x x 000 x x 900 x mL mL n O 00 n C O O xco y O x y y y + # = x+ x + = 7 # C% = n # 00% = 5. 5% n # n+ # n+ 6 # 9. CaCO x CaCO CaO CO xg 0 CaCO CO x # # 0.x 00 0.x ( ) x 7g CaCO % 7 # 00% ] 77% 9. T MnO Mn O O () s x y MnO Mn = 55.6 # = # O Mn O Mn O CaC O C Ca( O) 5 CaC = 5. mol O 7 8 = mol C + CaO ( ) ( g).5 #.5 mol O 5. # # 8 5 O = 7 5 = 8 S.T.P mol. 00% # # 00% 66. 7% 5. NaN Na () s () s N( g). N 0 # # NaN.7kJ mol NaN.7.kJ NaN Na N () s () s ( g).kj NaN Na () s () s N( g).kj C5O CO 8 O CO 9kcal O 68kcal = [ ( 9) # + ( 68) # ] [ ( ) # ] = 5 kcal Δ Δ C+O (g) C+O (g) CO Δ Δ 6.6 = [ #( 9.6 ) ] [ x # ] x 8.kJ N CO (N ) CO O CO # # CO 66 ( N) CO # #60 60 O # #8 8 CO O X C C O CO O C O O CO O COO CO 5 O W 6.6 # C C 0. 8 C 8 mol mol O C O CO O COO O CO O COOC O CO O C COO O CO O C COO 7 O CO 5 O C( COO ) O CO O
29 C 6 N 6 # N% 6 # 00% 66.7% 6 66.% 7 ] 6.% 6. V ( # 50% ) # # CO. # 0 8 ml C NN C O N 5N O C NN CO O 9N N N + (g) (g) (g) 0 0 x + x + x x x x x x x x 0.5 % 0.5 # # 00% 50% C O$ CO O * C5O $ COO 8 C C X N a O b N = n # a ) a O = + n # b+ b Na CO + Cl NaCl + O + CO # = 0.0mol = 0.0mol CO Na CO 0.0 mol C 9 O N C C C C C O C C O C N C C + O CO + O () g () g () g () l = 0. mol = 05. mol mol C O CO O ( g) ( g) ( g) ( l) = 05. mol 6 # ( ) # ) Fe O CO () s () g FeO CO Fe O Fe O () s () g CO () s () g CO () s () g Fe O Fe CO FeO CO () s () g () s () g CO () s () g Fe CO () s () g T = 8. 5kJ # T = kj # ( ) kj ) T = # T = 0. 5kJ. 0 mol CO = 7 = 05. mol + 6 CO = = mol + 6 # C + ( s) O( g) CO( g) T = 0. kj C + O CO T = 9. 5kJ ( s) ( g) ( g) = ( 0.) # ( 9.5) # 0.75 ].7 kj mg/l mg/l 80 # 0 C M = 6 L N NO N O O ( s) ( g) ( g) ( g) ] 0.08 M O N NO O O O O mol 7 mol mol N mol O mol O00 5
30 N NO #.75 mol MgC O n O 0.76 MgC O 0. O MgC O n O MgC O O n n 8 n ( g) O( g) O( l) T 85.8 kj ( g) O( g) O( g) T.8 kj O () l O ( g) T kj mol kj l.0 0. #. kj 8. 0 x Cu NO 65. x.00 # x 00 C CO 5 6 CO C C 6 C 8 C 0 C CO kcal/g kcal/ mol g / mol 68 = = C 08 = = 6 C 56 8 = =. 95 CO 8 5 = = 7. 6 = 99 =. 9 00g 80g 5g # # 560 = 50 kj = 50 = 500 kj / kg 00 # 0 kcal/g = kcal/ mol g / mol kcal g CO C kcal / g C CO = = = kcal/mol C CO 00 Pb( C 5 ) = 00 # 9% + 0 # 8% = = 5 # 0% + 00 # 90% = 9.5 PbSO 6
( )1. 已知 H 2 O (l) H 2(g) O 2(g) ΔH=285 kj C (s) +O 2(g) CO 2(g) ΔH=-394 kj C (s) +2H 2(g) CH 4(g) ΔH=-76 kj 則甲烷 (CH 4 ) 的莫耳燃燒熱為多少 kj? (A) 888 (
 ( )1. 已知 H 2 O (l) H 2(g) + 1 2 O 2(g) ΔH=285 kj C (s) +O 2(g) CO 2(g) ΔH=-394 kj C (s) +2H 2(g) CH 4(g) ΔH=-76 kj 則甲烷 (CH 4 ) 的莫耳燃燒熱為多少 kj? (A) 888 (B) 750 (C)-750 (D)-888 kj 答案 :(D) 解析 :H 2 O (L) H 2(g)
( )1. 已知 H 2 O (l) H 2(g) + 1 2 O 2(g) ΔH=285 kj C (s) +O 2(g) CO 2(g) ΔH=-394 kj C (s) +2H 2(g) CH 4(g) ΔH=-76 kj 則甲烷 (CH 4 ) 的莫耳燃燒熱為多少 kj? (A) 888 (B) 750 (C)-750 (D)-888 kj 答案 :(D) 解析 :H 2 O (L) H 2(g)
( )1. 關於氫氣的燃燒反應 :2H 2(g) +O 2(g) 2H 2 O (L) 的敘述, 下列何者正確? (A)ΔH 為正值 (B)1 atm 25 時, 此反應可以自然發生 (C) 生成物的熱含量總和較反應物的熱含量總和低 (D) 在 1 atm 100 時所放的熱量為標準反應熱 答案 :
 ( )1. 關於氫氣的燃燒反應 :2H 2(g) +O 2(g) 2H 2 O (L) 的敘述, 下列何者正確? (A)ΔH 為正值 (B)1 atm 25 時, 此反應可以自然發生 (C) 生成物的熱含量總和較反應物的熱含量總和低 (D) 在 1 atm 100 時所放的熱量為標準反應熱 答案 :(C) 解析 :(A) 燃燒為放熱反應,ΔH 必為負值 (B) 燃燒需點火, 溫度達到燃點, 才能發生燃燒反應,
( )1. 關於氫氣的燃燒反應 :2H 2(g) +O 2(g) 2H 2 O (L) 的敘述, 下列何者正確? (A)ΔH 為正值 (B)1 atm 25 時, 此反應可以自然發生 (C) 生成物的熱含量總和較反應物的熱含量總和低 (D) 在 1 atm 100 時所放的熱量為標準反應熱 答案 :(C) 解析 :(A) 燃燒為放熱反應,ΔH 必為負值 (B) 燃燒需點火, 溫度達到燃點, 才能發生燃燒反應,
答案 :(D) 解析 :C H 4 +3O CO +H O C H 6 O+3O CO +3H O C 3 H 8 O+(9/)O 3CO +4H O C 3 H 4 +4O 3CO +H O C 3 H 8 +5O 3CO +4H O 所以需要的 O, 以 C 3 H 8 最多 ( )7. 肼和四
 ( )1. 在下列反應中, axo4 by ch dx ey 8HO, 方程式係數 b d 分別為 (A)5,6 (B)10, (C)6, (D)10,5 答案 :(B) 解析 : 先平衡 O( 右邊 8 個 O), 再平衡 X( 左邊 個 X) d= 再平衡 H( 右邊 16 個 H) 得 XO 4 - +by - +16H + X + +ey +8H O 再平衡電荷 :--b+16=x=4 b=10,
( )1. 在下列反應中, axo4 by ch dx ey 8HO, 方程式係數 b d 分別為 (A)5,6 (B)10, (C)6, (D)10,5 答案 :(B) 解析 : 先平衡 O( 右邊 8 個 O), 再平衡 X( 左邊 個 X) d= 再平衡 H( 右邊 16 個 H) 得 XO 4 - +by - +16H + X + +ey +8H O 再平衡電荷 :--b+16=x=4 b=10,
AL O 2SiO 2H O AL O 2SiO + 2H O CaCO3 + CaO CO2 CaSO4 + CaO SO3 CaSO3 + CaO SO2 2AL O + 6SiO 3AL O 2SiO + 4SiO
 AL Si O OH 4 2 2 5 K AL Si O 2 3 8 2 3 8 2 3 8 Na AL Si O Ca AL Si O AL O 2SiO 2H O AL O 2SiO + 2H O 2 3 2 2 2 3 2 2 CaCO3 + CaO CO2 CaSO4 + CaO SO3 CaSO3 + CaO SO2 2AL O + 6SiO 3AL O 2SiO + 4SiO 2 3 2
AL Si O OH 4 2 2 5 K AL Si O 2 3 8 2 3 8 2 3 8 Na AL Si O Ca AL Si O AL O 2SiO 2H O AL O 2SiO + 2H O 2 3 2 2 2 3 2 2 CaCO3 + CaO CO2 CaSO4 + CaO SO3 CaSO3 + CaO SO2 2AL O + 6SiO 3AL O 2SiO + 4SiO 2 3 2
99710b45zw.PDF
 1 2 1 4 C && Zn H H H H H Cl H O H N H H H CH C H C H 3 2 5 3 7 H H H H CH 3 C2H 5 H H H O H H O K K O NO 2 H O NO 2 NO O 2 C2H5 H O C2H5 C H O C2H3 2 5 H H H O H H O 1826 O
1 2 1 4 C && Zn H H H H H Cl H O H N H H H CH C H C H 3 2 5 3 7 H H H H CH 3 C2H 5 H H H O H H O K K O NO 2 H O NO 2 NO O 2 C2H5 H O C2H5 C H O C2H3 2 5 H H H O H H O 1826 O
基 礎 化 學 ( 一 ) 講 義 目 次 第 1 章 物 質 的 組 成 1 1 物 質 的 分 類 1 1 2 原 子 與 分 子 16 1 3 原 子 量 與 分 子 量 31 1 4 溶 液 48 實 驗 二 硝 酸 鉀 的 溶 解 與 結 晶 74 國 戰 大 考 試 題 78 實 驗 相
 內 容 由 蔡 明 倫 老 師 和 李 雅 婷 老 師 編 纂 基 礎 化 學 ( 一 ) 講 義 第 1 章 物 質 的 組 成 班 級 : 拉 瓦 節 和 其 使 用 的 實 驗 儀 器 座 號 : 姓 名 : 基 礎 化 學 ( 一 ) 講 義 目 次 第 1 章 物 質 的 組 成 1 1 物 質 的 分 類 1 1 2 原 子 與 分 子 16 1 3 原 子 量 與 分 子 量 31 1
內 容 由 蔡 明 倫 老 師 和 李 雅 婷 老 師 編 纂 基 礎 化 學 ( 一 ) 講 義 第 1 章 物 質 的 組 成 班 級 : 拉 瓦 節 和 其 使 用 的 實 驗 儀 器 座 號 : 姓 名 : 基 礎 化 學 ( 一 ) 講 義 目 次 第 1 章 物 質 的 組 成 1 1 物 質 的 分 類 1 1 2 原 子 與 分 子 16 1 3 原 子 量 與 分 子 量 31 1
(CIP) : / :,, :,2000.5 ISBN 7-04 - 008822-3 - - N - 42 CIP (2000)60397 55 100009 010-64054588 010-64014048 / 8501168 1/ 32 7.875
 ( ) (CIP) : / :,, :,2000.5 ISBN 7-04 - 008822-3 - - N - 42 CIP (2000)60397 55 100009 010-64054588 010-64014048 http:/ / www.hep.edu.cn 8501168 1/ 32 7.875 190 000 8.40, ( ) 1 16 16 16 18 21 22 24 24 24
( ) (CIP) : / :,, :,2000.5 ISBN 7-04 - 008822-3 - - N - 42 CIP (2000)60397 55 100009 010-64054588 010-64014048 http:/ / www.hep.edu.cn 8501168 1/ 32 7.875 190 000 8.40, ( ) 1 16 16 16 18 21 22 24 24 24
zyk00124zw.PDF
 A B=AB( ) AB=AB( ) 4P 50 2 === 2P 2 O 5 2KClO 3 2KCl 3O 2 NH 3 H 2 O CO 2 =NH 4 HCO 3 2KMnO 4 K 2 MnO 4 MnO 2 O 2 CO CO 2 ( ) 1.250 / 1.977 / 1 1 1 0.02 2CO O2 2CO 2 CO CuO Cu CO 2 CO 2 C 2CO Ca(OH) 2
A B=AB( ) AB=AB( ) 4P 50 2 === 2P 2 O 5 2KClO 3 2KCl 3O 2 NH 3 H 2 O CO 2 =NH 4 HCO 3 2KMnO 4 K 2 MnO 4 MnO 2 O 2 CO CO 2 ( ) 1.250 / 1.977 / 1 1 1 0.02 2CO O2 2CO 2 CO CuO Cu CO 2 CO 2 C 2CO Ca(OH) 2
1 { ph
 !!!!!!!!!!!!!!!!!!!!!!!!!!! 1 1!!!!!!!!!!!!!!!!!!!!!! 1 2!!!!!!!!!!!!!!!!!!!!!!!!!! 7 3!!!!!!!!!!!!!!!!!!!!!!!!! 15 4!!!!!!!!!!!!!!!!!!!!!!!!!!! 21!!!!!!!!!!!!!!!!!!!!!!!!!!!! 30!!!!!!!!!!!!!!!!!!!!!!!
!!!!!!!!!!!!!!!!!!!!!!!!!!! 1 1!!!!!!!!!!!!!!!!!!!!!! 1 2!!!!!!!!!!!!!!!!!!!!!!!!!! 7 3!!!!!!!!!!!!!!!!!!!!!!!!! 15 4!!!!!!!!!!!!!!!!!!!!!!!!!!! 21!!!!!!!!!!!!!!!!!!!!!!!!!!!! 30!!!!!!!!!!!!!!!!!!!!!!!
FeS 2 在 晶 體 中 為 Fe 2+ S 22ˉ 故 選 (A) 4. 下 圖 代 表 某 反 應 座 標 圖, 下 列 敘 述 何 者 錯 誤? (A) B - A 為 活 化 能 (B) A - C 為 反 應 熱 (C) B 代 表 活 化 錯 合 物 的 相 對 能 量 (D) B -
 1. 在 含 有 0.050 M MgCl 2 及 1.0 M 氨 的 1.00 升 水 溶 液 中, 頇 加 入 多 少 克 的 氯 化 銨, 才 能 使 鎂 的 鹽 類 不 沉 澱? Mg(OH) 2 的 K sp 為 1.5 10-11,NH 3 的 K b 為 1.8 10-5 (A) 50 g (B) 56 g (C) 5.0 g (D) 4.3 g 答 案 :(B) [Mg 2+ ] =
1. 在 含 有 0.050 M MgCl 2 及 1.0 M 氨 的 1.00 升 水 溶 液 中, 頇 加 入 多 少 克 的 氯 化 銨, 才 能 使 鎂 的 鹽 類 不 沉 澱? Mg(OH) 2 的 K sp 為 1.5 10-11,NH 3 的 K b 為 1.8 10-5 (A) 50 g (B) 56 g (C) 5.0 g (D) 4.3 g 答 案 :(B) [Mg 2+ ] =
Microsoft Word - Z8I11A0-102.doc
 自 然 考 科 學 測 試 題 關 鍵 解 析 前 言 物 理 科 今 年 自 然 科 考 題 共 68 題, 其 中 物 理 科 占 了 17 題, 今 年 的 題 目 難 度 屬 中 偏 易, 考 題 分 配 十 分 平 均 由 於 是 新 課 綱 第 一 次 學 測, 所 以 新 的 內 容 大 致 上 均 入 題, 大 都 為 物 理 科 普 知 識 就 算 是 第 二 部 分 的 考 題,
自 然 考 科 學 測 試 題 關 鍵 解 析 前 言 物 理 科 今 年 自 然 科 考 題 共 68 題, 其 中 物 理 科 占 了 17 題, 今 年 的 題 目 難 度 屬 中 偏 易, 考 題 分 配 十 分 平 均 由 於 是 新 課 綱 第 一 次 學 測, 所 以 新 的 內 容 大 致 上 均 入 題, 大 都 為 物 理 科 普 知 識 就 算 是 第 二 部 分 的 考 題,
第三章化學計量
 第三章化學計量 1 第三章化學計量 3-1 化學式 化學式是以原子種類 ( 元素符號 ) 及原子個數來表示物質的組成, 分為 : 實驗式 分子式 結構式 示性式 路易斯結構式 ( 電子點式 ) 分子模型 一 實驗式 : 簡式 1. 實驗式只能顯示出物質粒子所含的原子種類及原子個數比, 但不知真正組成的原子數 (1) 由元素分析找出各成分元素的原子數比 ( 最簡單整數比 ), 可寫出實驗式 2. 不是以分子狀態存在的物質,
第三章化學計量 1 第三章化學計量 3-1 化學式 化學式是以原子種類 ( 元素符號 ) 及原子個數來表示物質的組成, 分為 : 實驗式 分子式 結構式 示性式 路易斯結構式 ( 電子點式 ) 分子模型 一 實驗式 : 簡式 1. 實驗式只能顯示出物質粒子所含的原子種類及原子個數比, 但不知真正組成的原子數 (1) 由元素分析找出各成分元素的原子數比 ( 最簡單整數比 ), 可寫出實驗式 2. 不是以分子狀態存在的物質,
99600936zw.PDF
 附 录 相对原子质量表 按照元素符号的字母次序排列 ( ) ( ) ( ) [ 1 1] ( 1 1) ( ) [ 1 2] ( ) [ 1 3] ( 1 3) [ 1 4] ( ) 4 1 2 3 4 [ ] 1 2 (1) (2) (3) (4) (5) (6) 3 0 1535 232 ( ) 101.325 101.325 100 357 2750 / 3 / 3 7.8 / 3 2.7
附 录 相对原子质量表 按照元素符号的字母次序排列 ( ) ( ) ( ) [ 1 1] ( 1 1) ( ) [ 1 2] ( ) [ 1 3] ( 1 3) [ 1 4] ( ) 4 1 2 3 4 [ ] 1 2 (1) (2) (3) (4) (5) (6) 3 0 1535 232 ( ) 101.325 101.325 100 357 2750 / 3 / 3 7.8 / 3 2.7
中國的煤
 課內活動及課後練習的建議答案 課內活動 討論區 ( 3 頁 ) 1 2 網上追蹤 ( 5 頁 ) 2008 年末世界各地煤的蘊藏量地區 蘊藏量 ( 百萬公噸 ) 佔全球的百分比 097 29.8% 15 00 1.8% 272 33.0% 1 38 0.2% 32 013 3.9% 259 253 114 500 31.4% 13.9% 82 001 100.0% 272.2.1 15.0 32.0
課內活動及課後練習的建議答案 課內活動 討論區 ( 3 頁 ) 1 2 網上追蹤 ( 5 頁 ) 2008 年末世界各地煤的蘊藏量地區 蘊藏量 ( 百萬公噸 ) 佔全球的百分比 097 29.8% 15 00 1.8% 272 33.0% 1 38 0.2% 32 013 3.9% 259 253 114 500 31.4% 13.9% 82 001 100.0% 272.2.1 15.0 32.0
zyk00217zw.PDF
 NH NO N 2H O 4 2 2 2 1 1 N2 + O2 === NO 2 2 /K 1000 1500 1811 2033 8.86 10 5 3.30 10 3 1.14 10 2 2.21 10 2 CaC2 N 2 CaCN 2C 1000 Na 2CO 34CN 2 2NaCN3CO /Pa NH / 1.01 5.05 1.01 3.03 6.06 10 6 10 6 10 7
NH NO N 2H O 4 2 2 2 1 1 N2 + O2 === NO 2 2 /K 1000 1500 1811 2033 8.86 10 5 3.30 10 3 1.14 10 2 2.21 10 2 CaC2 N 2 CaCN 2C 1000 Na 2CO 34CN 2 2NaCN3CO /Pa NH / 1.01 5.05 1.01 3.03 6.06 10 6 10 6 10 7
Suggested answers to in-text activities and unit-end exercises
 課內活動及課後練習的建議答案 小測試 P35.1( 第 5 頁 ) a) b) ΔH x = 97 kj mol 1 ΔH y = 144 kj mol 1 P35.( 第 56 頁 ) 1 a) 斜方晶硫較為穩定 b) 已知以下的數據 :` (1) S( 斜方晶 ) + O (g) SO (g) ΔH = 96.0 kj mol 1 () S( 單斜晶 ) + O (g) SO (g) ΔH =
課內活動及課後練習的建議答案 小測試 P35.1( 第 5 頁 ) a) b) ΔH x = 97 kj mol 1 ΔH y = 144 kj mol 1 P35.( 第 56 頁 ) 1 a) 斜方晶硫較為穩定 b) 已知以下的數據 :` (1) S( 斜方晶 ) + O (g) SO (g) ΔH = 96.0 kj mol 1 () S( 單斜晶 ) + O (g) SO (g) ΔH =
EXAMINATION RULES
 考 試 規 則 : 1. 競 賽 者 必 須 在 考 試 前 10 分 鐘 到 達 考 場 2. 競 賽 者 不 可 以 攜 帶 任 何 工 具, 但 是 個 人 所 需 要 的 醫 藥 用 品 及 器 具 不 在 此 限 3. 競 賽 者 必 須 坐 在 指 定 的 位 置 4. 在 考 試 開 始 前, 競 賽 者 必 須 檢 查 大 會 提 供 的 文 具 及 任 何 工 具 ( 筆 尺 計
考 試 規 則 : 1. 競 賽 者 必 須 在 考 試 前 10 分 鐘 到 達 考 場 2. 競 賽 者 不 可 以 攜 帶 任 何 工 具, 但 是 個 人 所 需 要 的 醫 藥 用 品 及 器 具 不 在 此 限 3. 競 賽 者 必 須 坐 在 指 定 的 位 置 4. 在 考 試 開 始 前, 競 賽 者 必 須 檢 查 大 會 提 供 的 文 具 及 任 何 工 具 ( 筆 尺 計
tbjxD219zw.PDF
 nm 1nm=10-9m CO 2 CO 2 1 1 A+B=AB 2H + O 2H O 2 2 2 AB=A+B A+BC=AC+B MnO 2 2KClO3 2KCl3O2 Zn+2HCl==ZnCl +H AB+CD=AD+CB NaOH+HC==NaCl+H O 1-2 S + O2 SO2 CuO + H Cu + H O 2 2 2 3 2Fe + 3CO 2 Fe O +
nm 1nm=10-9m CO 2 CO 2 1 1 A+B=AB 2H + O 2H O 2 2 2 AB=A+B A+BC=AC+B MnO 2 2KClO3 2KCl3O2 Zn+2HCl==ZnCl +H AB+CD=AD+CB NaOH+HC==NaCl+H O 1-2 S + O2 SO2 CuO + H Cu + H O 2 2 2 3 2Fe + 3CO 2 Fe O +
 é SI 12g C = 6 12 = 1 H2( g) + O2( g) H2O( l) + 286kJ ( 1) 2 1 1 H 2( g) + O2( g) H2O( l) H = 286kJ mol ( 2) 2 1 N 2 ( g) + O2( g) NO 2 ( g) 34kJ 2 1 1 N 2 ( g) + O2( g) NO 2 ( g) H = + 34kJ mol 2 1 N
é SI 12g C = 6 12 = 1 H2( g) + O2( g) H2O( l) + 286kJ ( 1) 2 1 1 H 2( g) + O2( g) H2O( l) H = 286kJ mol ( 2) 2 1 N 2 ( g) + O2( g) NO 2 ( g) 34kJ 2 1 1 N 2 ( g) + O2( g) NO 2 ( g) H = + 34kJ mol 2 1 N
(CIP) /,. :,2004 ( ) ISBN 7-5331 - 3713-2.............TG24-64 CIP (2004)034609 : : 16 : 250002 : ( 0531) 2065109 : : jn- public.
 (CIP) /,. :,2004 ( ) ISBN 7-5331 - 3713-2.............TG24-64 CIP (2004)034609 : : 16 : 250002 : ( 0531) 2065109 : www.lkj.com.cn : sdkj @ jn- public.sd.c ninfo.net : : 16 : 250002 : ( 0531) 2020432 :
(CIP) /,. :,2004 ( ) ISBN 7-5331 - 3713-2.............TG24-64 CIP (2004)034609 : : 16 : 250002 : ( 0531) 2065109 : www.lkj.com.cn : sdkj @ jn- public.sd.c ninfo.net : : 16 : 250002 : ( 0531) 2020432 :
物質科學_化學篇
 物 質 科 學 化 學 篇 ( 上 ) 講 義 編 者 : 陳 義 忠 55 物 質 科 學 _ 化 學 篇 ( 上 ) 第 四 章 溶 液 4-1 溶 液 的 性 質 : 1. 溶 液 : (1) 由 兩 種 或 兩 種 以 上 的 純 物 質 混 合 而 成 的 均 勻 混 合 物, 稱 為 溶 液 包 含 固 態 液 態 及 氣 態 () 溶 液 由 溶 質 和 溶 劑 所 組 成 在 形 成
物 質 科 學 化 學 篇 ( 上 ) 講 義 編 者 : 陳 義 忠 55 物 質 科 學 _ 化 學 篇 ( 上 ) 第 四 章 溶 液 4-1 溶 液 的 性 質 : 1. 溶 液 : (1) 由 兩 種 或 兩 種 以 上 的 純 物 質 混 合 而 成 的 均 勻 混 合 物, 稱 為 溶 液 包 含 固 態 液 態 及 氣 態 () 溶 液 由 溶 質 和 溶 劑 所 組 成 在 形 成
 3 3 4 4 3 3 3 1 6 ( n) 85 U 0 9 85 1 90 1 U + n + Kr + 3 n 9 36 0 =1 sp sp 3 sp 14. H + 1 O = H O( ) + 68 NH + 3 O = 3 1 N + 3H O( ) +18 N + 3 H = NH 3 CO( ) + 1 O ( ) = CO ( ) + 67. 6 (1) () (3) (4)
3 3 4 4 3 3 3 1 6 ( n) 85 U 0 9 85 1 90 1 U + n + Kr + 3 n 9 36 0 =1 sp sp 3 sp 14. H + 1 O = H O( ) + 68 NH + 3 O = 3 1 N + 3H O( ) +18 N + 3 H = NH 3 CO( ) + 1 O ( ) = CO ( ) + 67. 6 (1) () (3) (4)
cm CO Na CO HC NaO H CO SO
 cm CO Na CO HC NaO H CO SO C H Na CO CaCO Na CO CaCO ml mm mm cm cm b a b c d K CO A B C D E F G H F C A D B H G C F A KC O MnO MnO KC O MnO KClO MH NO H SO N H N O H SO NaO H Na O ml Na O O NaO
cm CO Na CO HC NaO H CO SO C H Na CO CaCO Na CO CaCO ml mm mm cm cm b a b c d K CO A B C D E F G H F C A D B H G C F A KC O MnO MnO KC O MnO KClO MH NO H SO N H N O H SO NaO H Na O ml Na O O NaO
校园之星
 CO Na HCO AL SO Na SO Al O H SiO C H O CO H O CH CH Cl KClO KCl O P O P O MgCO MgCO AgI Fe O H gs PbS PbCO Pb O H H S PbS CO H O PbS H O PbSO H O CuS Cu S CuCO Ca O H CoCl H O CoCl H O born to
CO Na HCO AL SO Na SO Al O H SiO C H O CO H O CH CH Cl KClO KCl O P O P O MgCO MgCO AgI Fe O H gs PbS PbCO Pb O H H S PbS CO H O PbS H O PbSO H O CuS Cu S CuCO Ca O H CoCl H O CoCl H O born to
※參考資料 原子量
 國立臺中第二高級中學 年級 班姓名 座號 號 101 學年度第 1 學期 1 年級類組化學科第 2 次期中考試題本科電腦代碼 :12 注意 : 未寫或未在規定位置填寫班級 姓名 座號者成績扣五分登記 本試卷計 張共 面 參考資料原子量 :H=1 C=12 N=14 O=16 Na=23 Mg=24 Al=27 P=31 S=32 Cl=35.5 K=39 Ca=40 總分超過 100 分者, 以 100
國立臺中第二高級中學 年級 班姓名 座號 號 101 學年度第 1 學期 1 年級類組化學科第 2 次期中考試題本科電腦代碼 :12 注意 : 未寫或未在規定位置填寫班級 姓名 座號者成績扣五分登記 本試卷計 張共 面 參考資料原子量 :H=1 C=12 N=14 O=16 Na=23 Mg=24 Al=27 P=31 S=32 Cl=35.5 K=39 Ca=40 總分超過 100 分者, 以 100
 1,, 90%,,,,, (, ),,, 1. 2. 3. 1., 90%, 40%, 2 ( ) 2.5% ph, (3) : 2. (3 ) 99%, (40 5 ), ph( 1% ) 6.0 7.5, : 3.,,, 1 088 ;,,,1% ph 12.5, 72.2 ph : 4.,,, 300,,, : 5.,,, ph 6.5 8.5,, ( ) 3, : 6.,,,,, : 7.
1,, 90%,,,,, (, ),,, 1. 2. 3. 1., 90%, 40%, 2 ( ) 2.5% ph, (3) : 2. (3 ) 99%, (40 5 ), ph( 1% ) 6.0 7.5, : 3.,,, 1 088 ;,,,1% ph 12.5, 72.2 ph : 4.,,, 300,,, : 5.,,, ph 6.5 8.5,, ( ) 3, : 6.,,,,, : 7.
 - [Ca 3(PO 4) 2] Ca ( PO ) + 3SiO + 5C = 3CaSiO + 5CO + 2P 3 4 2 2 3 2 1 4 39. 96 99. 60 + 37. 96 0. 96 + 3597. 34 = 39. 95 100 4096. 688. + 39. 96 001. + 38. 96 9308. = 3910. 100
- [Ca 3(PO 4) 2] Ca ( PO ) + 3SiO + 5C = 3CaSiO + 5CO + 2P 3 4 2 2 3 2 1 4 39. 96 99. 60 + 37. 96 0. 96 + 3597. 34 = 39. 95 100 4096. 688. + 39. 96 001. + 38. 96 9308. = 3910. 100
【中文名称】盐酸;氢氯酸
 1 ... 1... 9... 9... 10... 11... 11... 12... 13... 13... 14... 14... 15 1357-1357-3.3.1.1.3.7 HMTA... 16... 16... 17... 17... 18... 19... 19... 20... 20 33-4--13H-... 21 33-4--13H-... 21... 22 EDTA...
1 ... 1... 9... 9... 10... 11... 11... 12... 13... 13... 14... 14... 15 1357-1357-3.3.1.1.3.7 HMTA... 16... 16... 17... 17... 18... 19... 19... 20... 20 33-4--13H-... 21 33-4--13H-... 21... 22 EDTA...
á à
 á à + 2- NH 4 SO4 1 1 2 1 3 1 14 12 6 13 6 6 12 6 2 1 3 1 235 92 18 8 131 53 12 6 1 16 8 12 1 12 6 1 1 2 1 1 1 2 1 6 1 1 6 10 14 p d f 3 5 7 p d f 0 0 0 p d f NH + 4 A werner 1866 1919
á à + 2- NH 4 SO4 1 1 2 1 3 1 14 12 6 13 6 6 12 6 2 1 3 1 235 92 18 8 131 53 12 6 1 16 8 12 1 12 6 1 1 2 1 1 1 2 1 6 1 1 6 10 14 p d f 3 5 7 p d f 0 0 0 p d f NH + 4 A werner 1866 1919
 3 3 3 1.01 105 74 100 100 = 10 100 90 = 11.1 50 98 x 245 20 100 100 1 1 = = -12 1/ 12 = = 12 1/ 12-26 2.65710 = 11.6610-27 -12 6 6 2N 100% = 2 14 100% CO( NH ) 60 2 2
3 3 3 1.01 105 74 100 100 = 10 100 90 = 11.1 50 98 x 245 20 100 100 1 1 = = -12 1/ 12 = = 12 1/ 12-26 2.65710 = 11.6610-27 -12 6 6 2N 100% = 2 14 100% CO( NH ) 60 2 2
 + 7 1 5, Cl Cl + 4 + 6 HSO4 S S S + 6 + 6 HSO4 S S S 0 + 6 + 4 + S S S S + 7 + KMnO 4 Mn Mn + + + [I ] 0 1M 0 I E Fe3+ / Fe+ ( 0771. ) E 1 /1 ( 0536. ) 3+ 3+ + 3+ Fe I I Fe + I = Fe + I [ Fe ] = [ I ]
+ 7 1 5, Cl Cl + 4 + 6 HSO4 S S S + 6 + 6 HSO4 S S S 0 + 6 + 4 + S S S S + 7 + KMnO 4 Mn Mn + + + [I ] 0 1M 0 I E Fe3+ / Fe+ ( 0771. ) E 1 /1 ( 0536. ) 3+ 3+ + 3+ Fe I I Fe + I = Fe + I [ Fe ] = [ I ]
试卷
 玉 溪 一 中 高 2015 届 高 三 上 学 期 期 中 考 化 学 试 题 相 对 原 子 质 量 : N-14,Na-23,Cl-35.5, Cu-64 说 明 : 测 试 时 间 120 分 钟, 满 分 100 分 第 I 卷 ( 选 择 题 共 46 分 ) 一 选 择 题 ( 本 题 包 括 23 小 题, 每 小 题 2 分, 共 46 分 每 小 题 只 有 一 个... 选 项
玉 溪 一 中 高 2015 届 高 三 上 学 期 期 中 考 化 学 试 题 相 对 原 子 质 量 : N-14,Na-23,Cl-35.5, Cu-64 说 明 : 测 试 时 间 120 分 钟, 满 分 100 分 第 I 卷 ( 选 择 题 共 46 分 ) 一 选 择 题 ( 本 题 包 括 23 小 题, 每 小 题 2 分, 共 46 分 每 小 题 只 有 一 个... 选 项
教师招聘中学化学1-11.FIT)
 教 师 招 聘 考 试 中 学 化 学 历 年 真 题 汇 编 试 卷 渊 一 冤 渊 时 间 院 员 圆 园 分 钟 满 分 院 员 缘 园 分 冤 一 尧 单 项 选 择 题 渊 每 小 题 圆 分 袁 共 缘 园 分 冤 员 援 石 墨 烯 是 由 碳 原 子 构 成 的 单 层 片 状 结 构 的 新 材 料 渊 结 构 示 意 图 如 图 所 示 冤 袁 可 由 石 墨 剥 离 而 成 袁
教 师 招 聘 考 试 中 学 化 学 历 年 真 题 汇 编 试 卷 渊 一 冤 渊 时 间 院 员 圆 园 分 钟 满 分 院 员 缘 园 分 冤 一 尧 单 项 选 择 题 渊 每 小 题 圆 分 袁 共 缘 园 分 冤 员 援 石 墨 烯 是 由 碳 原 子 构 成 的 单 层 片 状 结 构 的 新 材 料 渊 结 构 示 意 图 如 图 所 示 冤 袁 可 由 石 墨 剥 离 而 成 袁
,,, ( CI P) /. :, ISBN :.T U56 CI P ( 2004 ) : 122 : / E mail: mail.w hu t.ed
 ,,, ( CI P) /. :, 2004.8 ISBN 7 5629 2094... :.T U56 CI P ( 2004 )003590 : 122 : 430070 http:/ / www.techbook.com.cn E mail: yangxuezh@ mail.w hu t.edu.cn : : : 7871092 1/ 16 : 19 : 474 : 2004 8 1 : 2004
,,, ( CI P) /. :, 2004.8 ISBN 7 5629 2094... :.T U56 CI P ( 2004 )003590 : 122 : 430070 http:/ / www.techbook.com.cn E mail: yangxuezh@ mail.w hu t.edu.cn : : : 7871092 1/ 16 : 19 : 474 : 2004 8 1 : 2004
 ( )C:H:O = 40.0 12 : 6.7 1 :53.3 = 3.33:6.7:3.33 = 1:2:1(10 ) 16 4.C + H O CO + H (3 ) 2 2 11.2 5.6 = 0.5 O 2 ; = 0.25) H 2 (3 22.4 22.4 0.322.41000 x = = 60 (4 ) 256 + + (1) K NH PO, 4 (, ): 4 (,
( )C:H:O = 40.0 12 : 6.7 1 :53.3 = 3.33:6.7:3.33 = 1:2:1(10 ) 16 4.C + H O CO + H (3 ) 2 2 11.2 5.6 = 0.5 O 2 ; = 0.25) H 2 (3 22.4 22.4 0.322.41000 x = = 60 (4 ) 256 + + (1) K NH PO, 4 (, ): 4 (,
35 C 58 B 1 :
 1 2 1. 0625522. 050061 120 120 46 60 40 20 2012 2011 2012 1 2 3 4 5 6 8 9 11 12 14 28 30 36 7 13 29 31 35 144 35 C 58 B 1 : 3 4 5 40 84 9 11 2 6 27 9 29 13 28 31 31 35 35 36 7 3 12 27 6 7 29 30 31 29 30
1 2 1. 0625522. 050061 120 120 46 60 40 20 2012 2011 2012 1 2 3 4 5 6 8 9 11 12 14 28 30 36 7 13 29 31 35 144 35 C 58 B 1 : 3 4 5 40 84 9 11 2 6 27 9 29 13 28 31 31 35 35 36 7 3 12 27 6 7 29 30 31 29 30
 MnO - 4 MnO 2-2+ MnO Mn - MnO MnO 4 4 2 CH2 = CH2 + Br2 BrH2C CH2Br CaS + 2H O = Ca( OH) + H S 2 2 2 Ca P + 6H O = 3Ca( OH) + 2PH 3 2 2 2 3 Ca As + 6H O = 3Ca( OH) + 2AsH 3 2 2 2 3 k Cr O + 4H SO + 3H
MnO - 4 MnO 2-2+ MnO Mn - MnO MnO 4 4 2 CH2 = CH2 + Br2 BrH2C CH2Br CaS + 2H O = Ca( OH) + H S 2 2 2 Ca P + 6H O = 3Ca( OH) + 2PH 3 2 2 2 3 Ca As + 6H O = 3Ca( OH) + 2AsH 3 2 2 2 3 k Cr O + 4H SO + 3H
0 0 = 1 0 = 0 1 = = 1 1 = 0 0 = 1
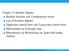 0 0 = 1 0 = 0 1 = 0 1 1 = 1 1 = 0 0 = 1 : = {0, 1} : 3 (,, ) = + (,, ) = + + (, ) = + (,,, ) = ( + )( + ) + ( + )( + ) + = + = = + + = + = ( + ) + = + ( + ) () = () ( + ) = + + = ( + )( + ) + = = + 0
0 0 = 1 0 = 0 1 = 0 1 1 = 1 1 = 0 0 = 1 : = {0, 1} : 3 (,, ) = + (,, ) = + + (, ) = + (,,, ) = ( + )( + ) + ( + )( + ) + = + = = + + = + = ( + ) + = + ( + ) () = () ( + ) = + + = ( + )( + ) + = = + 0
 t H θ m [] Q Q q [] 9. 69kJ g q 32.0 620kJmol - 1 0. 500g mol C(s) 1 2 O (g) = CO(g) 2 SI n mol H 2H+H22H2+O2 [N2H41+O2g N2g+2H2O1] 1.2.3 qp qv [4] 1 C( ) O 2 (g) = CO(g), ( 2), 2 CO(g) CO (g),co(g) +
t H θ m [] Q Q q [] 9. 69kJ g q 32.0 620kJmol - 1 0. 500g mol C(s) 1 2 O (g) = CO(g) 2 SI n mol H 2H+H22H2+O2 [N2H41+O2g N2g+2H2O1] 1.2.3 qp qv [4] 1 C( ) O 2 (g) = CO(g), ( 2), 2 CO(g) CO (g),co(g) +
解析 : 液態空氣中含氮氣和氧氣, 因此液態空氣必為混合物, 沒有一定的熔點及沸點 氮氣的性質安定, 在常溫下不易發生反應 ; 氧氣則是活性大, 容易產生反應的氣體 沸點和分子量有關, 氮氣的分子量較小, 沸點較低, 氧氣的沸點則較高 ( )3. 純物質依據下列何者可再分類為元素和化合物? (A)
 ( )1. 某物質經加熱 通電或照光後, 變成兩種或兩種以上的新物質, 此化學變化的過程稱為 (A) 分解 (B) 化合 (C) 燃燒 (D) 過濾 答案 :(A) 解析 : 將物質進行加熱 通電或照光的程序, 使物質產生化學變化, 生成兩種以上的物質, 稱為分解 分解反應的通式為 A B+C ( )2. 上列物質中, 何者屬於元素? (A) 乙 (B) 甲乙 (C) 甲乙丙 (D) 甲丙 答案 :(B)
( )1. 某物質經加熱 通電或照光後, 變成兩種或兩種以上的新物質, 此化學變化的過程稱為 (A) 分解 (B) 化合 (C) 燃燒 (D) 過濾 答案 :(A) 解析 : 將物質進行加熱 通電或照光的程序, 使物質產生化學變化, 生成兩種以上的物質, 稱為分解 分解反應的通式為 A B+C ( )2. 上列物質中, 何者屬於元素? (A) 乙 (B) 甲乙 (C) 甲乙丙 (D) 甲丙 答案 :(B)
 用 矿 物 质 丰 富 的 盐 炼 成 的 竹 盐 是 科 学 Contents 可 以 解 决 矿 物 质 缺 乏 的 生 命 之 盐 - 竹 盐 2 什 么 是 矿 物 质? 3 盐 不 是 单 纯 的 氯 化 钠 4 难 道 盐 是 高 血 压 的 元 凶 吗? 5 推 荐 用 盐 补 充 体 内 缺 乏 矿 物 质 8 什 么 是 竹 盐? 10 盐 与 竹 盐 的 成 分 分 析 11 竹
用 矿 物 质 丰 富 的 盐 炼 成 的 竹 盐 是 科 学 Contents 可 以 解 决 矿 物 质 缺 乏 的 生 命 之 盐 - 竹 盐 2 什 么 是 矿 物 质? 3 盐 不 是 单 纯 的 氯 化 钠 4 难 道 盐 是 高 血 压 的 元 凶 吗? 5 推 荐 用 盐 补 充 体 内 缺 乏 矿 物 质 8 什 么 是 竹 盐? 10 盐 与 竹 盐 的 成 分 分 析 11 竹
第三章气硬性胶凝材料
 第 三 章 气 硬 性 胶 凝 材 料 教 学 要 求 1 熟 悉 四 种 常 用 气 硬 性 胶 凝 材 料 的 性 质, 以 及 如 何 在 工 程 中 合 理 使 用 2 对 于 石 膏 和 石 灰 石, 要 了 解 其 原 料 生 产 凝 结 硬 化 及 质 量 要 求, 掌 握 其 性 质 与 应 用 3 水 玻 璃 与 菱 苦 土 要 着 重 了 解 其 性 质 和 应 用 特 点 内
第 三 章 气 硬 性 胶 凝 材 料 教 学 要 求 1 熟 悉 四 种 常 用 气 硬 性 胶 凝 材 料 的 性 质, 以 及 如 何 在 工 程 中 合 理 使 用 2 对 于 石 膏 和 石 灰 石, 要 了 解 其 原 料 生 产 凝 结 硬 化 及 质 量 要 求, 掌 握 其 性 质 与 应 用 3 水 玻 璃 与 菱 苦 土 要 着 重 了 解 其 性 质 和 应 用 特 点 内
沪教版初三化学(上)
 2010 中 考 化 学 试 题 汇 编 之 7 酸 碱 盐 一 选 择 1.(2010 肇 庆 ) 下 列 化 学 方 程 式 所 表 示 的 化 学 反 应 能 发 生 的 是 ( ) A.Cu+H 2 SO 4 CuSO 4 +H 2 B.Fe+ Zn( NO 3 ) 2 Fe(NO 3 ) 2 +Zn C.CuCl 2 +2NaOH Cu(OH) 2 +2NaCl D.Na 2 CO 3 +2KNO
2010 中 考 化 学 试 题 汇 编 之 7 酸 碱 盐 一 选 择 1.(2010 肇 庆 ) 下 列 化 学 方 程 式 所 表 示 的 化 学 反 应 能 发 生 的 是 ( ) A.Cu+H 2 SO 4 CuSO 4 +H 2 B.Fe+ Zn( NO 3 ) 2 Fe(NO 3 ) 2 +Zn C.CuCl 2 +2NaOH Cu(OH) 2 +2NaCl D.Na 2 CO 3 +2KNO
1 ( CIP) /,. :, ISBN X753 CIP ( 2005 ) : : : : /
 ( 50474050) ( 20040533011) 1 ( CIP) /,. :, 2005. 12 ISBN 7-81105-260-1............. X753 CIP ( 2005 ) 151885 : : 410083 : 0731-8876770 : 0731-8710482 880 1230 1 /32 11. 25 277 2006 3 1 2006 3 1 ISBN 7-81105-260-1
( 50474050) ( 20040533011) 1 ( CIP) /,. :, 2005. 12 ISBN 7-81105-260-1............. X753 CIP ( 2005 ) 151885 : : 410083 : 0731-8876770 : 0731-8710482 880 1230 1 /32 11. 25 277 2006 3 1 2006 3 1 ISBN 7-81105-260-1
YYHX.mps
 第 七 章 配 位 化 合 物 和 生 物 元 素 自 然 界 有 一 类 组 成 较 为 复 杂, 在 理 论 上 和 应 用 上 都 十 分 重 要 的 化 合 物, 这 类 化 合 物 的 核 心 部 分 是 以 配 位 键 相 连, 故 称 为 配 位 化 合 物, 简 称 配 合 物 近 几 十 年 来, 随 着 科 学 的 发 展 近 代 物 理 仪 器 的 涌 现 和 实 验 技 术
第 七 章 配 位 化 合 物 和 生 物 元 素 自 然 界 有 一 类 组 成 较 为 复 杂, 在 理 论 上 和 应 用 上 都 十 分 重 要 的 化 合 物, 这 类 化 合 物 的 核 心 部 分 是 以 配 位 键 相 连, 故 称 为 配 位 化 合 物, 简 称 配 合 物 近 几 十 年 来, 随 着 科 学 的 发 展 近 代 物 理 仪 器 的 涌 现 和 实 验 技 术
¦ÛµM¬ì²Ä3¦¸²Õ¨÷-¾Ç´ú¤ºŁ¶«ÊŁ±.prn, page Normalize ( <4D F736F F D20A6DBB54DACECB2C433A6B8B2D5A8F72DBEC7B4FAA4BAADB6ABCAADB12E646F63> )
 100 40 28 2B c 3 10 8 m s h 6.63 10 34 J s e 1.6 10 19 C hc 1240 E hf ev λ λ nm 1 ev 1.6 10-19 J 1 mol 6.02 10 23 ph 8 10 N 14 O 16 Fe 56 Ag 108 NO.99341003 103-E3 第壹部分 ( 占 80 分 ) 56 1 說明 : 第 1 題至第 k
100 40 28 2B c 3 10 8 m s h 6.63 10 34 J s e 1.6 10 19 C hc 1240 E hf ev λ λ nm 1 ev 1.6 10-19 J 1 mol 6.02 10 23 ph 8 10 N 14 O 16 Fe 56 Ag 108 NO.99341003 103-E3 第壹部分 ( 占 80 分 ) 56 1 說明 : 第 1 題至第 k
77 ( ) http: www. qdpub. com ( 0532) ( ) ( 850mm 1168mm) ISBN
 77 ( 266071) http: www. qdpub. com 13335059110 ( 0532) 85814750( ) 85814611-8664 2006 1 2 2006 1 2 20 ( 850mm 1168mm) 20 450 6001 12000 ISBN 7-5436 - 2391-9 29. 00 ( 0532) 85814926, ,,,,,,,,,,,,, 260,,,,
77 ( 266071) http: www. qdpub. com 13335059110 ( 0532) 85814750( ) 85814611-8664 2006 1 2 2006 1 2 20 ( 850mm 1168mm) 20 450 6001 12000 ISBN 7-5436 - 2391-9 29. 00 ( 0532) 85814926, ,,,,,,,,,,,,, 260,,,,
 ο ο ο ο 100 A 1000 A 20A 100 A 20A ο ο 20 A 327 ] [Al OH SO ] 3 m n 2 m 4 m n 3 2 ([Fe ( OH) ( SO ) ] [Fe OH Cl ] 2 m 4 m 3-2 n 2 m 6-m n D
ο ο ο ο 100 A 1000 A 20A 100 A 20A ο ο 20 A 327 ] [Al OH SO ] 3 m n 2 m 4 m n 3 2 ([Fe ( OH) ( SO ) ] [Fe OH Cl ] 2 m 4 m 3-2 n 2 m 6-m n D
untitled
 [] [] [] 15.1 1 2 Cu 2+ 2e=Cu Zn 2+ 2e=Zn 2H + 2eH 2 Cu2e=Cu 2+ Ni2e=Ni 2+ 2OH 2e=H 2 O 1/2O 2 2Cl 2e=Cl 2 1 1. 2. 15.2 z+ ze l H 3 O + e 2 1 H 2 O 2a H 2 O e 2 1 OH 2b O 2 2H 2 O 4e4OH 3 z+ ze 4 z+ (zh)e
[] [] [] 15.1 1 2 Cu 2+ 2e=Cu Zn 2+ 2e=Zn 2H + 2eH 2 Cu2e=Cu 2+ Ni2e=Ni 2+ 2OH 2e=H 2 O 1/2O 2 2Cl 2e=Cl 2 1 1. 2. 15.2 z+ ze l H 3 O + e 2 1 H 2 O 2a H 2 O e 2 1 OH 2b O 2 2H 2 O 4e4OH 3 z+ ze 4 z+ (zh)e
2 ( 1 ( 1 1m( (100cm( (1000mm( ( ( 1km( (1000m 1m(10 6 m 4 1nm(10 9 m 1 ( (A (B (C 1 ( 2 5 (D 1 ( 2 ( ( ( 3 ( 1 ( 1 ( 1 1 ( 1 ( 1 ( ( ( ( 1 1L( ( 1000
 1 0 1 1/3~2/3 ( ( ( 4 ( 1 ( ( ( ( ( 1 ( ( 1 ( 1 ( ( ( 1 ( ( ( 1 ( 1/3 1 1 ( 1 1 1 1 1 1 1 1 2 ( 1 ( 1 1m( (100cm( (1000mm( ( ( 1km( (1000m 1m(10 6 m 4 1nm(10 9 m 1 ( (A (B (C 1 ( 2 5 (D 1 ( 2 ( ( ( 3 (
1 0 1 1/3~2/3 ( ( ( 4 ( 1 ( ( ( ( ( 1 ( ( 1 ( 1 ( ( ( 1 ( ( ( 1 ( 1/3 1 1 ( 1 1 1 1 1 1 1 1 2 ( 1 ( 1 1m( (100cm( (1000mm( ( ( 1km( (1000m 1m(10 6 m 4 1nm(10 9 m 1 ( (A (B (C 1 ( 2 5 (D 1 ( 2 ( ( ( 3 (
<4D6963726F736F667420576F7264202D203130332D322DA5FEB0EABEC7B4FA2DA6DBB54DA6D2ACECB8D5C344>
 第 1 頁 3-2 學 測 自 然 考 科 第 壹 部 分 ( 占 80 分 ) 一 單 選 題 ( 占 56 分 ) 說 明 : 第 1 題 至 第 28 題, 每 題 均 計 分 每 題 有 n 個 選 項, 其 中 只 有 一 個 是 正 確 或 最 適 當 的 選 項, 請 畫 記 在 答 案 卡 之 選 擇 題 答 案 區 各 題 答 對 者, 得 2 分 ; 答 錯 未 作 答 或 畫
第 1 頁 3-2 學 測 自 然 考 科 第 壹 部 分 ( 占 80 分 ) 一 單 選 題 ( 占 56 分 ) 說 明 : 第 1 題 至 第 28 題, 每 題 均 計 分 每 題 有 n 個 選 項, 其 中 只 有 一 個 是 正 確 或 最 適 當 的 選 項, 請 畫 記 在 答 案 卡 之 選 擇 題 答 案 區 各 題 答 對 者, 得 2 分 ; 答 錯 未 作 答 或 畫
的 浓 度 为 0.1125 mol/ L. 7. 痕 量 Au 3+ 的 溶 液 在 盐 酸 介 质 中 能 被 阴 离 子 交 换 树 脂 交 换 而 得 到 富 集, 这 时 Au 3+ 是 以 AuCl 4 - 形 式 被 交 换 到 树 脂 上 去 的 8. 将 Fe 3+ 和 Al 3+
 二 填 空 题 原 子 吸 收 1. 空 心 阴 极 灯 是 一 种 ( 锐 性 ) 光 源, 它 的 发 射 光 谱 具 有 ( 谱 线 窄 强 度 大 ) 特 点 当 灯 电 流 升 高 时, 由 于 ( 自 吸 变 宽 热 变 宽 ) 的 影 响, 导 致 谱 线 轮 廓 ( 变 宽 ), 测 量 灵 敏 度 ( 下 降 ), 工 作 曲 线 ( 线 性 关 系 变 差 ), 灯 寿 命 (
二 填 空 题 原 子 吸 收 1. 空 心 阴 极 灯 是 一 种 ( 锐 性 ) 光 源, 它 的 发 射 光 谱 具 有 ( 谱 线 窄 强 度 大 ) 特 点 当 灯 电 流 升 高 时, 由 于 ( 自 吸 变 宽 热 变 宽 ) 的 影 响, 导 致 谱 线 轮 廓 ( 变 宽 ), 测 量 灵 敏 度 ( 下 降 ), 工 作 曲 线 ( 线 性 关 系 变 差 ), 灯 寿 命 (
法 去 对 待 : 溴 水 碘 水 氯 化 氢 水 溴 化 氢 水 碘 化 氢 水 氨 水 二 氧 化 硫 水 硫 化 氢 水 二 氧 化 碳 水 -------- 的 组 成 与 溶 解 过 程 从 氯 水 参 与 的 化 学 反 应 的 本 质 与 类 型 去 学 会 分 析 : 金 属 钠 过
 枝 乱 我 不 乱 高 考 化 学 总 复 习 的 策 略 与 思 路 措 施 与 方 法 从 容 看 万 条 一. 刍 议 河 北 省 用 高 考 试 题 抓 基 础 抓 主 干 抓 核 心 ; 重 能 力 重 理 解 重 应 用 ; 变 宽 度 降 难 度 改 深 度 ; 稳 求 变 稳 求 新 稳 求 进 试 题 导 向 健 康 难 度 控 制 得 当, 主 干 知 识 突 出, 区 分 度
枝 乱 我 不 乱 高 考 化 学 总 复 习 的 策 略 与 思 路 措 施 与 方 法 从 容 看 万 条 一. 刍 议 河 北 省 用 高 考 试 题 抓 基 础 抓 主 干 抓 核 心 ; 重 能 力 重 理 解 重 应 用 ; 变 宽 度 降 难 度 改 深 度 ; 稳 求 变 稳 求 新 稳 求 进 试 题 导 向 健 康 难 度 控 制 得 当, 主 干 知 识 突 出, 区 分 度
( ) 63 ( ) 68 ( ) 72 ( ) 77 ( ) 85 ( ) 91 ( ) ( ) 98 ( ) 103 ( ) 107 ( ) 111 ( ) 114 ( ) 117 ( ) 121 ( ) 125 ( ) 127 ( ) ( ) 133 ( ) 139
 1 ( ) 1 ( ) 2 ( ) 7 ( ) 9 ( ) 10 16 ( ) 16 ( ) 17 ( ) 19 ( ) 23 ( ) 25 ( ) 26 30 ( ) 30 ( ) 46 50 ( ) 50 ( ) 52 1 ( ) 63 ( ) 68 ( ) 72 ( ) 77 ( ) 85 ( ) 91 ( ) 94 98 ( ) 98 ( ) 103 ( ) 107 ( ) 111 ( )
1 ( ) 1 ( ) 2 ( ) 7 ( ) 9 ( ) 10 16 ( ) 16 ( ) 17 ( ) 19 ( ) 23 ( ) 25 ( ) 26 30 ( ) 30 ( ) 46 50 ( ) 50 ( ) 52 1 ( ) 63 ( ) 68 ( ) 72 ( ) 77 ( ) 85 ( ) 91 ( ) 94 98 ( ) 98 ( ) 103 ( ) 107 ( ) 111 ( )
中华人民共和国国家标准
 1 1 1.1 1.2 1.3 2 2.1 2.2 3 4 4.1 4.2 5 5.1 5.2 5.3 5.4 6 6.1 6.2 6.3 2 7 7.1 7.2 7.3 7.4 8 9 10 11 3 1 1.1 30% 20% 20% 45-50% 30% 15% 10000 50 5000 2.5 3 100 100 m 2 600 4 5 3000 4 38% 10% 24% 10 0.82t/m
1 1 1.1 1.2 1.3 2 2.1 2.2 3 4 4.1 4.2 5 5.1 5.2 5.3 5.4 6 6.1 6.2 6.3 2 7 7.1 7.2 7.3 7.4 8 9 10 11 3 1 1.1 30% 20% 20% 45-50% 30% 15% 10000 50 5000 2.5 3 100 100 m 2 600 4 5 3000 4 38% 10% 24% 10 0.82t/m
 1 cal = 4.18 J N 0 = 6.02 10 : 1.00 : 12.0 : 14.0 : 16.0 : 32.0 23 1 40 2 1. (A) (B) (C) (D) (E) (C) (A) ( ) (B) ( ) (D) (NaI KIO 3 ) (E) ( Ca 2+ Mg 2+ Fe 2+ ) (C) 1 2 3 75 6 (Ga 29.8 2403 ) 310 K 1.3
1 cal = 4.18 J N 0 = 6.02 10 : 1.00 : 12.0 : 14.0 : 16.0 : 32.0 23 1 40 2 1. (A) (B) (C) (D) (E) (C) (A) ( ) (B) ( ) (D) (NaI KIO 3 ) (E) ( Ca 2+ Mg 2+ Fe 2+ ) (C) 1 2 3 75 6 (Ga 29.8 2403 ) 310 K 1.3
试卷
 严 州 中 学 015 届 高 三 4 月 阶 段 测 试 理 科 综 合 试 卷 本 试 卷 分 第 Ⅰ 卷 ( 选 择 题 ) 和 第 Ⅱ 卷 ( 综 合 题 ) 两 部 分 满 分 300 分 考 试 时 间 150 分 钟 可 能 用 到 的 相 对 原 子 质 量 :H-1 C-1 N-14 O-16 Al-7 S-3 Cl-35.5 K-39 Fe-56 Cu-64 Ba-137 第 Ι
严 州 中 学 015 届 高 三 4 月 阶 段 测 试 理 科 综 合 试 卷 本 试 卷 分 第 Ⅰ 卷 ( 选 择 题 ) 和 第 Ⅱ 卷 ( 综 合 题 ) 两 部 分 满 分 300 分 考 试 时 间 150 分 钟 可 能 用 到 的 相 对 原 子 质 量 :H-1 C-1 N-14 O-16 Al-7 S-3 Cl-35.5 K-39 Fe-56 Cu-64 Ba-137 第 Ι
建 设 项 目 环 境 影 响 报 告 表 编 制 说 明 建 设 项 目 环 境 影 响 报 告 表 由 具 有 从 事 环 境 影 响 评 价 工 作 资 质 的 单 位 编 制 1. 项 目 名 称 指 项 目 立 项 批 复 时 的 名 称, 应 不 超 过 30 个 字 ( 两 个 英 文
 建 设 项 目 环 境 影 响 报 告 表 项 目 名 称 : 马 钢 股 份 公 司 冷 轧 总 厂 新 增 电 解 脱 脂 机 组 工 程 项 目 建 设 单 位 ( 盖 章 ): 马 鞍 山 钢 铁 股 份 有 限 公 司 编 制 日 期 : 二 0 一 五 年 八 月 国 家 环 境 保 护 总 局 制 建 设 项 目 环 境 影 响 报 告 表 编 制 说 明 建 设 项 目 环 境 影
建 设 项 目 环 境 影 响 报 告 表 项 目 名 称 : 马 钢 股 份 公 司 冷 轧 总 厂 新 增 电 解 脱 脂 机 组 工 程 项 目 建 设 单 位 ( 盖 章 ): 马 鞍 山 钢 铁 股 份 有 限 公 司 编 制 日 期 : 二 0 一 五 年 八 月 国 家 环 境 保 护 总 局 制 建 设 项 目 环 境 影 响 报 告 表 编 制 说 明 建 设 项 目 环 境 影
<4D6963726F736F667420576F7264202D20B2C4A44BB3B92020B8ADADB1AC49AACEAD6EBBE22E646F63>
 第 八 章 葉 面 施 肥 要 領 植 物 葉 片 兩 面 有 很 多 氣 孔, 可 以 吸 收 噴 在 葉 片 上 溶 液 狀 態 的 肥 料, 也 可 直 接 透 過 葉 片 角 質 層 細 胞 壁 和 原 形 質 膜 而 進 入 細 胞 內 部, 這 就 是 葉 面 施 肥 葉 面 施 肥 為 土 壤 施 肥 以 外, 補 充 養 分 的 一 個 經 濟 有 效 的 辦 法 葉 面 肥 料 一
第 八 章 葉 面 施 肥 要 領 植 物 葉 片 兩 面 有 很 多 氣 孔, 可 以 吸 收 噴 在 葉 片 上 溶 液 狀 態 的 肥 料, 也 可 直 接 透 過 葉 片 角 質 層 細 胞 壁 和 原 形 質 膜 而 進 入 細 胞 內 部, 這 就 是 葉 面 施 肥 葉 面 施 肥 為 土 壤 施 肥 以 外, 補 充 養 分 的 一 個 經 濟 有 效 的 辦 法 葉 面 肥 料 一
( 一 ) 關 卡 簡 介 各 關 名 稱 化 學 原 理 通 關 要 求 七 彩 變 色 龍 氧 化 還 原 反 應 錯 合 物 反 應 紅 : Fe 3+ + SCN - (FeSCN 2+ ) 橙 : (CrO 2-7 ) 抽 題 ( 多 拉 a 夢 皮 卡 丘 天 線 寶 寶 ) 並 配 出
 A-1 ( 一 ) 關 卡 簡 介 各 關 名 稱 化 學 原 理 通 關 要 求 七 彩 變 色 龍 氧 化 還 原 反 應 錯 合 物 反 應 紅 : Fe 3+ + SCN - (FeSCN 2+ ) 橙 : (CrO 2-7 ) 抽 題 ( 多 拉 a 夢 皮 卡 丘 天 線 寶 寶 ) 並 配 出 所 需 顏 色 完 成 圖 案 黃 : Cr 2 O 2-7 + OH - (CrO 2-4
A-1 ( 一 ) 關 卡 簡 介 各 關 名 稱 化 學 原 理 通 關 要 求 七 彩 變 色 龍 氧 化 還 原 反 應 錯 合 物 反 應 紅 : Fe 3+ + SCN - (FeSCN 2+ ) 橙 : (CrO 2-7 ) 抽 題 ( 多 拉 a 夢 皮 卡 丘 天 線 寶 寶 ) 並 配 出 所 需 顏 色 完 成 圖 案 黃 : Cr 2 O 2-7 + OH - (CrO 2-4
厨 房 垃 圾 D. 其 他 垃 圾 9.( 1 分 )(2015 西 城 区 一 模 )PM2.5 是 造 成 雾 霾 天 气 的 元 凶 之 一, 下 列 做 法 不 会 增 加 空 气 中 的 PM2.5 的 是 ( ) A. 焚 烧 秸 杆 B. 植 树 造 林 C. 燃 放 鞭 炮 D.
 2015 年 北 京 市 西 城 区 中 考 化 学 一 模 试 卷 一 第 一 部 分 选 择 题 ( 每 题 1 分, 每 小 题 只 有 一 个 选 项 符 合 题 意 ) 1.( 1 分 )(2015 西 城 区 一 模 ) 下 列 变 化 属 于 物 理 变 化 的 是 ( ) A. 冰 雪 融 化 B. 木 柴 燃 烧 C. 白 磷 自 燃 D. 食 物 变 质 2.( 1 分 )(2015
2015 年 北 京 市 西 城 区 中 考 化 学 一 模 试 卷 一 第 一 部 分 选 择 题 ( 每 题 1 分, 每 小 题 只 有 一 个 选 项 符 合 题 意 ) 1.( 1 分 )(2015 西 城 区 一 模 ) 下 列 变 化 属 于 物 理 变 化 的 是 ( ) A. 冰 雪 融 化 B. 木 柴 燃 烧 C. 白 磷 自 燃 D. 食 物 变 质 2.( 1 分 )(2015
1 S P Cl Pro 2 K Na Ca Mg K Na Ca Mg % 1 6%-9% 2 1%-3% 3 70%-80% 4 P Ca Fe Cu Co Zn Se Mn Mo Ni Cr P Ca 5 VB V B1 Vpp V B2 B3 VE
 1 2 1 V Pro 2 3 1 Pro 2 Fe2+ Fe3+ 3 Vc 4 Vc 5 1-12% 45-64% 4 1 S P Cl Pro 2 K Na Ca Mg K Na Ca Mg 3 1-2 11-14% 1 6%-9% 2 1%-3% 3 70%-80% 4 P Ca Fe Cu Co Zn Se Mn Mo Ni Cr P Ca 5 VB V B1 Vpp V B2 B3 VE
1 2 1 V Pro 2 3 1 Pro 2 Fe2+ Fe3+ 3 Vc 4 Vc 5 1-12% 45-64% 4 1 S P Cl Pro 2 K Na Ca Mg K Na Ca Mg 3 1-2 11-14% 1 6%-9% 2 1%-3% 3 70%-80% 4 P Ca Fe Cu Co Zn Se Mn Mo Ni Cr P Ca 5 VB V B1 Vpp V B2 B3 VE
第一章 总论
 陕 西 盛 华 冶 化 有 限 公 司 30000 吨 金 属 钙 ( 一 期 15000 吨 金 属 钙 生 产 线 ) 建 设 项 目 前 言 前 言 一 项 目 由 来 金 属 钙 是 一 种 活 泼 的 轻 有 色 金 属, 在 工 业 领 域 中 的 应 用 广 泛, 随 着 现 代 科 学 技 术 的 不 断 发 展, 其 应 用 范 围 与 应 用 领 域 在 不 断 拓 展, 国 际
陕 西 盛 华 冶 化 有 限 公 司 30000 吨 金 属 钙 ( 一 期 15000 吨 金 属 钙 生 产 线 ) 建 设 项 目 前 言 前 言 一 项 目 由 来 金 属 钙 是 一 种 活 泼 的 轻 有 色 金 属, 在 工 业 领 域 中 的 应 用 广 泛, 随 着 现 代 科 学 技 术 的 不 断 发 展, 其 应 用 范 围 与 应 用 领 域 在 不 断 拓 展, 国 际
4. 下 列 有 关 系 保 内 物 质 含 量 比 值 的 关 系, 正 确 的 是 A. 细 胞 内 结 合 水 / 自 由 水 的 比 值, 种 子 萌 发 时 比 休 眠 时 高 B. 人 体 细 胞 内 O /CO 的 比 值, 线 粒 体 内 比 细 胞 质 基 质 高 C. 神 经 纤
 绝 密 启 用 前 015 年 普 通 高 等 学 校 招 生 全 国 统 一 考 试 ( 山 东 卷 ) 理 科 综 合 注 意 事 项 : 1. 本 试 卷 分 第 I 卷 和 第 II 卷 两 部 分, 共 1 页 满 分 300 分 考 试 用 时 150 分 钟 答 题 前, 考 生 务 必 用 0.5 毫 米 黑 色 签 字 笔 将 自 己 的 姓 名 座 号 考 生 号 县 区 和 科
绝 密 启 用 前 015 年 普 通 高 等 学 校 招 生 全 国 统 一 考 试 ( 山 东 卷 ) 理 科 综 合 注 意 事 项 : 1. 本 试 卷 分 第 I 卷 和 第 II 卷 两 部 分, 共 1 页 满 分 300 分 考 试 用 时 150 分 钟 答 题 前, 考 生 务 必 用 0.5 毫 米 黑 色 签 字 笔 将 自 己 的 姓 名 座 号 考 生 号 县 区 和 科
1 10mg/kg 20mg/kg -91-
 1 10mg/kg 20mg/kg -91- 1 120-92- 0.01mg L 1,1,2-0.006mg L 0.03mg L 0.01mg L 0.01mg L 0.05mg L 1,3-0.002mg L 0.01mg L 0.006mg L 0.0005mg L 0.003mg L 0.02mg L 0.01mg L 0.02mg L 0.01mg L 0.002mg L 10mg L
1 10mg/kg 20mg/kg -91- 1 120-92- 0.01mg L 1,1,2-0.006mg L 0.03mg L 0.01mg L 0.01mg L 0.05mg L 1,3-0.002mg L 0.01mg L 0.006mg L 0.0005mg L 0.003mg L 0.02mg L 0.01mg L 0.02mg L 0.01mg L 0.002mg L 10mg L
第 13 章 氢和稀有气体
 第 11 章 氢 和 稀 有 气 体 教 学 要 求 1 掌 握 氢 原 子 的 性 质 成 键 特 征 氢 化 物 2 了 解 稀 有 气 体 的 原 子 结 构 性 质 和 用 途 教 学 重 点 氢 的 物 理 性 质 与 化 学 性 质 教 学 难 点 稀 有 气 体 化 合 物 的 性 质 教 学 时 数 4 学 时 教 学 内 容 11-1 氢 11-2 稀 有 气 体 教 学 方 法
第 11 章 氢 和 稀 有 气 体 教 学 要 求 1 掌 握 氢 原 子 的 性 质 成 键 特 征 氢 化 物 2 了 解 稀 有 气 体 的 原 子 结 构 性 质 和 用 途 教 学 重 点 氢 的 物 理 性 质 与 化 学 性 质 教 学 难 点 稀 有 气 体 化 合 物 的 性 质 教 学 时 数 4 学 时 教 学 内 容 11-1 氢 11-2 稀 有 气 体 教 学 方 法
untitled
 六 不 數 量 料 度 BOD 來 BOD 料 量 料 量 量 料 量 兩 1.84 0.56 2 若 量 28 列 量 N14O16NO 2 N 2 O N 2 O 4 N 2 O 5 靈 六 龍 立 亮 利 C 5 H 8 不 列 狀 2 狀 1 參 2 1 1 1 率 數 8 不 度 c 數 4 8 12 16 度 0.80 0.60 0.40 0.20 mg/100ml 數 數 零 若 度
六 不 數 量 料 度 BOD 來 BOD 料 量 料 量 量 料 量 兩 1.84 0.56 2 若 量 28 列 量 N14O16NO 2 N 2 O N 2 O 4 N 2 O 5 靈 六 龍 立 亮 利 C 5 H 8 不 列 狀 2 狀 1 參 2 1 1 1 率 數 8 不 度 c 數 4 8 12 16 度 0.80 0.60 0.40 0.20 mg/100ml 數 數 零 若 度
试卷
 江 西 省 三 校 2016 届 高 三 联 考 化 学 试 题 可 能 用 到 的 相 对 原 子 质 量 :H=1 O=16 C=12 N=14 S=32 Na=23 Fe=56 Cu=64 一 选 择 题 ( 每 小 题 只 有 一 个 正 确 答 案, 每 小 题 3 分, 共 计 48 分 ) 1. 下 列 有 关 化 学 用 语 表 示 正 确 的 是 ( ) A. 水 分 子 的 球
江 西 省 三 校 2016 届 高 三 联 考 化 学 试 题 可 能 用 到 的 相 对 原 子 质 量 :H=1 O=16 C=12 N=14 S=32 Na=23 Fe=56 Cu=64 一 选 择 题 ( 每 小 题 只 有 一 个 正 确 答 案, 每 小 题 3 分, 共 计 48 分 ) 1. 下 列 有 关 化 学 用 语 表 示 正 确 的 是 ( ) A. 水 分 子 的 球
五花八门宝典(一).doc
 BBS...5... 11...23...26...31...46...49...54...55...57...59...62... 110... 114... 126... 132... 149 I "108" 1 2 3 4 BBS 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 M ( ) Kg S ( ) A ( ) K (
BBS...5... 11...23...26...31...46...49...54...55...57...59...62... 110... 114... 126... 132... 149 I "108" 1 2 3 4 BBS 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 M ( ) Kg S ( ) A ( ) K (
 1 1 1.1 1 1.1.1 1 1.1.2 2 1.1.3 3 1.2 3 1.2.1 3 1.2.2 4 1.2.3 5 1.2.4 5 1.2.5 6 1.3 8 1.3.1 8 1.3.2 10 1.3.3 10 1.3.4 11 1.3.5 11 1.4 12 1.4.1 12 1.4.2 15 1.4.3 16 2 18 2.1 18 2.1.1 18 2.1.2 20 2.1.3 24
1 1 1.1 1 1.1.1 1 1.1.2 2 1.1.3 3 1.2 3 1.2.1 3 1.2.2 4 1.2.3 5 1.2.4 5 1.2.5 6 1.3 8 1.3.1 8 1.3.2 10 1.3.3 10 1.3.4 11 1.3.5 11 1.4 12 1.4.1 12 1.4.2 15 1.4.3 16 2 18 2.1 18 2.1.1 18 2.1.2 20 2.1.3 24
An,,,,, 2, w(na 2O), w(cao),(ca B+Na B ) 1.34(B ),Na B<0.67,,, 1mm, ( 5-a) 1 Table1 Compositionandcalculationresultofplagioclaseinthequa
 1 : - - U-Pb 35 3 (CL) Fig.3 Cathodoluminescence(CL)imagesofzircongrainsfromtheJitoupluton 1600, : 15kV, 7 10-8 A, 1μm, ZAF Isoplot/Ex ver3 [9] [7] Fe 2+ Fe 3+ 2.2.2 U-Pb 3.1, 3.1.1, 150, ( 2-a,b),,, 0.5~2mm
1 : - - U-Pb 35 3 (CL) Fig.3 Cathodoluminescence(CL)imagesofzircongrainsfromtheJitoupluton 1600, : 15kV, 7 10-8 A, 1μm, ZAF Isoplot/Ex ver3 [9] [7] Fe 2+ Fe 3+ 2.2.2 U-Pb 3.1, 3.1.1, 150, ( 2-a,b),,, 0.5~2mm
< B2C43130B4C1A4C6BEC7ABFCA6D2B4C1A55A2E696E6464>
 2017 第9期 獨家發行 CHEMISTRY 專刊 電子檔索取QR http://www.facebook.com/chwachemistry https://goo.gl/6js7dx ፓ ᒙᡡ ᾦ ፍᚯ 員林高中 陳品誌老師 一 前言 依據 99 學年度實施之 普通高級中學課程綱要 簡稱 99 課綱 自 民國 102 年開始命題迄今為止共 5 年 且今年 106 年為 103 年課綱微調後 的第一年
2017 第9期 獨家發行 CHEMISTRY 專刊 電子檔索取QR http://www.facebook.com/chwachemistry https://goo.gl/6js7dx ፓ ᒙᡡ ᾦ ፍᚯ 員林高中 陳品誌老師 一 前言 依據 99 學年度實施之 普通高級中學課程綱要 簡稱 99 課綱 自 民國 102 年開始命題迄今為止共 5 年 且今年 106 年為 103 年課綱微調後 的第一年
Ps22Pdf
 (IP). /,. :, 2004 ISBN 7800159868.... G63383 IP ( 2004 ) 032949 / / 010-80602977 / ttp:wwwmagic365com / ( 34 : 100832) / / / ( : 010-80602977) / 8801230 1/ 16 / / / / / 4032 126 2005 1 1 2005 1 1 ISBN
(IP). /,. :, 2004 ISBN 7800159868.... G63383 IP ( 2004 ) 032949 / / 010-80602977 / ttp:wwwmagic365com / ( 34 : 100832) / / / ( : 010-80602977) / 8801230 1/ 16 / / / / / 4032 126 2005 1 1 2005 1 1 ISBN
Ⅰ Ⅱ Ⅲ Ⅳ
 Ⅰ Ⅱ Ⅲ Ⅳ !!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!
Ⅰ Ⅱ Ⅲ Ⅳ !!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!
Ⅰ Ⅱ1 2 Ⅲ Ⅳ
 Ⅰ Ⅱ1 2 Ⅲ Ⅳ 1 1 2 3 2 3 4 5 6 7 8 9 10 12 13 14 15 16 17 18 19 20 21 ~ 22 23 24 25 26 27 28 29 30 31 32 ~ 34 35 36 37 38 39 40 41 42 43 44 45 ~ 46 47 ~ ~ 48 49 50 51 52 54 55 56 57 58 59 60 61 62 63
Ⅰ Ⅱ1 2 Ⅲ Ⅳ 1 1 2 3 2 3 4 5 6 7 8 9 10 12 13 14 15 16 17 18 19 20 21 ~ 22 23 24 25 26 27 28 29 30 31 32 ~ 34 35 36 37 38 39 40 41 42 43 44 45 ~ 46 47 ~ ~ 48 49 50 51 52 54 55 56 57 58 59 60 61 62 63
 Ⅰ Ⅱ1 2 3 Ⅲ Ⅳ !!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!
Ⅰ Ⅱ1 2 3 Ⅲ Ⅳ !!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!
滴 加 液 体 解 析 :A 稀 释 浓 硫 酸 时, 要 把 浓 硫 酸 缓 缓 地 沿 器 壁 注 入 水 中, 同 时 用 玻 璃 棒 不 断 搅 拌, 以 使 热 量 及 时 地 扩 散 ; 一 定 不 能 把 水 注 入 浓 硫 酸 中 ; 图 中 所 示 操 作 正 确 B 铁 丝 在
 2015 年 贵 州 省 黔 西 南 州 中 考 真 题 化 学 一 选 择 题 ( 共 6 个 小 题, 每 小 题 2 分, 共 12 分 每 小 题 4 个 选 项 中 只 有 一 个 符 合 题 意, 多 选 不 选 错 选 均 不 得 分 ) 1.(2 分 ) 诗 词 名 著 是 中 华 民 族 灿 烂 文 化 的 瑰 宝 下 列 诗 句 或 名 著 事 件 的 描 述 中 只 涉 及 物
2015 年 贵 州 省 黔 西 南 州 中 考 真 题 化 学 一 选 择 题 ( 共 6 个 小 题, 每 小 题 2 分, 共 12 分 每 小 题 4 个 选 项 中 只 有 一 个 符 合 题 意, 多 选 不 选 错 选 均 不 得 分 ) 1.(2 分 ) 诗 词 名 著 是 中 华 民 族 灿 烂 文 化 的 瑰 宝 下 列 诗 句 或 名 著 事 件 的 描 述 中 只 涉 及 物
电 化 电 化 学 学 第 2 讲 原 电 池 一 教 学 目 标 理 解 原 电 池 的 工 作 原 理 并 正 确 书 写 电 极 反 应 和 总 反 应 方 程 式 知 识 导 航 构 造 条 件 构 造 及 工 作 原 理 工 作 原 理 燃 料 电 池 原 电 池 电 极 反 应 及 现
 www.xdf.cn 1 电 化 电 化 学 学 第 2 讲 原 电 池 一 教 学 目 标 理 解 原 电 池 的 工 作 原 理 并 正 确 书 写 电 极 反 应 和 总 反 应 方 程 式 知 识 导 航 构 造 条 件 构 造 及 工 作 原 理 工 作 原 理 燃 料 电 池 原 电 池 电 极 反 应 及 现 象 常 规 电 池 新 型 电 池 综 合 训 练 二 教 学 重 点 和
www.xdf.cn 1 电 化 电 化 学 学 第 2 讲 原 电 池 一 教 学 目 标 理 解 原 电 池 的 工 作 原 理 并 正 确 书 写 电 极 反 应 和 总 反 应 方 程 式 知 识 导 航 构 造 条 件 构 造 及 工 作 原 理 工 作 原 理 燃 料 电 池 原 电 池 电 极 反 应 及 现 象 常 规 电 池 新 型 电 池 综 合 训 练 二 教 学 重 点 和
( g/ cm 3 kg/ m 3 ) ; m ; V0, (cm 3 m 3 ), ;,,,,,,, ( ), ( ) ( ) : 0 = m V 0 ( 1.3) 0 ( kg/ m 3 ) ; m ( k g) ; V0( m 3 ),, ( k
 1,,, ( ),, ;, ;,,, 1.1 1.1.1 1.1.1.1 ( ),, : = m V (1.1 ) ( g/ cm 3 ) ; m ( g) ; V () (cm 3 ),,,,,,, 1.1.1.2,, : 0 = m V0 (1.2 ) 1.1 7 0 ( g/ cm 3 kg/ m 3 ) ; m ; V0, (cm 3 m 3 ), ;,,,,,,, 1.1.1.3 ( ),
1,,, ( ),, ;, ;,,, 1.1 1.1.1 1.1.1.1 ( ),, : = m V (1.1 ) ( g/ cm 3 ) ; m ( g) ; V () (cm 3 ),,,,,,, 1.1.1.2,, : 0 = m V0 (1.2 ) 1.1 7 0 ( g/ cm 3 kg/ m 3 ) ; m ; V0, (cm 3 m 3 ), ;,,,,,,, 1.1.1.3 ( ),
原子結構
 順序 1 2 3 4 5 化學式及化學反應式 內 容影 部聲 部 內容摘要 標題投影片 : 背景音樂 內容摘要 : 先備知識 分子式 化學反應方程式 反應方程式均衡 開場白 : 教師影像 各位同學大家 好 今天我們要 向各位同學介紹 化學式及化學反 應式 轉場投影片 標題投影片 : 背景音樂 先備知識 說明先備知識 : 教師影像 在說明化學式及 元素 : 化學反應方程式 組成所有物質的基本材料, 不
順序 1 2 3 4 5 化學式及化學反應式 內 容影 部聲 部 內容摘要 標題投影片 : 背景音樂 內容摘要 : 先備知識 分子式 化學反應方程式 反應方程式均衡 開場白 : 教師影像 各位同學大家 好 今天我們要 向各位同學介紹 化學式及化學反 應式 轉場投影片 標題投影片 : 背景音樂 先備知識 說明先備知識 : 教師影像 在說明化學式及 元素 : 化學反應方程式 組成所有物質的基本材料, 不
<4D6963726F736F667420576F7264202D20B5DAC1F9D5C22020BBD2B7D6BCB0BCB8D6D6D6D8D2AABFF3CEEFD4AACBD8BAACC1BFB5C4B2E2B6A8A3A8B8C4B9FDA3A92E646F63>
 第 六 章 灰 分 及 几 种 重 要 矿 物 元 素 含 量 的 测 定 第 一 节 灰 分 的 测 定 一 概 述 食 品 的 组 成 十 分 复 杂, 除 含 有 大 量 有 机 物 质 外, 还 含 有 丰 富 的 无 机 成 分, 这 些 无 机 成 分 包 括 人 体 必 须 的 无 机 盐 ( 或 称 矿 物 质 ), 其 中 含 量 较 多 的 有 Ca Mg K Na S P C1
第 六 章 灰 分 及 几 种 重 要 矿 物 元 素 含 量 的 测 定 第 一 节 灰 分 的 测 定 一 概 述 食 品 的 组 成 十 分 复 杂, 除 含 有 大 量 有 机 物 质 外, 还 含 有 丰 富 的 无 机 成 分, 这 些 无 机 成 分 包 括 人 体 必 须 的 无 机 盐 ( 或 称 矿 物 质 ), 其 中 含 量 较 多 的 有 Ca Mg K Na S P C1
侧 为 两 个 半 电 池 习 惯 上 把 正 极 写 在 右 边, 负 极 写 在 左 边 1.1.1.2 电 位 分 析 法 的 分 类 和 特 点 电 位 分 析 法 是 将 一 支 电 极 电 位 与 被 测 物 质 的 活 ( 浓 ) 度 1 有 关 的 电 极 ( 称 指 示 电 极 )
 1 电 位 分 析 法 1.1 基 本 原 理 1.2 直 接 电 位 法 1.3 电 位 滴 定 法 1.4 实 验 1.1 基 本 原 理 1.1.1 概 述 1.1.2 电 位 分 析 法 的 理 论 依 据 1.1.3 参 比 电 极 1.1.4 指 示 电 极 1.1.1 概 述 电 位 分 析 法 是 电 化 学 分 析 法 的 一 个 重 要 组 成 部 分 电 化 学 分 析 是 利
1 电 位 分 析 法 1.1 基 本 原 理 1.2 直 接 电 位 法 1.3 电 位 滴 定 法 1.4 实 验 1.1 基 本 原 理 1.1.1 概 述 1.1.2 电 位 分 析 法 的 理 论 依 据 1.1.3 参 比 电 极 1.1.4 指 示 电 极 1.1.1 概 述 电 位 分 析 法 是 电 化 学 分 析 法 的 一 个 重 要 组 成 部 分 电 化 学 分 析 是 利
Unit_19(C)N.indd
 5 19 19.1 18 3-19.1 (II) Mg(s) Mg 2+ (aq) + 2e + 2e 2e Mg 2+ Cu 2+ (II) 19.1-24 ionic half-equation 19 (II) Cu 2+ (aq) + 2e Cu(s) Mg(s) Mg 2+ (aq) + 2e Cu 2+ (aq) + 2e Cu(s) Mg(s) + Cu 2+ (aq) Mg 2+ (aq)
5 19 19.1 18 3-19.1 (II) Mg(s) Mg 2+ (aq) + 2e + 2e 2e Mg 2+ Cu 2+ (II) 19.1-24 ionic half-equation 19 (II) Cu 2+ (aq) + 2e Cu(s) Mg(s) Mg 2+ (aq) + 2e Cu 2+ (aq) + 2e Cu(s) Mg(s) + Cu 2+ (aq) Mg 2+ (aq)
生物考科 3 A B C D 答案 A 命題出處 7 12 測驗目標 評 析 2 AB C D 析 4 A B C D 答案 B 命題出處 2 測驗目標 析 A C H O N S B C D 21
 指定科目考試生物試題詳 臺南一中 郭人仲老師 第壹部分 : 選擇題 ( 占 71 分 ) 1 p 1 1/3 1 A B B C RNA D 答案 B 命題出處 4 2 11 測驗目標 析 A T C RNA D 2 A B C D T 20 答案 D 命題出處 6 11 測驗目標 析 A B C 生物考科 3 A B C D 答案 A 命題出處 7 12 測驗目標 評 析 2 AB C D 析 4
指定科目考試生物試題詳 臺南一中 郭人仲老師 第壹部分 : 選擇題 ( 占 71 分 ) 1 p 1 1/3 1 A B B C RNA D 答案 B 命題出處 4 2 11 測驗目標 析 A T C RNA D 2 A B C D T 20 答案 D 命題出處 6 11 測驗目標 析 A B C 生物考科 3 A B C D 答案 A 命題出處 7 12 測驗目標 評 析 2 AB C D 析 4
第九章 元素概论
 1. 2. 5 1. 2. 3. 4. p393:467p394:915p395: 16 12.1 VA ns 2 np 3 1. NH 4 ClNaNO 2 NH 4 NO 2 NaCl NH 4 NO 2 N22H 2 O 2. N 2 COP 351 1. N 2 3H 2 2NH ( ) 3 2NH 4 ClCa(OH) 2 CaCl22NH 3 2H 2 O 2NH 3 NH 4 NH 2
1. 2. 5 1. 2. 3. 4. p393:467p394:915p395: 16 12.1 VA ns 2 np 3 1. NH 4 ClNaNO 2 NH 4 NO 2 NaCl NH 4 NO 2 N22H 2 O 2. N 2 COP 351 1. N 2 3H 2 2NH ( ) 3 2NH 4 ClCa(OH) 2 CaCl22NH 3 2H 2 O 2NH 3 NH 4 NH 2
分 的 理 解 和 把 握, 对 基 础 知 识 多 回 顾 多 记 忆 北 京 新 东 方 学 校 优 能 中 学 高 中 理 综 项 目 3. 流 式 细 胞 仪 可 根 据 细 胞 中 DNA 含 量 的 不 同 对 细 胞 分 别 计 数 研 究 者 用 某 抗 癌 药 物 处 理 体 外
 北 京 市 2015 年 高 考 理 综 试 题 逐 题 解 析 北 京 新 东 方 优 能 中 学 高 中 理 综 项 目 1. 乙 肝 疫 苗 的 有 效 成 分 是 乙 肝 病 毒 的 一 种 抗 原, 接 种 该 疫 苗 后, 人 体 会 产 生 相 应 抗 体 该 抗 体 A. 由 T 淋 巴 细 胞 产 生 B. 可 与 多 种 抗 原 结 合 C. 可 裂 解 乙 肝 病 毒 D. 可
北 京 市 2015 年 高 考 理 综 试 题 逐 题 解 析 北 京 新 东 方 优 能 中 学 高 中 理 综 项 目 1. 乙 肝 疫 苗 的 有 效 成 分 是 乙 肝 病 毒 的 一 种 抗 原, 接 种 该 疫 苗 后, 人 体 会 产 生 相 应 抗 体 该 抗 体 A. 由 T 淋 巴 细 胞 产 生 B. 可 与 多 种 抗 原 结 合 C. 可 裂 解 乙 肝 病 毒 D. 可
( ) 039 (CIP) /. :, ISBN TS CIP ( 2005) : : : : * ( ) : ( 010 ) / www. cip. com. cn
 ( ) 039 (CIP) /. :, 2005. 3 ISBN 7-5025-6678-3... -. TS211. 4 CIP ( 2005) 012222 : : : : * ( 3 100029 ) : ( 010 ) 64982530 http:/ / www. cip. com. cn * 850mm 1168mm 1/ 32 7 196 2005 4 1 2005 4 1 ISBN 7-5025-6678-3/
( ) 039 (CIP) /. :, 2005. 3 ISBN 7-5025-6678-3... -. TS211. 4 CIP ( 2005) 012222 : : : : * ( 3 100029 ) : ( 010 ) 64982530 http:/ / www. cip. com. cn * 850mm 1168mm 1/ 32 7 196 2005 4 1 2005 4 1 ISBN 7-5025-6678-3/
zw.PDF
 1 He2+ 4 2 2.1 SI C SI kg * u ** e -1.6022 10-19 -1 9.1096 10-31 0.00055 p +1.6022 10-19 +1 1.6726 10-27 1.0073 n 0 1.6749 10-27 1.0087 H 1.673 10-27 1.008 * 1 ** u 12 C=12.000000 1u=1.6605 10-27 kg
1 He2+ 4 2 2.1 SI C SI kg * u ** e -1.6022 10-19 -1 9.1096 10-31 0.00055 p +1.6022 10-19 +1 1.6726 10-27 1.0073 n 0 1.6749 10-27 1.0087 H 1.673 10-27 1.008 * 1 ** u 12 C=12.000000 1u=1.6605 10-27 kg
Microsoft PowerPoint - senior2-1 [相容模式]
![Microsoft PowerPoint - senior2-1 [相容模式] Microsoft PowerPoint - senior2-1 [相容模式]](/thumbs/76/73920043.jpg) 第一章物質的狀態及其反應 1-11 物質的狀態變化 1-2 粒子概念 1-3 化學式與化學反應式 1-4 化學反應的類型 1-5 化學反應熱 相 (phase) 定義 : 相, 就是 相態 介面 的意思 具有同一密度 ( 或同一範圍 ) 的範圍, 稱之 同一相 物質的三個相 : 固相 (solid) 液相 (liquid) 氣相 (gas)( 又稱物質三態 ) 氣體液體固體 三相的比較 固相 (solid)
第一章物質的狀態及其反應 1-11 物質的狀態變化 1-2 粒子概念 1-3 化學式與化學反應式 1-4 化學反應的類型 1-5 化學反應熱 相 (phase) 定義 : 相, 就是 相態 介面 的意思 具有同一密度 ( 或同一範圍 ) 的範圍, 稱之 同一相 物質的三個相 : 固相 (solid) 液相 (liquid) 氣相 (gas)( 又稱物質三態 ) 氣體液體固體 三相的比較 固相 (solid)
校园之星
 K K K Keration K K K K K K K K Kt GF K K ppm CO Fe Fe Mn Cu TiFeMnCr NiYU Fe Fe Smaragdos Al O Al O A Sio F OH Opal Zr SiO BaSO Fe O ph Na BOH H O FeMnAl MgFeSiAl
K K K Keration K K K K K K K K Kt GF K K ppm CO Fe Fe Mn Cu TiFeMnCr NiYU Fe Fe Smaragdos Al O Al O A Sio F OH Opal Zr SiO BaSO Fe O ph Na BOH H O FeMnAl MgFeSiAl
碳石墨產品表面處理和新研發產品 / 技術服務 東洋炭素相信碳的無限可能, 而且我們積極開展的基礎和應用研究永無止境 表面處理產品 PYROGRAPH 產品 55 PERMA KOTE 產品 56 新研發產品 59 技術服務 62 分析技術 65
 碳石墨產品表面處理和新研發產品 / 技術服務 東洋炭素相信碳的無限可能, 而且我們積極開展的基礎和應用研究永無止境 表面處理產品 PYROGRAPH 產品 55 PERMA KOTE 產品 56 新研發產品 59 技術服務 62 分析技術 65 表面處理產品 PYROGRAPH 產品 PYROGRAPH (CVD) PYROGRAPH 產品特點 PYROGRAPH 20 µm 用途 OLED PYROGRAPH
碳石墨產品表面處理和新研發產品 / 技術服務 東洋炭素相信碳的無限可能, 而且我們積極開展的基礎和應用研究永無止境 表面處理產品 PYROGRAPH 產品 55 PERMA KOTE 產品 56 新研發產品 59 技術服務 62 分析技術 65 表面處理產品 PYROGRAPH 產品 PYROGRAPH (CVD) PYROGRAPH 產品特點 PYROGRAPH 20 µm 用途 OLED PYROGRAPH
第一章 绪 论
 环 境 监 测 主 编 : 王 怀 宇 姚 运 先 高 等 教 育 出 版 社 内 容 提 要 本 书 将 环 境 监 测 的 对 象 进 行 了 明 确 的 分 类, 详 细 讲 述 了 各 种 监 测 技 术 的 基 础 理 论 和 手 段 内 容 包 括 环 境 监 测 绪 论 环 境 监 测 质 量 控 制 水 体 监 测 大 气 监 测 噪 声 监 测 土 壤 与 固 体 废 物 监 测
环 境 监 测 主 编 : 王 怀 宇 姚 运 先 高 等 教 育 出 版 社 内 容 提 要 本 书 将 环 境 监 测 的 对 象 进 行 了 明 确 的 分 类, 详 细 讲 述 了 各 种 监 测 技 术 的 基 础 理 论 和 手 段 内 容 包 括 环 境 监 测 绪 论 环 境 监 测 质 量 控 制 水 体 监 测 大 气 监 测 噪 声 监 测 土 壤 与 固 体 废 物 监 测
在餐點設計時, 往往會運用不同的質地做搭配, 以達到食用者口感的最佳平衡與變化
 百變的 廚房世界 廚藝與感官的饗宴 5 26 2014 2 494 在餐點設計時, 往往會運用不同的質地做搭配, 以達到食用者口感的最佳平衡與變化 2014 2 494 27 28 2014 2 494 食物的物理變化 5 廚房好比是一個食物實驗室, 運作時, 都在進行無數的物理與化學變化, 才能把樸實的原料食材轉為一道道令人驚嘆的美味 食物的化學變化 C 2014 2 494 29 62 65 廚房的魔術秀
百變的 廚房世界 廚藝與感官的饗宴 5 26 2014 2 494 在餐點設計時, 往往會運用不同的質地做搭配, 以達到食用者口感的最佳平衡與變化 2014 2 494 27 28 2014 2 494 食物的物理變化 5 廚房好比是一個食物實驗室, 運作時, 都在進行無數的物理與化學變化, 才能把樸實的原料食材轉為一道道令人驚嘆的美味 食物的化學變化 C 2014 2 494 29 62 65 廚房的魔術秀
>> 韩 业 军 钢 铁 事 业 部 TEL: 基 础 研 发 报 告 2013 年 9 月 16 日 铁 矿 石 基 础 知 识 铁 矿 石 是 自 然 界 中 存 在 的 可 用 做 炼 铁 原 料 的 含 铁 的 矿 物, 是 钢 铁 生 产 企 业 的 重 要 原
 目 录 一 铁 矿 石 分 类... 2 二 铁 矿 石 的 品 位 影 响 因 素... 3 三 铁 矿 石 质 量 评 价... 4 四 铁 矿 石 的 处 理 方 法... 8 五 铁 矿 石 资 源 分 布... 10 1. 世 界 铁 矿 石 资 源 分 布... 10 2. 我 国 铁 矿 石 资 源 分 布... 12 3. 我 国 铁 矿 石 进 口 情 况... 13 4. 铁 矿
目 录 一 铁 矿 石 分 类... 2 二 铁 矿 石 的 品 位 影 响 因 素... 3 三 铁 矿 石 质 量 评 价... 4 四 铁 矿 石 的 处 理 方 法... 8 五 铁 矿 石 资 源 分 布... 10 1. 世 界 铁 矿 石 资 源 分 布... 10 2. 我 国 铁 矿 石 资 源 分 布... 12 3. 我 国 铁 矿 石 进 口 情 况... 13 4. 铁 矿
<4D6963726F736F667420576F7264202D20BBB7C6C0B1A8B8E6CAE9D7CAD6CA312E646F63>
 天 锰 新 材 料 生 产 项 目 环 境 影 响 报 告 书 编 制 人 员 名 单 表 主 持 编 制 机 构 : 重 庆 市 环 境 保 护 工 程 设 计 研 究 院 有 限 公 司 编 制 主 持 人 职 ( 执 ) 业 资 登 记 ( 注 册 证 ) 姓 名 专 业 类 别 格 证 书 编 号 编 号 肖 骏 0008882 B31060080400 化 工 石 化 医 药 类 本 人
天 锰 新 材 料 生 产 项 目 环 境 影 响 报 告 书 编 制 人 员 名 单 表 主 持 编 制 机 构 : 重 庆 市 环 境 保 护 工 程 设 计 研 究 院 有 限 公 司 编 制 主 持 人 职 ( 执 ) 业 资 登 记 ( 注 册 证 ) 姓 名 专 业 类 别 格 证 书 编 号 编 号 肖 骏 0008882 B31060080400 化 工 石 化 医 药 类 本 人
<433A5C446F63756D656E747320616E642053657474696E67735C41646D696E6973747261746F725CD7C0C3E65CB9ABCABEB8E55C31D6D3C9BDBAEAD4B4BFF3D2B5B1A8B8E6A3A8B9ABCABEA3A92E646F63>
 钟 山 县 宏 源 矿 业 有 限 公 司 金 盘 地 铅 锌 银 矿 环 境 影 响 报 告 书 公 示 稿 中 国 有 色 桂 林 矿 产 地 质 研 究 院 有 限 公 司 二 零 一 五 年 八 月 目 录 前 言...1 1 建 设 项 目 的 特 点... 1 2 环 境 影 响 评 价 的 工 作 过 程... 1 3 关 注 的 主 要 环 境 问 题... 2 4 环 境 影 响
钟 山 县 宏 源 矿 业 有 限 公 司 金 盘 地 铅 锌 银 矿 环 境 影 响 报 告 书 公 示 稿 中 国 有 色 桂 林 矿 产 地 质 研 究 院 有 限 公 司 二 零 一 五 年 八 月 目 录 前 言...1 1 建 设 项 目 的 特 点... 1 2 环 境 影 响 评 价 的 工 作 过 程... 1 3 关 注 的 主 要 环 境 问 题... 2 4 环 境 影 响
第四章 自然环境及社会经济概况
 证 书 编 号 : 国 环 评 证 乙 字 第 2904 号 崇 左 红 狮 水 泥 窑 协 同 处 置 10 万 吨 / 年 工 业 废 物 项 目 环 境 影 响 报 告 书 ( 公 示 稿 ) 建 设 单 位 : 崇 左 红 狮 环 保 科 技 有 限 公 司 编 制 单 位 : 广 西 宇 宏 环 保 咨 询 有 限 公 司 编 制 时 间 : 二 〇 一 五 年 十 一 月 前 言 项
证 书 编 号 : 国 环 评 证 乙 字 第 2904 号 崇 左 红 狮 水 泥 窑 协 同 处 置 10 万 吨 / 年 工 业 废 物 项 目 环 境 影 响 报 告 书 ( 公 示 稿 ) 建 设 单 位 : 崇 左 红 狮 环 保 科 技 有 限 公 司 编 制 单 位 : 广 西 宇 宏 环 保 咨 询 有 限 公 司 编 制 时 间 : 二 〇 一 五 年 十 一 月 前 言 项
,3? 1 1,2 1 1,2 ::90 1 1,1 1 1,3 1 1,2 1 1,4 1 1, ,2 1 1,1 1 1,4 ( ) 1 1,1 2 :1 1,1 1 1,8 1 1,1 1 1,4 1 1,2 1 1,10 1 1,6 1 1,
 2002 2000 1 1,1 :1 1,6 : : 1 1,1 :1 1,5 1 1,1 1 1,2 :1 1,4 1 1,10 1 1,12 1 1,1 1 1,2 1 1,6 20 1 1,6 1 1, 202 2002 1 1,3? 1 1,2 1 1,2 ::90 1 1,1 1 1,3 1 1,2 1 1,4 1 1,1 3 2 1 1,2 1 1,1 1 1,4 (1935 1937
2002 2000 1 1,1 :1 1,6 : : 1 1,1 :1 1,5 1 1,1 1 1,2 :1 1,4 1 1,10 1 1,12 1 1,1 1 1,2 1 1,6 20 1 1,6 1 1, 202 2002 1 1,3? 1 1,2 1 1,2 ::90 1 1,1 1 1,3 1 1,2 1 1,4 1 1,1 3 2 1 1,2 1 1,1 1 1,4 (1935 1937

 Ⅰ Ⅱ1 2 Ⅲ Ⅳ 1 2 1
Ⅰ Ⅱ1 2 Ⅲ Ⅳ 1 2 1 