3. 使用 etanercept adalimumab ustekinumab 或 secukinumab 時 cyclosporine 及照光治療, 考慮 etanercept adalimumab ustekinumab 或 secukinumab 於乾癬療效可能較慢, 及立即停藥之可能反彈現象
|
|
|
- 面 靳
- 9 years ago
- Views:
Transcription
1 財團法人醫藥品查驗中心 Center For Drug Evaluation 可善挺注射液劑 / 凍晶乾粉注射劑 150 毫克 / 毫升 (Cosentyx ) 醫療科技評估報告 104CDR09027_Cosentyx 藥物納入全民健康保險給付建議書 - 藥品專用 資料摘要 藥品名稱建議者藥品許可證持有商含量規格劑型主管機關許可適應症建議健保給付之適應症內容建議健保給付條件 可善挺注射液劑成分 secukinumab 可善挺凍晶乾粉注射劑台灣諾華股份有限公司同上 (1). 單位含量 :150 毫克 (2). 包裝規格量 : (a) 注射液劑 150 毫克 / 毫升 (b) 凍晶乾粉注射劑 150 毫克 / 毫升 (3). 劑型 : 注射液劑 / 凍晶乾粉注射劑治療適合接受全身性治療的中至重度斑塊性乾癬成人患者 同其他乾癬生物製劑之健保給付範圍 無 有 Secukinumab(Cosentyx): 用於乾癬治療 1. 給付條件 : 限用於經照光治療及其他系統性治療無效, 或因醫療因素而無法接受其他系統性治療之全身慢性中 重度之乾癬或頑固之掌蹠性乾癬, 且影響功能之患者 (1)~(5) 略 2. 需經事前審查核准後使用 : (1). 初次申請時, 以 6 個月為 1 個療程, 持續使用時每 6 個月需再申報一次, 且應於期滿前 1 個月提出 (2). 紅皮症乾癬病患以 6 個月為限, 於 6 個月療程結束後, 應回復使用 cyclosporin, 除非產生腎功能異常 (Creatinine 基礎值上升 30%), 或其他無法有效控制之副作用, 減藥後乾癬仍無法有效控制 (3)~(7) 略 (8) secukinumab 起始時於第 週投予 300mg, 接著於第 4 週開始每 4 週投予 300mg( 體重 60kg, 投予 150mg 的劑量 ), 且於 12 週時, 需先行評估, 至少有 PASI 25 療效 1/68
2 3. 使用 etanercept adalimumab ustekinumab 或 secukinumab 時 cyclosporine 及照光治療, 考慮 etanercept adalimumab ustekinumab 或 secukinumab 於乾癬療效可能較慢, 及立即停藥之可能反彈現象, 治療前兩個月得合併使用, 但 etanercept adalimumab ustekinumab 或 secukinumab 療效出現時即應逐漸停用 4. 需排除使用的情形應參照藥物仿單, 重要之排除使用狀況包括 : (1). 懐孕或正在授乳的婦女 (2). 罹患活動性的感染症的病患 (3). 未經完整治療之結核病的病患 ( 包括潛伏結核感染治療未達四週者, 申請時應檢附潛伏結核感染篩檢紀錄及治療紀錄供審查 ) (4). 身上帶有人工關節者, 罹患或先前曾罹患過嚴重的敗血病 (sepsis) 者 (5). 惡性腫瘤或具有癌症前兆 (pre-malignancy) 的病患 (6). 免疫功能不全者 (immunodeficiency) 5. 需停止治療情形, 如果發生下列現象應停止治療 : (1). 不良事件, 包括 : i. 惡性腫瘤 ii. 該藥物引起的嚴重性毒性 iii. 懷孕 ( 暫時停藥即可 ) iv. 嚴重的間發性感染症 (intercurrent infection)( 暫時停藥即可 ) (2). 療效不彰 : 患者經過 6 個月治療 ( 初次療程 ) 後未達療效者, 療效定義指 PASI 或體表面積改善未達 50% 6. 暫緩續用之相關規定 : (1). 暫緩續用時機 : 使用生物製劑治療 2 年後符合 PASI 10 者 (2). 因使用一種生物製劑治療後療效不彰, 而轉用另一種不同藥理機轉之生物製劑, 以轉用後者之起始日重新計算 2 年後開始減量之時機 但因無法忍受副作用而轉用相同藥理機轉之生物製劑, 轉用前後所使用生物製劑之期間均應計入 7. 暫緩續用後若疾病再復發, 可重新申請使用, 需符合至少有 50% 復發 ( 需附上次療程治療前 後, 及本次照片 ) 建議療程每日劑量 : (1). 一般劑量 :secukinumab 300 毫克 2/68
3 建議者自評是否屬突破創新新藥健保是否還有給付其他同成分藥品 (2). 最大劑量 : 無 非突破創新新藥 突破創新新藥 無同成分 ( 複方 ) 健保給付藥品 有, 藥品名為, 從民國年月日起開始給付 醫療科技評估報告摘要 摘要說明 : 一 參考品 : 以 etanercept 與 ustekinumab 為療效參考品, 以 ustekinumab 為核價參考首選 二 主要醫療科技評估組織之給付建議 : 參考表二 三 相對療效與安全性 ( 人體健康 ): 相關資料包括四項隨機分派 雙盲 平行分組 多中心之第三期臨床試驗 (A2302 [ERASURE] A2303 [FIXTURE] A2308 [FEATURE] A2309 [JUNCTURE]) 總結 secukinumab 的療效與藥物安全性分析結果如下 : 療效評估部份 : 試驗 12 周的統合分析結果顯示, 針對共同主要療效指標的評估,secukinumab 150 毫克與 300 克的表現皆優於安慰劑 ( 具統計顯著意義 ), 而這個結果也與個別試驗的結果方向一致 ;A2303 試驗則顯示與 etancercpt 比較的結果,secukinumab 150 毫克與 300 克的表現皆優於 etanercept( 具統計顯著意義 ) 試驗 52 周的統合分析結果顯示,secukinumab 組的療效皆得以良好延續至 52 周, 尤其以 300 毫克組表現更佳 共同療效指標的表現於試驗第 16 周達到平原期, 隨後緩慢下降 受試者的復發率也以 secukinumab 300 毫克組最低 (7.4%;150 毫克 17.1%;etancercept 21.1%, 安慰劑 28.6%) 安全性評估部份 : 300 毫克的安全性表現並未統計顯著與 150 毫克之表現有所差異 用於乾癬治療的生物製劑的典型不良事件, 例如感染 嗜中性白血球低下 (neutropenia) 過敏反應 (hypersensitivity) 等同樣被觀察到, 但是, 沒有觀察到分枝桿菌感染 (mycobacterial infection) 或嚴重伺機性感染 (opportunistic infection) 增加的情形 與其他用於乾癬治療的全身性療法相比, 並沒有需要額外注意之處 四 醫療倫理 : 無相關系統性收集之資訊可供參考 五 成本效益 : 建議者有提供國內藥物經濟學研究, 其分析結果顯示乾癬中度至重 3/68
4 度病人在基礎方案中, 預期平均每位接受 secukinumab 300mg 治療病人之第一 二及十年的醫療花費約為新台幣 319,094 元 506,849 元及 1,403,732 元 ; 與其他組別相比之下的遞增 QALYs 及遞增成本效益比值 (incremental cost-effectiveness ratio, ICER) 如下 : (1) 分析時間為一年時,secukinumab 300mg 分別與 ustekinumab 45 mg etanercept 及 adalimumab 相比之下的 ICER 值 ( 新臺幣 /QALY) 為 : 8,052,740 元 6,554,137 元及 5,136,024 元 ; 增加的 QALYs 分別為 及 0.04 QALY (2) 分析時間為兩年時,secukinumab 300mg 分別與 ustekinumab 45 mg etanercept 及 adalimumab 相比之下的 ICER 值 ( 新臺幣 /QALY) 為 : 6,378,570 元 5,255,886 元及 4,438,153 元 ; 增加的 QALYs 分別為 及 QALY (3) 分析時間為十年時,secukinumab 300mg 分別與 ustekinumab 45 mg etanercept 及 adalimumab 相比之下的 ICER 值 ( 新臺幣 /QALY) 為 : 4,981,114 元 4,280,180 元及 3,913,706 元 ; 增加的 QALYs 分別為 及 QALY 查驗中心認為建議者所提出的國內藥物經濟學研究報告的研究主題與研究設計與其建議給付規定大抵相近, 惟存有部分疑義與限制 在療效部分使用間接比較所得參數, 使得不確定性增加 ; 且在單維敏感度分析部分並沒有呈現納入分析參數之高低值, 無法判別其不確定性來源 藥費部分, 依建議者藥費計算處敘述, 藥品單價較建議者申請健保給付價低, 且少算了施打起始及維持劑量各一次, 藥費應為低估值, 連帶造成 secukinumab 比上另外三種生物製劑之 ICER 值可能被低估 六 財務衝擊 : 建議者認為本品若納入給付, 每年接受治療患者約 名, 年度藥費影響約 1,800 萬元至 5,500 萬元 查驗中心認為建議者預算影響分析架構大致清楚, 但病人數可能因估算方式及市占率等種種假設而低估藥費影響 查驗中心重新估算後, 認為本品若納入健保給付, 各年使用人數約 230 至 2,000 人, 扣除可取代的現有治療費用後, 額外增加之年度藥費約 3 千 3 百萬至 2.9 億元 惟考量國內流行病學資料尚有不足, 乾癬處方型態複雜, 且可使用本品之病人數應不會一直維持高成長率, 許多參數估計具有不確定性, 決策者應謹慎解釋預算影響分析結果 4/68
5 表一本次提案藥品與目前健保已收載藥品 ( 參考品 ) 之比較資料 本案藥品參考品 1 商品名可善挺 Cosentyx 主成分 / 含量 Secukinumab 150mg 喜達諾 Stelara Ustekinumab 45mg/0.5mL 及 90mg/1mL 劑型 / 包裝注射液劑 / 凍晶乾粉注射劑預充填式注射劑 WHO/ATC 碼 主管機關許可適應症 健保給付條件 L04AC10 治療適合接受全身性治療的中至重度斑瑰性乾癬成人患者 擬訂中 L04AC05 1. 乾癬 (Ps) Stelara 適用於治療適合接受光療法或全身性治療的中至重度斑塊性乾癬成人患者 (18 歲 ( 含 ) 以上 ) 2. 乾癬性關節炎 (PsA) Stelara 適用於治療對疾病緩解型抗風濕性藥物 (DMARDs) 療效不佳之成人 (18 歲及以上 ) 活動性乾癬性關節炎 Stelara 可單獨使用, 亦可與 methotrexat(mtx) 併用 第 8 節免疫製劑 Immunologic agents Etanercept( 如 Enbrel); adalimumab( 如 Humira); ustekinumab( 如 Stelara)(98/11/1 100/7/1 101/5/1 101/12/1 102/1/1 104/4/1): 用於乾癬治療部分 健保給付價擬訂中 100,329 仿單建議劑量與用法 仿單建議每次劑量為 secukinumab 300 mg 起始時於第 0,1,2,3 和 4 週皮下注射, 接著於第 4 週開始每 4 週皮下注射 每次 300 mg 劑量為給與兩次 150 mg 皮下注射 有些病人 ( 例如體重較輕者,<=60 kg), 可給與 150 mg 的劑量 乾癬 對體重 100 公斤 (220 磅 ) 的患者, 建議劑量為於開始時及 4 週後投予 45 毫克, 然後每 12 週投予 45 毫克 對體重 >100 公斤 (220 磅 ) 的患者, 建議劑量為於開始時及 4 週後投予 90 毫克, 然後每 12 週投予 5/68
6 療程符合給付條件下長期使用同左 90 毫克 對體重 >100 公斤的患者,45 毫克的劑量也證實可產生療效 不過, 這類患者使用 90 毫克的劑量可達到較佳的療效 乾癬性關節炎 建議劑量為於開始時及 4 週後投予 45 毫克, 然後每 12 週投予 45 毫克 對併有中至重度斑塊性乾癬且體重 >100 公斤 (220 磅 ) 的患者, 建議劑量為於開始時及 4 週後投予 90 毫克, 然後每 12 週投予 90 毫克 每療程 花費 擬訂中 具直接比較試驗 (head-to-head comparison) 具間接比較 (indirect comparison) 近年來, 最多病人使用或使用量最多的藥品 目前臨床治療指引建議的首選 一年約 50 萬 ˇ ˇ ˇ 其他考量因素, 請說明 : 註 : 若經審議認定本品屬於突破創新新藥, 則表列之參考品僅供療效比較, 而不做為核價之依據 ; 若審 議認定本品尚不屬於突破創新新藥, 則表列之參考品可做為療效比較及核價之依據 6/68
7 表二主要醫療科技評估組織之給付建議 來源 CADTH/pCODR ( 加拿大 ) PBAC( 澳洲 ) NICE( 英國 ) 最新給付建議民國 104 年 10 月 28 日公告, 委員會建議給付 secukinumab, 做為適合接受全身性治療 (systemic therapy) 或照光治療 (phototherapy) 的中至重度斑塊性乾癬成人患者的治療藥物, 且符合以下條件者 : (1). 治療 12 周後, 如果乾癬面積暨嚴重度指數 (Psoriasis Area Severity Index) PASI75 評估未達標, 則停止治療 (2). Secukinumab 的治療費用不得超過已給付用於中至重度斑塊性乾癬之生物製劑中價格最低者 於民國 104 年 3 月公告, 基於與 adalimumab 比較符合最小成本的基礎 (cost-minimisation basis), 委員會同意在設定給付規範的條件下給付 secukinumab, 做為非生物性疾病修飾抗風濕類藥物 (DMARDs) 治療失敗的慢性重度斑塊性乾癬病人的治療用藥 詳細給付規定內容請參閱附錄二 於民國 104 年 7 月公告, 委員會建議給付 secukinumab 做為符合下列條件之斑塊性乾癬成年病人的治療用藥 : (1). 疾病嚴重度屬於重度, 定義為 PASI(Psoriasis Area Severity Index) 分數在 10 分或以上, 而且,DLQI(Dermatology Life Quality Index) 分數也大於 10 分 (2). 經過標準全身性治療失敗後的病人, 例如,cyclosporine methotrexate 光化學療法(psoralen and long-wave ultraviolet radiation, PUVA), 或者, 屬於這些治療禁忌症的病人, 或者, 病人無法耐受這些治療 (3). 廠商同意提供價格折讓 ( 進行風險分攤方案 ) 如果病人接受 secukinumab 治療 12 周後, 乾癬症狀未有適當反應者應停藥 治療獲得適當反應的定義為 : (1). 與起始治療時的表現相比,PASI 分數有 75% 的降低 (PASI 75); 或 (2). 與起始治療時的表現相比, PASI 分數有 50% 的降低 (PASI50), 而且 DLQI 分數降低五分 註 :CADTH 為 Canadian Agency for Drugs and Technologies in Health 加拿大藥品及醫療科技評估機構的縮寫 ; pcodr 為 pan-canadian Oncology Drug Review 加拿大腫瘤藥物共同評估組織的縮寫, 於 2010 年成立成為 CADTH 的合作夥伴, 主要負責評估新腫瘤藥物的臨床證據及成本效益 ; 7/68
8 PBAC 為 Pharmaceutical Benefits Advisory Committee 藥品給付諮詢委員會的縮寫 ; NICE 為 National Institute for Health and Care Excellence 國家健康暨照護卓越研究院的縮寫 8/68
9 可善挺注射液劑 / 凍晶乾粉注射劑 醫療科技評估報告 前言 : 報告撰寫人 : 財團法人醫藥品查驗中心醫藥科技評估組 報告完成日期 : 民國 104 年 11 月 27 日 近年來世界各國積極推動醫療科技評估制度, 做為新藥 新醫材給付決策參考, 以促使有限的醫療資源能發揮最大功效, 提升民眾的健康福祉 醫療科技評估乃運用系統性回顧科學實證證據的方式, 對新穎醫療科技進行療效與經濟評估 為建立一專業 透明 且符合科學性的醫療科技評估機制, 財團法人醫藥品查驗中心 ( 以下簡稱查驗中心 ) 受衛生福利部委託, 對於建議者向衛生福利部中央健康保險署 ( 以下簡稱健保署 ) 所提出之新醫療科技給付建議案件, 自收到健保署來函後, 在 42 個日曆天內完成療效與經濟評估報告 ( 以下稱本報告 ), 做為全民健康保險審議藥品給付時之參考, 並於健保署網站公開 惟報告結論並不代表主管機關對本案藥品之給付與核價決議 本報告彙整國外主要醫療科技評估組織對本案藥品所作之評估結果與給付建議, 提醒讀者各國流行病學數據 臨床治療型態 資源使用量及單價成本或健康狀態效用值可能與我國不同 另本報告之臨床療效分析僅針對本建議案論述, 讀者不宜自行引申為其醫療決策之依據, 病人仍應與臨床醫師討論合適的治療方案 一 疾病治療現況 [1-7] 針對本案藥品 Cosentyx(secukinumab) 此次申請健保給付的適應症 斑塊性乾癬, 以 乾癬 斑塊性乾癬 psoriasis plaque psoriasis 等關鍵字進行網頁搜尋, 獲得數篇由國內醫事人員發表的文章 台灣皮膚科醫學會發表的病人衛教手冊, 以及美國皮膚科醫學會 (The American Academy of Dermatology) 發表的診療指引 以下將綜合所有資料簡要介紹乾癬 乾癬是一項影響身體多重系統的疾病, 主要侵犯皮膚與關節 典型的皮膚表現為紅斑 (erythema) 及脫屑 (scaling), 又稱為銀屑病 [5] 乾癬成因不明, 除遺傳外, 其他都只能算是乾癬的誘發或是惡化因素, 包括外傷 感染 壓力 藥物 內分泌等 [5] 乾癬皮膚病灶的形態相當多樣化, 所有皮膚都有產生乾癬的可能 乾癬的皮膚表現有四大特點 :(1) 界限清楚而明顯 ; (2) 表面有鬆散的銀屑 ; (3) 在皮屑之下的皮膚為滑亮均質的紅斑 ; (4) 有 Auspitz sign, 也就是用機械性方式移去皮屑後在紅色表皮上出現小血滴,20% 的病人會有 Koebner's 現象, 就是皮膚受傷處會誘發乾癬形成 除此之外, 有相當比例的乾癬會造成關節疾患, 也就是乾癬性關節病 9/68
10 變,50% 的病人手指甲及 35% 病人的腳趾甲會被侵犯, 產生指甲凹陷 黃斑 嚴 重變形, 常被誤認為黴菌感染 [5] 臨床上乾癬主要可分為斑塊型 (plaque) 乾癬 反轉型 (inverse) 乾癬 紅皮型 (erythrodermic) 乾癬 膿疱型 (pustular) 乾癬 點滴狀 (guttate) 乾癬等類型 其中, 斑塊型乾癬是最常見的類型, 約占所有乾癬病人的 80%~90%, 主要表現為界線 清楚的紅色斑塊, 大小由一公分至數公分不等, 病人體表可能僅有少數幾個斑塊 或者斑塊佈滿全身 這些斑塊多為不規則形, 分布於頭皮 軀幹 臀部或四肢 根據研究顯示,80% 的乾癬病人其疾病嚴重程度屬輕至中度,20% 的病人屬中至 重度, 而這些中至重度的乾癬病人多半有超過 5% 的體表面積受到影響, 或者, 影響到身體其他重要部位, 如手 足 臉部 生殖器等 一般來說, 乾癬可經由臨床症狀診斷, 個別可疑個案作病理切片可能有幫 助, 但是也可能導致局部切片處乾癬惡化 實驗室檢查不具特異性, 除了全身膿 疱型乾癬和紅皮型乾癬性之外, 多數病人都無異常 [5] 乾癬的治療方式依照個別病人的病史 疾病嚴重度 ( 輕至中度 中至重度 ) 藥物耐受程度與副作用而定, 可以分為局部治療與全身性治療 (systemic therapy) 局部治療包含局部照光 a (phototherapy) 或塗藥 b c, 全身性治療包含全身 性照光 口服藥物 針劑注射等 全身性治療效果較好, 而局部治療較安全, 適 合病灶範圍小且病情穩定的患者 [5] 表一所呈現者, 為美國皮膚科醫學會建議 之治療流程及我國健保署的給付規定 表一 乾癬治療方案 ( 美國皮膚科醫學會建議 vs. 台灣健保署給付規定 ) 單位美國皮膚科醫學會建議 [1, 2] 台灣健保署給付規定 [8] 目標族群 e 建議內容 第一線 慢性斑塊性乾癬成年男性病患 ( 病灶 >5% 體表面積 ) 不具乾癬性關節炎者 d UVB 照光治療 ; 或 UVB 照光治療 +acitretin; 或 PUVA 照光治療 ; 或 UVB 照光治療 +MTX 乾癬病人 照光治療 ; 或 / 和 系統性治療 f 第二線 Acitretin+ 生物製劑 g ; 或生物製劑 Adalimumab a 照光療法包括光化學療法 (PUVA) 浸泡式光化學療法 中波紫外線光療 (UVB) 等 b 外用藥物包括外用維生素 D 及衍生物 外用維生素 A 酸 焦油 類固醇 保濕劑等 c 用於全身性治療的藥物包括 methotrexate(mtx) 環孢黴素 (cyclosporine) 口服維生素 A 酸 全身性類固醇 生物製劑 ( 如 adalimumab etanercept infliximab ustekinumab 等 ) d 醫學會同時針對一般婦女 意欲懷孕婦女 同時患有乾癬性關節炎之成年患者皆分別給予治療建議, 因主要建議內容相近, 故而, 此處予以略過 e 此處建議之第一線與第二線治療選項, 其內容並非依照療效表現優劣而前後排序 f 此處所指之系統性治療包括 methotrexate acitretin cyclosporine 等藥物 g 此處之生物製劑包含 alefacept efalizumab adalimumab etanercept infliximab 等藥品 於食品藥物管理署 西藥 醫 10/68
11 單位 美國皮膚科醫學會建議 [1, 2] 台灣健保署給付規定 [8] Cyclosporine+ 生物製劑 ; Cyclosporine+MTX; 或 MTX+ 生物製劑 ; 或 UVB 照光治療 +MTX etanercept ustekinumab 用於經照光治療及其他系統性治療無效 h, 或因醫療因素而無法接受其他系統性治療之全身慢性中 重度之乾癬或頑固之掌蹠性乾癬, 且影響功能之患者 乾癬雖然是一種遺傳體質, 但後天因素的影響也很重要, 乾癬患者日常生活 中做到以下六點可以避免乾癬惡化 [5]: (1). 避免感染 : 包括細菌及病毒 ( 如感冒 扁桃腺炎 愛滋病 ) (2). 避免外傷 : 不要用力搔抓皮膚或去除皮屑, 特別是頭皮屑 癢時輕拍皮膚 冰敷或服用抗組織氨, 並將指甲剪短 (3). 避免藥物濫用 : 部分口服藥可能引起乾癬惡化, 尤其是口服及注射的類固 醇, 強效外用類固醇突然停用也會惡化乾癬 (4). 避免長期暴露在低濕 低溫的工作或居住環境 (5). 保持情緒平穩, 睡眠充足避免過勞 (6). 避免服用市售抗癌的免疫增強食品, 如靈芝 巴西磨菇 藍藻 ( 螺旋藻 ) 桑 黃 二 疾病治療藥品於我國之收載現況 [8-10] 在世界衛生組織藥物統計方法整合中心 (WHO Collaborating Center for Drug Statistics Methodology) 頁面下, 查詢到本案申請藥品 secukinumab 之 ATC 碼為 L04AC10, 屬免疫抑制類 (L04A, immunosuppressants) 之介白素抑制劑 (L04AC, interleukin inhibitors) 成分 此一分類層級下, 共有 11 項不同的藥物成分, 經逐一查核, 除本案申請藥品外, 目前已經獲得我國上市許可者共有 ustekinumab tocilizumab canakinumab 等三項 其中, 僅 ustekinumab 此一成分可用於乾癬治療 在食品藥物管理署 西藥 醫療器材 含藥化妝品許可證查詢 頁面下, 鍵入關鍵字 斑塊性乾癬 未註銷, 可獲得兩筆資料, 即本案申請藥品 如果將關鍵字改為 乾癬 未註銷, 則可以獲得 167 筆資料 經過逐一查核, 其中包含 dexamethasone triamcinolone neomycin sulfadiazine prednisolone hydrocortisone acetate, crotamiton gentamicin dexamethasone, crotamiton 療器材 含藥化妝品許可證查詢 頁面查證, 未查獲 alefacept 與 efalizumab 等兩種成分資料 [9] h 治療必須包括足量之照光治療及包括以下兩種系統性治療之至少兩種, 包括 methotrexate acitretin cyclosporin 11/68
12 fluocinolone betamethasone thimerosal tolnaftate, benzocaine hydrocortisone, crotamiton beclomethasone dipropionate clobetasol propionate clobetasol propionate fluocinonide methylprednisolone flumethasone pivalate leflunomide fluticasone propionate calcitriol tazarotene cyclosporine etanercept adalimumab ustekinumab 等 28 種成分 表二所彙整者, 係與本案藥品具有相同治療地位藥品之 ATC 分類碼 [10] 藥 品許可證查詢 [9] 健保藥品給付規定 [8] 的搜尋結果 表二 與本案藥品具有相近治療地位之藥品 ATC 分類碼 成分名 L04AB01 Etanercept ( 抗腫瘤壞死因子製劑 ) 我國許可適應症 適用於對疾病緩解型抗風濕性藥物 ( 即 DMARDs, 例如 methotrexate) 無適當療效之成人活動性類風濕性關節炎 也適用於先前未使用 methotrexate 治療之成人中度至重度活動性類風濕性關節炎 這些病人的 X 光檢查顯示, 本品可以減緩疾病造成的關節結構性受損 亦適用於 methotrexate 治療無效或無法耐受的 2 歲以上兒童及青少年的活動性多關節幼年型慢性關節炎 尚未對不足 2 歲的兒童進行試驗 適用於對疾病緩解型抗風濕性藥物無療效之成人活動性與進行性乾癬性關節炎 治療活動性僵直性脊椎炎 適用於對其他全身性治療 ( 包括 cyclosporine methotrexate 或光化療法 (PUVA) ) 無效 有禁忌或無法耐受之中度至重度乾癬成 人患者 適用於對其他全身性治療或光化療法無法有效 控制或無法耐受之 6 歲以上兒童及青少年的重度乾癬 劑型注射劑 健保現行給付條件限用於經照光治療及其他系統性治療無效, 或因醫療因素而無法接受其他系統性治療之全身慢性中 重度之乾癬或頑固之掌蹠性乾癬, 且影響功能之患者 i L04AB04 Adalimumab ( 抗腫瘤壞死因子製劑 ) 1. 類風濕性關節炎 : Humira 適用於患有中度至重度類風濕性關節炎, 並且曾經對一種或超過一種的 DMARDs 藥物有不適當反應的成人病患, 可減輕症狀與徵兆 ( 包括主要臨床反應和臨床緩解 ) 抑制結構上損害的惡化 Humira 可單獨使用也可以和 MTX 或其他 DMARDs 藥物併用 2. 乾癬性關節炎 : 適用於對疾病緩解型抗風濕藥物無療效之成人活動性與進行性乾癬性關節炎 Humira 可單獨使用也可以和 MTX 或其他 DMARDs 藥物併用 3. 僵直性脊椎炎 : 適用於減輕患有活動性僵直性脊椎炎的病患之症狀與徵兆 4. 克隆氏症 : 適用於對傳統治療無效之成人中度至重度克隆氏症 (CD), 可減輕症狀與徵兆及誘導與維持臨床緩解 Humira 亦適用於對 infliximab 已經失去療效或無耐受性之成人中度至重度克隆氏症, 可減輕症狀與徵兆及誘導與維持臨床緩解 5. 乾癬 : 對其他全身性治療, 包括 cyclosporine MTX 或其他光化學療法無效 有禁忌或無法耐受之中度至重度乾癬成人患者 6. 潰瘍性結腸炎 : Humira 適用於對於皮質類固醇和 / 或 6- mercaptopurine (6-MP) 或 azathioprine (AZA) 等傳統治療無效 或對這種療法不耐受或有醫療禁忌之中度至嚴重活動性潰瘍性結腸炎成人病患 7. 小兒適應症 :(1) 幼年型自發性多關節炎 : Humira 與 Methotrexate 併用適用於 2 歲及以上患有活動性幼年型自發性多關節炎, 並且曾經對一種或超過一種 DMARDs 藥物反應不佳之患者 Humira 可單獨用於對 Methotrexate 無法耐受或不適合持續使用之患者 (2) 小兒克隆氏症 : Humira 適用於對皮質類固醇及免疫調節劑 (Immunomodulators) 反應不佳之 6 歲 注 射 劑 同上 i 完整給付規定內容請參閱附錄一 12/68
13 ATC 分類碼成分名 L04AC05 Ustekinumab ( 抗介白素 12/23 單株抗體製劑 ) L04AC10 Secukinumab ( 抗介白素 17 我國許可適應症 或大於 6 歲中度至重度克隆氏症患者, 可減輕症狀與徵兆及誘導與維持臨床緩解 1. 乾癬 (Ps) Stelara 適用於治療適合接受光療法或全身性治療的中至重度斑塊性乾癬成人患者 (18 歲 ( 含 ) 以上 ) 2. 乾癬性關節炎 (PsA) Stelara 適用於治療對疾病緩解型抗風濕性藥物 (DMARDs) 療效不佳之成人 (18 歲及以上 ) 活動性乾癬性關節炎 Stelara 可單獨使用, 亦可與 methotrexat(mtx) 併用 治療適合接受全身性治療的中至重度斑 瑰性乾癬成人患者 劑型注射劑注射劑 健保現行給付條件 同上 本案申請藥品 單株抗體製劑 ) 三 療效評估報告 ( 含文獻回顧摘要 ) 本報告主要參考 CADTH/pCODR PBAC 及 NICE 之醫療科技評估報告及建議者提供之資料 ; 視需要輔以其他醫療科技評估組織報告或 Cochrane Library/PubMed/Embase 相關文獻, 以瞭解主要醫療科技評估組織之給付建議及目前相關臨床研究結果 來源 CADTH/pCODR ( 加拿大 ) PBAC( 澳洲 ) NICE( 英國 ) 其他實證資料建議者提供之資料 報告日期於 2015 年 10 月公告 於 2015 年 3 月公告 於 2015 年 7 月公告 SMC( 蘇格蘭 ) 醫療科技評估報告 歐洲藥物管理局 (EMA)/ 美國食品藥物管理局 (US FDA) 審查資料 Cochrane Library/PubMed/Embase 的搜尋結果 於 2015 年 10 月 7 日接獲廠商完整送審資料一份 註 :SMC 為 Scottish Medicines Consortium 蘇格蘭藥物委員會的縮寫 ( 一 ) CADTH/pCODR( 加拿大 )[11, 12] 13/68
14 2015 年 10 月 8 日, 在 CADTH 網頁鍵入關鍵字 secukinumab 後, 共獲得五筆資料, 其中, 一份 [11] 案件審議進度與本案相關, 即 CADTH 於 2014 年 12 月 22 日接獲廠商送審資料,2015 年 3 月 27 日其共同藥物審查部門 (Common Drug Review) 完成評估報告並送達廠商, 委員會於同年 5 月 20 日開會評估是否給付 secukinumab, 會中決議請廠商針對降價後的預算影響重新評估 11 月 3 日再次搜尋 CADTH 網頁, 發現最新公告之評估報告一份 [12], 以下將重點摘要該份報告內容以供參考 1. 委員會建議 委員會建議給付 secukinumab, 做為適合接受全身性治療 (systemic therapy) 或照光治療 (phototherapy) 的中至重度斑塊性乾癬成人患者的治療藥物, 且符合以 下條件者 : (1). 治療 12 周後, 如果乾癬面積暨嚴重度指數 (Psoriasis Area Severity Index, PASI)PASI75 評估未達標, 則停止治療 (2). Secukinumab 的治療費用不得超過已給付用於中至重度斑塊性乾癬之生物製劑中價格最低者 2. 建議理由 ( 療效部份 ) (1). 四項隨機分派試驗 (ERASURE FEATURE JUNCTURE FIXTURE) 結果顯示, 治療 12 周後, 在 PASI75 分數此一指標上,secukinumab 300 毫克的表現優於 (superior to) 安慰劑 (2). 一項隨機分派試驗 (FIXTURE) 結果顯示, 治療 12 周後, 在 PASI75 分數此一指標上,secukinumab 300 毫克的表現優於 (superior to)etanercept 50 毫克 ( 每周兩次 ) 註 : 委員會瞭解到, 在審查完成後, 有一項新發表的隨機分派試驗 (CLEAR), 比 較 secukinumab 與 ustekinumab 用於乾癬治療的表現差異 而這些資料廠商並未 於送審資料中呈現 3. 委員會評估的資料 委員會考量的資訊包括一份系統性文獻回顧 一份針對廠商經濟評估的評值 (critique) 以及病人代表團體的意見 4. 病人代表團體意見 以下資訊源自三個病人代表團體 14/68
15 (1). 乾癬病人會經驗皮膚出血 裂開 結痂 脫屑 斑塊等情況 某些時候會經驗嚴重的搔癢或者關節痛 (2). 從社會心理層面來說, 乾癬患者可能會出現憂鬱 自殺的意念 覺得恥辱 感覺無助或沮喪 憂鬱和自尊受損對患者人際關係造成負面的影響 某些病人的乾癬症狀出現在身體敏感部位, 可能影響到他人對他們的吸引力或性慾的看法 (3). 乾癬患者表示, 疾病限制他們的活動力 工作與參與運動的能力, 並因此可能導致生產力降低 經常請假甚至失掉工作 某些病人因為睡眠狀況不佳, 可能會有注意力的問題 由於皮膚脫屑和出血需要持續清理, 對於病人來說亦是一項負擔 5. 療效資料 療效評估資料源自於四項 (ERASURE FEATURE JUNCTURE FIXTURE) 雙盲 隨機分派 安慰劑對照 多中心之臨床試驗結果 由於 CADTH 報告僅摘 要部分數據, 故而此處予以略過 詳細試驗內容請參閱本報告第 ( 四 ) 節 6. 委員會其他考量要點 委員會注意到以下兩點問題 : (1). 廠商建議對於 secukinumab 治療的評估應在第 16 周進行, 持續治療應給予對治療有反應者 但是, 委員會注意到, 樞紐試驗的試驗設計, 是在試驗第 12 周評估病人的 PASI 分數, 而且, 經濟評估是假設治療 12 周後, 無反應者將中止治療 (2). 委員會注意到目前仍缺乏的實證資料, 包括 secukinumab 的長期療效和安全性資料 secukinumab 與目前臨床斑塊性乾癬常用藥物的直接比較結果 secukinumab 用於症狀較不嚴重斑塊性乾癬病人的研究 ( 二 ) PBAC( 澳洲 )[13] 2015 年 10 月 8 日, 在澳洲衛福部網頁鍵入關鍵字 secukinumab 後, 共獲得 11 筆資料 其中, 一份 [13] 於 2015 年 3 月公告的會議報告與本案研究主題相同, 以下將重點摘要其內容以供參考 1. 廠商送審目的 廠商請求給付 secukinumab 150mg, 在病人符合給付規範條件下, 做為非生 物性疾病修飾抗風濕藥物 (non-biological disease modifying anti rheumatic drugs, DMARDs) 治療失敗之慢性重度斑塊性乾癬病人的治療用藥 15/68
16 本案為廠商首次送審, 屬平行送審之案件, 即澳洲治療用品管理局 (Therapeutic Goods Administration, TGA) 與藥品給付諮詢委員會 (PBAC) 同時審查 之案件 2. 藥物許可證內容 2015 年元月 8 日, 澳洲治療用品管理局 (Therapeutic Goods Administration, TGA) 核准 secukinumab 上市, 許可適應症為 用於適合接受全身性治療或光照 治療的中至重度斑塊性乾癬成人患者 k 3. 廠商申請給付條件 廠商申請的給付範圍與澳洲已給付用於慢性重度斑塊性乾癬的其他藥物 ( 包 括 ustekinumab adalimumab etanercept 與 infliximab) 給付範圍相近, 內容如表 三所示 廠商於送審資料中, 同時請求將目前已同意給付之一個治療周期用藥, 由三 項生物製劑擴增為四項, 但是, 並未提供支持性證據以供參考 表三 澳洲廠商申請之 secukinumab 給付條件 [13] 嚴重度疾病治療期治療標準 重度全身 ( 基礎值 PASI>15) 或臉部, 一隻手的手掌或一隻腳的足部 (PASI 分數評分屬 重度 [severe] 或 極重度 [very severe] 或身體 30% 或以上之面積受到影響 ) 斑塊性乾癬初始治療與持續治療由皮膚科醫師處方, 且做為全身性之單一療法用藥 (systemic monotherapy)( 除 methotrexate 外 ) 給付條件 (1). 至少以下列四種方式中之三種治療, 並以 PASI 分數評估, 未獲得適當的反應 無法耐受或屬使用禁忌之病人 : 接受每周三次照光治療 (UVB 或 PUVA) 至少六周 ; 接受 Methotrexate 每周劑量至少 10 毫克的治療至少六周 ; 接受 cyclosporine 每天每公斤體重至少 2 毫克的治療至少六周 ; 接受 acitretin 每天每公斤體重至少 0.4 毫克的治療至少六周 k 原文為 For treatment of moderate to severe plaque psoriasis in adults who are candidates for systemic therapy or phototherapy. 16/68
17 (2). 核准之初始治療時間為 16 周 病人在接受至少 12 周治療後, 需評估治療成效 (3). 病人需要展現適當的治療成效, 或者, 接受持續治療時, 繼續維持適當的治療成效, 亦即, 針對症狀已影響至全身的病人, 治療後的 PASI 值較其基礎值有 75% 的下降 (PASI 75); 針對症狀僅影響臉部 手掌或足部的病人, 治療後之 PASI 三項嚴重度評估 (sub-scores) 皆屬 輕度 (slight) 或 無症狀 (none) 等級, 或者,PASI 值較其基礎值有 75% 的下降 (PASI 75) (4). 核准之持續治療時間為 26 周 ( 等同六個月 ) 目前澳洲健保已給付之生物製劑, 包含同屬抗腫瘤壞死因子製劑類 (anti-tnf) 的 adalimumab etanercept infliximab, 以及抗介白素 Interleukin-12/23 單株抗體的 ustekinumab PBAC 委員會之次委員會 (Economics Sub-Committee, ESC) 注意到, 如果維持一個治療周期可以使用的藥品為三項, 則代表 secukinumab 與這些藥物為取代關係, 但是, 如果擴增為四項時, 給付 secukinumab 的費用將會增加整體給付支出 基於 secukinumab 屬抗介白素 Interleukin-17 單株抗體藥物, 所以, 即使一個治療周期准許使用的藥品數仍維持為三項, 病人可以在使用包含 secukinumab 情況下, 用到每一類生物製劑的一種藥物, 廠商於 PBAC 會議前, 同意撤回擴增一個治療周期用藥由三項生物製劑擴增為四項的提議 4. Secukinumab 的臨床治療地位 Secukinumab 用於慢性重度斑塊性乾癬的臨床治療地位, 被視為生物性疾病 修飾抗風濕類藥物 (biological disease modifying anti rheumatic drugs, bdmards, 包含 ustekinumab adalimumab etanercept 與 infliximab) 之外的替代選項 5. 比較品 廠商於送審資料中, 基於健保 (Medicare Australia) 已給付藥品之使用量多 寡, 選擇以 ustekinumab( 使用量最高,44%) 做為主要比較藥品, 其他藥品如 adalimumab(37%) etanercept(10%) 與 infliximab(9%) 做為次要比較藥品 另一個觀點則是, 由於所有已給付藥品中, 包含三項同藥物作用機轉之抗腫 瘤壞死因子藥品, 基於臨床醫師可能會在一個治療周期中給予病人三種作用機轉 不同的藥物治療, 因此,secukinumab 將會取代 etanercept 或 infliximab 6. 臨床資料的考量 廠商要求列席會議 17/68
18 臨床醫師則在會議中提出選擇 ustekinumab 與 adalimumab 做為比較品是否合適的問題 臨床醫師認為, 目前尚未建立使用各項生物性疾病修飾抗風濕類藥物 (bdmards) 治療慢性重度斑塊性乾癬的前後順序 (hierarchy), 各種藥物的使用皆根據每位病人的病情與藥物特性決定 臨床醫師認為廠商於送審資料中提出 ustekinumab 及 adalimumab 做為參考品是合適的, 並且說明 etanercept 的療效較其他現存之生物性疾病修飾抗風濕類藥物為差 (inferior to) 臨床醫師同時亦表態支持廠商送審資料中的宣稱 PBAC 委員會認為此項會議提供許多資訊 沒有任何消費者代表針對本案提出意見 7. 臨床試驗 首先, 廠商於送審資料中提出一項間接比較分析結果, 包括 secukinumab ustekinumab adalimumab 與 infliximab 等藥品, 但主要分析方向為 seckinumab 與 ustekinumab 的比較, 簡要內容如表四所示 其次, 廠商亦提出一項預計 2015 年 7 月份完成之直接比較臨床試驗資料 (CLEAR,NCT , 比較 secukinumab 300 毫克與 ustekinumab 45/90 毫克 ) l 表四 澳洲廠商進行之間接比較內容 [13] 藥品方法試驗內容分析 病人數 Secukinumab 統合四項臨床 三項試驗比較 secukinumab 與安慰 1377 人 m 試驗結果 劑, 一項試驗比較 secukinumab 與 etanercept 及安慰劑 Ustekinumab 統合六項臨床 六項試驗使用 45 毫克劑量, 四項試 2596 人 試驗結果 驗使用 90 毫克劑量 五項試驗比較 ustekinumab 與安慰 劑, 一項試驗比較 ustekinumab 與 etanercept Adalimumab 統合四項臨床 四項試驗皆比較 adalimumab 與安慰 1560 人 試驗結果 劑 Infliximab 統合六項臨床六項試驗皆比較 infliximab 與安慰 1255 人 l 經本中心於 ClinicalTrials.gov 網頁查證,NCT 試驗 (Efficacy of Secukinumab compared to Ustekinumab in patients with plaque-type psoriasis) 於 2014 年 2 月份開始進行, 計畫於 2016 年 7 月份完成最終的資料搜集 預計納入之 676 位受試者中, 亞洲部份包含來自於台灣及韓國的受試者 [14] 該試驗重點內容請參閱第 ( 四 ) 節電子資料庫搜尋結果 m 這四項臨床試驗為 ERASURE FEATURE JUNCTURE FIXTURE 試驗 由於 PBAC 報告僅摘要部分數據, 故而此處予以略過, 詳細試驗內容請參閱本報告第 ( 四 ) 節 18/68
19 藥品方法試驗內容分析 試驗結果劑 病人數 整體而言, 分析結果如下 : 相對療效 (1). 直接比較分析 納入分析之四項生物性疾病修飾抗風濕類藥物 (bdmards) 與安慰劑的比較 結果, 皆顯示有較高比例使用這些生物製劑的受試者, 達到 PASI75 的評估標準 ( 具統計顯著意義 ) 與每周使用 etanercept 100 毫克比較, 有較高比例接受 secukinumab 與 ustekinumab 治療的受試者, 達到 PASI75 的評估標準 ( 具統計顯著意義 ) (2). 間接比較分析 間接比較分析結果請參閱下頁表五 針對 secukinumab 與 ustekinumab 的比較, 整體而言, 間接比較並未獲得方向一致的結果, 端視所使用之共同比較品為 etanercept 或安慰劑而定 基於 etanercept 在 secukinumab 與 ustekinumab 個別臨床試驗中的表現不同, 委員會認為, 以安慰劑做為共同比較品的間接比較分析結果較為可信 以安慰劑做為共同比較品時, 於試驗第 12 周,secukinumab 組與 ustekinumab 組受試者達到 PASI75 評估標準的比例沒有統計顯著差異 ; 當與 adalimumab 比較時 (12-16 周 ), secukinumab 組受試者 (12 周 ) 有較高比例達到 PASI75 評估標準 ( 具統計顯著意義 ) 值得注意之處是, 試驗中 ustekinumab 組受試者的 PASI75 評估是在第 12 周進行, 而澳洲給付單位規定第 28 周評估 ustekinumab 的治療成效, 因此, 廠商提供的間接比較結果可能有低估 ustekinumab 療效之虞 表五 澳洲廠商進行的間接比較分析結果 [13] 比較 共同比較品 Etanercept 安慰劑 SEC 全部 SEC 100kg SEC>100kg SEC 全部 SEC 100kg SEC>100kg UST45 - 全部病人 (12 周 ) V N/A N/A V N/A N/A UST90 - V N/A N/A NS N/A N/A 19/68
20 比較 共同比較品 Etanercept 安慰劑 SEC 全部 SEC 100kg SEC>100kg SEC 全部 SEC 100kg SEC>100kg 全部病人 (12 周 ) UST45 & 90 - 全部病人 (12 周 ) UST45-100kg(12 周 ) UST90 - >100kg(12 周 ) ADA (12-16 周 ) IFX (10 周 ) V N/A N/A NS N/A N/A N/A V N/A N/A NS N/A N/A N/A NS N/A N/A NS N/A N/A N/A V N/A N/A N/A N/A N/A NS N/A N/A V: 有較高比例受試者達到 PASI75 評估標準 ( 具統計顯著意義 ), 比較結果以 secukinumab 300 毫克 (12 周 ) 的表現較佳 ; NS: 不具統計顯著差異 ;N/A: 無法進行比較 相對安全性 廠商於送審資料中, 並未完整比較 secukinumab 與其他用於治療乾癬之生物 性疾病修飾抗風濕類藥物 (bdmards), 在藥物安全性方面的表現 廠商僅以間 接比較方式呈現受試者至少經歷一次不良事件的結果 總結來說, 以安慰劑做為共同比較品, 比較 secukinumab 與 ustekinumab adalimumab infliximab 等藥品, 各組受試者至少經歷一次不良事件的表現, 沒 有獲得具統計顯著差異的結果 ( 觀察 12~30 周 ) 相對療效 / 安全性評估總結 基於廠商送審資料中提出的間接比較分析, 獲得以下結果 : (1). 針對每 100 位體重小於等於 100 公斤接受 secukinumab 或 ustekinumab(45 毫 克 ) 治療的病人 經過 12 周治療後,secukinumab 組約有額外 10 個病人可以達到 PASI75 評估標準 雖然, 這項以風險差 (risk difference) 計算出來的結果具統計顯著意義, 但是, 如果以相對風險 (relative risk) 進行計算, 則無法獲得統計顯著意義的結果 所以, 解讀這項分析時應謹慎 20/68
21 (2). 針對每 100 位接受 secukinumab 或 adalimumab 治療的病人 經過 12 周治療 後,secukinumab 組約有 15 個病人可以達到 PASI75 評估標準 這項結果可以經由兩組之風險差或勝算比 (odds ratio) 的間接比較計算出 來, 但是以相對風險進行計算時, 則無法獲得相同的結果 (3). 針對每 100 位體重大於 100 公斤接受 secukinumab 或 ustekinumab(90 毫克 ) 治療的病人 經過 12 周治療後, 兩組病人達到 PASI75 評估標準的表現沒有差異, 方向一致的結果也出現在 secukinumab 與 infliximab 的比較上 (4). 上述 secukinumab 表現較 ustekinumab(45 毫克 ) 或 adalimumab 為佳的結果 (12~16 周 ), 並沒有實證資料支持這些效益能夠延續至長期 (5). Secukinumab 與 ustekinumab(45 毫克或 90 毫克 ) adalimumab infliximab 等藥品在藥物安全性方面的比較, 各組病人至少經歷一次不良事件的表現沒有差異 (12~30 周 ) 8. 廠商宣稱 廠商於送審資料中宣稱 : 相對療效 優於 etanercept 100 毫克 / 周 ; 優於 ustekinumab 45/90 毫克 ; 優於 adalimumab 40 毫克 ; 短期不劣於 infliximab(10 周 ), 長期則較 infliximab 為佳 相對安全性 與 etanercept 100 毫克 / 周相當 ; 與 ustekinumab 45/90 毫克相 當 ; 與 adalimumab 40 毫克相當 ; 優於 infliximab 9. 委員會建議 基於與 adalimumab 比較符合最小成本的基礎 (cost-minimisation basis), 委員會同意在設定給付規範的條件下給付 secukinumab, 做為非生物性疾病修飾抗風濕類藥物 (DMARDs) 治療失敗的慢性重度斑塊性乾癬病人的治療用藥 等療效劑量為 secukinumab 300 毫克治療四周, 相當於每兩周 adalimumab 40 毫克的治療 詳細給付規定內容請參閱附錄二 ( 三 ) NICE( 英國 )[15] 2015 年 10 月 8 日在 NICE 網頁鍵入關鍵字 secukinumab 後, 共獲得八筆資 料 其中, 一份 [15] 公告於 2015 年 7 月份的醫療科技評估報告與本案研究主題 相同, 以下將重點摘要其內容以供參考 21/68
22 1. 委員會建議 委員會建議給付 secukinumab 做為符合下列條件之斑塊性乾癬成年病人的治 療用藥 : A. 疾病嚴重度屬於重度, 定義為 PASI(Psoriasis Area Severity Index) 分數在 10 分或以上, 而且,DLQI(Dermatology Life Quality Index) 分數也大於 10 分 B. 經過標準全身性治療失敗後的病人, 例如,cyclosporine methotrexate 光化學療法 (psoralen and long-wave ultraviolet radiation, PUVA), 或者, 屬於這些治療禁忌症的病人, 或者, 病人無法耐受這些治療 C. 廠商同意提供價格折讓 ( 進行風險分攤方案 ) 如果病人接受 secukinumab 治療 12 周後, 乾癬症狀未有適當反應者應停藥 治療獲得適當反應的定義為 : A. 與起始治療時的表現相比,PASI 分數有 75% 的降低 (PASI 75); 或 B. 與起始治療時的表現相比,PASI 分數有 50% 的降低 (PASI50), 而且 DLQI 分數降低五分 2. 委員會評估資料 委員會主要評估資料包括廠商送審資料, 以及實證資料審閱小組 (Evidence Review Group, ERG) 對於廠商送審資料的評值報告 (1). 廠商送審資料 經過系統性文獻搜尋步驟, 廠商共納入五項 secukinumab 之雙盲隨機分派試驗, 其中, 三項試驗 (ERASURE JUNCTURE FEATURE) 與安慰劑比較, 一項試驗 (FIXTURE) 與 etanercept 及安慰劑比較, 一項試驗 (SCULPTURE) 比較 secukinumab 不同劑量的治療方案 文獻搜尋結果顯示, 並未有任何直接比較試驗可供參考, 因此, 廠商進行一項網絡統合分析 (network meta-analysis), 間接比較 secukinumab 和其他五項比較品 ( 最佳支持療法 etanercept ustekinumab adalimumab infliximab) 除此之外, 文獻搜尋過程亦未發現任何非隨機分派試驗或觀察性研究可供參考 雖然, 廠商於送審資料中同時呈現 secukinumab 150 毫克與 300 毫克的臨床 試驗結果, 但是, 基於英國僅有 secukinumab 300 毫克獲得上市許可, 所以,NICE 報告中僅呈現 300 毫克的分析結果 A. 四項與安慰劑直接比較的臨床試驗結果 22/68
23 n 這四項試驗皆以試驗第 12 周之 PASI75 分數與 IGA 分數 o (0 或 1) 做為共同 主要療效指標, 分析納入試驗之意圖治療 (intention-to-treat) 族群表現 整體而言, 這四項試驗結果皆顯示 secukinumab 在主要療效指標的表現較佳 ( 具統計顯著意 義 ) 次族群分析 ( 包含性別 年齡 體重 地域位置 診斷時的年齡 已患病時 間長短 生活品質 先前接受過的治療 [ 生物性或非生物性製劑 ]) 結果與主要分析 結果方向一致, 具體數據廠商以機密為由未公開 生活品質分析 (EQ-5D) 結果顯示,secukinumab 組受試者表現較安慰劑組為佳 ( 具統計顯著意義 ) B. 間接比較結果 廠商以隨機效應模型進行網絡統合分析, 比較 secukinumab 與其他四項生物製劑 (adalimumab etanercept infliximab ustekinumab) 在 PASI 分數的表現差異 這項分析共納入 30 項臨床試驗數據, 其中, 包括 ustekinumab 的五項試驗 分析結果如表六所示 整體而言,secukinumab 300 毫克較安慰劑 secukinumab 150 毫克 etanercept adalimumab 等藥品在 PASI 50 PASI 75 PASI 90 等指標表現為佳 ( 具統計顯著意義 ) 然而, 與 ustekinumab 及 infliximab 等藥品相比時, 其表現則未獲得具統計顯著差異的結果 表六 Secukinumab 300 毫克與其他比較品的網絡統合分析結果 ( 治療效果之相 對風險 [ 信賴區間 ])[15] 比較品 PASI 50 PASI 75 PASI 90 安慰劑 7.99(7.05~9.11) 22.25(18.7~26.62) 92.53(71.67~119.3) Secukinumab 150mg 1.08(1.05~1.12) 1.17(1.10~1.26) 1.36(1.22~1.54) Etanercept 1.52(1.35~1.75) 2.15(1.76~2.71) 3.71(2.69~5.33) Ustekinumab 45mg 1.07(1.02~1.12) 1.15(1.05~1.28) 1.30(1.09~1.61) Ustekinumab 90mg 1.03(0.99~1.08) 1.07(0.98~1.19) 1.15(0.96~1.40) Adalimumab 1.21(1.12~1.34) 1.46(1.26~1.76) 2.0(1.54~2.76) Infliximab 1.0(0.96~1.05) 1.01(0.92~1.13) 1.02(0.84~1.28) (2). 實證資料審閱小組的評值意見 ( 部份摘要 ) A. 針對廠商進行的系統性文獻回顧, 實證資料審閱小組認為執行方法完整 品 n 乾癬面積暨嚴重度指數 (Psoriasis Area Severity Index, PASI) PASI75 代表 PASI 評估分數與基礎值相比降低 75% o IGA(investigator s global assessment) 分數 0 或 1 分代表乾癬症狀清除或幾乎清除 23/68
24 質良好, 納入之各項臨床試驗品質亦良好 據此, 實證資料審閱小組認為, 試驗 12 周時,secukinumab 300 毫克組受試者的 PASI 評估優於安慰劑組的結果, 具有較強的實證等級支持 B. 針對廠商進行的網絡統合分析, 實證資料審閱小組認為其方法學與執行步驟適當, 唯獨僅分析一項療效指標與缺乏生活品質的分析略有不足 C. 針對廠商在藥物不良事件的分析, 基於生物製劑抑制人體免疫系統可能會增加罹癌比例, 實證資料審閱小組提出此一問題討論 實證資料審閱小組同時亦說明, 目前並沒有實證資料顯示, 乾癬病人使用生物製劑增加其罹患淋巴癌的比例, 但是照光療法會增加黑色素瘤與非黑色素瘤皮膚癌的風險, 而 cyclosporine 治療時間延長亦與淋巴癌相關 3. 委員會考量要點 ( 療效部份摘要 ) (1). 委員會認為廠商於送審資料中提出的臨床試驗品質良好, 比較品包含安慰劑與活性對照藥 (active comparator), 對於決策評估是適當的 (2). 委員會針對各項臨床試驗受試者的納入標準 廠商提出給付申請的 secukinumab 適用範圍提出討論 問題點在於, 臨床試驗納入部份未曾接受過任何全身性療法 ( 或生物製劑 ) 的病人, 而廠商申請給付用於全身性療法治療無效 無法耐受或屬使用禁忌病人, 兩者涵蓋範圍不盡相同 雖然, 臨床專家說明, 尚無實證資料證明先前治療方案會影響目前治療方案的療效, 但是, 委員會仍舊認為, 廠商應針對申請給付範圍之族群進行個別分析為佳 委員會總結這項討論, 認為臨床試驗結果大致可以外推至重度乾癬病人群, 對於評估 secukinumab 療效亦屬適當 (3). 委員會討論臨床試驗之主要療效指標 (PASI 分數降低 ) 與臨床實務的相關性 委員對於測量 PASI 分數是否客觀有所討論 臨床專家說明, 當醫師有過使用經驗, 可以在短時間完成評估並且在不同醫師間不會有明顯的評估差異 另外, 委員會同意 PASI75 結果可以高度反應乾癬的治療成效, 但是, 基於乾癬症狀對於生活品質造成顯著影響, 所以, 病人自覺是否完成治療 (PASI100) 也相當重要 委員會總結這項討論, 認為除了以 PASI75 做為療效評估標準之外, 亦需納入 PASI100 結果做為治療成效之依據 (4). 委員會討論臨床試驗結果, 並總結認為在主要及次要療效指標的評估, secukinumab 的表現優於 (superior to) 安慰劑和 etancercept (5). 委員會對於廠商進行的統合分析進行討論 委員會注意到幾項侷限之處, 包括並未說明納入病人群異質性的問題, 以及間接比較與直接比較結果差異等問題 最終, 委員會總結這項討論, 認為雖然統合分析有侷限之處, 但其提供的資訊仍足以供決策討論之用 (6). 委員會討論是否有任何次族群更適用 secukinumab 治療 委員會由臨床專家處瞭解到, 合併有乾癬性關節炎的病人是重要的次族群, 特別是那些手部關節受到疾病影響而自行注射藥劑有困難的病人, 因為 24/68
25 secukinumab 的使用次數不如其他生物製劑頻繁, 使得病人接受治療更為便利 委員會也注意到, 廠商已經申請 secukinumab 用於乾癬性關節炎的新適應症, 最佳的情況即是, 給予 secukinumab 一個處方可以同時治療乾癬及乾癬性關節炎兩種病況 最終委員會總結此項討論, 認為目前沒有足夠的實證資料得以瞭解, 病人先前接受不同的治療是否會有更適合接受 secukinumab 方案的次族群 (7). 針對 secukinumab 不良事件的討論, 委員會總結 secukinumab 在藥物安全性的表現, 並未有與其他生物製劑表現不同之處 ( 四 ) 其他實證資料 1. 其他醫療科技評估組織 (1) SMC( 蘇格蘭 )[16] 在蘇格蘭藥物委員會 (Scottish Medicines Consortium) 網頁, 鍵入關鍵字 secukinumab 後, 獲得一筆 [16] 資料, 即 2015 年 5 月公告之本案給付審查會議 報告, 以下將摘要會議結論以供參考 A. SMC 建議 基於 secukinumab 在改善中至重度斑塊性乾癬病人症狀的表現優於安慰劑以及腫瘤壞死因子藥物, 且廠商同意持續執行風險分擔方案 ( 降價以改善 secukinumab 的成本效益分析結果 ) 的情況下, 蘇格蘭藥物委員會同意有條件給付 secukinumab, 條件如下 : 用於經過標準之全身性治療 ( 包含 cyclosporine methotrexate 與照光治療 ) 失 敗 無法耐受, 或者對於這些治療有使用禁忌的中至重度斑塊性乾癬病人 B. 藥物許可證內容 Secukinumab 在英國蘇格蘭地區的適應症為 用於治療適合接受全身性治療 的中至重度斑塊性乾癬成年患者 p 2. 歐洲藥物管理局 (EMA) [17] / 美國食品藥物管理局 [18](US FDA) 審查資料 在歐洲藥物管理局 (European Medicines Agency, EMA) 網頁, 經鍵入關鍵字 secukinumab 後, 共獲得一份 [17] 公告於 2014 年 11 月份之審查報告與本案主題 相關, 即 secukinumab 獲得歐盟國家上市許可, 適應症為 適合接受全身性治療 p 適應症原文為 Treatment of moderate to severe plaque psoriasis in adults who are candidates for systemic therapy. 25/68
26 的中至重度斑塊性乾癬成人患者 q 的治療用藥, 核准的用法用量, 起始劑量為第 周皮下注射 secukinumab 300 毫克, 並自第 4 周開始, 每四周注射 300 毫克一次, 治療至多至 16 周, 如果藉時病人對治療仍未有反應, 應停止治療 美國食品藥物管理局 (US FDA) 於 2015 年 1 月核准 secukinumab 上市, 核准的藥品適應症 藥物用量與歐洲藥物管理局所核准者略有差異 美國核准的適應症內容為 適合接受全身性治療或照光治療的中至重度斑塊性乾癬成人患者 r, 核准的用法與歐洲相同, 惟在維持劑量部份, 歐洲藥物管理局建議, 無論病人體重為何, 每次治療皆給予 300 毫克, 而美國食品藥物管理局則說明建議劑量為每次 300 毫克, 針對某些病人,150 毫克是可以接受的劑量 我國所核准之適應症與歐洲藥物管理局相同, 藥品用量部份則與美國食品藥 物管理局相同 以下將重點摘要歐洲藥物管理局審查報告內容以供參考 廠商於送審資料中共提出四項第二期臨床試驗及六項第三期臨床試驗以供 歐洲藥物管理局審查, 其中, 與本案較相關者為四項隨機分派 雙盲 平行分組 多中心之第三期臨床試驗 (A2302 A2303 A2308 A2309) 總結 secukinumab 的療效與藥物安全性分析結果如下 : 首先, 在療效評估部份,A2302 A2303 A2308 與 A2309 的個別試驗結果 如表七所示 試驗第 12 周與 52 周的統合分析結果則如表八所示 s 總結來說 : 試驗 12 周的統合分析結果顯示, 針對共同主要療效指標的評估,secukinumab 150 毫克與 300 克的表現皆優於安慰劑 ( 具統計顯著意義 ), 而這個結果也與個別試驗的結果方向一致 ;A2303 試驗另外分析與 etancercpt 比較的結果, 亦顯示 secukinumab 150 毫克與 300 克的表現皆優於 etanercept( 具統計顯著意義 ) 試驗 52 周的統合分析結果顯示,secukinumab 組的療效皆得以良好延續至 52 周, 尤其以 300 毫克組表現更佳 共同療效指標的表現於試驗第 16 周達到平原期, 隨後緩慢下降 受試者的復發率也以 secukinumab 300 毫克組最低 (7.4%; 150 毫克 17.1%;etancercept 21.1%, 安慰劑 28.6%) 其次, 安全性評估的部份, 廠商提出三套分析結果以供歐洲藥物管理局審 查 這三套分析納入的受試者族群與觀察時間長短皆不相同, 如表九所示, 分析 q 原文為 Cosentyx is indicated for the treatment of moderate to severe plaque psoriasis in adults who are candidates for systemic therapy. [17] r 原文為 Cosentyx is a human interleukin-il-17a antagonist indicated for the treatment of moderate to severe plaque psoriasis in adult patients who are candidates for systemic therapy or phototherapy. [18] s 統合分析納入所有接受隨機分派受試者 (3366 人 ) 的數據 (full analysis set, FAS, 全分析集 ) 第 12 周的分析包含 A2302 A2303 A2308 A2309 等四項試驗 第 52 周的試驗則包含 A2302 A2303 A2304 等三項試驗 26/68
27 結果則如表十所示 總結來說,Secukinumab 的整體安全性表現良好,300 毫克的安全性表現並未統計顯著與 150 毫克之表現有所差異 用於乾癬治療的生物製劑的典型不良事件, 例如感染 嗜中性白血球低下 (neutropenia) 過敏反應 (hypersensitivity) 等同樣被觀察到, 但是, 沒有觀察到分枝桿菌感染 (mycobacterial infection) 或嚴重伺機性感染 (opportunistic infection) 增加的情形 與其他用於乾癬治療的全身性療法相比, 並沒有需要額外注意之處 27/68
28 表七 Secukinumab 四項樞紐試驗資料彙整表 t [17] 試驗號碼 / 名稱 試驗時間 / 人數 試驗藥物 u 主要療效指標 受試者納入 / 排除標準 ( 摘要 ) 試驗結果 ( 未呈現安全性部份結果 ) A2302 ERASURE 導入期 12 周維持期 40 周追蹤期 8 周 738 人 受試者被隨機分派至 S 300mg 組 S150mg 組或安慰劑組 至試驗第 12 周時, 安慰劑組受試者依照其 PASI 分數高低, 轉至 S300mg S150mg 組, 或維持在安慰劑組 試驗第 12 周 時, 共同療效指 標 PASI 75 與 IGA mod 2011(0 或 1) 評估,S 藥 表現優於安慰 劑 納入標準 : (1). 年齡 18 歲以上之成人 ; (2). 進入試驗前至少 6 個月, 診斷為慢性斑塊性乾癬 ; (3). 基於 PASI 與 IGA 分數評估, 屬中至重度乾癬病人 ; (4). 適合接受全身性治療者 v 排除標準 : (1). 其他類型之乾癬患者 ; (2). 藥物誘發之乾癬患者 ; 共有 738 人被隨機分派至三組,95% 受試者完成導入期的試驗, 因為不良事件退出比例為 1.6% 之後, 將近 90% 受試者完成了維持期的試驗, 最常見退出試驗的原因為不良事件 (3.4%) 與缺乏療效 (2.3%) 受試者平均年齡 45 歲,92% 小於 65 歲,70% 為男性,20% 為亞裔族群, 平均 PASI 分數為 22 分, 45% 之 PASI 大於 20 分,77% 受試者沒有乾癬性關節炎,63% 接受過全身性治療 ( 失敗率 67%),30% 接受過生物製劑治療 (47% 為 IL-12/23,67% 為 anti-tnf-α) 共同療效指標結果如下表所示 S 藥的表現優於安慰劑, 針對體重 先前用藥的次族群分析, 結果與主要分析方向一致 (1). PASI75% T vs. C T(%) C(%) OR P 值 S150 vs. P (28.4,116.9) < S300 vs. P (38.7,176.7) < (2). IGA0/1 T vs. C T(%) C(%) OR P 值 S150 vs. P (18.2,107.2) < S300 vs. P (28.8,172.7) < t S: secukinumab;e: etanercept;u:ustekinumab;t: treatment;c: control;or: odds ratio u PASI(Psoriasis Area and Severity Index): 乾癬病灶範圍及嚴重度改善狀況,PASI75 意指與基礎值相比有 75% 的改善 IGA(Investigators Global Assessment 2011): 評估斑塊性乾癬疾病嚴重度的指標, 分為 v 五級, 第 0 級代表病人沒有乾癬症狀, 第 1 級代表症狀幾乎清除 適合接受全身性治療者的定義為, 先前 局部治療 和 / 或 照光治療 和 / 或 先前接受之全身性治療 無效者 28/68
29 試驗號碼 試驗時間 / 試驗藥物 u 主要療效指標 受試者納入 / 排除標準 試驗結果 ( 未呈現安全性部份結果 ) / 人數 ( 摘要 ) 名稱 A2303 試驗時間同 受試者被隨機 與 A2302 試驗 與 A2302 試驗相同, 除了再 1306 人被隨機分派至四組,95% 受試者完成導入期的試驗, 因為不良 FIXTURE 上 分派至 E50mg 相同 額外排除先前使用過 事件退出比例為 1.1% 之後, 將近 90% 受試者完成了維持期的試驗, 1306 人 組 S 300mg 組 S150mg 組 ( 本試驗之次要 療效指標為 S 藥 etanercept 者 因為不良事件退出的比例為 1.6% 缺乏療效而退出的比例為 2.1% 受試者平均年齡 44 歲,92% 小於 65 歲,70% 為男性,22% 為亞裔族 或安慰劑組 至 與 E 藥之比較 群, 平均 PASI 分數為 24 分,64% 接受過全身性治療 ( 失敗率 82%) 試驗第 12 周 首先, 在試驗第 共同療效指標結果如下表所示 S 藥的表現優於安慰劑, 針對體重的 時, 安慰劑組受 12 周時, 先觀察 次族群分析,S 藥的表現優於安慰劑及 E 藥 針對 223 位先前使用過 試者依照其 S 藥是否不劣於 生物製劑的次族群分析顯示, 未接受過生物製劑與生物製劑治療未失 PASI 分數高 E 藥, 之後, 再 敗者之反應較佳 低, 轉至 觀察 S 藥是否優 (1). PASI75 S300mg S150mg 組, 或維持在安慰劑組 於 E 藥 其次, 在試驗第 52 周 時, 觀察 S 藥表 現優於 E 藥的結 果是否持續維 持 w ) T vs. C T(%) C(%) OR P 值 S150 vs. P (23.6,77.6) < S300 vs. P (36.1,20.6) < S150 vs. E (1.9, 3.8) < S300 vs. E (3.3, 6.7) < (2). IGA0/1 T vs. C T(%) C(%) OR P 值 S150 vs. P (19.8,83.4) < S300 vs. P (35.9,174.1) < S150 vs. E (2.1, 4.2) < S300 vs. E (3.5, 6.9) < w 試驗結果顯示,S 藥 ( 兩種劑量 ) 的表現在第 12 周與 52 周皆優於 E 藥 ( 具統計顯著差異 ) 第 12 周時,S300mg 表現較 S150mg 為佳, 但是在第 52 周時, 兩者表現相近 29/68
30 試驗號碼 試驗時間 / 試驗藥物 u 主要療效指標 受試者納入 / 排除標準 試驗結果 ( 未呈現安全性部份結果 ) / 人數 ( 摘要 ) 名稱 A2308 試驗時間同 受試者被隨機 與 A2302 試驗 與試驗 A2302 相同 177 人被隨機分派至三組,96% 受試者完成導入期的試驗, 兩 FEATURE 上 分派至 S 300mg 相同 位受試者因為不良事件退出試驗 三位受試者失去聯絡 受試 177 人 組 S150mg 組或安慰劑組 ( 受 者年齡中位數為 46 歲,66% 為男性,92% 為白人受試者, 平均 PASI 分數為 20.8 分, 初始診斷至今平均 19.5 年,67% 接受 試者自行注射 過全身性治療,44% 接受過生物製劑治療 (53% 治療失敗 ) 藥劑 ) 至試驗第 12 周時, 評估其 PASI 表現 共同療效指標結果如下表所示 S 藥的表現優於安慰劑, 針對體重的次族群分析,S 藥的表現優於安慰劑 針對先前使用過的藥物進行次族群分析, 是否接受過全身性治療不影響此次試 驗結果, 未接受過生物製劑治療者之反應較佳 (1). PASI75 T vs. C T(%) C(%) OR P 值 S150 vs P (53.9,81.4) < S300 vs P (61.5,86.1) < (2). IGA0/1 T vs. C T(%) C(%) OR P 值 S150 vs P (35.1,67.2) < S300 vs P (53.5,80.5) < /68
31 試驗號碼 試驗時間 / 試驗藥物 u 主要療效指標 受試者納入 / 排除標準 試驗結果 ( 未呈現安全性部份結果 ) / 人數 ( 摘要 ) 名稱 A2309 試驗時間同 與試驗 A2308 與 A2302 試驗 與試驗 A2302 相同 182 人被隨機分派至三組,97% 受試者完成導入期的試驗, 兩 JUNCTURE 上 相同, 差異之處 相同 位受試者因為不良事件退出試驗 一位受試者缺乏療效退出 182 人 僅在於所使用之注射醫材不 受試者年齡中位數為 46 歲,66% 為男性,92% 為白人受試者, 平均 PASI 分數為 20.8 分, 初始診斷至今平均 19.5 年,67% 接 同 ( 注射筆 ) 受過全身性治療,44% 接受過生物製劑治療 (53% 治療失敗 ) 共同療效指標結果如下表所示 S 藥的表現優於安慰劑, 針對 體重的次族群分析,S 藥的表現優於安慰劑 針對先前使用過 的藥物進行次族群分析, 是否接受過全身性治療不影響此次試 驗結果, 未接受過生物製劑治療者之反應較佳 (1). PASI75 T vs. C T(%) C(%) OR P 值 S150 vs. P (53.1,79.8) < S300 vs. P (70.7,91.7) < (2). IGA0/1 T vs. C T(%) C(%) OR P 值 S150 vs. P (36.6,66.7) < S300 vs. P (58.8,83.9) < /68
32 x 表八 Secukinumab 相關試驗於試驗第 12 周與 52 周的統合分析結果 S150mg S300mg 安慰劑 etanercept 試驗第 12 周的分析結果 PASI 75 達到有反應標準的比例統合結果 69.2 * 79.4 *# IGA 0/1 達到有反應標準的比例統合結果 51.4 * 65.0 *# 試驗第 52 周的分析結果 PASI 75 達到有反應標準的比例統合結果 IGA 0/1 達到有反應標準的比例統合結果 * : 表示與安慰劑及 etanercept 的比較具統計顯著差異 ( 至少 p<0.05) # : 表示 secukinumab 300 毫克與 150 毫克的表現具統計顯著差異 x 本表分別呈現 secukinumab 相關試驗於試驗第 12 周及 52 周數據統合的結果, 惟試驗第 52 周的分析結果未包含各組表現差異評估之統計數值可以參考 32/68
33 表九 Secukinumab 樞紐試驗安全性分析 - 背景資料表 [17] 統合組人數觀察時間納入試驗分析資料 A 2399 人 最長至 12 周 四項樞紐試驗 A2302 A2303 A2308 A2309 B 3993 人 最長至 52 周 四項第二期臨床試驗與六項第 三期臨床試驗 A2211 A2211e1 A2212 A2220 A2302 A2303 A2307 A2308 A2309 C 5044 人 無資料 包含 39 項第一 二 三期臨床 試驗中之 34 項 ( 排除第一期試 驗中之健康受試者數據 ) S150mg n=692,157 病人年 S300mg n=690,155 病人年 E50mg n=323,73 病人年 76% 之總病人年暴露於 S 藥,3430 人暴露於 S 藥 (1641 人至少一年,2751 人至少六個月 ) 12 周 S150mg n=1174,268 病人年 S300mg n=1173,268 病人年安慰劑 n=694,155 病人年 E50mg n=323,73 病人年 52 周 S150mg n=1395,1142 病人年 S300mg n=1410,1178 病人年安慰劑 n=793,201 病人年 E50mg n=323,294 病人年 S 藥 n=4498, 大於 3588 病人年安慰劑 n=1158, 大於 339 病人年 33/68
34 表十 Secukinumab 樞紐試驗安全性分析結果彙整表 [17] 分析組別 A 組 試驗前 12 周資料 B 組 試驗 52 周所有資料 試驗藥物 S150mg S300mg 安慰劑 E50mg S150mg S300mg 安慰劑 E50mg 分析人數 N=692 N=690 N=694 N=323 N=1395 N=1410 N=793 N=323 n(%) n(%) n(%) n(%) n(ir y ) n(ir) n(ir) n(ir) 所有不良事件 412(59.5) 388(56.2) 340(49.0) 186(57.6) 1066(239.9) 1091(236.1) 413(351.8) 253(243.4) 所有嚴重不良事件 14(2.0) 14(2.0) 12(1.7) 3(0.9) 76(6.8) 85(7.4) 15(7.5) 20(7.0) 個別不良事件 ( 摘要 ) 感染 203(29.3) 195(28.3) 134(19.3) 83(25.7) 653(85.3) 704(91.1) 173(101.9) 172(93.7) 主要心血管不良事件 0(0.0) 2(0.3) 0(0.0) 0(0.0) 5(0.44) 6(0.51) 1(0.50) 1(0.34) 心腦血管相關事件 7(1.0) 3(0.4) 11(1.6) 6(1.9) 30(2.7) 82(3.0) 13(6.5) 14(4.9) 惡性或未特定部位腫瘤 3(0.4) 1(0.1) 3(0.4) 0(0.0) 11(1.0) 9(0.8) 3(1.5) 2(0.7) z 過敏反應 31(4.5) 31(4.5) 9(1.3) 15(4.6) 115(10.1) 132(11.9) 9(4.5) 27(9.7) y z IR: exposure-adjusted incidence rate per 100 patient-years. 此處之分析數據係依據 narrow SMQ(standardized MedDRA query) 而來 SMQ 為一種協助識別與攫取試驗之安全性數據的工具 [19] 34/68
35 3. 電子資料庫相關文獻 (1) 搜尋方法 本報告用於搜尋 The Cochrane Library/PubMed/Embase 電子資料庫之方法說 明如下 : 以下列 PICOS 做為搜尋條件, 即搜尋符合本次建議新藥給付條件下之病人 群 (population) 治療方法 (intervention) 療效對照品 (comparator) 療效測 量指標 (outcome) 及研究設計與方法 (study design), 其搜尋條件整理如下 : Population 納入條件 : 斑塊性乾癬成年病人 排除條件 : 斑塊性乾癬孩童病人 Intervention Comparator Outcome Study design secukinumab 未設限未設限系統性文獻回顧或統合分析類 依照上述之 PICOS, 透過 The Cochrane Library/PubMed/Embase 等文獻資料 庫, 於 2015 年 10 月 29 日, 以 (secukinumab) 做為主要關鍵字進行搜尋, 搜尋 策略請見附錄表一 (2) 搜尋結果 A. The Cochrane Library[20, 21] 在 Cochrane Library 網頁, 經鍵入關鍵字 secukinumab 後, 共獲得 111 筆資料, 其中, 包括五篇科技評估報告 (Technology Assessments) 以及 106 篇臨床試驗文獻 針對初步納入之五篇科技評估報告, 經過逐筆標題與摘要閱讀, 共有兩筆資料之研究主題與本案相符 aa 惟其中一筆資料為英國國家健康暨照護卓越研究院 (NICE) 委託英國國家衛生研究院 (National Institute for Health Research, NIHR) 進行的研究 [20], 相關資料已於第三章節呈現, 此處予以略過 ; 另外一筆資料則為英國國家科技偵測中心 (National Horizon Scanning Centre, NHSC) 的新興科技前瞻性偵測評估報告 [21], 不屬於相對療效評估報告, 故而此處亦予以略過 總結在 Cochrane Library 的文獻搜尋結果, 並沒有納入任何文獻進一步彙整 aa 所排除之三篇文獻為 secukinumab 用於類風濕性關節炎 僵直性脊椎炎 乾癬性關節炎治療的研究 35/68
36 B. PubMed[22, 23] 在 PubMed 網頁, 經鍵入關鍵字 secukinumab, 共獲得 122 筆資料 如果增加關鍵字 plaque psoriasis 後, 共獲得 26 筆資料, 其中, 屬系統性文獻回顧或統合分析類文獻者有兩篇 [22, 23] 經過逐筆資料摘要與標題閱讀, 僅納入一篇統合分析研究 [22], 所排除者係無法找到全文之文獻 總結在 PubMed 的文獻搜尋結果, 共納入一篇文獻進一步彙整 C. Embase[22, 23] 在 Embase 網頁, 經鍵入關鍵字 secukinumab, 共獲得 636 筆資料 如果增加關鍵字 plaque psoriasis 並設定研究對象為人類 以英文發表之系統性文獻回顧或統合分析類研究, 共獲得五筆資料 經過逐筆標題與摘要閱讀後, 共有兩篇 [22, 23] 文獻與本案研究主題相符 bb, 惟這兩篇研究與 PubMed 搜尋結果重覆, 故而此處予以略過 總結在 Embase 的文獻搜尋結果, 並沒有納入任何文獻進一步彙整 (3) 電子資料庫搜尋總結 在 Cochrane Library PubMed Embase 等電子資料庫, 經鍵入主要關鍵字 secukinumab, 可以獲得 869 筆資料, 如果同時合併關鍵字 plaque psoriasis 並設定以英文發表之系統性文獻回顧或統合分析類研究, 則得到七筆資料, 其中, 包含系統性文獻回顧與統合分析類研究兩篇以及科技評估報告五篇 經過逐筆標題和摘要閱讀, 共納入一篇發表於 2015 年的統合分析研究 另一方面, 在文獻搜尋過程中, 我們亦瞭解到 secukinumab 目前有一項正在進行的臨床試驗, 直接比較其與 ustekinumab 的療效表現差異 該項試驗 (NCT ,Efficacy of Secukinumab compared to Ustekinumab in patients with plaque-type psoriasis) 於 2014 年 2 月份開始進行, 計畫於 2016 年 7 月份完成最終的資料收集 ; 預計納入之 676 位受試者中, 亞洲部份包含來自於台灣及韓國的受試者 今年六月已於 Journal of American Academy of Dermatology 期刊發表試驗前 16 周的結果 [24] 基於此項試驗為 secukinumab 與 ustekinumab 之直接比較結果, 具重要參考價值, 故而, 此處亦納入彙整 以下將重點摘要納入之一篇統合分析與一篇臨床試驗內容 A. 統合分析 bb 所排除之三篇文獻為一篇成本效益分析研究 一篇針對作用在第 17 型介白素 A(IL-17A) 的單株抗體生物製劑介紹文獻, 以及一篇針對 brodalumab 用於乾癬治療的研究 36/68
37 Xiong 等人的研究 [22] Secukinumab 用於中至重度斑塊性乾癬治療的療效及安全性表現 - 一項針對隨機分派試驗的統合分析, 於 2015 年 3 月在 International Journal of Clinical and Experimental Medicine 期刊發表, 為第一項針對 secukinumab 相關試驗進行的統合分析研究 本研究主要由中國國家自然科學基金會支持完成, 所有作者亦宣告沒有任何利益衝突關係 作者主要在 Cochrane Library MEDLINE EMBASE Wangfang Database 等電子資料庫, 以 psoriasis 及 secukinumab 做為主要關鍵字搜尋所有相關 文獻, 未針對研究類型 語言或發表年代進一步設限 最終, 自 208 篇相關文獻中, 篩選出八篇發表於 1989~2014 年的隨機分派 雙盲 安慰劑對照研究進一步分析, 包含 3213 位受試者 總結來說, 在試驗第 12 周, 針對主要療效指標 ( 包括 PASI75/90 以及 IGA0/1) 的評估,secukinumab 150 毫克與 300 毫克的表現皆優於安慰劑, 其中,300 毫克組的表現較 150 毫克組為佳 藥物安全性部份, 與安慰劑相比,secukinumab 組並未有顯著不良事件發生率 B. 臨床試驗 Thaci 等人的研究 [24] Secukinumab 用於中重度斑塊型乾癬皮膚症狀的治療優於 ustekinumab:clear 隨機分派試驗, 於 2015 年 6 月在 Journal of American Academy of Dermatology 期刊發表, 是一項為期 52 周的雙盲 隨機分派 活性對照 平行分組試驗 (NCT ) 的早期 (16 周 ) 結果報告 cc 本研究由廠商支持完成 本試驗共納入 676 位年齡 18 歲以上, 曾接受過局部治療 照光治療 全身性治療無效之中重度斑塊性乾癬病人, 依據體重多寡 ( 100kg 或 >100kg) 以 1:1 比例隨機分派至 secukinumab 300 毫克組或 ustekinumab 45 毫克 /90 毫克組 主要療效指標為試驗第 16 周時,secukinumab 組的 PASI90 分數表現較 ustekinumab 組為佳 次要療效指標為試驗第 4 周時,secukinumab 組在 PASI75 的表現優於 ustekinumab, 以及在試驗第 52 周時,secukinumab 組在 PASI90 的表現優於 ustekinumab 除此之外, 本試驗亦針對 IGA0/1 分數與生活品質進行評估 試驗結果顯示, 兩組受試者的基礎值相近, 惟 ustekinumab 組病人有較高比例同時患有乾癬性關節炎 (20.5% vs. 15.9%) 受試者平均年齡約 45 歲 七成為男性 近九成為白人 PASI 分數為 22 分 平均體表受影響面積約 33% 近七成接受過全身性治療 15% 接受過生物製劑治療 ( 其中 10% 治療失敗 ) cc 經本中心於 ClinicalTrials.gov 網頁查證,NCT 試驗 (Efficacy of Secukinumab compared to Ustekinumab in patients with plaque-type psoriasis) 於 2014 年 2 月份開始進行, 計畫於 2016 年 7 月份完成最終的資料搜集 預計納入之 676 位受試者中, 亞洲部份包含來自於台灣及韓國的受試者 [14] 37/68
38 在療效評估部份, 試驗第 16 周時,secukinumab 組在主要療效指標的表現優於 ustekinumab 組 (79.0% vs. 57.6%;p<0.0001), 進一步達到 PASI100 標準的受試者, 也以 secukinumab 組顯著較多 (44.3% vs. 28.4%;p<0.0001) 次要療效指標部份, 試驗第 4 周達到 PASI75 指標的比例亦以 secukinumab 組表現較佳 (50.0% vs. 20.6%;p<0.0001) 生活品質評估結果亦顯示, 自評量起點至試驗第 16 周為止, secukinumab 組受試者的生活品質較佳 (71.9% vs. 57.4%;p<0.0001) 在藥物安全性評估部份, 兩組受試者接受試驗藥物的時間長短相近 受試者至少經歷一次不良事件的比例, 分別為 secukinumab 組 64.2% 與 ustekinumab 組 58.3% 其中, 最常見者為感染, 兩組的表現分別為 secukinumab 組 29.3% 與 ustekinumab 組 25.3% 嚴重不良事件的發生率低, 兩組皆為 3% 左右 試驗 16 周內, 沒有受試者死亡案例通報 總結上述兩項研究, 本案之電子資料庫文獻搜尋, 我們可以獲得以下結果 : 根據 2015 年 3 月發表的一項統合分析研究, 針對所有在 1989~2014 年發表的 secukinumab 隨機分派研究, 篩選出八篇試驗進行分析 ( 包含 3213 位受試者 ), 總結來說, 在試驗第 12 周, 針對主要療效指標 ( 包括 PASI75/90 以及 IGA0/1) 的評估,secukinumab 150 毫克與 300 毫克的表現皆優於安慰劑, 其中,300 毫克組的表現較 150 毫克組為佳 藥物安全性部份, 與安慰劑相比,secukinumab 組並未有顯著不良事件發生率 根據 2015 年 6 月發表的一項直接比較試驗早期結果, 試驗第 16 周時 (676 人 ),secukinumab 組在主要療效指標 PASI90 的表現優於 ustekinumab 組 (79.0% vs. 57.6%;p<0.0001), 進一步達到 PASI100 標準的受試者, 也以 secukinumab 組顯著較多 (44.3% vs. 28.4%;p<0.0001) 在藥物安全性評估部份, 兩組表現相近 ( 五 ) 建議者提供之資料 根據廠商所提供的送審資料, 在療效部份, 共引用九篇文獻用以證明 secukinumab 用於斑塊性乾癬病人的治療成效 其中, 包含兩項第二期臨床試驗與七項第三期臨床試驗結果 dd 惟廠商並未對其文獻搜尋過程與篩選步驟給予說明, 我們無法確定這些資料是否足以完整代表 secukinumab 的療效表現 dd 包含 ERASURE FIXTURE ERASURE( 日本病人結果 ) JUNCTURE FEATURE STATURE CLEAR SCULPTURE 等試驗 38/68
39 四 療效評估結論 1. 療效參考品 針對本案申請藥品 Cosentyx(secukinumab) 之目標病人群 適合接受全身性治療的中至重度斑塊性乾癬成人患者, 綜合考量臨床指引建議與健保署給付規定, 同屬相同臨床治療地位之療效參考品包括 etanercept addalimumab 與 ustekinumab 等三種藥物成份 其中, 與 secukinumab 有直接比較試驗結果者, 包含 etanercept 與 ustekinumab 等兩種成份 雖然,ustekinumab 與 secukinumab 具有相同之 ATC 前五碼, 然基於 secukinumab 與 etanercept 之直接比較試驗有 52 周較長期的結果, 與 ustekinumab 的直接比較目前僅有 16 周的結果可供參考, 所以, 查驗中心針對本案建議的療效參考品包含 etanercept 與 ustekinumab 兩項 ( 無先後優先順序 ) 2. 相對療效與相對安全性 根據歐洲藥物管理局 2014 年 11 月公告的審查報告, 廠商於送審資料中共提出四項第二期臨床試驗及六項第三期臨床試驗用以證明 secukinumab 的療效 其中, 與本案較相關者為四項隨機分派 雙盲 平行分組 多中心之第三期臨床試驗 (A2302 [ERASURE] A2303 [FIXTURE] A2308 [FEATURE] A2309 [JUNCTURE]) 總結 secukinumab 的療效與藥物安全性分析結果如下 : 首先, 在療效評估部份,A2302 A2303 A2308 與 A2309 的個別試驗結果 如表七所示 試驗第 12 周與 52 周的統合分析結果則如表八所示 ee 總結來說 : 試驗 12 周的統合分析結果顯示, 針對共同主要療效指標的評估,secukinumab 150 毫克與 300 克的表現皆優於安慰劑 ( 具統計顯著意義 ), 而這個結果也與個別試驗的結果方向一致 ;A2303 試驗則顯示與 etancercpt 比較的結果,secukinumab 150 毫克與 300 克的表現皆優於 etanercept( 具統計顯著意義 ) 試驗 52 周的統合分析結果顯示,secukinumab 組的療效皆得以良好延續至 52 周, 尤其以 300 毫克組表現更佳 共同療效指標的表現於試驗第 16 周達到平原期, 隨後緩慢下降 受試者的復發率也以 secukinumab 300 毫克組最低 (7.4%; 150 毫克 17.1%;etancercept 21.1%, 安慰劑 28.6%) 其次, 安全性評估的部份, 廠商提出三套分析結果以供歐洲藥物管理局審 查 這三套分析納入的受試者族群與觀察時間長短皆不相同, 如表九所示, 分析 ee 統合分析納入所有接受隨機分派受試者 (3366 人 ) 的數據 (full analysis set, FAS, 全分析集 ) 第 12 周的分析包含 A2302 A2303 A2308 A2309 等四項試驗 第 52 周的試驗則包含 A2302 A2303 A2304 等三項試驗 39/68
40 結果則如表十所示 總結來說,Secukinumab 的整體安全性表現良好,300 毫克的安全性表現並未統計顯著與 150 毫克之表現有所差異 用於乾癬治療的生物製劑的典型不良事件, 例如感染 嗜中性白血球低下 (neutropenia) 過敏反應 (hypersensitivity) 等同樣被觀察到, 但是, 沒有觀察到分枝桿菌感染 (mycobacterial infection) 或嚴重伺機性感染 (opportunistic infection) 增加的情形 與其他用於乾癬治療的全身性療法相比, 並沒有需要額外注意之處 3. 主要醫療科技評估組織之給付建議 (1). 加拿大 CADTH 2015 年 10 月 8 日在 CADTH 網頁鍵入關鍵字 secukinumab 後, 共獲得五筆資料, 其中, 一份 [11] 案件審議進度與本案相關, 即 CADTH 於 2014 年 12 月 22 日接獲廠商送審資料,2015 年 3 月 27 日其共同藥物審查部門 (Common Drug Review) 完成評估報告並送達廠商, 委員會於同年 5 月 20 日開會評估是否給付 secukinumab, 會中決議請廠商針對降價後的預算重新評估 11 月 3 日再次搜尋 CADTH 網頁, 發現最新公告之評估報告一份 [12] 委員會基於四項隨機分派試驗 (ERASURE FEATURE JUNCTURE FIXTURE) 結果顯示, 治療 12 周後, 在 PASI75 分數此一指標上,secukinumab 300 毫克的表現優於 (superior to) 安慰劑及 etanercept 50 毫克 ( 每周兩次, 僅 FIXTURE 試驗比較 secukinumab 與 etanercept), 建議給付 secukinumab 做為適合接受全身性治療 (systemic therapy) 或照光治療 (phototherapy) 的中至重度斑塊性乾癬成人患者的治療藥物, 且符合以下條件者 : A. 治療 12 周後, 如果乾癬面積暨嚴重度指數 (Psoriasis Area Severity Index, PASI)75 評估未達標, 則停止治療 B. Secukinumab 的治療費用不得超過已給付用於中至重度斑塊性乾癬之生物製劑中價格最低者 註 : 委員會瞭解到, 在審查完成後有一項新發表的隨機分派試驗 (CLEAR), 比較 secukinumab 與 ustekinumab 用於乾癬治療的表現差異 而這些資料廠商並未於 送審資料中呈現 (2). 澳洲 PBAC 2015 年 10 月 8 日在澳洲衛福部網頁鍵入關鍵字 secukinumab 後, 共獲得 11 筆資料 其中, 一份 [13] 於 2015 年 3 月公告的會議報告與本案研究主題相同 根據該份報告內容, 委員會基於與 adalimumab 比較符合最小成本的基礎 (cost-minimization basis), 同意在設定給付規範的條件下給付 secukinumab, 做為 40/68
41 非生物性疾病修飾抗風濕類藥物 (DMARDs) 治療失敗的慢性重度斑塊性乾癬病 人的治療用藥 等療效劑量為 secukinumab 300 毫克治療四周, 相當於每兩周 adalimumab 40 毫克的治療 詳細給付規定內容請參閱附錄二 (3). 英國 NICE 2015 年 10 月 8 日在 NICE 網頁鍵入關鍵字 secukinumab 後, 共獲得八筆資料 其中, 一份 [15] 公告於 2015 年 7 月份的醫療科技評估報告與本案研究主題相同 委員會建議給付 secukinumab 做為符合下列條件之斑塊性乾癬成年病人的治療用藥 : A. 疾病嚴重度屬於重度, 定義為 PASI(Psoriasis Area Severity Index) 分數在 10 分或以上, 而且,DLQI(Dermatology Life Quality Index) 分數也大於 10 分 B. 經過標準全身性治療失敗後的病人, 例如,cyclosporine methotrexate 光化學療法 (psoralen and long-wave ultraviolet radiation, PUVA), 或者, 屬於這些治療禁忌症的病人, 或者, 病人無法耐受這些治療 C. 廠商同意提供價格折讓 ( 進行風險分攤方案 ) 如果病人接受 secukinumab 治療 12 周後, 乾癬症狀未有適當反應者應停藥 治療獲得適當反應的定義為 : A. 與起始治療時的表現相比,PASI 分數有 75% 的降低 (PASI 75); 或 B. 與起始治療時的表現相比,PASI 分數有 50% 的降低 (PASI50), 而且 DLQI 分數降低五分 4. 醫療倫理 無相關系統性收集之資訊可供參考 5. 電子資料庫文獻搜尋結果 在 Cochrane Library PubMed Embase 等電子資料庫, 經鍵入主要關鍵字 secukinumab, 可以獲得 869 筆資料, 如果同時合併關鍵字 plaque psoriasis 並設定以英文發表之系統性文獻回顧或統合分析類研究, 則得到七筆資料, 其中, 包含系統性文獻回顧與統合分析類研究兩篇以及科技評估報告五篇 經過逐筆標題和摘要閱讀, 共納入一篇發表於 2015 年的統合分析研究 除此之外, 在閱讀相關文獻過程中, 我們亦瞭解到 secukinumab 目前有一項正在進行的臨床試驗, 直接比較其與 ustekinumab 的療效表現差異 該項試驗 (NCT ,Efficacy of Secukinumab compared to Ustekinumab in patients with plaque-type psoriasis) 於 2014 年 2 月份開始進行, 計畫於 2016 年 7 月份完成最終 41/68
42 的資料搜集 ; 預計納入之 676 位受試者中, 亞洲部份包含來自於台灣及韓國的受試者 而今年六月已於 Journal of American Academy of Dermatology 期刊發表試驗前 16 周的結果 [24] 基於此項試驗為 secukinumab 與 ustekinumab 之直接比較結果, 具重要參考價值, 故而, 此處亦納入彙整 總結上述兩項研究, 本案之電子資料庫文獻搜尋, 我們可以獲得以下結果 : 根據一項統合分析研究結果, 針對所有在 1989~2014 年發表的 secukinumab 隨機分派研究, 篩選出八篇試驗進行分析 ( 包含 3213 位受試者 ), 總結來說, 在試驗第 12 周, 針對主要療效指標 ( 包括 PASI75/90 以及 IGA0/1) 的評估, secukinumab 150 毫克與 300 毫克的表現皆優於安慰劑, 其中,300 毫克組的表現較 150 毫克組為佳 藥物安全性部份, 與安慰劑相比,secukinumab 組並未有顯著不良事件發生率 根據一項目前仍在進行之直接比較試驗 (CLEAR) 的早期結果, 試驗第 16 周時 (676 人 ),secukinumab 組在主要療效指標 PASI90 的表現優於 ustekinumab 組 (79.0% vs. 57.6%;p<0.0001), 進一步達到 PASI100 標準的受試者, 也以 secukinumab 組顯著較多 (44.3% vs. 28.4%;p<0.0001) 在藥物安全性評估部份, 兩組表現相近 42/68
43 五 成本效益評估 ( 一 ) 建議者提出之國內藥物經濟學研究 建議者提供之本土經濟評估報告係採用健保署觀點, 執行 secukinumab 用於治療中度至重度乾癬 (moderate to severe psoriasis) 病人之成本效用分析 (cost-utility analysis), 以經健康生活品質校正人年 (quality-adjusted life-years, 簡稱 QALYs) 為健康效果指標 此模型採用之介入策略為皮下注射 secukinumab (150 mg, 300 mg) 第 0 到 4 週為每週一次, 之後每 4 週一次 比較策略為 : (1) Adalimumab: 第一週皮下注射 80 mg, 此後兩週一次皮下注射 40 mg (2) Ustekinumab 45 mg ( 病患體重小於等於 100 公斤 ): 第 0 4 週皮下注射 45 mg, 此後每 12 週一次皮下注射 45 mg (3) Ustekinumab 90 mg ( 病患體重大於 100 公斤 ): 第 0 4 週皮下注射 90 mg, 此後每 12 週一次皮下注射 90 mg (4) Etanercept: 前 12 週為 2 週皮下注射一次 50 mg, 此後為每週皮下注射一次 50 mg 在以上策略中, 若病人第 或 52 週 PASI<50, 則停止該生物製劑療程, 轉為他種生物製劑療程 此分析採用決策樹 ( 模擬 52 週治療情形, 最長為 2 年 ) 及馬可夫模型模擬病程 用藥期間之隨治療效果更改療法以決策樹模擬之, 評估療效時間為第 及 52 週, 其後馬可夫模型則以年為循環單位 分析病人進入模型後一年 兩年及十年的健康結果與醫療成本,QALYs 與成本皆以 3% 為年折現率進行折現 模型考慮的健康狀態分為 : 使用生物製劑療法 使用生物製劑療法效果不佳或退出改用標準療法及死亡 以下陳述各重要參數及結果 : 療效參數 模型應用的比較療效證據, 主要依據建議者委外由相關臨床試驗所做的交錯療效比較法 (Mixed treatment comparison) 研究得來 ; 而病人第一年退出治療率主要由 ERASURE study 得來, 第二年之後由其他文獻假設之 此研究中之病人效用值 (utility) 隨 PASI 改變, 由 FIXTURE study 之 EQ-5D 結果假設之 醫療成本 藥費方面,secukinumab 150mg 依建議者自訂價格 (300mg 為 150mg 的雙倍價格 ), 其餘藥品費用皆照 2015 年健保給付價格, 療程藥費計算主要依照前面療程敘述, 但在 secukinumab 的療程藥費計算中, 起始劑量 (loading dose) 只計算第 1 至 4 週每週一次, 共 4 劑劑量 其餘醫療費用來自全民健保資料庫分析結果, 包括診 43/68
44 察費用 使用 methotrexate 或 cyclosporin 之監測費用 ( 肝穿刺檢查 相關實驗室檢測費用 ) UVB 光療費用 使用生物製劑療程前檢測費用 使用生物製劑療程期間檢測費用 相關住院或嚴重副作用之醫療費用 成本效用分析結果 建議者的分析結果顯示, 乾癬中度至重度病人在基礎方案中, 其他組別相比之下的遞增 QALYs 及遞增成本效益比值 (incremental cost-effectiveness ratio, ICER) 如下 : 分析時間為一年時,secukinumab 300mg 分別與 ustekinumab 45 mg etanercept 及 adalimumab 相比之下的 ICER 值 ( 新臺幣 /QALY) 為 : 8,052,740 元 6,554,137 元及 5,136,024 元 ; 增加的 QALYs 分別為 及 0.04 QALY 分析時間為兩年時,secukinumab 300mg 分別與 ustekinumab 45 mg etanercept 及 adalimumab 相比之下的 ICER 值 ( 新臺幣 /QALY) 為 : 6,378,570 元 5,255,886 元及 4,438,153 元 ; 增加的 QALYs 分別為 及 QALY 分析時間為十年時,secukinumab 300mg 分別與 ustekinumab 45 mg etanercept 及 adalimumab 相比之下的 ICER 值 ( 新臺幣 /QALY) 為 : 4,981,114 元 4,280,180 元及 3,913,706 元 ; 增加的 QALYs 分別為 及 QALY 1. 查驗中心評論 對於建議者所提出的經濟評估報告, 查驗中心認為該報告的研究主題與研究設計與建議者建議給付規定大抵相近, 惟存有部分疑義與限制, 若要援引前述報告結果宜先釐清相關細節 查驗中心依 國內實施藥物經濟學研究之品質評估報告 彙整該報告的疑義與限制如下 : (1) 參數蒐集品質與反應國情適切程度 : 在藥費方面,secukinumab 在此藥物經濟學報告中放入的藥品單價為建議者申請健保給付價約 0.9 倍, 無法在此藥物經濟學研究中完全反映其所申請之健保價可能帶來的影響 效用 ( 健康生活品質校正權重 ) 取自國外臨床試驗, 需要進一步說明是否能反應我國臨床治療現況 (2) 整體執行品質 : 無專章說明模型驗證及相關假設之合理性 (3) 敏感度分析 : 敏感度分析並無呈現機率型敏感度分析之結果以及單維敏感度分析所使用之上下界 又療效參數由間接比較而來, 故此處必須有完整敏感度分析結果進一步說明間接比較所帶來的不確定性 在單維敏感度分析方面, 報告內文中敘述會呈現分析時間為十年的結果, 但 44/68
45 結果處並無呈現 (4) 數據引用 計算之正確性與結果之完整性需進一步說明與確認 : 沒有提供產出療效參數之交錯療效比較研究全文 嚴重不良反應此節裡, 所提到嚴重不良反應相關醫療花費的引用文章中, 病人族群為類風濕性關節炎之病人與本研究之病人族群不符 無提供模型及計算結果過程, 無法驗證 並在總療程藥費中,secukinumab 藥費計算有誤, 第一年應施打 17 次, 第二年維持劑量應施打 13 次, 共少算了 2 次 在結果部分, 只使用 secukinumab 300 mg 的組別分析其成本效用 (5) 報告撰寫邏輯與陳述可再清楚陳述 : 報告中只提及病人轉換治療方式是由健保給付規範而來, 但無清楚說明如何選擇之後的治療組別 在 secukinumab 療法撰寫上分散, 無法完整說明模型圖中之療法 結果的圖表呈現編排分散且不清楚, 較難理解 報告中某些圖表編排上有誤, 易造成混淆 ( 二 ) 其他經濟評估報告 本報告主要參考 CADTH/pCODR PBAC 及 NICE 之醫療科技評估報告及建議者提供之資料 ; 視需要輔以其他醫療科技評估組織報告或 CRD/INAHTA/Cochrane/PubMed 相關文獻, 以瞭解主要醫療科技評估組織之給付建議及目前成本效益研究結果 來源 CADTH/pCODR ( 加拿大 ) PBAC( 澳洲 ) NICE( 英國 ) 其他醫療科技評估組織電子資料庫 報告日期至 201 年 10 月 30 日止查無資料 於 2015 年 3 月公告 於 2015 年 7 月公告 SMC( 蘇格蘭 ) 醫療科技評估報告於 2015 年 5 月公告 CRD/INAHTA/Cochrane/PubMed 的搜尋結果 建議者提供之資料 註 :CRD 為 Centre for Reviews and Dissemination, University of York, England. 的縮寫 INAHTA 為 International Network of Agencies for Health Technology Assessment 的縮寫 1. CADTH/pCODR( 加拿大 )[11] 加拿大藥物專家委員會 (Canadian Drug Expert Committee, 以下簡稱 CDEC) 在 2015 年 8 月公布 secukinumab 評議結果, 建議收載此品項用在適用全身性治療 45/68
46 (systemic therapy) 或光療法之中度至重度斑塊型乾癬 (plaque psoriasis) 病人且符 合以下條件者 : (1) 治療 12 週後, 如果乾癬面積暨嚴重度指數 (Psoriasis Area Severity Index, PASI)75 評估未達標, 則停止治療 (2) Secukinumab 的治療費用不得超過已給付用於中至重度斑塊性乾癬之生物製劑中價格最低者 其中, 經濟部分評論敘述如下 : 建議者送交一份成本效用評估分析 (cost-utility analysis), 比較 secukinumab 300 mg 與 secukinumab 150 mg etanercept 50 mg ustekinumab(45 mg, 90 mg) adalimumab 40 mg infliximab(5 mg/kg) 及標準療法 ( 此處定義為口服全身性治療 光療法或外用療法 ) 用於中至重度斑塊型乾癬病人之成本效用 此研究採保險支付者觀點, 分析時間為十年, 以馬可夫模型 (Markov model) 來模擬病程, 療效參數採自建議者贊助所執行的交錯療效比較研究得來 而共同藥物審查 (Common Drug Review, 以下簡稱 CDR) 注意到此研究有以下 幾點限制 : (1) secukinumab 300 mg 療效數據由維持劑量為一年 13 劑得來, 但在藥費部分只計入 12 劑 (2) 因為由交錯療效比較法得到療效參數, 故在 secukinumab 與其他生物製劑之相對療效具不確定性 (3) 在基礎方案中, 缺乏 infliximab 生物相似性藥品的價格資料 (4) 效用值方面採取間接定位 (indirect mapping), 會帶來不確定性 (5) 缺乏針對之前已治療過的病人之分組分析 (subgroup analysis) 在經 CDR 重新分析建議者所提供的藥物經濟學模型後,CDR 建議 secukinumab 與標準療法 (standard of care) 相比之下的遞增成本效用比值 (incremental cost-utility ratio, 以下簡稱 ICUR 值 ) 約在 82,534 加幣至 122,365 加幣間 此外, 依據現今已收載的其他競爭藥品之藥價, 使用 secukinumab 300 mg 第一年總藥費高於 adalimumab 及 ustekinumab, 並且低於 etanercept infliximab and SEB-infliximab 在第二年以後的年總藥價中, 使用 secukinumab 300 mg 較以上生物製劑療法的藥費低 (19,249 加幣至 32,096 加幣 ) 2. PBAC( 澳洲 )[13] 澳洲藥物福利諮詢委員會 (Pharmaceutical Benefits Advisory Committee, 以 下簡稱 PBAC) 針對 secukinumab 於 2015 年七月發布一則公開摘要,PBAC 在 46/68
47 最小成本的考量下建議將本品納入收載, 作為重度慢性斑塊型乾癬病人經非生物性疾病修飾性抗風濕藥 (non-biological disease modifying anti-rheumatic drugs, non-biological DMARDs) 治療復發後用藥 ( 詳細病人使用條件限制請見表三 ) 其經濟部分考量如下 : 在建議者送交 secukinumab 與 adalimumab 比較之最低成本分析 (cost minimization analysis) 中, 療效證據以間接比較 (indirect comparison) 得來, 其中 secukinumab 在十二週後病人達到 PASI 75 的比例較優效於 (superior) adalimumab, 但無長期藥品 - 藥品直接比較 (head to head comparison) 資料支持 因建議者在此份報告中, 藥品維持使用劑量假設為一年須施打 12 次, 但 PBAC 認為在臨床試驗中維持劑量的給藥頻率皆為每四週一次, 故再更改為一年施打 13 次再分析評估之 另外, 建議者在預估 secukinumab 納入收載後之藥品用量及財務影響上, 假設 secukinumab 的使用者來自於會使用目前已收載的生物製劑類 DMARDs (bdmards), 如 ustekinumab adalimumab etanercept 和 infliximab 而建議者預估納入收載後第五年, 使用病人數會少於 10,000 人 在預估 secukinumab 納入收載後的財務節省方面, 建議者估計 secukinumab 會減少 ustekinumab 的使用人年數, 而使用 ustekinumab 的病患每人每年平均藥費較高, 故可節省財務支出 然而 PBAC 認為, 建議者所提出之使用 secukinumab 的病患每人每年該藥物費用極可能被低估, 因為建議者假設維持劑量每病人一年只施打 12 次, 而非 13 次 此外, 在財務節省方面,PBAC 認為建議者的算法只反映出 secukinumab 與 ustekinumab 在最低成本分析及財務分析中假設之相對使用劑量的差異 ( 分別為 2.4:1 及 2.9:1), 如建議者主張在最小成本的考量下建議將 secukinumab 納入收載, 則委員會覺得這樣的財務節省是不被認為可實現的 並且 PBAC 提出, 即便假設收載 secukinumab 並不會造成市場的成長且只取代現存的三種 bdmards, 建議者預估的對於政府的財務影響還是可能被低估 PBAC 提出, 建議者申請 secukinumab 的藥價比 adalimumab 要高上許多, 但依據送件資料 PBAC 並沒有看到令他們滿意的顯著療效改善或毒性減少, 又建議者預估的財務影響不太合理 但 PBAC 同意如果基於最小成本的考量下收載 secukinumab, 理論上對健保藥品輔助系統 (Pharmaceutical Benefits Scheme, PBS) 所牽涉到的財務衝擊極小 最後,PBAC 建議收載 secukinumab 的給付條件與現存的 bdmards 相同, 且用於嚴重慢性斑塊型乾癬 3. NICE( 英國 )[15] 47/68
48 依據英國國家健康及照護卓越研究院 (National Institute for Health and Care Excellence, 以下簡稱 NICE) 在 2015 年 7 月發布的 NICE 單一科技評值指引 (technology appraisal guidance 350) 在一項用藥可近性計畫 (patient access scheme) 提供藥價折讓的前提下, 建議收載 secukinumab 用於嚴重斑塊型乾癬病人 (total PASI>10 且 DLQI>10) 且曾接接受過標準全身性治療失敗者 ( 詳細規定請見療效部分 ) 在經濟評估方面, 建議者提交成本效用評估分析, 比較 secukinumab 與 etanercept ustekinumab(45 mg, 90 mg) adalimumab infliximab 及最佳支持性療法 (best supportive care) 六種治療選項之成本效用 此分係採英國國民健康服務中心 (National Health Service, 簡稱 NHS) 觀點, 分析時間設為 10 年, 其中第一年使用決策樹 (decision tree) 模擬病人接受治療的狀況, 後九年假設病人進入馬可夫模型 (Markov model) 以模擬病程 在療效參數部分由建議者執行網絡統合分析 (network meta-analysis ) 而得之 委員會認為建議者的模型因沒有考慮治療失敗後轉換別種生物製劑療法且分析時間太短, 並無法反映英國真實臨床執業狀況, 會增加此分析的不確定性 另外因為使用間接比較得到療效參數, 委員會提出這也會對此成本效用評估分析所產出的結果增加不確定性 在 NICE 的實證評估小組 (Evidence Review Group, ERG) 修正建議者的參數後 ( 如 : 增加因使用生物製劑而導致的嚴重副作用費用 secukinumab 的維持劑量改為一年施打 13 次 ), 委員會同意 secukinumab 與其他療法相比之遞增成本效果比值 (incremental cost-effectiveness ratio, 以下簡稱 ICER) 約為 17,700 英鎊 ( 與 ustekinumab 90 mg 相比 ) 至 42,400 英鎊 ( 與 etanercept 相比 ) 之間, 但同時委員會也認為因分析時間太短和沒有納入標準支持性治療所帶來的負效用 (disutility) 會使此 ICER 值可能有高估之虞 最後,NICE 考慮建議者提供藥價折讓 臨床數據及專家意見後, 認為 secukinumab 的 ICER 值會與其他已收載的生物製劑藥品大約類似, 決議收載 secukinumab 用於嚴重斑塊型乾癬病人 (total PASI>10 且 DLQI>10) 且曾接接受過標準全身性治療失敗者 4. 其他醫療科技評估組織 (1) SMC( 蘇格蘭 )[16] 蘇格蘭藥物委員會 (Scottish Medicines Consortium, 以下簡稱 SMC) 於 2015 年 5 月發布的第 1054/15 號建議, 基於現存資料中 secukinumab 組療效較優性於 安慰劑組及腫瘤壞死因子拮抗劑 (tumor necrosis factor antagonist) 組 ( 於療效部 48/68
49 分說明 ), 且建議者提出病人用藥可近性計畫 (patient access scheme, 以下簡稱 PAS) 後會增加成本效益, 故建議收載 secukinumab 治療中度至重度斑塊型乾癬且曾經標準全身性治療 ( 包含 ciclosporin methotrexate 及 phototherapy) 失敗或對於標準全身性治療有使用禁忌患者 建議者提供一份比較 secukinumab 與 etanercept adalimumab ustekinumab(45 mg, 90 mg) infliximab 用於治療中度至重度斑塊型乾癬且曾經標準全身性治療 ( 包含 ciclosporin methotrexate 及 phototherapy) 失敗或對於標準全身性治療有使用禁忌患者的最低成本分析 此分析時間為五年, 療效參數藉由執行貝氏網絡統合分析 (Bayesian network meta-analysis ) 而得之 在建議者的基礎方案分析結果中,secukinumab 跟不同比較組相比之下, 五年內所節省下的每病患每年平均花費為 19,494 英鎊到 23,083 英鎊 如以建議者折扣過後的藥價計算,SMC 認為 secukinumab 為具有成本效益 (cost-effective) 的治療選項, 但值得注意的是, 即使在有提供 PAS 折扣的藥價之下, 在治療第一年時,secukinumab 組的藥費並不是最低的, 還是會比某些治療組別高 在敏感度分析方面, 建議者假設治療第二年後的停藥率增減 10%, 且分析時間增減兩年 當分析時間減至三年時, secukinumab 相較於大部分的治療組別, 能帶來醫療費用的節省 雖然此份分析報告的分析時間只有五年, 但 SMC 專家意見認為觀察時間五年即可模擬出此慢性病程 在提供 PAS 折扣的藥價之下, 分析時間為第五年時, secukinumab 比起其他組別為最節省醫療花費的方案 最後,SMC 建議收載 secukinumab 用於治療中度至重度斑塊型乾癬且曾經標準全身性治療 ( 包含 ciclosporin methotrexate 及 phototherapy) 失敗或對於標準全身性治療有使用禁忌患者 5. 電子資料庫相關文獻 (1) 搜尋方法 本報告用於搜尋 CRD/INAHTA/Cochrane/PubMed/Embase 子資料庫之方法說 明如下 : 以下列 PICOS 做為搜尋條件, 即搜尋符合本次建議新藥給付條件下之病人 群 (population) 治療方法 (intervention) 療效對照品 (comparator) 結果測 量指標 (outcome) 及研究設計與方法 (study design), 其搜尋條件整理如下 : Population Intervention plaque psoriasis secukinumab 49/68
50 Comparator Outcome Study design 未設限未設限 Cost-effectiveness analysis; cost-utility analysis; cost-minimization analysis; cost-benefit analysis; cost analysis(taiwan only). 依照上述之 PICOS, 透過 CRD/INAHTA/Cochrane/PubMed 等文獻資料庫, 於 2015 年 11 月 3 日, 以 (secukinumab) 做為關鍵字進行搜尋, 搜尋策略 請見附錄二 (2) 搜尋結果 無符合條件之文獻 6. 建議者提供之其他成本效益研究資料 無提供 六 疾病負擔與財務影響 ( 一 ) 疾病負擔 根據 2013 年全民健保醫療統計年報, 牛皮癬及類似疾患 (Psoriasis and similar disorders) 的人數為 126,684 人 (ICD-9-CM 為 696), 此統計數據除了乾癬, 尚包含其他乾癬性關節病變 類乾癬等疾病 [25] Tsai 等人在 2011 年發表一篇利用 2005 年臺灣健保抽樣歸人檔, 得到臺灣乾癬病人的流行病學及共病症等相關資訊 [26] 其中, 他們利用 ICD-9-CM code 來定義乾癬病人, 計算出在臺灣, 乾癬的盛行率為 2.35 在另一篇 2009 年 Chang 等人發表的文章中, 利用 2000 至 2006 年的健保資料庫之百萬人歸人檔, 得到乾癬一年平均盛行率為 1.9 [27] ( 二 ) 核價參考品之建議 本品在 WHO ATC/DDD Index 2015 編碼為 L04AC10, 屬 L04A : immunosuppressants 的 L04AC:interleukin inhibitors 類, 而同屬 interleukin inhibitors 類的藥品共有 11 項 ( 包括 :daclizumab basiliximab anakinra 50/68
51 rilonacept ustekinumab mepolizumab tocilizumab canakinumab briakinumab secukinumab 及 siltuximab)[10] 若考慮本品之申請適應症, 目前我國健保收載用於治療乾癬病人的生物製劑僅有兩種 TNF-α 抑制劑包括 etanercept 與 adalimumab, 及一種 interleukin inhibitors ustekinumab [28], 此三種藥品的適應症與本品許可證所核准之適應症 治療適合接受全身性治療的中至重度斑瑰性乾癬成人患者 [9] 相符, 治療地位相近 其中, 因本品與 ustekinumab 作用機轉較相近, 查驗中心建議以 ustekinumab 為核價參考品的首選 ( 三 ) 財務影響 依據建議者所提供之財務衝擊分析, 若給付本品後, 每年將有約 名 左右的患者可接受本品的治療, 新藥年度藥費影響約為 1,800 萬元至 5,500 萬元 左右 建議者採用的主要假設與理由臚列如下 : 1. 臨床使用定位 : 建議者建議本品給付適應症為 治療適合接受全身性治療的中至重度斑瑰性乾癬成人患者, 臨床地位與現有藥品 etanercept adalimumab 和 ustekinumab 相當 2. 可能的市場規模 : (1) 符合適應症範圍的病人數推估 : 建議者分析 2009 年至 2013 年健保資料庫, 得到乾癬就診人數及使用照光治療 (phototherapy) 病人數, 進而推估線性公式預測 2014 至 2021 年乾癬就診人數及估算出平均每年有 19% 的乾癬就診人數會使用照光治療, 最後得到 2014 至 2021 年使用照光治療病人數 在計算 2014 至 2021 年使用生物製劑病人總數時, 建議者使用 2013 年健保資料庫所得人數加上 2014 新使用生物製劑病人數 ( 為 2.6% 的乾癬病人使用照光治療人數 ) 得到 2014 年人數, 以後依此類推至 2021 年 (2) 可能會使用本品的人數 : 建議者預測會使用各藥品的人數由轉換生物製劑病人數 (20% 使用生物製劑病人總數 ) 加上每年新使用生物製劑病人數 ( 為 2.6% 的乾癬病人使用照光治療人數 ), 再乘與各自藥品不同市占率得來, 建議者以自行假設的第一至第五年市占率計算, 預計未來五年間 (2016~2020 年 ), 每年會使用 secukinumab 的人數約為 150 至 900 人 3. 未來五年現有藥品和 secukinumab 市占率變化 : 51/68
52 (1) secukinumab: 以建議者自行假設之市占率估計之 (2) 現有藥品治療選擇 : 建議者列出不同藥品具不同的市占率並無說明假設原因 Etanercept adalimumab 及 ustekinumab 皆會因 secukinumab 進入市場而降低市占率 4. 現有治療藥費總成本 : 建議者計算出每人使用 etanercept adalimumab 和 ustekinumab 第一年及第二年療程花費 (20% 的病患會在第二年時會轉換或退出治療 ), 再用各藥品的使用人數算出第一至第五年各藥品的總計療程花費 5. secukinumab 的總藥費成本 : 建議者計算藥費依據以下劑量 : 第 1 週到第 5 週每週施打一次 300 mg, 之後則為 4 週施打一次 300 mg 建議者以第一年施打 16 次, 第二年施打 12 次來計算每人總藥費, 據此再用建議者自行預估的市占率及病人數 (20% 的病患會在第二年時會轉換療法 ), 推估出若本品納入給付第一年至第五年的年度藥費約 1 億元至 5 億元 6. 健保藥費預算影響觀點 : 在考慮本品給付範圍, 臨床地位為可能取代 etanercept adalimumab 或 ustekinumab, 估算預算影響約在 1,800 萬元至 5,500 萬元 查驗中心對於建議者所作之預算衝擊分析的評論如下 : 1. 使用人數推估 : (1) 使用人數算法 : 建議者的 2009 至 2013 年乾癬就診人數及使用光療法治療乾癬人數取自於分析健保資料庫所得之數據, 並 2014 至 2021 年的每年使用生物製劑病人總數根據此數據推估出, 卻未詳細說明方法學及相關 ICD-9 診斷碼定義, 較不容易再次驗證 另外, 在推論時可能使用本品人數時, 建議者假設為每年轉換生物製劑的乾癬病人 ( 為 20% 每年使用生物製劑病人總數 ) 加上每年新使用生物製劑病人數, 但在臨床使用上, 使用各藥品後再轉換至其他療法之比例不一, 這樣的估計方法可能會使病人數的估算具有不確定性 查驗中心委請健保署提供每年使用生物製劑病人總數, 以診斷碼 696.1, 且當年新使用生物製劑等定義, 並以建議者推估的轉換率, 推估每年乾癬病人使用生物製劑人數 ( 分為新使用及非新使用 ), 再乘上建議者預估之市占率, 預計未來五年間 (2016~2020 年 ), 每年會使用本品人數約為 230 至 2,000 人 (2) 市占率 : 建議者預估之市占率會直接影響使用到藥品人數, 查驗中心依照建議者對 etanercept adalimumab 和 ustekinumab 的估計進行預算衝擊分析, 其中建議者預期 secukinumab 納入給付後,ustekinumab 的市占率會大幅減少, 但市占率難以估計, 故此處會具有相當程度的不確定性 2. 藥費計算 : 52/68
53 (1) 建議者在送審文件中所擬定的健保給付規範療程為 起始時於第 和 4 週投予 300 mg, 接著於第 4 週開始每 4 週投予 300 mg( 體重 60 kg, 投予 150 mg 的劑量 ), 且於 12 週時, 需先行評估, 至少有 PASI 25 療效 在計算藥費部分, 建議者自述以第 1 週到第 5 週每週施打一次 300 mg, 之後則為 4 週施打一次 300 mg 來計算, 並且不分體重計算, 具不一致性 (2) 在施打次數估算方面, 建議者以第一及第二年維持劑量為施打 12 次估算之, 但以一年具 52 週, 每 4 週施打一次來計算, 維持劑量一年應施打 13 次 (3) 查驗中心假設醫師處方 cosentyx 維持劑量時, 可能會有同一處方情境 ( 同建議者假設所有病人皆處方 300mg) 或是混合處方型態 ( 依據建議者提供之國內臨床試驗資料,80% 病人大於 60kg,20% 病人小於 60kg, 故假設 80% 開方 300mg,20% 開方 150mg) 兩種狀況計算第一年 ( 施打 17 次 ) 及第二年藥費 ( 施打 13 次 ), 以取得預算衝擊預估範圍 綜合 1 2, 查驗中心重新估算病人數及藥費後, 認為本品若納入健保, 若為同一處方情境, 預估本品的藥費約為 1.5 億元至 12 億元間, 扣除可取代的現有生物製劑藥費, 將額外為健保帶來約 5 千萬至 2.9 億元的藥費支出 ; 若為混合處方型態情境, 預估本品的藥費約為 1.3 億元至 9.9 億元間, 扣除可取代的現有生物製劑藥費, 將額外為健保帶來約 3 千 3 百萬至 1.7 億元的藥費支出 考量國內流行病學資料尚顯不足, 乾癬處方型態複雜, 且可使用本品之病人數應不會一直維持高成長率, 許多參數估計具有不確定性, 決策者應謹慎解釋預算影響分析結果 七 經濟評估結論 1. 建議者針對本案遞送一份國內藥物經濟學研究, 建議者的分析結果顯示, 乾癬中度至重度病人在基礎方案中, 預期平均每位接受 secukinumab 300mg 治療的病人其第一 二及十年的醫療花費約為新台幣 319,094 元 506,849 元及 1,403,732 元 ; 與其他組別相比之下的遞增 QALYs 及遞增成本效益比值 (incremental cost-effectiveness ratio, ICER) 如下 : (1) 分析時間為一年時,secukinumab 300mg 分別與 ustekinumab 45 mg etanercept 及 adalimumab 相比之下的 ICER 值 ( 新臺幣 /QALY) 為 : 8,052,740 元 6,554,137 元及 5,136,024 元 ; 增加的 QALYs 分別為 及 0.04 QALY (2) 分析時間為兩年時,secukinumab 300mg 分別與 ustekinumab 45 mg etanercept 及 adalimumab 相比之下的 ICER 值 ( 新臺幣 /QALY) 為 : 6,378,570 元 5,255,886 元及 4,438,153 元 ; 增加的 QALYs 分別為 及 QALY (3) 分析時間為十年時,secukinumab 300mg 分別與 ustekinumab 45 mg etanercept 及 adalimumab 相比之下的 ICER 值 ( 新臺幣 /QALY) 為 : 4,981,114 元 4,280,180 元及 3,913,706 元 ; 增加的 QALYs 分別為 及 QALY 53/68
54 2. 查驗中心認為建議者所提出的國內藥物經濟學研究報告的研究主題與研究設計與其建議給付規定大抵相近, 惟存有部分疑義與限制 在療效部分使用間接比較得到參數, 使得不確定性增加 ; 且在單維敏感度分析部分並沒有呈現納入分析參數之高低值, 無法判別其不確定性來源 藥費部分, 依建議者藥費計算處敘述, 藥品單價較建議者申請健保給付價低, 且少算了施打起始及維持劑量各一次, 藥費應為低估值, 連帶造成 secukinumab 比上另外三種生物製劑之 ICER 值可能被低估 3. 加拿大 CADTH 澳洲 PBAC 英國 NICE 及蘇格蘭 SMC 皆建議收載使用於中至重度或重度斑塊型乾癬 (plaque psoriasis) 病人, 其中只有加拿大 CADTH 沒有限制用於曾經全身性治療復發之病人 4. 預算影響分析方面, 查驗中心認為建議者預算影響分析架構大致清楚, 但病人數可能因估算方式及市占率等種種假設而低估可能帶來的健保藥費影響 查驗中心重新估算後認為本品若納入健保給付後各年會約增加 230 至 2,000 人左右使用本品, 扣除可取代的現有治療費用後, 額外為健保帶來的年度藥費增加約 3 千 3 百萬至 2.9 億元 考量國內流行病學資料尚顯不足, 乾癬處方型態複雜, 且可使用本品之病人數應不會一直維持高成長率, 許多參數估計具有不確定性, 決策者應謹慎解釋預算影響分析結果 54/68
55 參考資料 1. Guidelines of care for the management of psoriasis and psoriatic arthritis - Section 1 Overview of psoriasis and guidelines of care for the treatment of psoriasis with biologics. J Am Acad Dermatol 2008; 58: Alan Menter, Neil J. Korman, Craig A. Elmets, et al. Guidelines of care for the management of psoriasis and psoriatic arthritis - Section 6. Guidelines of care for the treatment of psoriasis and psoriatic arthritis: Case-based presentations and evidence-based conclusions. J Am Acad Dermatol 2011; 65: Steven R Feldman, Robert P Dellavalle, Kristina Callis Duffin, Abena O Ofori. Treatment of psoriasis UpToDate. 2F5666&elapsedTimeMs=7&view=print&displayedView=full#. Published Accessed Oct.30th /29 世界乾癬日衛教手冊. 台灣皮膚科醫學會. Published Accessed Oct. 30th 蔡呈芳醫師. 衛教天地 - 乾癬. 台大醫院皮膚部. %E7%99%AC.aspx. Accessed Nov. 3rd., 過敏免疫風濕科衛教資訊 - 乾癬. 彰化基督教醫院. =7&pID=59&sNO=222. Published Accessed Nov. 4th 吳命選藥師, 陳怡靜藥師, 陳立奇藥師. 乾癬與治療. 藥學雜誌電子報. Published Accessed Nov. 4th 全民健康保險藥物給付項目及支付標準之藥品給付規定 -104 年版. 衛生福利部中央健康保險署. data_id=2919. Published Accessed Aug. 11th, 西藥 醫療器材 含藥化妝品許可證查詢. 衛生福利部食品藥物管理署. Published Accessed Nov. 5th ATC / DDD Index WHO Collaborating Centre for Drug Statistics Methodology. Published Accessed Nov. 5th Common Drug Review - Submission Status Report (Secukinumab). Canadian Agency for Drugs and Technologies in Health. Published Accessed Oct. 08th 55/68
56 Common Drug Review - Secukinumab. Canadian Agency for Drugs and Technologies in Health. Published Accessed Nov. 3rd., Public Summary Document - Secukinumab. Australian Government Department of Health. Published Accessed Oct. 08th Efficacy of Secukinumab Compared to Ustekinumab in Patients With Plaque-type Psoriasis. U.S. National Institute of Health &rank=1. Published Accessed Nov. 2nd,, Secukinumab for treating moderate to severe plaque psoriasis (NICE technology appraisal guidance 350). National Institute for Health and Care Excellence. Published Accessed Oct. 08th SMC Advice - secukinumab (Cosentyx). Scottish Medicines Consortium. mab_cosentyx/secukinumab_cosentyx. Published Accessed Oct. 08th Assessment Report - Cosentyx. European Medicines Agency. nes/003729/human_med_ jsp&mid=wc0b01ac058001d124. Published Accessed Oct. 08th Label information - Secukinumab. U.S. Food and Drug Administration. earch.drugdetails. Published Accessed Nov. 06th Introductory guide for standardised MedDRA queries (SMQs) Version International Conference on Harmonisation (ICH). Published Accessed Nov. 10th, Aberdeen Uo. Secukinumab (1st or 2nd line) for plaque, moderate to severe psoriasis. National Institute for Health Research. Published Accessed Oct. 29th, Secukinumab for plaque psoriasis National Horizon Scanning Centre. 56/68
57 me.html. Published Accessed Oct. 29th Xiong HZ, Gu JY, He ZG, et al. Efficacy and safety of secukinumab in the treatment of moderate to severe plaque psoriasis: a meta-analysis of randomized controlled trials. Int J Clin Exp Med 2015; 8(3): Tausend W, Downing C, Tyring S. Systematic review of interleukin-12, interleukin-17, and interleukin-23 pathway inhibitors for the treatment of moderate-to-severe chronic plaque psoriasis: ustekinumab, briakinumab, tildrakizumab, guselkumab, secukinumab, ixekizumab, and brodalumab. J Cutan Med Surg 2014; 18(3): Thaçi D, Blauvelt A, Reich K, et al. Secukinumab is superior to ustekinumab in clearing skin of subjects with moderate to severe plaque psoriasis: CLEAR, a randomized controlled trial. J Am Acad Dermatol 2015; 73(3): 年度全民健康保險醫療統計年報. 衛生福利部統計處 Published Accessed Nov. 3rd, Tsai TF, Wang TS, Hung ST, et al. Epidemiology and comorbidities of psoriasis patients in a national database in Taiwan. Journal of dermatological science 2011; 63(1): Chang YT, Chen TJ, Liu PC, et al. Epidemiological study of psoriasis in the national health insurance database in Taiwan. Acta dermato-venereologica 2009; 89(3): 健保用藥品項查詢. 行政院衛生署中央健康保險局. _id=3510&wd_id=851. Published Accessed Nov. 3rd, The Pharmaceutical Benefits Scheme - Secukinumab. Australian Government Department of Health. Accessed Nov. 2nd, /68
58 附錄 附錄一健保署藥品給付規定 (104 年版 )[8] 第八節免疫製劑 (Immunologic agents) Etanercept( 如 Enbrel); adalimumab( 如 Humira); ustekinumab( 如 Stelara) (98/11/1 100/7/1 101/5/1 101/12/1 102/1/1 104/4/1): 用於乾癬治療部分 1. 給付條件 : 限用於經照光治療及其他系統性治療無效, 或因醫療因素而無法接 受其他系統性治療之全身慢性中 重度之乾癬或頑固之掌蹠性乾癬, 且影響功能 之患者 (1) 所稱 慢性, 指病灶持續至少 6 個月, 且 Psoriasis area severity index (PASI) 10 ( 不適用 PASI 測定如膿疱性乾癬, 則以範圍 10% 體表面積 ) (2) 頑固之掌蹠性乾癬 : 指非膿疱性掌蹠廣泛性角化, 嚴重影響行走或日常作習, 申請時需附照片以供審查 照片應包括前 後 左 右至少四張, 並視需要加附 頭部 掌 蹠照片 (3) 慢性紅皮症乾癬 : 範圍 75% 體表面積, 病史超過 1 年, 以 cyclosporin 足量 (5mg/kg/d, 除非有明顯不良反應 ) 治療 6 個月以上, 停藥未滿 3 個月即復發到 PASI>10 或體表面積 >30( 需經皮膚科醫師評估 ), 可不經照光治療, 只需 methotrexate 及 acitretin 治療無效後直接申請 (101/12/1) (4) 所稱治療無效, 指治療後嚴重度仍符合上列第 (1) 及第 (2) 點情況, 或 PASI 或體 表面積改善 <50% ( 101/5/1) i. 治療必須包括足量之照光治療及包括以下兩種系統性治療之至少兩種, 包括 methotrexate acitretin cyclosporin ( 101/12/1) ii. 治療需至少使用 3 個月, 但育齡女性, 得不經 acitretin 使用 iii. 照光治療應依學理, 如光化療法 (PUVA) 及窄頻 UVB(nb-UVB) 必須每週至少 2 次, 寬頻 UVB 併用焦油每週至少 3 次, 並依學理逐漸增加至有效可忍受劑量 申請時必須附病歷影印及詳細照光劑量紀錄 iv.methotrexate 合理劑量需達每週 15mg, cyclosporin 為 mg/kg/d, acitretin 為 mg/kg/d 但若因為藥物毒性無法耐受, 使用劑量可酌情降低 58/68
59 (5) 所稱無法接受治療 : i.methotrexate: 指因肝功能異常或切片第三期 a 異常, 經 6 個月後切片仍無改善, 或第三期 b 以上之肝切片異常, 病毒性肝炎帶原或腎功能異常而無法使用 methotrexate 治療者 ii.acitretin: 指有明顯肝功能異常 高血脂無法有效控制, 或 cyclosporin 有效但 停藥後迅速復發, 已持續使用超用 1 年, 或已產生腎毒性經減量後無法有效控制 者 2. 需經事前審查核准後使用 : (1) 初次申請時, 以 6 個月為 1 個療程, 持續使用時每 6 個月需再申報一次, 且 應於期滿前 1 個月提出 (101/12/1) (2) 紅皮症乾癬病患以 6 個月為限, 於 6 個月療程結束後, 應回復使用 cyclosporin, 除非產生腎功能異常 (Creatinine 基礎值上升 30%), 或其他無法有效控制之副作 用, 減藥後乾癬仍無法有效控制 (101/12/1) (3)Etanercept 初期 3 個月可使用 50mg biw, 之後則為 25mg biw, 且於 12 週時, 需先行評估, 至少有 PASI25 療效 (4)Adalimumab 初次投予為 80mg, 之後則為 40mg qow, 且於 12 週時, 須先行 評估, 至少有 PASI25 療效 (100/7/1) (5)Ustekinumab 初次及 4 週後投予 45mg, 之後則為 45mg q12w, 且於 16 週時, 需先行評估, 至少有 PASI25 療效 (101/5/1) (6) 原先使用 cyclosporin 控制有效且腎功能異常 (Creatinine 基礎值上升 30%) 者, 於 6 個月療程結束後, 應回復使用 cyclosporin, 除非產生腎功能異常, 或其他無法有效控制之副作用, 減藥後乾癬仍無法有效控制, 否則下次申請應於 1 年後 (7) 初次申請後每六個月須再次申請續用, 續用時, 與初次治療前之療效達 PASI50 方可使用 ; 且 etanercept 再次申請時僅限使用 25mg biw 之劑量 停藥超過 3 個 月再申請者, 視同新申請案件, 否則視為續用案件 (101/12/1 104/4/1) 3. 使用 etanercept adalimumab 或 ustekinumab 時 cyclosporine 及照光治療, 考慮 etanercept adalimumab 或 ustekinumab 於乾癬療效可能較慢, 及立即停藥之可能反彈現象, 治療前兩個月得合併使用, 但 etanercept adalimumab 或 ustekinumab 療效出現時即應逐漸停用 (101/5/1) 59/68
60 4. 需排除使用的情形應參照藥物仿單, 重要之排除使用狀況包括 : (1) 懐孕或正在授乳的婦女 (2) 罹患活動性的感染症的病患 (3) 未經完整治療之結核病的病患 ( 包括潛伏結核感染治療未達四週者, 申請時 應檢附潛伏結核感染篩檢紀錄及治療紀錄供審查 ) (102/1/1) (4) 身上帶有人工關節者, 罹患或先前曾罹患過嚴重的敗血病 (sepsis) 者 (5) 惡性腫瘤或具有癌症前兆 (pre-malignancy) 的病患 (6) 免疫功能不全者 (immunodeficiency) 5. 需停止治療情形, 如果發生下列現象應停止治療 : (1) 不良事件, 包括 : i. 惡性腫瘤 ii. 該藥物引起的嚴重性毒性 iii. 懷孕 ( 暫時停藥即可 ) iv. 嚴重的間發性感染症 (intercurrent infection)( 暫時停藥即可 ) (2) 療效不彰 : 患者經過 6 個月治療 ( 初次療程 ) 後未達療效者, 療效定義指 PASI 或體表面積改善未達 50% 6. 暫緩續用之相關規定 :(104/4/1) (1) 暫緩續用時機 : 使用生物製劑治療 2 年後符合 PASI 10 者 (2) 因使用一種生物製劑治療後療效不彰, 而轉用另一種不同藥理機轉之生物製 劑, 以轉用後者之起始日重新計算 2 年後開始減量之時機 但因無法忍受副作用 而轉用相同藥理機轉之生物製劑, 轉用前後所使用生物製劑之期間均應計入 7. 暫緩續用後若疾病再復發, 可重新申請使用, 須符合至少有 50% 復發 ( 需附上 次療程治療前 後, 及本次照片 ) (104/4/1) 60/68
61 附錄二 Secukinumab 在澳洲的給付規定內容 [25] Authority Required Severe chronic plaque psoriasis Treatment Phase: Initial treatment Initial 1, Whole body (new patient (no prior biological agent) or patient recommencing treatment after a break of 5 years or more) Clinical criteria: Patient must have severe chronic plaque psoriasis where lesions have been present for at least 6 months from the time of initial diagnosis, AND Patient must not have received any prior PBS-subsidised treatment with a biological agent for this condition; OR Patient must not have received PBS-subsidised treatment with a biological agent for at least 5 years, if they have previously received PBS-subsidised treatment with a biological agent for this condition and wish to commence a new Treatment Cycle, AND Patient must have failed to achieve an adequate response, as demonstrated by a Psoriasis Area and Severity Index (PASI) assessment, to at least 3 of the following 4 treatments: (i) phototherapy (UVB or PUVA) for 3 treatments per week for at least 6 weeks; and/or (ii) methotrexate at a dose of at least 10 mg weekly for at least 6 weeks; and/or (iii) cyclosporin at a dose of at least 2 mg per kg per day for at least 6 weeks; and/or (iv) acitretin at a dose of at least 0.4 mg per kg per day for at least 6 weeks, AND Patient must have signed a patient and prescriber acknowledgement indicating they understand and acknowledge that PBS-subsidised treatment will cease if they do not meet the predetermined response criterion for ongoing PBS-subsidised treatment, as outlined in the restriction for continuing treatment (whole body), AND The treatment must be as systemic monotherapy (other than methotrexate), AND Patient must not receive more than 16 weeks of treatment under this restriction. Population criteria: Patient must be aged 18 years or older. Treatment criteria: Must be treated by a dermatologist. For the purposes of this restriction 'biological agent' means adalimumab, etanercept, infliximab, secukinumab or ustekinumab. The following criterion indicates failure to achieve an adequate response to prior treatment and must be demonstrated in the patient at the time of the application: 61/68
62 (a) A current Psoriasis Area and Severity Index (PASI) score of greater than 15, as assessed, preferably whilst still on treatment, but no longer than 1 month following cessation of the most recent prior treatment. (b) A PASI assessment must be completed for each prior treatment course, preferably whilst still on treatment, but no longer than 1 month following cessation of each course of treatment. (c) The most recent PASI assessment must be no more than 1 month old at the time of application. Note A PASI assessment of the patient's response to this initial course of treatment must be made after at least 12 weeks of treatment so that there is adequate time for a response to be demonstrated. This assessment, which will be used to determine eligibility for continuing treatment, must be submitted to the Department of Human Services no later than 1 month from the date of completion of this initial course of treatment. Where a response assessment is not undertaken and submitted to the Department of Human Services within these timeframes, the patient will be deemed to have failed to respond to treatment with this drug. Authority Required Severe chronic plaque psoriasis Treatment Phase: Initial treatment Initial 2, Whole body (change or recommencement of treatment) Clinical criteria: Patient must have a documented history of severe chronic plaque psoriasis, AND Patient must have received prior PBS-subsidised treatment with a biological agent for this condition in this Treatment Cycle, AND Patient must not have already failed, or ceased to respond to, PBS-subsidised treatment with 3 biological agents for this condition within this Treatment Cycle, AND Patient must not have failed, or ceased to respond to, PBS-subsidised therapy with this drug for the treatment of this condition in the current Treatment Cycle, AND The treatment must be as systemic monotherapy (other than methotrexate), AND Patient must not receive more than 16 weeks of treatment under this restriction. Population criteria: 62/68
63 Patient must be aged 18 years or older. Treatment criteria: Must be treated by a dermatologist. For the purposes of this restriction 'biological agent' means adalimumab, etanercept, infliximab, secukinumab or ustekinumab. An adequate response to treatment is defined as: A Psoriasis Area and Severity Index (PASI) score which is reduced by 75% or more, or is sustained at this level, when compared with the prebiological treatment baseline value for this Treatment Cycle. Note Patients who fail to demonstrate a response to treatment with 3 biological agents are deemed to have completed this Treatment Cycle and must cease PBS-subsidised therapy. These patients may recommence a new Biological Treatment Cycle after a minimum of 5 years has elapsed between the date the last prescription for a PBS-subsidised biological agent was approved in this Cycle and the date of the first application under the new Cycle. Authority Required Severe chronic plaque psoriasis Treatment Phase: Initial treatment Initial 1, Face, hand, foot (new patient (no prior biological agent) or patient recommencing treatment after a break of 5 years or more) Clinical criteria: Patient must have severe chronic plaque psoriasis of the face, or palm of a hand or sole of a foot where the plaque or plaques have been present for at least 6 months from the time of initial diagnosis, AND Patient must not have received any prior PBS-subsidised treatment with a biological agent for this condition; OR Patient must not have received PBS-subsidised treatment with a biological agent for at least 5 years, if they have previously received PBS-subsidised treatment with a biological agent for this condition and wish to commence a new Treatment Cycle, AND Patient must have failed to achieve an adequate response, as demonstrated by a Psoriasis Area and Severity Index (PASI) assessment, to at least 3 of the following 4 treatments: (i) phototherapy (UVB or PUVA) for 3 treatments per week for at least 6 weeks; and/or (ii) methotrexate at a dose of at least 10 mg weekly for at least 6 weeks; and/or (iii) cyclosporin at a dose of at least 2 mg per kg per day for at least 6 weeks; and/or (iv) acitretin at a dose of at least 0.4 mg per kg per day for at least 6 weeks, 63/68
64 AND Patient must have signed a patient and prescriber acknowledgement indicating they understand and acknowledge that PBS-subsidised treatment will cease if they do not meet the predetermined response criterion for ongoing PBS-subsidised treatment, as outlined in the restriction for continuing treatment (face, hand, foot), AND The treatment must be as systemic monotherapy (other than methotrexate), AND Patient must not receive more than 16 weeks of treatment under this restriction. Population criteria: Patient must be aged 18 years or older. Treatment criteria: Must be treated by a dermatologist. For the purposes of this restriction 'biological agent' means adalimumab, etanercept, infliximab, secukinumab or ustekinumab. The following criterion indicates failure to achieve an adequate response to prior treatment and must be demonstrated in the patient at the time of the application: (a) Chronic plaque psoriasis classified as severe due to a plaque or plaques on the face, palm of a hand or sole of a foot where: (i) at least 2 of the 3 Psoriasis Area and Severity Index (PASI) symptom subscores for erythema, thickness and scaling are rated as severe or very severe, as assessed, preferably whilst still on treatment, but no longer than 1 month following cessation of the most recent prior treatment; or (ii) the skin area affected is 30% or more of the face, palm of a hand or sole of a foot, as assessed, preferably whilst still on treatment, but no longer than 1 month following cessation of the most recent prior treatment; (b) A PASI assessment must be completed for each prior treatment course, preferably whilst still on treatment, but no longer than 1 month following cessation of each course of treatment. (c) The most recent PASI assessment must be no more than 1 month old at the time of application. Authority Required Severe chronic plaque psoriasis Treatment Phase: Initial treatment Initial 2, Face, hand, foot (change or recommencement of treatment) Clinical criteria: Patient must have a documented history of severe chronic plaque psoriasis of the face, 64/68
65 or palm of a hand or sole of a foot, AND Patient must have received prior PBS-subsidised treatment with a biological agent for this condition in this Treatment Cycle, AND Patient must not have already failed, or ceased to respond to, PBS-subsidised treatment with 3 biological agents for this condition within this Treatment Cycle, AND Patient must not have failed, or ceased to respond to, PBS-subsidised therapy with this drug for the treatment of this condition in the current Treatment Cycle, AND The treatment must be as systemic monotherapy (other than methotrexate), AND Patient must not receive more than 16 weeks of treatment under this restriction. Population criteria: Patient must be aged 18 years or older. Treatment criteria: Must be treated by a dermatologist. For the purposes of this restriction 'biological agent' means adalimumab, etanercept, infliximab, secukinumab or ustekinumab. An adequate response to treatment is defined as the plaque or plaques assessed prior to biological treatment showing: (i) a reduction in the Psoriasis Area and Severity Index (PASI) symptom subscores for all 3 of erythema, thickness and scaling, to slight or better, or sustained at this level, as compared to the pre-biological treatment baseline values; or (ii) a reduction by 75% or more in the skin area affected, or sustained at this level, as compared to the pre-biological treatment baseline value. Authority Required Severe chronic plaque psoriasis Treatment Phase: Initial treatment - Initial 1, Whole body or Face, hand, foot (new patient or patient recommencing treatment after a break of 5 years or more) or Initial 2, Whole body or Face, hand, foot (change or recommencement of treatment) - balance of supply Clinical criteria: Patient must have received insufficient therapy with this drug under the Initial 1, Whole body (new patient or patient recommencing treatment after a break of 5 years or more) restriction to complete 16 weeks treatment; OR 65/68
66 Patient must have received insufficient therapy with this drug under the Initial 2, Whole body (change or recommencement of treatment) restriction to complete 16 weeks treatment; OR Patient must have received insufficient therapy with this drug under the Initial 1, Face, hand, foot (new patient or patient recommencing treatment after a break of 5 years or more) restriction to complete 16 weeks treatment; OR Patient must have received insufficient therapy with this drug under the Initial 2, Face, hand, foot (change or recommencement of treatment) restriction to complete 16 weeks treatment, AND The treatment must be as systemic monotherapy (other than methotrexate), AND The treatment must provide no more than the balance of up to 16 weeks treatment available under the above restrictions. Treatment criteria: Must be treated by a dermatologist. 66/68
67 附錄表一療效評估文獻搜尋記錄 資料庫查詢日期關鍵字篇數 Cochrane Library 'ustekinumab' PubMed "secukinumab"[supplementary Concept] OR "secukinumab"[all Fields] ("secukinumab"[supplementary Concept] OR "secukinumab"[all Fields]) AND (("plaque, amyloid"[mesh Terms] OR ("plaque"[all Fields] AND "amyloid"[all Fields]) OR "amyloid plaque"[all Fields] OR "plaque"[all Fields] OR "dental plaque"[mesh Terms] OR ("dental"[all Fields] AND "plaque"[all Fields]) OR "dental plaque"[all Fields]) AND ("psoriasis"[mesh Terms] OR "psoriasis"[all Fields])) ("secukinumab"[supplementary Concept] OR "secukinumab"[all Fields]) AND (("plaque, amyloid"[mesh Terms] OR ("plaque"[all Fields] AND "amyloid"[all Fields]) OR "amyloid plaque"[all Fields] OR "plaque"[all Fields] OR "dental plaque"[mesh Terms] OR ("dental"[all Fields] AND "plaque"[all Fields]) OR "dental plaque"[all Fields]) AND ("psoriasis"[mesh Terms] OR "psoriasis"[all Fields])) AND (Meta-Analysis[ptyp] OR systematic[sb]) 2 EMBASE #1 'secukinumab'/exp OR 'secukinumab' #2 'plaque psoriasis' #3 #1 AND #2 #4 #1 AND #2 AND ([systematic review]/lim OR [meta analysis]/lim) AND [humans]/lim AND [english]/lim /68
68 附錄表二經濟評估文獻搜尋紀錄 資料庫 查詢日期 關鍵字 篇數 篩選後篇數 PubMed #1 (secukinumab or 0 cosentyx) #2 ("cost effectiveness" or "cost benefit" or "cost utility" or "cost minimization" or "economic evaluation") #3 plaque psoriasis #4 #1 AND #2 AND #3 Cochrane secukinumab or cosentyx 0 Library Limited to economic evaluation INAHTA secukinumab or cosentyx 0 CRD (secukinumab or cosentyx) 0 AND (plaque psoriasis) AND (cost effectiveness or cost benefit or cost utility or cost minimization or economic evaluation) Embase (secukinumab or cosentyx) AND (plaque psoriasis) AND (cost effectiveness or cost benefit or cost utility or cost minimization or economic evaluation) 0 68/68
Zytiga... Zytiga... Zytiga Zytiga Zytiga
 250 本資料僅提供醫護人員衛教使用 ............... Zytiga... Zytiga... Zytiga... 2 3 4 5 6 7 8 9 Zytiga... 10 Zytiga... 10...... 13 18 Zytiga Zytiga 2 25% 3 PSA PSA 3~4 ng/ml PSA bone scan CT scan MRI 4 5 攝護腺癌之治療 治療方面
250 本資料僅提供醫護人員衛教使用 ............... Zytiga... Zytiga... Zytiga... 2 3 4 5 6 7 8 9 Zytiga... 10 Zytiga... 10...... 13 18 Zytiga Zytiga 2 25% 3 PSA PSA 3~4 ng/ml PSA bone scan CT scan MRI 4 5 攝護腺癌之治療 治療方面
二 主要醫療科技評估組織之給付建議 : 如表二 三 相對療效與安全性 ( 人體健康 ):( 詳細內文請參閱表六至表九 ) 共尋獲 3 項第三期 雙盲 隨機分派直接比較試驗,VOYAGE 1 VOYAGE 2 及 NAVIGATE 試驗 ; 以及 1 項 Cochrane 的網絡統合分析 1. VOY
 財團法人醫藥品查驗中心 Center For Drug Evaluation 特諾雅注射液 (Tremfya Solution for Injection 100mg) 醫療科技評估報告 藥物納入全民健康保險給付建議書 - 藥品專用 資料摘要 藥品名稱 建議者 藥品許可證持有商 含量規格劑型 主管機關許可適應症 建議健保給付之適應 症內容 建議健保給付條件 Tremfya Solution for
財團法人醫藥品查驗中心 Center For Drug Evaluation 特諾雅注射液 (Tremfya Solution for Injection 100mg) 醫療科技評估報告 藥物納入全民健康保險給付建議書 - 藥品專用 資料摘要 藥品名稱 建議者 藥品許可證持有商 含量規格劑型 主管機關許可適應症 建議健保給付之適應 症內容 建議健保給付條件 Tremfya Solution for
老人憂鬱症的認識與老人自殺問題
 18-24 25-44 45-64 65 10 8 6 4 2 0 ( 40% 15% Affect Cognition : drive Behavior DSM-V major depressive episode 2 9 5 Electronic Convulsion Therapy; ECT Rabins65 1% Rabins, 1992 20%-30% Blazer, 1994 65 12.9
18-24 25-44 45-64 65 10 8 6 4 2 0 ( 40% 15% Affect Cognition : drive Behavior DSM-V major depressive episode 2 9 5 Electronic Convulsion Therapy; ECT Rabins65 1% Rabins, 1992 20%-30% Blazer, 1994 65 12.9
本報告經文獻查詢到 1 篇 ixekizumab 與 secukinumab 的間接比較結果, 但統計結果 (PASI 75 PASI 90 及 PASI 100) 會因為共同參考品 (etanercept ustekinumab, 或合 併分析 ) 風險統計量 (RD 或 OR), 以及分析方法而
 財團法人醫藥品查驗中心 Center For Drug Evaluation 達癬治注射劑 (Taltz ) 醫療科技評估報告 藥物納入全民健康保險給付建議書 - 藥品專用 資料摘要 藥品名稱 達癬治注射劑 成分 ixekizumab 建議者 台灣禮來股份有限公司 藥品許可證持有商 同上 含量規格劑型 Ixekizumab 80 mg / 注射劑 主管機關許可適應症 治療適合接受全身性治療的中至重度斑塊性乾癬之成人患者
財團法人醫藥品查驗中心 Center For Drug Evaluation 達癬治注射劑 (Taltz ) 醫療科技評估報告 藥物納入全民健康保險給付建議書 - 藥品專用 資料摘要 藥品名稱 達癬治注射劑 成分 ixekizumab 建議者 台灣禮來股份有限公司 藥品許可證持有商 同上 含量規格劑型 Ixekizumab 80 mg / 注射劑 主管機關許可適應症 治療適合接受全身性治療的中至重度斑塊性乾癬之成人患者
F A F G F H F F A F G F H doi : / NRD 1032 PK PK 攻防首部曲 在藥品查驗登記時, 必須檢附相關藥動學資料支持藥品的療效與安全性以備核准
 藥物在體內的 PK 攻防 36 藥物動力學 PharmacokineticsADME Absorption Z Disposition Distribution Elimination Metabolism D Excretion T C T C Z pharmacokinetics PK absorption distribution metabolism excretion ADME 2015
藥物在體內的 PK 攻防 36 藥物動力學 PharmacokineticsADME Absorption Z Disposition Distribution Elimination Metabolism D Excretion T C T C Z pharmacokinetics PK absorption distribution metabolism excretion ADME 2015
 2013~2015 保健食品產業專業人才 供需調查 2011 5 2011529 2012 2013~2015 2012 44.67% 2011 11.96% 2013~2015 ... 1... 1... 5... 10... 12... 13... 14... 19... 20... 22... 24... 12... 19... 21... 22 III IV 1... 1 2... 3
2013~2015 保健食品產業專業人才 供需調查 2011 5 2011529 2012 2013~2015 2012 44.67% 2011 11.96% 2013~2015 ... 1... 1... 5... 10... 12... 13... 14... 19... 20... 22... 24... 12... 19... 21... 22 III IV 1... 1 2... 3
目錄
 2014 年度 企業社會責任報告 目錄 1 4 2 5 3 7 3.1 7 3.2 8 3.3 8 4 9 4.1 9 4.2 2014 10 4.3 11 5 16 5.1 16 5.2 18 5.3 20 5.4 21 6 22 6.1 22 6.2 23 6.3 24 6.4 25 6.5 26 6.6 27 6.7 27 6.8 27 7 28 7.1 28 7.2 29 7.3 30 7.4
2014 年度 企業社會責任報告 目錄 1 4 2 5 3 7 3.1 7 3.2 8 3.3 8 4 9 4.1 9 4.2 2014 10 4.3 11 5 16 5.1 16 5.2 18 5.3 20 5.4 21 6 22 6.1 22 6.2 23 6.3 24 6.4 25 6.5 26 6.6 27 6.7 27 6.8 27 7 28 7.1 28 7.2 29 7.3 30 7.4
表二 105 年國中教育會考英語科閱讀與聽力答對題數對應整體能力等級加標示對照表 閱讀答 對題數 聽力答對題數 待加強待加強待加強待加強待加強待加強待加強待加強待加強待加強待加強待加強
 表一 105 年國中教育會考國文科 社會科與自然科能力等級加標示與答對題數對照表 國文社會自然 A++ 46-48 60-63 51-54 A+ 42-48 44-45 54-63 58-59 46-54 49-50 A 42-43 54-57 46-48 B++ 37-41 45-53 37-45 B+ 20-41 31-36 24-53 38-44 20-45 30-36 B 20-30 24-37
表一 105 年國中教育會考國文科 社會科與自然科能力等級加標示與答對題數對照表 國文社會自然 A++ 46-48 60-63 51-54 A+ 42-48 44-45 54-63 58-59 46-54 49-50 A 42-43 54-57 46-48 B++ 37-41 45-53 37-45 B+ 20-41 31-36 24-53 38-44 20-45 30-36 B 20-30 24-37
<4D F736F F D20A4A4C3C4B2A3B77EB56FAE69ABD8C4B3AED15F66756C6C>
 ... 3... 10... 12... 13 3.1... 13 3.2... 13 3.3... 14 3.4... 15 3.5... 17 3.6... 21 3.7... 23 3.8 GMP... 24 3.9... 26... 28 4.1... 28 4.2... 29... 30 5.1... 30 5.2.... 30 5.3... 37 5.4... 38 5.5... 39
... 3... 10... 12... 13 3.1... 13 3.2... 13 3.3... 14 3.4... 15 3.5... 17 3.6... 21 3.7... 23 3.8 GMP... 24 3.9... 26... 28 4.1... 28 4.2... 29... 30 5.1... 30 5.2.... 30 5.3... 37 5.4... 38 5.5... 39
 24 24. Special Issue 名 人 講 堂 專 題 研 究 表3 新加坡政府對銷售給不同屬性投資人的對沖基金管理指引 25 焦 點 視 界 27 26 市 場 掃 描 證 交 集 錦 資料來源 新加坡金融管理局(Monetary Authority of Singapore)網站 25 機構投資人定義 (1)依銀行法設立的銀行 (2)商業銀行 (3)財務公司 (4)保險公司 (5)信託公司
24 24. Special Issue 名 人 講 堂 專 題 研 究 表3 新加坡政府對銷售給不同屬性投資人的對沖基金管理指引 25 焦 點 視 界 27 26 市 場 掃 描 證 交 集 錦 資料來源 新加坡金融管理局(Monetary Authority of Singapore)網站 25 機構投資人定義 (1)依銀行法設立的銀行 (2)商業銀行 (3)財務公司 (4)保險公司 (5)信託公司
乾 癬 介 紹 及 治 療 永 康 院 區 林 佳 靜 藥 師 壹 前 言 乾 癬 又 稱 為 銀 屑 病, 傳 統 俗 稱 牛 皮 癬, 它 並 非 為 黴 菌 感 染 所 造 成 的 癬, 而 是 一 種 慢 性 自 體 免 疫 性 疾 病 (chronic autoimmune disease
 奇 美 藥 訊 一 百 零 四 年 七 月 二 十 日 第 壹 佰 壹 拾 捌 期 奇 美 藥 訊 Chi Mei Medical Center Drug Bulletin 發 行 人 : 邱 仲 慶 總 編 輯 : 王 慧 瑜 主 編 : 王 雅 萱 發 行 所 : 奇 美 醫 療 財 團 法 人 奇 美 醫 院 藥 劑 部 網 址 :http://chimeipharm.org/index.php/drugbulletin
奇 美 藥 訊 一 百 零 四 年 七 月 二 十 日 第 壹 佰 壹 拾 捌 期 奇 美 藥 訊 Chi Mei Medical Center Drug Bulletin 發 行 人 : 邱 仲 慶 總 編 輯 : 王 慧 瑜 主 編 : 王 雅 萱 發 行 所 : 奇 美 醫 療 財 團 法 人 奇 美 醫 院 藥 劑 部 網 址 :http://chimeipharm.org/index.php/drugbulletin
 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 243,1052,272 791222101452 2014719 58339347 396634355 196413164 28269 26 27 28 29 () () () () () () () () () () () () () () () () () () ()
2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 243,1052,272 791222101452 2014719 58339347 396634355 196413164 28269 26 27 28 29 () () () () () () () () () () () () () () () () () () ()
 第二節 研究方法 本論文第一章 緒論 說明研究動機與目的 研究方法及研究的範圍及限制 並對 飲食散文的義界 作一觀念的釐清 第二章 文獻探討 就將本研究的理 論建構中的概念作釐清 分別為 現代文學 飲食文學的重要論著 等兩個部 分來描述目前文獻的研究成果 並探討其不足待補述的地方 本研究以 文化研 究 為主要研究基礎 統攝整個研究架構 在不同章節裡 佐以相關研究方法進 行論述 茲圖示如下 研究方法
第二節 研究方法 本論文第一章 緒論 說明研究動機與目的 研究方法及研究的範圍及限制 並對 飲食散文的義界 作一觀念的釐清 第二章 文獻探討 就將本研究的理 論建構中的概念作釐清 分別為 現代文學 飲食文學的重要論著 等兩個部 分來描述目前文獻的研究成果 並探討其不足待補述的地方 本研究以 文化研 究 為主要研究基礎 統攝整個研究架構 在不同章節裡 佐以相關研究方法進 行論述 茲圖示如下 研究方法
Microsoft PowerPoint - SAGE 2010
 SAGE Journals Online -Communication Studies 大綱 SAGE 簡介 Communication Studies 收錄內容 SJO 平台功能介紹 首頁 瀏覽功能 檢索功能 進階服務 SAGE Content 超過 520 種人文 社會科學 理工 科技領域電子期刊 SAGE 與超過 245 個國際知名的學會合作 ( 包括 American Sociological
SAGE Journals Online -Communication Studies 大綱 SAGE 簡介 Communication Studies 收錄內容 SJO 平台功能介紹 首頁 瀏覽功能 檢索功能 進階服務 SAGE Content 超過 520 種人文 社會科學 理工 科技領域電子期刊 SAGE 與超過 245 個國際知名的學會合作 ( 包括 American Sociological
財團法人醫藥品查驗中心醫療科技評估報告補充資料 106BTD _Blincyto 商品名 :Blincyto for Injection 學名 :Blinatumomab 事由 : 有關台灣安進藥品有限公司建議將 Blincyto 納入健保給付用於治療 費城染色體陰性復發型或頑固型 B
 商品名 :Blincyto for Injection 學名 :Blinatumomab 事由 : 有關台灣安進藥品有限公司建議將 Blincyto 納入健保給付用於治療 費城染色體陰性復發型或頑固型 B 細胞前驅因子之急性淋巴芽細胞白血病 (ALL) 之成人病患 一案, 本中心於 106 年 5 月已完成醫療科技評估報告 ; 由於建議者於 106 年 6 月提出建議調降藥品價格, 因此, 健保署於
商品名 :Blincyto for Injection 學名 :Blinatumomab 事由 : 有關台灣安進藥品有限公司建議將 Blincyto 納入健保給付用於治療 費城染色體陰性復發型或頑固型 B 細胞前驅因子之急性淋巴芽細胞白血病 (ALL) 之成人病患 一案, 本中心於 106 年 5 月已完成醫療科技評估報告 ; 由於建議者於 106 年 6 月提出建議調降藥品價格, 因此, 健保署於
中期 12 中期 % 報告期 報告 44 中期 報 年中期報告 中國鋁業股份有限公司
 2016 2016 6 30 6 2016 2016 www.hkex.com.hk www.chalco.com.cn 2 6 8 10 中期 12 中期 12 13 16 22 25 26 27 5% 28 29 29 報告期 29 30 31 31 31 32 35 35 36 38 報告 44 中期 報 46 1 2016 年中期報告 中國鋁業股份有限公司 1. ALUMINUM CORPORATION
2016 2016 6 30 6 2016 2016 www.hkex.com.hk www.chalco.com.cn 2 6 8 10 中期 12 中期 12 13 16 22 25 26 27 5% 28 29 29 報告期 29 30 31 31 31 32 35 35 36 38 報告 44 中期 報 46 1 2016 年中期報告 中國鋁業股份有限公司 1. ALUMINUM CORPORATION
% % % 獨立 廉正 專業 創新
 101 99 102 101 1. 2. 3. 4. 5. 6. 7. 8. 9. 10. 99 102 8 4 34 11 101826 594 71.91% 160 19.37% 72 8.72% 101 100 27 18100 21 101 35 獨立 廉正 專業 創新 1. 7,290 8,677 26,180 26,011 1,272 1,346 142 157 7 7 1,757 1,795
101 99 102 101 1. 2. 3. 4. 5. 6. 7. 8. 9. 10. 99 102 8 4 34 11 101826 594 71.91% 160 19.37% 72 8.72% 101 100 27 18100 21 101 35 獨立 廉正 專業 創新 1. 7,290 8,677 26,180 26,011 1,272 1,346 142 157 7 7 1,757 1,795
_BK07.ps, page Preflight ( _BK07.indd )
 1 2 3 4 5 6 7 8 9 10 11 12 7.3 家庭變遷對健康的影響 在經濟起伏時 家庭支持十分重要 在 兩地三岸社會政策 一書中 魏雁濱 曾群 在 社會排斥 一文提及一項研究發現 在北歐六國和蘇格蘭 家人支持對防止失業 青年陷入貧窮發揮重要作用 在福利制度相對比北歐較弱的南歐國家如意大利 家庭 和社會網絡對失業者起較大的支持和保護作用 在中國人社會 家庭支持也十分重要 根據本港社會服務聯會
1 2 3 4 5 6 7 8 9 10 11 12 7.3 家庭變遷對健康的影響 在經濟起伏時 家庭支持十分重要 在 兩地三岸社會政策 一書中 魏雁濱 曾群 在 社會排斥 一文提及一項研究發現 在北歐六國和蘇格蘭 家人支持對防止失業 青年陷入貧窮發揮重要作用 在福利制度相對比北歐較弱的南歐國家如意大利 家庭 和社會網絡對失業者起較大的支持和保護作用 在中國人社會 家庭支持也十分重要 根據本港社會服務聯會
0 0 = 1 0 = 0 1 = = 1 1 = 0 0 = 1
 0 0 = 1 0 = 0 1 = 0 1 1 = 1 1 = 0 0 = 1 : = {0, 1} : 3 (,, ) = + (,, ) = + + (, ) = + (,,, ) = ( + )( + ) + ( + )( + ) + = + = = + + = + = ( + ) + = + ( + ) () = () ( + ) = + + = ( + )( + ) + = = + 0
0 0 = 1 0 = 0 1 = 0 1 1 = 1 1 = 0 0 = 1 : = {0, 1} : 3 (,, ) = + (,, ) = + + (, ) = + (,,, ) = ( + )( + ) + ( + )( + ) + = + = = + + = + = ( + ) + = + ( + ) () = () ( + ) = + + = ( + )( + ) + = = + 0
選擇學校午膳供應商手冊適用於中、小學 (2014年9月版)
 2014 年 9 月版 選擇 學校午膳供應商手冊 適用於中 小學 i 1 1 2 3 4 5 6 7 8 9 1 2 2 i. ii. iii. iv. v. i. ii. iii. iv. v. vi. vii. 3 i. ii. iii. iv. v. 4 i. ii. 1. 2. 3. 4. 5. iii. iv. 5 6 3 4 5 6 i. ii. i. ii. iii. iv. v.
2014 年 9 月版 選擇 學校午膳供應商手冊 適用於中 小學 i 1 1 2 3 4 5 6 7 8 9 1 2 2 i. ii. iii. iv. v. i. ii. iii. iv. v. vi. vii. 3 i. ii. iii. iv. v. 4 i. ii. 1. 2. 3. 4. 5. iii. iv. 5 6 3 4 5 6 i. ii. i. ii. iii. iv. v.
戒菸實務個案自助手冊105年Ver.2
 本計劃經費來自 品健康福利捐支應 衛生福利部國民健康署 我 名字 為了 以下理由 1. 2. 3. 4. 5. 決定從 年 月 日起 簽署人 (簽章) 見證人 (簽章) 年 月 日 a 準備戒 V 環境的準備 排除讓自己想吸 自己戒 的環境 V 心理的準備 瞭解自己的吸 的環境 建立能提醒 行為 強化戒 決心 V 身體的準備 評估身體的尼古丁依賴度 必要時找尋 藥物降低戒 戒 的難度
本計劃經費來自 品健康福利捐支應 衛生福利部國民健康署 我 名字 為了 以下理由 1. 2. 3. 4. 5. 決定從 年 月 日起 簽署人 (簽章) 見證人 (簽章) 年 月 日 a 準備戒 V 環境的準備 排除讓自己想吸 自己戒 的環境 V 心理的準備 瞭解自己的吸 的環境 建立能提醒 行為 強化戒 決心 V 身體的準備 評估身體的尼古丁依賴度 必要時找尋 藥物降低戒 戒 的難度
1 500 表 1: 各國平均分數
 2012 年多益測驗全球考生資料統計報告 A < 1> 2012 B < 2> 100% 500 2012 2012 / 21 25 (38%) 57% (58%) 25% / 20% 35% 53% 31% 17% / 31% 12% 6 45 1-10% 81% 6 2012 48 3 30% 1 編註 1: 請見 P.15 編註 2: 請見 P.17 1 500 表 1: 各國平均分數 466
2012 年多益測驗全球考生資料統計報告 A < 1> 2012 B < 2> 100% 500 2012 2012 / 21 25 (38%) 57% (58%) 25% / 20% 35% 53% 31% 17% / 31% 12% 6 45 1-10% 81% 6 2012 48 3 30% 1 編註 1: 請見 P.15 編註 2: 請見 P.17 1 500 表 1: 各國平均分數 466
 46 2011 11 467 數位遊戲式學習系統 7 2011 11 467 47 3 DBGameSys 48 2011 11 467 正規化資料模組 如何配置並儲存電子化資料 以 便減少資料被重覆儲存的程序 DBGameSys的主要功能模組包 學習者 審核評分模組 含 正規化資料模組 審核評分 模組 高分列表模組3大區塊 系統資料庫 在正規化資料模組的執行 高分列表模組 過程中 先要求學習者瀏覽遊戲
46 2011 11 467 數位遊戲式學習系統 7 2011 11 467 47 3 DBGameSys 48 2011 11 467 正規化資料模組 如何配置並儲存電子化資料 以 便減少資料被重覆儲存的程序 DBGameSys的主要功能模組包 學習者 審核評分模組 含 正規化資料模組 審核評分 模組 高分列表模組3大區塊 系統資料庫 在正規化資料模組的執行 高分列表模組 過程中 先要求學習者瀏覽遊戲
Microsoft PowerPoint - 9807關節炎用藥衛教及溝通技巧_1.ppt [相容模式]
![Microsoft PowerPoint - 9807關節炎用藥衛教及溝通技巧_1.ppt [相容模式] Microsoft PowerPoint - 9807關節炎用藥衛教及溝通技巧_1.ppt [相容模式]](/thumbs/42/22826474.jpg) 關 節 炎 用 藥 衛 教 與 溝 通 技 巧 三 軍 總 醫 院 臨 床 藥 學 部 黃 志 偉 藥 師 授 課 大 綱 什 麼 是 關 節 炎? 骨 關 節 炎 介 紹 類 風 濕 性 關 節 炎 介 紹 Q & A 2 關 節 炎 的 定 義 關 節 炎 : 關 節 發 炎 關 節 炎 其 實 是 指 100 多 種 造 成 關 節 和 結 締 組 織 問 題 的 疾 病, 其 症 狀 有 :
關 節 炎 用 藥 衛 教 與 溝 通 技 巧 三 軍 總 醫 院 臨 床 藥 學 部 黃 志 偉 藥 師 授 課 大 綱 什 麼 是 關 節 炎? 骨 關 節 炎 介 紹 類 風 濕 性 關 節 炎 介 紹 Q & A 2 關 節 炎 的 定 義 關 節 炎 : 關 節 發 炎 關 節 炎 其 實 是 指 100 多 種 造 成 關 節 和 結 締 組 織 問 題 的 疾 病, 其 症 狀 有 :
Microsoft Word - 文件1
 染牛隻的臨床症狀狀包括情緒不安 敏感 有攻擊性 磨牙 動作失調 後肢無力 躺臥死亡等症狀狀, 死亡後病理解剖, 會發現其腦部組織出 現空洞, 呈現海綿狀狀病變 被製成肉骨粉, 且掺入飼料中餵養牛隻, 因而使牛隻有受到感染的機 會 根據流行行病學調查研究顯示, 牛海綿狀狀腦病不會透過空氣傳播, 也不會因牛與牛之間的直接或間接接觸 ( 經口 鼻 交配 ) 而平行行感 切實檢驗食品安全
染牛隻的臨床症狀狀包括情緒不安 敏感 有攻擊性 磨牙 動作失調 後肢無力 躺臥死亡等症狀狀, 死亡後病理解剖, 會發現其腦部組織出 現空洞, 呈現海綿狀狀病變 被製成肉骨粉, 且掺入飼料中餵養牛隻, 因而使牛隻有受到感染的機 會 根據流行行病學調查研究顯示, 牛海綿狀狀腦病不會透過空氣傳播, 也不會因牛與牛之間的直接或間接接觸 ( 經口 鼻 交配 ) 而平行行感 切實檢驗食品安全
 第一篇文概說第七章公文的用語及標點符號公本篇內容 第一章 緒論 第二章 公文的意義 第三章 公文與高 普 特各類考試 第四章 公文程式之意義及演變 第五章 公文之分類及其行文系統 第六章 公文之結構與行款 第一篇 第一章緒論 003 第一章緒論 等 等 004 最新應用公文 第一篇 第二章公文的意義 005 第二章公文的意義 第一節 一 須為公務員製作之文書 二 須為公務員 職務上 製作之文書 006
第一篇文概說第七章公文的用語及標點符號公本篇內容 第一章 緒論 第二章 公文的意義 第三章 公文與高 普 特各類考試 第四章 公文程式之意義及演變 第五章 公文之分類及其行文系統 第六章 公文之結構與行款 第一篇 第一章緒論 003 第一章緒論 等 等 004 最新應用公文 第一篇 第二章公文的意義 005 第二章公文的意義 第一節 一 須為公務員製作之文書 二 須為公務員 職務上 製作之文書 006
 2014 : 706 2 3 4 5 6 12 15 簡明綜合損益及其他全面收入報表 截至二零一四年六月三十日止六個月 二零一三年 3 3,796 4,738 3,796 4,738 4 1,983 1,837 (27,319) (26,934) (21,540) (20,359) 5 (64) (92) (21,604) (20,451) 6 159 196 期 7 (21,445) (20,255)
2014 : 706 2 3 4 5 6 12 15 簡明綜合損益及其他全面收入報表 截至二零一四年六月三十日止六個月 二零一三年 3 3,796 4,738 3,796 4,738 4 1,983 1,837 (27,319) (26,934) (21,540) (20,359) 5 (64) (92) (21,604) (20,451) 6 159 196 期 7 (21,445) (20,255)
項次 名稱 ICD-9-CM ICD-10-CM 備註 1 全民健康保險思覺失調症醫療給付改善方案 295 F20 全民健康保險思覺失調症醫療給付改善方案 295 F25 全民健康保險思覺失調症醫療給付改善方案 S00-T88 全民健康保險思覺失調症醫療給付改善方案 E-CODE V
 1 全民健康保險思覺失調症醫療給付改善方案 295 F20 全民健康保險思覺失調症醫療給付改善方案 295 F25 全民健康保險思覺失調症醫療給付改善方案 800-999 S00-T88 全民健康保險思覺失調症醫療給付改善方案 E-CODE V00-Y99 2 全民健康保險腦血管疾病西醫住院病患中醫輔助醫療試辦計畫 430-437 G450-G468 全民健康保險腦血管疾病西醫住院病患中醫輔助醫療試辦計畫
1 全民健康保險思覺失調症醫療給付改善方案 295 F20 全民健康保險思覺失調症醫療給付改善方案 295 F25 全民健康保險思覺失調症醫療給付改善方案 800-999 S00-T88 全民健康保險思覺失調症醫療給付改善方案 E-CODE V00-Y99 2 全民健康保險腦血管疾病西醫住院病患中醫輔助醫療試辦計畫 430-437 G450-G468 全民健康保險腦血管疾病西醫住院病患中醫輔助醫療試辦計畫
治療血管的雷射 port wine stain 1988 FDA KTP KTP
 您選對雷射了嗎 40 1917 1959 Maiman 1963 20 1983 AndersonParrish 22 2013 5 485 以往須以手術 磨皮等方法才能去除的刺青, 現在用雷射就可以輕易處理 此外, 各種皮膚血管病變 痣 疤痕, 乃至於皺紋的去除, 也可以用雷射來達成 治療血管的雷射 port wine stain 1988 FDA 585 590 595 600 1.5 40 4
您選對雷射了嗎 40 1917 1959 Maiman 1963 20 1983 AndersonParrish 22 2013 5 485 以往須以手術 磨皮等方法才能去除的刺青, 現在用雷射就可以輕易處理 此外, 各種皮膚血管病變 痣 疤痕, 乃至於皺紋的去除, 也可以用雷射來達成 治療血管的雷射 port wine stain 1988 FDA 585 590 595 600 1.5 40 4
GEM GEM GEM GEMGEM GEM GEMGEM
 GEM GEM GEM GEMGEM GEM GEMGEM 3 4 5 8 9 11 19 35 46 55 58 59 61 63 65 129 130 曉 曉 Conyers Corporate Services (Bermuda) Limited Clarendon House 2 Church Street Hamilton HM 11 Bermuda 183 22 Clarendon House
GEM GEM GEM GEMGEM GEM GEMGEM 3 4 5 8 9 11 19 35 46 55 58 59 61 63 65 129 130 曉 曉 Conyers Corporate Services (Bermuda) Limited Clarendon House 2 Church Street Hamilton HM 11 Bermuda 183 22 Clarendon House
10 中央銀行季刊第三十一卷第一期民國 98 年 3 月 0.84% 1.73% 25.6% GDP 1.52% 0.44% 29.37% 0.90% 2.18% (4) a b c d e f 壹 前言 2004 (WTI) % 200
 能源價格波動對國內物價與經濟活動的影響 9 * 能源價格波動對國內物價與經濟活動的影響 ** 梁啟源 摘 要 (1) (2) (1) 2004~2008 a b c d (2) OPEC 2008 30 30~80 (3) 13% GDP 0.88% 0.34% 12.42% * ** 10 中央銀行季刊第三十一卷第一期民國 98 年 3 月 0.84% 1.73% 25.6% GDP 1.52%
能源價格波動對國內物價與經濟活動的影響 9 * 能源價格波動對國內物價與經濟活動的影響 ** 梁啟源 摘 要 (1) (2) (1) 2004~2008 a b c d (2) OPEC 2008 30 30~80 (3) 13% GDP 0.88% 0.34% 12.42% * ** 10 中央銀行季刊第三十一卷第一期民國 98 年 3 月 0.84% 1.73% 25.6% GDP 1.52%
老人 社 交 活 動 McAuley et al., 2000 Glass 1999 Mendes de Leon ~2 1~ % 10.56% 9.23% 6.05% 24.72% 14.18% 12.12% 影響老人社交活動的因素一 生理功能的改變 Bar
 社交活動對老人的影響 文 / 張麗芳 RN, 新樓醫院護理部督導, 導輔英科技大學護理系研究所進修中 前言 7 28 1993 7 2007 10 65 233 133 10.16 57.6 95 2.4 2005 65 29.52% 65.20% 55.16% Mendes de Leon Glass Berkman 2002 34.1% 43.2% 2005 社交活動的概念一 社交活動的定義 social
社交活動對老人的影響 文 / 張麗芳 RN, 新樓醫院護理部督導, 導輔英科技大學護理系研究所進修中 前言 7 28 1993 7 2007 10 65 233 133 10.16 57.6 95 2.4 2005 65 29.52% 65.20% 55.16% Mendes de Leon Glass Berkman 2002 34.1% 43.2% 2005 社交活動的概念一 社交活動的定義 social
 2 3 13 17 22 26 1 2 8 100738 +86 (10) 8508 5000 +86 (10) 8518 5111 www.kpmg.com.cn 2006 4 2002 2006 1 28% 2006 17 8 500 2006 2006 2006 7 2.5 2 1 500 500 40% 500 10 16 14 12 10 8 6 4 2 2002-2006 5.1 5.9
2 3 13 17 22 26 1 2 8 100738 +86 (10) 8508 5000 +86 (10) 8518 5111 www.kpmg.com.cn 2006 4 2002 2006 1 28% 2006 17 8 500 2006 2006 2006 7 2.5 2 1 500 500 40% 500 10 16 14 12 10 8 6 4 2 2002-2006 5.1 5.9
Microsoft Word - ACI chapter00-1ed.docx
 前言 Excel Excel - v - 財務管理與投資分析 -Excel 建模活用範例集 5 相關 平衡 敏感 - vi - 前言 模擬 If-Then 規劃 ERP BI - vii - 財務管理與投資分析 -Excel 建模活用範例集 ERP + BI + ERP BI Excel 88 Excel 1. Excel Excel 2. Excel 3. Excel - viii - 前言 1.
前言 Excel Excel - v - 財務管理與投資分析 -Excel 建模活用範例集 5 相關 平衡 敏感 - vi - 前言 模擬 If-Then 規劃 ERP BI - vii - 財務管理與投資分析 -Excel 建模活用範例集 ERP + BI + ERP BI Excel 88 Excel 1. Excel Excel 2. Excel 3. Excel - viii - 前言 1.
SW cdr
 1~2 3 4 5~6 7~8 9~10 11 12 13 14 15 16~18 16 16 17 17 18 18 18 19 19 19 20 21 22 23~26 23 24 24 25 26 27 27 27 : 110V 1 110V 110V 15A 2 3 23 24 4 ( ) 5 6 1 2 26 20 l 1 7 3 4 5 15 17 18 12 7~13 6 ~ 8 ~
1~2 3 4 5~6 7~8 9~10 11 12 13 14 15 16~18 16 16 17 17 18 18 18 19 19 19 20 21 22 23~26 23 24 24 25 26 27 27 27 : 110V 1 110V 110V 15A 2 3 23 24 4 ( ) 5 6 1 2 26 20 l 1 7 3 4 5 15 17 18 12 7~13 6 ~ 8 ~
台資企業在中國大陸的發展 – 十二五規劃的展望
 & CRETA 財團法人商業發展研究院 2011 10 5 ( & ) 2011.10.05 2 1. ( & ) 2011.10.05 3 GDP 1981-2010 13 ( & ) 2011.10.05 4 GDP ( & ) 2011.10.05 5 ( & ) 2011.10.05 6 GDP 1981-2010 GDP GDP 100% ( & ) 2011.10.05 7 ( & )
& CRETA 財團法人商業發展研究院 2011 10 5 ( & ) 2011.10.05 2 1. ( & ) 2011.10.05 3 GDP 1981-2010 13 ( & ) 2011.10.05 4 GDP ( & ) 2011.10.05 5 ( & ) 2011.10.05 6 GDP 1981-2010 GDP GDP 100% ( & ) 2011.10.05 7 ( & )
....V....VII.... VIII
 ....V....VII.... VIII................................. 002... 002... 004... 006... 012... 014... 019.... 022.... 023................................. 026... 026... 027... 039 XIII...043... 043... 045....
....V....VII.... VIII................................. 002... 002... 004... 006... 012... 014... 019.... 022.... 023................................. 026... 026... 027... 039 XIII...043... 043... 045....
Chapter 3 Camera Raw Step negative clarity +25 ] P / Step 4 0 ( 下一頁 ) Camera Raw Chapter 3 089
![Chapter 3 Camera Raw Step negative clarity +25 ] P / Step 4 0 ( 下一頁 ) Camera Raw Chapter 3 089 Chapter 3 Camera Raw Step negative clarity +25 ] P / Step 4 0 ( 下一頁 ) Camera Raw Chapter 3 089](/thumbs/50/27027900.jpg) Photoshop CC Camera Raw Photoshop Camera Raw Step 1 3 1 2 3 SCOTT KELBY Step 2 B Camera Raw 088 Chapter 3 Camera Raw Chapter 3 Camera Raw Step 3-4 -100 negative clarity +25 ] P / -75-50 Step 4 0 ( 下一頁
Photoshop CC Camera Raw Photoshop Camera Raw Step 1 3 1 2 3 SCOTT KELBY Step 2 B Camera Raw 088 Chapter 3 Camera Raw Chapter 3 Camera Raw Step 3-4 -100 negative clarity +25 ] P / -75-50 Step 4 0 ( 下一頁
目錄
 2013 年度 企業社會責任報告 目錄 1 4 2 5 3 6 3.1 6 3.2 7 3.3 7 4 8 4.1 8 4.2 2013 9 4.3 10 5 15 5.1 15 5.2 16 5.3 18 6 19 6.1 19 6.2 20 6.3 21 6.4 22 6.5 23 6.6 24 6.7 24 6.8 24 7 25 7.1 25 7.2 26 7.3 27 7.4 27 7.5
2013 年度 企業社會責任報告 目錄 1 4 2 5 3 6 3.1 6 3.2 7 3.3 7 4 8 4.1 8 4.2 2013 9 4.3 10 5 15 5.1 15 5.2 16 5.3 18 6 19 6.1 19 6.2 20 6.3 21 6.4 22 6.5 23 6.6 24 6.7 24 6.8 24 7 25 7.1 25 7.2 26 7.3 27 7.4 27 7.5
( ) (1) (2) (3) (4) 2
 2007 11 29 1. ( ) 2. ( ) 3. 1 ( ) 1. 2. (1) (2) (3) (4) 2 1. (1) (2) 2. ( ) $20,000,000 X1 1 1 $3,000,000 X1 1 1 1,000,000 $12,000,000 $4,000,000 $5,000,000 $10 X1 1 1 $13 (1) ( ) $5,000,000 $8,000,000
2007 11 29 1. ( ) 2. ( ) 3. 1 ( ) 1. 2. (1) (2) (3) (4) 2 1. (1) (2) 2. ( ) $20,000,000 X1 1 1 $3,000,000 X1 1 1 1,000,000 $12,000,000 $4,000,000 $5,000,000 $10 X1 1 1 $13 (1) ( ) $5,000,000 $8,000,000
< B4C1A55AA5D8BFFD2E786C73>
 AACN:Nursing scan in critical v.5:no.1-6 Jan-Dec 護理學 Advances In Anatomic Pathology v.1:1-2:4 - 解剖病理科 v.3:1-6:6 1996-1999 Adverse drug reactiions & v.16:1-21:4 1997 Mar-2002 藥劑科 toxicological reviews Dec
AACN:Nursing scan in critical v.5:no.1-6 Jan-Dec 護理學 Advances In Anatomic Pathology v.1:1-2:4 - 解剖病理科 v.3:1-6:6 1996-1999 Adverse drug reactiions & v.16:1-21:4 1997 Mar-2002 藥劑科 toxicological reviews Dec
(A)3 4 (B)5 6 (C)7 9 (D)10 2 (E) (A) (B) (C) (D) (E) ( ) ( ) ( ) (A) (B) (C) (D) (E) (A) (B) (C) (D) (E). (A) (B) (C) (D) (E). (A) (B) (C) (D) (
 . (A) (B) (C) (D) (E). (A) (B) (C) (D) (E) (A) (B) (C) (D) (E) (A) (B) (C) (D) (E).. (E) (A) (B) (C) (D). (A) (B) (C) (D) (E). (A) (B) (C) (D) (E). (A) (B) (C) (D) (E) (A) (C) (D) (E) (A) (B) (C) (D) (E)
. (A) (B) (C) (D) (E). (A) (B) (C) (D) (E) (A) (B) (C) (D) (E) (A) (B) (C) (D) (E).. (E) (A) (B) (C) (D). (A) (B) (C) (D) (E). (A) (B) (C) (D) (E). (A) (B) (C) (D) (E) (A) (C) (D) (E) (A) (B) (C) (D) (E)
Microsoft Word - ch02
 附錄二 相關身心障礙類別 ICD-9-CM 與對應之 ICD-10-CM 障 國際疾病編碼 礙類別 ICD-9-CM ICD-10-CM F20.0 Paranoid schizophrenia 妄想型思覺失調症 ' 性精神病患者 295 295.* 295.** 296 296.* 296.** 297 297.* 298 298.* F20.1 Disorganized schizophrenia
附錄二 相關身心障礙類別 ICD-9-CM 與對應之 ICD-10-CM 障 國際疾病編碼 礙類別 ICD-9-CM ICD-10-CM F20.0 Paranoid schizophrenia 妄想型思覺失調症 ' 性精神病患者 295 295.* 295.** 296 296.* 296.** 297 297.* 298 298.* F20.1 Disorganized schizophrenia
簡 介 第 1 節 關 於 ALIGNMENT HEALTH PLAN CALPLUS (HMO) 的 重 要 資 訊 10 1 2 14 8 8 7 2 15 9 30 8 8 1-866-634-2247711 1-888-979-2247711
 2017 福利摘要 009 加州 洛杉磯縣 橘縣 河濱縣 聖伯納迪諾縣 聖華金縣 聖塔克拉拉縣及 斯坦尼斯勞斯縣 Alignment Health Plan 是一項簽有 Medicare 合約的 HMO 計劃 能否在 Alignment Health Plan 註冊參保視合約續簽情況而定 本手冊概述了本計劃的承保範圍及您需要支付的費用 本文件並未羅列出我們承保的所有服務 亦未列舉所有限制或不保項目
2017 福利摘要 009 加州 洛杉磯縣 橘縣 河濱縣 聖伯納迪諾縣 聖華金縣 聖塔克拉拉縣及 斯坦尼斯勞斯縣 Alignment Health Plan 是一項簽有 Medicare 合約的 HMO 計劃 能否在 Alignment Health Plan 註冊參保視合約續簽情況而定 本手冊概述了本計劃的承保範圍及您需要支付的費用 本文件並未羅列出我們承保的所有服務 亦未列舉所有限制或不保項目
衛教專欄 子宮頸癌診斷與治療 邱婉昀藥師撰稿李典錕醫師審閱 一. 簡介與現況子宮頸癌的發生率一直是台灣女性癌症的第一名 根據 2000 年衛生署年度癌症報告, 台灣每十萬名女性, 就有 53.8 名發生在子宮頸癌以及子宮頸原位癌 子宮頸癌, 就是由子宮所長出的癌症 在人體子宮頸的細胞可能因長期受到刺
 台中慈濟藥訊 The Buddhist Tzuchi Taichung General Hospital Drug Bulletin Vol. 04. No. 01 發行人 簡守信 總編輯 陳綺華 執行編輯 臨床藥學組 電 話 04 36060666-4029 傳 真 04 25362258 2013 年02 月號 雙月刊 目 錄 衛教專欄 子宮頸癌診斷與治療...p.02 衛教專欄 胃輕癱的診斷與治療...p.06
台中慈濟藥訊 The Buddhist Tzuchi Taichung General Hospital Drug Bulletin Vol. 04. No. 01 發行人 簡守信 總編輯 陳綺華 執行編輯 臨床藥學組 電 話 04 36060666-4029 傳 真 04 25362258 2013 年02 月號 雙月刊 目 錄 衛教專欄 子宮頸癌診斷與治療...p.02 衛教專欄 胃輕癱的診斷與治療...p.06
貳 肆 公司治理報告 一 組織系統 ( 一 ) 組織結構 ( 二 ) 組織系統圖 14 中華民國 98 年中華郵政年報
 14 16 24 30 24 25 26 26 27 27 28 29 29 一 組織系統二 董事 監察人 總經理 副總經理 各部門及分支機構主管資料三 公司治理運作情形 ( 一 ) 董事會運作情形 ( 二 ) 公司治理運作情形及其與上市上櫃公司治理實務守則差異情形及原因 ( 三 ) 揭露公司治理守則及相關規章之查詢方式 ( 四 ) 揭露其他足以增進對公司治理運作情形瞭解之重要資訊 ( 五 ) 內部控制制度執行狀況
14 16 24 30 24 25 26 26 27 27 28 29 29 一 組織系統二 董事 監察人 總經理 副總經理 各部門及分支機構主管資料三 公司治理運作情形 ( 一 ) 董事會運作情形 ( 二 ) 公司治理運作情形及其與上市上櫃公司治理實務守則差異情形及原因 ( 三 ) 揭露公司治理守則及相關規章之查詢方式 ( 四 ) 揭露其他足以增進對公司治理運作情形瞭解之重要資訊 ( 五 ) 內部控制制度執行狀況
100 年華僑經濟年鑑 2011 華僑經濟年鑑 IT % % % % % WEF
 壹 總論 五 美洲地區經濟總論 ( 一 ) 美洲地區總體經濟情勢分析與展望 North American Free Trade Agreement, NAFTA CUSFTA IMD DR-CAFTA - U.S.-CAFTA-DRFTAALADI 2011 2011 WEF 2011 1 5 2012 1 2011 9.0% 3.5% 2011 3.2% 2010 1.6% 2011 WEF 10
壹 總論 五 美洲地區經濟總論 ( 一 ) 美洲地區總體經濟情勢分析與展望 North American Free Trade Agreement, NAFTA CUSFTA IMD DR-CAFTA - U.S.-CAFTA-DRFTAALADI 2011 2011 WEF 2011 1 5 2012 1 2011 9.0% 3.5% 2011 3.2% 2010 1.6% 2011 WEF 10
財團法人醫藥品查驗中心 Center For Drug Evaluation 試驗 A2303 (GLOW-2) 為一項為期 52 周之隨機分派 雙盲 安慰劑對照 tiotropium 公開標籤 平行分組的第三期臨床試驗, 用以評估 glycopyrronium bromide 在治療年齡大於等於
 財團法人醫藥品查驗中心 Center For Drug Evaluation 吸補力吸入膠囊 50 微克 (Seebri Breezhaler 50μg Inhalation Power, hard capsules) 醫療科技評估報告 藥物納入全民健康保險給付建議書 - 藥品專用 資料摘要 藥品名稱吸補力吸入膠囊 50 微克成分 Glycopyrronium bromide 建議者 藥品許可證持有商
財團法人醫藥品查驗中心 Center For Drug Evaluation 吸補力吸入膠囊 50 微克 (Seebri Breezhaler 50μg Inhalation Power, hard capsules) 醫療科技評估報告 藥物納入全民健康保險給付建議書 - 藥品專用 資料摘要 藥品名稱吸補力吸入膠囊 50 微克成分 Glycopyrronium bromide 建議者 藥品許可證持有商
2874_Product Brochure_630mm(w)x285mm(h)_Health_Chi_02_WEB
 CHINA TAIPING LIFE INSURANCE(HONG KONG)COMPANY LIMITED 太平安康危疾終身保計劃概覽 公司簡介 與我們聯絡取得更多資料 周全的保障, 全面涵蓋 142 項危疾 1, 包括 76 項早期危疾預支賠償病況 早期危疾預支賠償 4, 能讓您有充足的經濟支援, 接受優質治療 有 6 項供款年期選擇 2, 3 除人壽及危疾保障外, 更享有靈活運用保單儲備 可享有期滿紅利
CHINA TAIPING LIFE INSURANCE(HONG KONG)COMPANY LIMITED 太平安康危疾終身保計劃概覽 公司簡介 與我們聯絡取得更多資料 周全的保障, 全面涵蓋 142 項危疾 1, 包括 76 項早期危疾預支賠償病況 早期危疾預支賠償 4, 能讓您有充足的經濟支援, 接受優質治療 有 6 項供款年期選擇 2, 3 除人壽及危疾保障外, 更享有靈活運用保單儲備 可享有期滿紅利
38 嬰兒猝死症候群 (SIDS) 急性支氣管炎及急性細支 其他 9, 臺灣地區 總計 0 歲 死亡數 名 原因 Number Crude 名 原因 Number of Deaths Death Rate of Deaths 所有死亡原因 64,
 臺灣地區 總計 0 歲 死亡數 名 原因 Number Crude 名 原因 Number of Deaths Death Rate of Deaths 所有死亡原因 97,979 838.0 所有死亡原因 446 1 惡性腫瘤 28,476 243.6 1 源於周產期的特定病況 195 2 心臟疾病 ( 高血壓性疾病 11,484 98.2 2 先天性畸形變形及染色體 99 3 腦血管疾病 6,980
臺灣地區 總計 0 歲 死亡數 名 原因 Number Crude 名 原因 Number of Deaths Death Rate of Deaths 所有死亡原因 97,979 838.0 所有死亡原因 446 1 惡性腫瘤 28,476 243.6 1 源於周產期的特定病況 195 2 心臟疾病 ( 高血壓性疾病 11,484 98.2 2 先天性畸形變形及染色體 99 3 腦血管疾病 6,980
untitled
 Taipei Medical University Municipal Wanfang Hospital EBM Center 料 路 http://www.wanfang.gov.tw/ebm/ 2005/11/10 聯 Taipei Medical University Municipal Wanfang Hospital EBM Center Learning map Question formation
Taipei Medical University Municipal Wanfang Hospital EBM Center 料 路 http://www.wanfang.gov.tw/ebm/ 2005/11/10 聯 Taipei Medical University Municipal Wanfang Hospital EBM Center Learning map Question formation
 Special Issue 名 人 講 堂 專 題 研 究 保證金收取 合格之擔保品種類為何 非現金擔保品之折扣率 haircut 為何 CCP是否將會員所繳擔保品用於投資 其孳息是否回饋給會員 限制措施 焦 點 視 界 是否對會員之委託金額 信用 部位及風險訂定限額 會員是否必須對其客戶制定限額 洗價 mark-to-market 之時間及方法為何 結算交割 市 場 掃 描 交割週期 T+1或T+3
Special Issue 名 人 講 堂 專 題 研 究 保證金收取 合格之擔保品種類為何 非現金擔保品之折扣率 haircut 為何 CCP是否將會員所繳擔保品用於投資 其孳息是否回饋給會員 限制措施 焦 點 視 界 是否對會員之委託金額 信用 部位及風險訂定限額 會員是否必須對其客戶制定限額 洗價 mark-to-market 之時間及方法為何 結算交割 市 場 掃 描 交割週期 T+1或T+3
Middle East Respiratory Syndrome Coronavirus, MERS-CoV WHO Qatar 2013 MERS MERS 耗費巨大的社會成本 MERS V
 54 2015 1 505 新興的中東呼吸症候群 冠狀病毒 Those who cannot remember the past are condemned to repeat it. 忘記過去的人, 注定要重蹈覆轍 2012 4 Zarqa 13 2 2012 9 WHO Middle East Respiratory Syndrome Coronavirus, MERS 11 MERS 9 2
54 2015 1 505 新興的中東呼吸症候群 冠狀病毒 Those who cannot remember the past are condemned to repeat it. 忘記過去的人, 注定要重蹈覆轍 2012 4 Zarqa 13 2 2012 9 WHO Middle East Respiratory Syndrome Coronavirus, MERS 11 MERS 9 2
全民健康保險藥事小組第6屆第20次會議紀錄
 全 民 健 康 保 險 藥 事 小 組 第 8 屆 第 18 次 (99 年 9 月 ) 會 議 紀 錄 時 間 :99 年 9 月 2 日 及 9 月 9 日 上 午 9 時 15 分 地 點 : 中 央 健 康 保 險 局 9 樓 第 1 會 議 室 出 席 人 員 : 如 會 議 簽 到 單 主 席 : 陳 召 集 人 燕 惠 壹 主 席 致 詞 ( 略 ) 貳 上 次 會 議 紀 錄 確 認
全 民 健 康 保 險 藥 事 小 組 第 8 屆 第 18 次 (99 年 9 月 ) 會 議 紀 錄 時 間 :99 年 9 月 2 日 及 9 月 9 日 上 午 9 時 15 分 地 點 : 中 央 健 康 保 險 局 9 樓 第 1 會 議 室 出 席 人 員 : 如 會 議 簽 到 單 主 席 : 陳 召 集 人 燕 惠 壹 主 席 致 詞 ( 略 ) 貳 上 次 會 議 紀 錄 確 認
Microsoft PowerPoint - 20090926-臨床護理指引(台南護專).ppt [相容模式]
![Microsoft PowerPoint - 20090926-臨床護理指引(台南護專).ppt [相容模式] Microsoft PowerPoint - 20090926-臨床護理指引(台南護專).ppt [相容模式]](/thumbs/41/22341989.jpg) 臨 床 護 理 指 引 的 發 展 Clinical Practice Guidelines (CPG) 臺 北 醫 學 大 學 萬 芳 醫 院 護 理 部 陳 可 欣 督 導 長 2009.09.26. 實 證 護 理 五 大 步 驟 萬 芳 醫 院 實 證 護 理 推 展 歷 程 簡 圖 循 序 漸 進 多 元 進 行 原 則 全 面 深 耕 期 實 證 護 理 習 慣 化 初 步 接 觸 期
臨 床 護 理 指 引 的 發 展 Clinical Practice Guidelines (CPG) 臺 北 醫 學 大 學 萬 芳 醫 院 護 理 部 陳 可 欣 督 導 長 2009.09.26. 實 證 護 理 五 大 步 驟 萬 芳 醫 院 實 證 護 理 推 展 歷 程 簡 圖 循 序 漸 進 多 元 進 行 原 則 全 面 深 耕 期 實 證 護 理 習 慣 化 初 步 接 觸 期
2 (a 1 6. (b 7. (c 8. (d 9. (e (a
 CB(1 907/02-03(05 立法會財經事務委員會 破產管理署角色檢討顧問研究 目的 背景 2. / 3. (CB(1 2152/01-02(06 ( A 24 B 公眾諮詢所得結果 4. C 5. / 2 (a 1 6. (b 7. (c 8. (d 9. (e 2 10. (a 11. 1 20 2 3 (b ( 12. (c 13. (d 14. (a 15. (b / 16. (c (
CB(1 907/02-03(05 立法會財經事務委員會 破產管理署角色檢討顧問研究 目的 背景 2. / 3. (CB(1 2152/01-02(06 ( A 24 B 公眾諮詢所得結果 4. C 5. / 2 (a 1 6. (b 7. (c 8. (d 9. (e 2 10. (a 11. 1 20 2 3 (b ( 12. (c 13. (d 14. (a 15. (b / 16. (c (
 - ( 青少年篇 ) ( ) 40043 32 12 10 (04)2229-1661 40043 32 12 11 (04) 2229-5550 (04) 2229-5607 10041 2 2 203 (02) 2371-1406 (02) 2371-1478 [email protected] www.lourdes.org.tw 2015 9 2 台灣露德協會 6 8 9 12 16
- ( 青少年篇 ) ( ) 40043 32 12 10 (04)2229-1661 40043 32 12 11 (04) 2229-5550 (04) 2229-5607 10041 2 2 203 (02) 2371-1406 (02) 2371-1478 [email protected] www.lourdes.org.tw 2015 9 2 台灣露德協會 6 8 9 12 16
本月專題 科學新聞判讀力 Article.aspx?a= 目前並沒有充足證據證明基改作物會讓人生病或危害環境 109 Greenpeace https://www.you
 / 嚇死我了 這些究竟能不能吃?/ 嚇死我了 這些究竟能不能吃? 文 / 李暉 食安與媒體 2010 73 14 科學研習 OCT 2016 No.55-10 本月專題 科學新聞判讀力 1 2 2014 3 53-3 http://www.ntsec.gov.tw/user/ Article.aspx?a=2657 2016 5 目前並沒有充足證據證明基改作物會讓人生病或危害環境 109 Greenpeace
/ 嚇死我了 這些究竟能不能吃?/ 嚇死我了 這些究竟能不能吃? 文 / 李暉 食安與媒體 2010 73 14 科學研習 OCT 2016 No.55-10 本月專題 科學新聞判讀力 1 2 2014 3 53-3 http://www.ntsec.gov.tw/user/ Article.aspx?a=2657 2016 5 目前並沒有充足證據證明基改作物會讓人生病或危害環境 109 Greenpeace
Ferriman-Gallwey 資料來源 : 參考資料 ) testosterone 150 ng/dl (5.2 nmol/ L) free testosterone2 ng/dl (0.07 nmol/l) DHEA-S700 mcg/dl (13.6 µmol/l
 家庭醫業 前言及定義 病態生理學 F e r r i m a n - G a l l w e y hirsutism scoring system 9 04 Ferriman-Gallwey score8 (hirsutism) hypertrichosis hypertrichosis hirsutism androgen t e s t o s t e r o n e d i h y d r o
家庭醫業 前言及定義 病態生理學 F e r r i m a n - G a l l w e y hirsutism scoring system 9 04 Ferriman-Gallwey score8 (hirsutism) hypertrichosis hypertrichosis hirsutism androgen t e s t o s t e r o n e d i h y d r o
人為疏失 人與人之間的溝通合作, 往往是事故的最終防線, 若能發揮團隊合作的功能, 則比較能克服其他因素所造成的危害
 人為因素與 飛航安全 人為因素 7 7 8 人為因素的類別 H 1972 E. Edward SHELL S S L E software, H handware, E environment, L liveware L SHELL 20 2014 3 495 人為疏失 人與人之間的溝通合作, 往往是事故的最終防線, 若能發揮團隊合作的功能, 則比較能克服其他因素所造成的危害 2014 3 495
人為因素與 飛航安全 人為因素 7 7 8 人為因素的類別 H 1972 E. Edward SHELL S S L E software, H handware, E environment, L liveware L SHELL 20 2014 3 495 人為疏失 人與人之間的溝通合作, 往往是事故的最終防線, 若能發揮團隊合作的功能, 則比較能克服其他因素所造成的危害 2014 3 495
低功率電波輻射性電機管理辦法 第十二條經型式認證合格之低功率射頻電機, 非經許可, 公司 商號或使用者均不得擅自變更頻率 加大功率或變更原設計之特性及功能 第十四條低功率射頻電機之使用不得影響飛航安全及干擾合法通訊 ; 經發現有干擾現象時, 應立即停用, 並改善至無干擾時方得繼續使用 前項合法通訊,
 使用說明書 TMAX 機車 在騎乘機車之前, 請務必仔細閱讀這本使用說明書 XP00 XP00A PW--T 低功率電波輻射性電機管理辦法 第十二條經型式認證合格之低功率射頻電機, 非經許可, 公司 商號或使用者均不得擅自變更頻率 加大功率或變更原設計之特性及功能 第十四條低功率射頻電機之使用不得影響飛航安全及干擾合法通訊 ; 經發現有干擾現象時, 應立即停用, 並改善至無干擾時方得繼續使用 前項合法通訊,
使用說明書 TMAX 機車 在騎乘機車之前, 請務必仔細閱讀這本使用說明書 XP00 XP00A PW--T 低功率電波輻射性電機管理辦法 第十二條經型式認證合格之低功率射頻電機, 非經許可, 公司 商號或使用者均不得擅自變更頻率 加大功率或變更原設計之特性及功能 第十四條低功率射頻電機之使用不得影響飛航安全及干擾合法通訊 ; 經發現有干擾現象時, 應立即停用, 並改善至無干擾時方得繼續使用 前項合法通訊,
完全照護手冊
 20 13.6 9.910 17.8 13.3 20 1996 () 1. 2. 1998 20012000 2014 0800-507272 5 55% 30.1% 16.9% 40.7% 25.3%13.2 72.5%30-6012.1% 3015.4%60 60.8%22.3% 45 2013 3700 37.4% 2-319.8%121 0800-507272 1421 11 5 70% 7
20 13.6 9.910 17.8 13.3 20 1996 () 1. 2. 1998 20012000 2014 0800-507272 5 55% 30.1% 16.9% 40.7% 25.3%13.2 72.5%30-6012.1% 3015.4%60 60.8%22.3% 45 2013 3700 37.4% 2-319.8%121 0800-507272 1421 11 5 70% 7
3 QE3 時 評 ~0.25% Quantitative Easing, QE FED QE 1 3 FED QE1 QE2 QE3 貳 美國推出 QE3 之動機意涵與過去 2 次 QE 措施之主要差異 FED QE MBS
 PROSPECT EXPLORATION 第 10 卷第 10 期中華民國 101 年 10 月 美國實施第 3 輪量化寬鬆 (QE3) 政策對全球經濟之影響 The Impact of the US s Implementation of Round III Quantitative Easing Policy on the Global Economy 聶建中 (Nieh, Chien-Chung)
PROSPECT EXPLORATION 第 10 卷第 10 期中華民國 101 年 10 月 美國實施第 3 輪量化寬鬆 (QE3) 政策對全球經濟之影響 The Impact of the US s Implementation of Round III Quantitative Easing Policy on the Global Economy 聶建中 (Nieh, Chien-Chung)
臺北市及死亡率 - 別 ( 續 1)( 修正 ) ( 二 ) 松山區 中華民國 105 年單 : 人 ; 人 / 十萬人 ;% 所有 1, 所有 所有 惡腫瘤 4
 臺北市及死亡率 - 別 ( 修正 ) ( 一 ) 臺北市 中華民國 105 年單 : 人 ; 人 / 十萬人 ;% 所有 18,039 668.05 33.75 100.00 所有 10,369 80.5 44.60 100.00 所有 7,670 544.83 55.48 100.00 1 惡腫瘤 5,19 193.8 105.00 8.93 惡腫瘤,90 5.9 17.78 8.16 惡腫瘤,99
臺北市及死亡率 - 別 ( 修正 ) ( 一 ) 臺北市 中華民國 105 年單 : 人 ; 人 / 十萬人 ;% 所有 18,039 668.05 33.75 100.00 所有 10,369 80.5 44.60 100.00 所有 7,670 544.83 55.48 100.00 1 惡腫瘤 5,19 193.8 105.00 8.93 惡腫瘤,90 5.9 17.78 8.16 惡腫瘤,99
ThemeGallery PowerTemplate
 L/O/G/O 癌症免疫療法 KRESTIN 杏昌醫藥科技股份有限公司 唯一醫藥級雲芝 Krestin (Polysaccharide K, PSK) 克速鎮 2 標竿臨床試驗參考期刊 : Gastric Cancer 臨床試驗 : 1. Efficacy of Immunochemotherapy as Adjuvant Treatment after Curative Resection of
L/O/G/O 癌症免疫療法 KRESTIN 杏昌醫藥科技股份有限公司 唯一醫藥級雲芝 Krestin (Polysaccharide K, PSK) 克速鎮 2 標竿臨床試驗參考期刊 : Gastric Cancer 臨床試驗 : 1. Efficacy of Immunochemotherapy as Adjuvant Treatment after Curative Resection of
乾癬與治療 手掌或腳底之掌蹠膿皰症 手指中段及腳底前端先出現有許多無菌 不易破的小膿皰, 附著厚厚痂皮 常見於中年女性,2 另, 罕見的 Hallopeau 氏肢皮炎, 是 圖二水滴狀乾癬 三 反轉型乾癬 (inverse psoriasis) 亦稱屈曲性乾癬 (flexural psoriasis
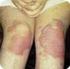 臨床藥學 Clinical Pharmacy 乾癬與治療 台北市立聯合醫院林森院區藥劑科藥師吳命選 台北市立聯合醫院藥劑部藥師陳怡靜 陳立奇 摘要乾癬是發生在皮膚組織的慢性自體免疫疾病, 時好時壞 無法根治 它有斑塊型 水滴狀 反轉型 膿皰症 紅皮症等類型 ; 病因至今尚未完全明瞭, 醫學界目前認為其主要為先天性 後天性及其他疾病所引起 ; 需依臨床變化來治療, 方式有塗抹外用藥膏 口服或注射藥物
臨床藥學 Clinical Pharmacy 乾癬與治療 台北市立聯合醫院林森院區藥劑科藥師吳命選 台北市立聯合醫院藥劑部藥師陳怡靜 陳立奇 摘要乾癬是發生在皮膚組織的慢性自體免疫疾病, 時好時壞 無法根治 它有斑塊型 水滴狀 反轉型 膿皰症 紅皮症等類型 ; 病因至今尚未完全明瞭, 醫學界目前認為其主要為先天性 後天性及其他疾病所引起 ; 需依臨床變化來治療, 方式有塗抹外用藥膏 口服或注射藥物
投影片 1
 一 前言 類風濕性關節炎新機轉藥物 - Tofacitinib 陳怡樺吳奕璋 類風濕性關節炎 (Rheumatoid arthritis; RA) 為一種原因尚不明確之慢性 全身性 發炎性的自體免疫疾病 疾病的特徵是許多個關節同時發生發炎反應, 一開始發炎的關節並不對稱, 經疾病進展後會逐漸發展成對稱之關節發炎 流行病學的部分以女性發病率大於男性, 比率約為 3:1, 好發的年齡層在 40-60 歲間
一 前言 類風濕性關節炎新機轉藥物 - Tofacitinib 陳怡樺吳奕璋 類風濕性關節炎 (Rheumatoid arthritis; RA) 為一種原因尚不明確之慢性 全身性 發炎性的自體免疫疾病 疾病的特徵是許多個關節同時發生發炎反應, 一開始發炎的關節並不對稱, 經疾病進展後會逐漸發展成對稱之關節發炎 流行病學的部分以女性發病率大於男性, 比率約為 3:1, 好發的年齡層在 40-60 歲間
Microsoft Word - statistics04-1_doc.docx
 入學新生體檢及異常統計表 (102 學年度 ) 國立成功大學 102 學年度新生體檢表概況 學院別 未檢 比例 不合格 比例 合格 比例 總 文學院 16 4.68 290 88.96 36 11.04 342 理學院 48 9.86 345 78.59 94 21.41 487 工學院 256 12.59 1432 80.54 346 19.46 2034 管理學院 42 5.10 672 85.93
入學新生體檢及異常統計表 (102 學年度 ) 國立成功大學 102 學年度新生體檢表概況 學院別 未檢 比例 不合格 比例 合格 比例 總 文學院 16 4.68 290 88.96 36 11.04 342 理學院 48 9.86 345 78.59 94 21.41 487 工學院 256 12.59 1432 80.54 346 19.46 2034 管理學院 42 5.10 672 85.93
經 口 服 以 提 升 運 動 表 現 的 物 質 中, 運 動 禁 藥 是 運 動 員 不 得 使 用 的 物 質, 不 在 這 規 範 中 的 則 可 稱 為 營 養 補 充 劑 運 動 營 養 學 的 應 用 4 3 2013 12 492 25
 運 動 員 的 營 養 與 禁 藥 World Anti-doping Agency, WADA 運 動 營 養 學 運 動 員 與 一 般 人 相 同, 為 了 健 康 會 經 口 攝 取 食 物 與 藥 物, 更 進 一 步 則 希 望 藉 此 提 升 運 動 表 現 24 2013 12 492 經 口 服 以 提 升 運 動 表 現 的 物 質 中, 運 動 禁 藥 是 運 動 員 不 得
運 動 員 的 營 養 與 禁 藥 World Anti-doping Agency, WADA 運 動 營 養 學 運 動 員 與 一 般 人 相 同, 為 了 健 康 會 經 口 攝 取 食 物 與 藥 物, 更 進 一 步 則 希 望 藉 此 提 升 運 動 表 現 24 2013 12 492 經 口 服 以 提 升 運 動 表 現 的 物 質 中, 運 動 禁 藥 是 運 動 員 不 得
X 傳統育種技術 分子育種技術 基因改良育種
 06 2015 7 511 72 92? 2010? X 傳統育種技術 1960 1980 30 60 20 分子育種技術 5 10 3 5 基因改良育種 2015 7 511 07 改良後的基因及其生產的蛋白質都需經過嚴格的動物及田間生物安全試驗才會上市, 程序就跟新藥一樣 20 基改產品禁得起考驗 12 2013 1.75 50 1 5 1996 80 2013 156 35 21 6 90 08
06 2015 7 511 72 92? 2010? X 傳統育種技術 1960 1980 30 60 20 分子育種技術 5 10 3 5 基因改良育種 2015 7 511 07 改良後的基因及其生產的蛋白質都需經過嚴格的動物及田間生物安全試驗才會上市, 程序就跟新藥一樣 20 基改產品禁得起考驗 12 2013 1.75 50 1 5 1996 80 2013 156 35 21 6 90 08
l l l l l
 衛生福利之整合 突破與新視野 INTEGRATION, BREAKTHROUGH, NEW VISION IN HEALTH AND SOCIAL WELFARE 衛生福利部綜合規劃司司長 石崇良 2014/06/20 1 l l l l l " (public health) the science and art of preven5ng disease, prolonging life and
衛生福利之整合 突破與新視野 INTEGRATION, BREAKTHROUGH, NEW VISION IN HEALTH AND SOCIAL WELFARE 衛生福利部綜合規劃司司長 石崇良 2014/06/20 1 l l l l l " (public health) the science and art of preven5ng disease, prolonging life and
三 相對療效與安全性 ( 人體健康 ): 相對療效實證資料來自於一篇由歐洲醫藥品管理局公布之 ipilimumab 樞紐試驗報告 1. 樞紐試驗 MDX (study CT-20): 本試驗為一隨機 雙盲 多國多中心第三期臨床試驗, 比較 ipilimumab 單方 ipilimumab
 益伏注射劑 (Yervoy Injection) 醫療科技評估報告 103BTD02005_Yervoy Injection 財團法人醫藥品查驗中心 Center For Drug Evaluation 藥物納入全民健康保險給付建議書 - 藥品專用 資料摘要 藥品名稱建議者藥品許可證持有商含量規格劑型主管機關許可適應症建議健保給付之適應症內容建議健保給付條件建議療程建議者自評是否屬突破創新新藥健保是否還有給付其他同成分藥品
益伏注射劑 (Yervoy Injection) 醫療科技評估報告 103BTD02005_Yervoy Injection 財團法人醫藥品查驗中心 Center For Drug Evaluation 藥物納入全民健康保險給付建議書 - 藥品專用 資料摘要 藥品名稱建議者藥品許可證持有商含量規格劑型主管機關許可適應症建議健保給付之適應症內容建議健保給付條件建議療程建議者自評是否屬突破創新新藥健保是否還有給付其他同成分藥品
(1) (2) (3) 1. (1) 2
 0386 71.32% 14A 1 (1) (2) (3) 1. (1) 2 (a) (b) (i) (ii) (iii) 3 (iv) (a) (b) (c) (d) 6% 4 2013 3 26 [2013]624 10 5 2013 6 28 [2013]1246 2015 3 [2015]351 0.2 6 [2015]748 180C 7 * * 8 14A (2) 417,800,000
0386 71.32% 14A 1 (1) (2) (3) 1. (1) 2 (a) (b) (i) (ii) (iii) 3 (iv) (a) (b) (c) (d) 6% 4 2013 3 26 [2013]624 10 5 2013 6 28 [2013]1246 2015 3 [2015]351 0.2 6 [2015]748 180C 7 * * 8 14A (2) 417,800,000
目錄表 年中期報告
 目錄表 2 4 5 13 28 29 31 33 35 36 67 1 2015 年中期報告 公司資料 公司 22 公司 www.boyaa.com.hk 0434 博雅互動國際有限公司 2 公司資料 中 1001 TCL E D3 9B-C 518000 183 17 1712-1716 Maples Fund Services (Cayman) Limited PO Box 1093, Boundary
目錄表 2 4 5 13 28 29 31 33 35 36 67 1 2015 年中期報告 公司資料 公司 22 公司 www.boyaa.com.hk 0434 博雅互動國際有限公司 2 公司資料 中 1001 TCL E D3 9B-C 518000 183 17 1712-1716 Maples Fund Services (Cayman) Limited PO Box 1093, Boundary
注入新能量明確新方向
 股份代號 598 Stock Code : 598 注入新能 量 明 確 新方 向 2015 Interim Report 2015 中 期 報 告 中期報告 R O F A Y NE W D T I L A T I V IR E C New Ti Interim Report on 2015 注入新能量明確新方向 2 3 4 5 7 9 10 38 49 50 公司資料 公司 公司 SINOTRANS
股份代號 598 Stock Code : 598 注入新能 量 明 確 新方 向 2015 Interim Report 2015 中 期 報 告 中期報告 R O F A Y NE W D T I L A T I V IR E C New Ti Interim Report on 2015 注入新能量明確新方向 2 3 4 5 7 9 10 38 49 50 公司資料 公司 公司 SINOTRANS
二 診斷 評估與治療流程 1. 基本檢查 A. History taking (Especially family history), physical exams B. Check lipid profile (Total cholesterol, LDL-C, HDL-C, Triglyceri
 一 血脂異常之分類與定義 中華民國血脂異常分類之建議 美國國家膽固醇教育計畫血脂小組血脂肪異常分級 歐洲動脈硬化學會對血脂異常之治療性分類 二 診斷 評估與治療流程 1. 基本檢查 A. History taking (Especially family history), physical exams B. Check lipid profile (Total cholesterol, LDL-C,
一 血脂異常之分類與定義 中華民國血脂異常分類之建議 美國國家膽固醇教育計畫血脂小組血脂肪異常分級 歐洲動脈硬化學會對血脂異常之治療性分類 二 診斷 評估與治療流程 1. 基本檢查 A. History taking (Especially family history), physical exams B. Check lipid profile (Total cholesterol, LDL-C,
Chinasoft International Limited 中軟國際有限公司 * 於開曼群島註冊成立之有限公司 股份代號 0354 * 僅供識別
 Chinasoft International Limited * 於開曼群島註冊成立之有限公司 股份代號 0354 * 僅供識別 1 內容.......................................................... 2...................................................... 3...................................................
Chinasoft International Limited * 於開曼群島註冊成立之有限公司 股份代號 0354 * 僅供識別 1 內容.......................................................... 2...................................................... 3...................................................
PNA 國家圖 各種語言的 MSC 生態標章 P N A W W F P N A M S C stakeholders Moody Marine Ltd PNA MSC EUROTHON ISSF OPAGAC ISSF Moody Mar
 6 漁業新知 海洋管理委員會 (MSC) 水產認證標章介紹 文 圖 / 王譽善 張水鍇 ( 國立中山大學海洋事務研究所 ) A: 已認證的永續水產品 B: 海洋管理委員會的英文縮寫 C: 海洋管理委員會的網址 D: 白框線的內容及魚圖必須出現在標章內 E: 代表此為註冊標章 F: 魚圖註冊標章 Parties to the Nauru Agreement, PNA Marine Stewardship
6 漁業新知 海洋管理委員會 (MSC) 水產認證標章介紹 文 圖 / 王譽善 張水鍇 ( 國立中山大學海洋事務研究所 ) A: 已認證的永續水產品 B: 海洋管理委員會的英文縮寫 C: 海洋管理委員會的網址 D: 白框線的內容及魚圖必須出現在標章內 E: 代表此為註冊標章 F: 魚圖註冊標章 Parties to the Nauru Agreement, PNA Marine Stewardship
®
 中 草 药 Chinese Traditional and Herbal Drugs 第 45 卷 第 15 期 214 年 8 月 2277 稳 心 颗 粒 治 疗 心 律 失 常 的 Meta 分 析 * 何 颖, 刘 莹, 邹 爱 英 天 津 中 医 药 大 学 第 二 附 属 医 院, 天 津 15 摘 要 : 利 用 Meta 分 析 法 评 价 稳 心 颗 粒 治 疗 心 律 失 常 的
中 草 药 Chinese Traditional and Herbal Drugs 第 45 卷 第 15 期 214 年 8 月 2277 稳 心 颗 粒 治 疗 心 律 失 常 的 Meta 分 析 * 何 颖, 刘 莹, 邹 爱 英 天 津 中 医 药 大 学 第 二 附 属 医 院, 天 津 15 摘 要 : 利 用 Meta 分 析 法 评 价 稳 心 颗 粒 治 疗 心 律 失 常 的
青少年政策白皮書
 ... 1... 1... 2... 2... 3... 4... 4... 7... 7... 15... 18... 21... 21... 21... 31... 34... 39... 39... 40... 48... 49... 53... 55... 55... 56... 60... 62... 65... 65... 66... 68... 69... 73... 73... 73...
... 1... 1... 2... 2... 3... 4... 4... 7... 7... 15... 18... 21... 21... 21... 31... 34... 39... 39... 40... 48... 49... 53... 55... 55... 56... 60... 62... 65... 65... 66... 68... 69... 73... 73... 73...
( )... 5 ( ) ( )
 2016 大學校院招收大陸地區學生聯合招生委員會 71005 臺南市永康區南臺街 1 號 E-mail:[email protected] WEB:http://rusen.stust.edu.tw TEL:+886-6-2435163 FAX:+886-6-2435165 2 0 1 6 0 1 1 9 2016... 2... 3... 5 ( )... 5 ( )... 5 1... 6 2...
2016 大學校院招收大陸地區學生聯合招生委員會 71005 臺南市永康區南臺街 1 號 E-mail:[email protected] WEB:http://rusen.stust.edu.tw TEL:+886-6-2435163 FAX:+886-6-2435165 2 0 1 6 0 1 1 9 2016... 2... 3... 5 ( )... 5 ( )... 5 1... 6 2...
 11 4 3 46 46 44 48 50 50 84 148 42 47 54 41 46 10 46 149 291AA 150 S.21111 44 151 48 25 152 291AA 291AA 291AA 750 751(1) 153 50 La Trobe University 25 La Trobe University I II 1132 8088 273 64,400,000
11 4 3 46 46 44 48 50 50 84 148 42 47 54 41 46 10 46 149 291AA 150 S.21111 44 151 48 25 152 291AA 291AA 291AA 750 751(1) 153 50 La Trobe University 25 La Trobe University I II 1132 8088 273 64,400,000
1 2 3 7 10 14 20 30 31 32 41 2012/13 43 47 48 51 53 GRI 55 62 2012/13
 合 和 同 心 共 創 可 持 續 發 展 2012/13 年 度 可 持 續 發 展 報 告 1 2 3 7 10 14 20 30 31 32 41 2012/13 43 47 48 51 53 GRI 55 62 2012/13 http://www.hopewellholdings.com/zh-hk/corporate-sustainability/sustainability-report
合 和 同 心 共 創 可 持 續 發 展 2012/13 年 度 可 持 續 發 展 報 告 1 2 3 7 10 14 20 30 31 32 41 2012/13 43 47 48 51 53 GRI 55 62 2012/13 http://www.hopewellholdings.com/zh-hk/corporate-sustainability/sustainability-report
: ( ),,
 Case Discussion: ( ), RN, ScD, MPH : 24,,,,,,, ( ) ) ( ), : ( ),, randomized controlled trial (RCT). minimization program,,,, : : ; Apgar score > 7 ;, : ; ; ; ; (BT180/min; 2, 83,50 (60.2%).,
Case Discussion: ( ), RN, ScD, MPH : 24,,,,,,, ( ) ) ( ), : ( ),, randomized controlled trial (RCT). minimization program,,,, : : ; Apgar score > 7 ;, : ; ; ; ; (BT180/min; 2, 83,50 (60.2%).,
本公司(銀行)銷售○○投信「○○基金」所收取之通路報酬如下:
 20180824 版 ( 都柏林 ) 本公司銷售 ( 都柏林 ) 法盛國際系列 法盛 - 盧米斯賽勒斯高收益債券基金 ( 原名稱 : 法儲銀 - 盧米斯賽勒斯高收益債券型基金 )( 本基金主要係投資於非投資等級之高風險債券 ) 所收取之通路報酬如下 : 台端支付的基金申購手續費不多於 2%, 其中本公司收取不多於 2% 台端支付的基金轉換手續費為 0% 二 基金公司 ( 或總代理人 / 境外基金機構
20180824 版 ( 都柏林 ) 本公司銷售 ( 都柏林 ) 法盛國際系列 法盛 - 盧米斯賽勒斯高收益債券基金 ( 原名稱 : 法儲銀 - 盧米斯賽勒斯高收益債券型基金 )( 本基金主要係投資於非投資等級之高風險債券 ) 所收取之通路報酬如下 : 台端支付的基金申購手續費不多於 2%, 其中本公司收取不多於 2% 台端支付的基金轉換手續費為 0% 二 基金公司 ( 或總代理人 / 境外基金機構
財團法人醫藥品查驗中心 Center For Drug Evaluation 三 相對療效與安全性 ( 人體健康 ): 1. abiraterone acetate vs. placebo 相對療效實證來自於一個直接比較 abiraterone acetate 與安慰劑的樞紐試驗 Study COU
 澤珂錠 250 毫克 (Zytiga Tablets 250mg) 醫療科技評估報告 財團法人醫藥品查驗中心 Center For Drug Evaluation 藥物納入全民健康保險給付建議書 - 藥品專用 資料摘要 藥品名稱澤珂錠 250 毫克成分 Abiraterone acetate 建議者 藥品許可證持有商 嬌生股份有限公司 同上 含量規格劑型 250mg / 8~1000 錠塑膠瓶裝 (
澤珂錠 250 毫克 (Zytiga Tablets 250mg) 醫療科技評估報告 財團法人醫藥品查驗中心 Center For Drug Evaluation 藥物納入全民健康保險給付建議書 - 藥品專用 資料摘要 藥品名稱澤珂錠 250 毫克成分 Abiraterone acetate 建議者 藥品許可證持有商 嬌生股份有限公司 同上 含量規格劑型 250mg / 8~1000 錠塑膠瓶裝 (
5-2
 Healthcare Matrix 中 國 醫 藥 大 學 陳 偉 德 副 校 長 1 (Safe) 2 (Timely) 3 (Effective) 4 (Efficient) 5 (Equitable) 6 (Patient-Centered) 76 a (Patient Care) b c (Medical Knowledge and Skills) (Interpersonal and Communication
Healthcare Matrix 中 國 醫 藥 大 學 陳 偉 德 副 校 長 1 (Safe) 2 (Timely) 3 (Effective) 4 (Efficient) 5 (Equitable) 6 (Patient-Centered) 76 a (Patient Care) b c (Medical Knowledge and Skills) (Interpersonal and Communication
2012_A4.indd
 查 尔 斯 沃 思 中 国 在 线 医 学 期 刊 简 介 www.charlesworth.com.cn 新 英 格 兰 医 学 杂 志 The New England Journal of Medicine 马 萨 诸 塞 州 医 学 会 (Massachusetts Medical Society) 成 立 于 1781 年, 是 美 国 一 个 州 属 专 业 医 学 会, 拥 有 2 万
查 尔 斯 沃 思 中 国 在 线 医 学 期 刊 简 介 www.charlesworth.com.cn 新 英 格 兰 医 学 杂 志 The New England Journal of Medicine 马 萨 诸 塞 州 医 学 会 (Massachusetts Medical Society) 成 立 于 1781 年, 是 美 国 一 个 州 属 专 业 医 学 会, 拥 有 2 万
理性真的普遍嗎 注意力的爭奪戰 科學發展 2012 年 12 月,480 期 13
 12 科學發展 2012 年 12 月,480 期 你可能不知道的媒體影響 劉正山若用 選戰 的角度來看選舉和參與選舉, 你大腦裡情感的作用一定大過理性的作用, 便會很習慣地拿各種媒體或別人的觀點來使自己的選擇合理化 2012 理性真的普遍嗎 注意力的爭奪戰 科學發展 2012 年 12 月,480 期 13 14 科學發展 2012 年 12 月,480 期 agendasetting 報紙和網路新聞的頭版空間有限,
12 科學發展 2012 年 12 月,480 期 你可能不知道的媒體影響 劉正山若用 選戰 的角度來看選舉和參與選舉, 你大腦裡情感的作用一定大過理性的作用, 便會很習慣地拿各種媒體或別人的觀點來使自己的選擇合理化 2012 理性真的普遍嗎 注意力的爭奪戰 科學發展 2012 年 12 月,480 期 13 14 科學發展 2012 年 12 月,480 期 agendasetting 報紙和網路新聞的頭版空間有限,
* B0335H J (1) 7 (2) 42 (3) 63 (4) 67 (5) 75 (6)
 2018 6 30 Chongqing Rural Commercial Bank Co., Ltd. * 2018 6 30 2018 6 30 (www.cqrcb.com) (www.hkexnews.hk) 2018 6 30 2018 8 30 * Chongqing Rural Commercial Bank Co., Ltd.* * B0335H250000001 91500000676129728J
2018 6 30 Chongqing Rural Commercial Bank Co., Ltd. * 2018 6 30 2018 6 30 (www.cqrcb.com) (www.hkexnews.hk) 2018 6 30 2018 8 30 * Chongqing Rural Commercial Bank Co., Ltd.* * B0335H250000001 91500000676129728J
HKSTPC-Annual Report Chi
 企業管治報告 14 企業管治架構 股東 ( 香港特別行政區政府 ) 董事會 管理層 企業合規 - 90 - 企業發展 董事會 17 1 16 董事會成員組成 2015 11 20 80 85 簡介會 2016 1 成員與時並進 2015 利益申報 14 利益衝突 - 91 - 董事會職能 77% 專業建議 承擔責任 6 常務委員會 95 企業拓展及批租委員會 9 8 80% - 92 - 企業發展
企業管治報告 14 企業管治架構 股東 ( 香港特別行政區政府 ) 董事會 管理層 企業合規 - 90 - 企業發展 董事會 17 1 16 董事會成員組成 2015 11 20 80 85 簡介會 2016 1 成員與時並進 2015 利益申報 14 利益衝突 - 91 - 董事會職能 77% 專業建議 承擔責任 6 常務委員會 95 企業拓展及批租委員會 9 8 80% - 92 - 企業發展
