第五章 重量分析法和沉淀滴定法
|
|
|
- 鹄浚 姜
- 5 years ago
- Views:
Transcription
1 第 9 章 重量分析法 基本内容. 重量分析的分类和特点重量分析法是化学分析中最经典的一种方法 是直接用分析天平称量物质的质量来进行测定结果的 不用基准物质进行比较 相对误差一般为 0.%~0.% 准确度较高 但耗时多 周期长 根据被测组分与其他组分分离方法的不同 分为沉淀法 气化法 ( 又叫挥发法 ) 和电解法三种 其中以沉淀法最为重要 在此只介绍沉淀法. 重量分析对测定形式和称量形式的要求利用沉淀反应进行重量分析时 通过加入适当的沉淀剂 先将被测组分转化为沉淀形式析出 然后再经过过滤 洗涤 烘干和灼烧 将沉淀形式转化为称量形式称量 沉淀形式和称量形式可以相同也可以不同 为了保证测定有足够的准确度并便于操作 重量分析法对沉淀形式和称量形式有如下要求 :. 重量分析法对沉淀形式的要求 :. 沉淀的溶解度要小 b. 沉淀应易于过滤和洗涤 c. 沉淀要力求纯净 d. 沉淀应易于转化为称量形式. 重量分析法对称量形式的要求 :. 称量形式必须有确定的化学组成 b. 称量形式必须稳定 不受空气中水分 CO 和 O 等的影响 c. 称量形式的摩尔质量要大 以减小称量误差. 沉淀的溶解度及其影响因素在沉淀法中 沉淀是否完全 可以根据反应达到平衡后 溶液中剩余被测组分的量来衡量 影响沉淀溶解度的因素很多 主要有同离子效应 酸效应 络合效应和盐效应等 此外还有温度 介质 晶体结构和颗粒大小也对溶解度有影响 溶解度是指微溶化合物在溶剂中的实际溶解度 即总溶解度 总溶解度包括分子溶
2 解度 即固有溶解度和离子溶解度 在溶液中微溶化合物以分子状态或离子对状态存在 的浓度为一常数 常用 S 0 表示 称为该物质的分子溶解度 即固有溶解度 它与微溶化 合物的性质有关 除少数沉淀外 大多数沉淀的固有溶解度较小 在计算溶解度时可以 忽略不计. 同离子效应 在微溶化合物的饱和溶液中 加入组成沉淀的离子 ( 即构晶离子 ) 时 微溶化合物 的溶解度降低 这种现象叫同离子效应 同离子效应减小微溶化合物的溶解度 在实际 工作中 通常利用同离子效应 即加大沉淀剂的用量 使被测组分沉淀完全 一般情况 下 沉淀剂过量 50%~0% 是合适的 如果沉淀剂不易挥发 则以过量 0%~0% 为宜. 盐效应 在微溶化合物的饱和溶液中 加入非构晶离子的强电解质时 微溶化合物的溶解度 增大 这种现象叫盐效应 盐效应增大微溶化合物的溶解度 构晶离子的电荷愈高 影 响也愈严重 故在实际工作中应尽量避免不必要的各种电解质的存在. 酸效应 酸度对微溶化合物溶解度的影响称为酸效应 酸效应的发生 主要是由于溶液中 [H ] 浓度大小对弱酸离解平衡的影响 应当指出 : 对于弱酸盐在纯水中溶解度的计算是比较 复杂的 应根据具体情况进行具体分析 通常对于溶解度很小的弱酸盐 只考虑水的酸 效应 即 [H ] 以 -7 mol L - 来计算 ; 对于溶解度较大的弱酸盐 由于溶液中阴离子浓度 较大 则主要考虑其阴离子的水解对溶解度的影响. 络合效应 在微溶化合物的饱和溶液中 若有能与构晶离子生成可溶性络合物的络合剂存在时 微溶化合物的溶解度将增大 这种现象称为络合效应 络合效应使微溶化合物溶解度增 大的程度与微溶化合物的溶度积及络合物的稳定常数的大小有关 形成的络合物越稳定 络合效应越显著 微溶化合物的溶解度就增大的越多 例如在一定温度下 设有一弱酸微溶化合物 m n 在水溶液中建立了两相平衡 饱 和溶液的溶解度为 S; 若溶液中既有盐效应 又加入 c 的同离子效应 而且 和 还有 副反应 则溶解度 S 的计算公式推导如下 : m n ( ) m m n m n m n c m c m m [ ] γ m γ m γ m m m
3 n [ ] m n γ n γ ( c n mγ ) ( ) m n m m n n n m m n m n 则 m m n m n m γ γ c m n. 弱酸微溶化合物溶解度计算在定量分析中 计算沉淀溶解度对于估算测量误差 选择最佳沉淀条件 判定所选方法的可行性等都具有非常重要的意义 但溶解度的计算十分复杂 影响微溶化合物溶解度的因素很多 主要有同离子效应 酸效应 络合效应和盐效应 在这几种影响因素中 酸效应的影响较难处理 所以在微溶化合物溶解度的计算中 又以弱酸微溶化合物的计算最为复杂 如果溶液的 ph 值是个定值 并且已知 则可直接代入教材中的公式进行计算 但是在很多情况下 溶液的 ph 值不是一个固定值 溶液中存在着多重平衡 确定溶液中的氢离子浓度有一定的困难 在这种情况下 虽然根据电荷平衡和物料平衡的原理 可以确定溶液中氢离子的浓度与溶解度的关系 但是计算溶解度需要解高次方程 因而在教学中总是先作近似处理 然后再求解 并假定 在酸溶液中 只要外加强酸的浓度 c 不是很小 弱酸又不是极弱时 溶液中的氢离子浓度以 c 来计算 在纯水中 当微溶化合物的溶解度很小时 水中的氢离子浓度以 -7 mol L - 来计算 ; 当微溶化合物的溶解度较大 并且酸根离子碱式离解程度较大时 要考虑水解的影响. 不难看出 这些假定没有一个严格的界限 所以在实际的近似计算中仍然困难重重 我在此提出采用数值逼近法来计算微溶化合物的溶解度 此法即不要考虑上述的那些假定 又可避免解高次方程 而且还可以保证一定的准确度. 数值逼近法 : 在一定温度下 设有一弱酸微溶化合物 mn() 在水中达到饱和时 即建立了两相平衡 饱和溶液的浓度就是溶解度 平衡关系式如下 : m n mn() m 在没有外加惰性电解质时 溶液的离子强度很小 所以溶液中盐效应的影响通常不予考虑 当考虑酸效应和络合效应的影响时 弱酸微溶化合物的溶解度计算公式为 : n m- m p m n n m δ n (H) m n () 当考虑酸效应和络合效应的影响 同离子为外加构晶阳离子时 弱酸微溶化合物的
4 溶解度计算公式为 : m p n () n m n δ(h) c 当考虑酸效应和络合效应的影响 同离子为外加构晶阴离子时 弱酸微溶化合物的溶解度计算公式为 : m p m () n n m δ(h) c 式中 :S 是弱酸微溶化合物的溶解度 (mol L - ) 是溶度积常数 和 δ (H) 分 别是络合效应总副反应系数和酸效应分布系数 ; c 和 c 分别是外加构晶阴 阳离子的 浓度 (mol L - );n 和 m 分别表示阴 阳离子的系数 近 : 当 在酸溶液中 当外加强酸的浓度为 c mol L - 时 用 c 作初值 按下式进行数值逼 c 时 溶液中 [ H ] c [ ] H () c 时 不必进行逼近 在纯水中 首先考虑水解效应的影响 基于下列平衡关系式 : 并得公式 : mn() nh n (m-)- - O m nh noh n p w (5) m n m n ( m n) 用 (5) 式求出的 作初值 然后按下式进行数值逼近 : w [ H ] -7 n 当 n<< -7-7 时 溶液中的 [H ] 不必进行逼近 ; 当 n>> -7 时 不考虑水解离的 影响 以 [H ] 进行逼近 n w. 数值逼近法的应用 : n x 例 : 计算 CF 在.0 mol L - 的 HCl 溶液中 并且外加 C 的浓度为.0 mol L - 时的溶解度 5
5 解 : 已知 CF 的 HF 的 7. p.7 c.0 mol L - c c.0 mol L δ F ( H ) 代入 () 式 : 6. (mol L - ) [ H ] c (mol L - ) [ H ] δf(h) (mol L - ) 5 再逼近一次 S S 6.0 mol L - 5 所以溶解度为 6.0 mol L - 例 : 计算 gcn 在纯水中的溶解度 解 : 已知 gcn 的 HCN 的 6. 6 p 由 (5) 式求初值 : 0. (mol L - ) 6. w.0 8 [ H ].5 (mol L - ) δcn(h). 8 [ H ] p. 8 代人 () 式 : 9. (mol L - ) δ. CN(H) w.0 8 [ H ] 5. (mol L - ) δcn(h). 8 [ H ] p 7.0 (mol L - ) δcn(h). 7 再逼近一次 S S 所以溶解度为.0 mol L - 6
6 5. 沉淀的类型和形成过程 5. 沉淀的类型沉淀按其物理性质不同 可大致分为两类 : 一类是晶形沉淀 另一类是无定形沉淀 也叫非晶形沉淀 从沉淀的颗粒大小来看 晶形沉淀最大 无定形沉淀最小 5. 沉淀形成的过程聚集大于定向 无定形沉淀成核作用长大过程构晶离子 晶核 沉淀微粒 定向大于聚集 晶形沉淀晶核的形成有两种情况 : 一种是均相成核作用 ; 另一种是异相成核作用 在进行沉淀反应时 异相成核作用总是存在的 不同的沉淀 形成均相成核作用时所需的相对过饱和程度不一样 相对过饱和程度愈大 愈易引起均相成核作用 生成的沉淀是晶形沉淀还是非晶形沉淀 主要由聚集速度和定向速度所决定 定向速度与沉淀物的性质 极性 溶剂的性质以及温度有关 而聚集速度主要与溶液的过饱和程度有关 当定向速度大于聚集速度时 生成晶形沉淀 ; 当定向速度小于聚集速度时 则生成无定形沉淀 6. 影响沉淀纯度的主要因素 6. 共沉淀当一种沉淀从溶液中析出时 溶液中的某些其他组分 在该条件下本来是可溶的 但它们却被沉淀带下来而混杂于沉淀之中 这种现象称为共沉淀 共沉淀现象主要有以下三类 :. 表面吸附 : 吸附在沉淀表面第一层上的离子是有选择性的构晶离子 抗衡离子的吸附规则是优先吸附能与构晶离子形成溶解度小或离解度小的化合物离子 离子价态越高 浓度越大 则越易被吸附 ; 比表面积越大 吸附杂质越多 ; 温度升高 吸附杂质量减少 b. 吸留和包夹 : 吸留和包夹也是沉淀玷污的主要原因之一 采用陈化或重结晶的方法 可以减少此类玷污 c. 混晶和固溶体 : 混晶和固溶体会使沉淀严重不纯 消除混晶和固溶体影响的最好方法就是将杂质事先除去 6. 继沉淀沉淀析出后 在放置过程中 另一种本难于析出的组分在该沉淀表面上析出成为沉淀的现象称为继沉淀也叫后沉淀 继沉淀引入的杂质量有时比共沉淀还要多 而且随沉淀放置时间延长而增多 温度升高而严重 减少继沉淀的主要方法是缩短沉淀的放置时间 要提高沉淀的纯度 则应根据沉淀的性质和杂质混入的规律采取适当的措施 以减 7
7 少杂质的引入 较常用的措施有 : 改善沉淀的条件 改变杂质的存在形式 选择较合适的沉淀剂 选择合适的分析步骤和再沉淀等 7. 沉淀条件的选择在重量分析中 为了获得准确得分析结果 要求被测组分沉淀完全 所得的沉淀纯净 而且易于过滤洗涤 为此 应选择在合适的条件下进行沉淀 由于不同形态的沉淀性质不一样 因此 它们的沉淀条件不同 为了便于记忆 将晶形沉淀和无定形沉淀的条件分别归纳成五个字如下 : 7. 晶体沉淀条件 : 稀 慢 搅 热 陈. 稀 : 沉淀应当在适当的稀溶液中进行 ; b. 慢和搅 : 应在不断搅拌下缓慢地加入沉淀剂 ; c. 热 : 应在热溶液中进行 ; d. 陈 : 陈化 7. 无定形沉淀条件 : 浓 热 电 不陈. 浓 : 在较浓的溶液中进行 ; b. 热 : 在热溶液中进行 ; c. 电 : 加入大量强电解质 ; d. 不陈 : 不必陈化 趁热过滤 8. 均匀沉淀法在一般的沉淀方法中 沉淀剂是在不断搅拌下缓慢地加入 但沉淀剂的局部过浓现象仍然很难避免 为此可采用均匀沉淀法 在这种方法中 加入到溶液中的试剂是通过缓慢的化学反应过程 逐步地 均匀地在溶液内部产生出来 使沉淀在整个溶液中慢慢地 均匀地析出避免了局部过浓现象 此法的优点是 : 得到的沉淀颗粒较大 表面吸附杂质少 易过滤 易洗涤 ; 缺点是 : 仍不能避免后沉淀和混晶共沉淀现象的发生 9. 重量分析结果的计算沉淀经过滤 洗涤 烘干和灼烧后便得到沉淀的称量形式 若被测组分的表示形式与沉淀的称量形式不相一致时 则应将称量形式存在时的质量 (m) 通过换算因数 (F) 换算成以被测组分形式存在时的质量进行计算 m m x w x 0% 0% m 称 m r(x) 换算因子 Fn r( 称量形 ) 式中 w 为被测组分的含量 m 为称量形式的质量 m 为试样的质量 8
8 . 已知 [ CCO ] [ C ][ SO ] β 习题解答 并计算饱和 CSO 溶液中 非离子形式 C 的百分数 解 : 查表知 :CSO 的 9. 6 固有溶解度 : [ CSO] β[ C ][ SO ] β 在饱和 CSO 溶液中 离解了 CSO 的浓度为 : 00 忽略离子强度的影响 计算 CSO 的固有溶解度 6 [ C ] [ SO ] mol L - mol L - 非离子形式的的百分数为 :.8 0% 7.6%.8.0. 已知某金属氢氧化物 (OH) 的 5 向 0. mol L - 溶液中加入 NOH 忽略体积变化和各种氢氧基络合物 计算下列不同情况生成沉淀时的 ph. 有 % 沉淀 ;b. 有 50% 沉淀 ;c. 有 99% 沉淀 OH c 0. mol L - 5 解 : 已知 : [ ][ ]. 当有 % 的 沉淀时 [ ]0. (-%)0.099 mol L [ OH ].0 mol L - poh6.70ph ; b. 当有 50% 的 沉淀时 [ ]0. (-50%)0.050 mol L [ OH ].8 mol L - poh6.55ph ; c. 当有 99% 的 沉淀时 [ ]0. (-99%)0.00 mol L [ OH ].0 mol L - poh5.70ph 考虑盐效应 计算下列微溶化合物的溶解度.BSO 在 0. mol L - NCl 溶液中 ; b.bso 在 0. mol L - BCl 溶液中 解 : 查表知 :BSO 的. 由表查得 : γ 0. 8 γ 在 0. mol L - NCl 溶液中 : I ( ) 0. B SO 设 BSO 在 0. mol L - NCl 溶液中的溶解度为 则 9
9 [ B ] [ SO ] γ γ B SO..9 5 mol L b. 在 0. mol L - BCl 溶液中 : I ( ) 0. 0 由德拜 休克公式计算 : 0.0 lg γ B γ 0. 6 B ; 0.0 lg γ SO γ 0. ; SO 设 BSO 在 0. mol L - BCl 溶液中的溶解度为 则. 8 [ SO ].9 mol L - B γ γ B [ ] [ ] B SO. 考虑酸效应 计算下列微溶化合物的溶解度.CF 在 ph.0 的溶液中 ; b.bso 在.0 mol L - 的 HCl 中 ; c.pbso 在 0. mol L - 的 HNO 中 ; d.cus 在 ph0.5 的饱和 H S 溶液中 ([H S] 0. mol L - ) 解 :. 查表知 :CF 的.7 HF 的 6.6 ph.0 CF C F - 设 CF 在 ph.0 的溶液中的溶解度为 6.6 [ F ] δ c 0. F F ( 0.) b. 查表知 :BSO 的. H SO 的.0 在.0 mol L - 的 HCl 中 [H ].0 mol L - BSO B SO -. mol L - ; 设 BSO 在.0 mol L - 的 HCl 中的溶解度为.0 SO δ SO.0.0 [ ] mol L - ; c. 查表知 :PbSO 的.6 8 H SO 的.0 在 0. mol L - 的 HNO 中 [H ]0. mol L - PbSO Pb - SO 设 PbSO 在 0. mol L - HNO 中的溶解度为 0
10 .0 SO SO 0..0 [ ] δ mol L - ; d. 查表知 :CuS 的 H S 的 在 ph0.5 的饱和 H S 溶液中 [H S] 0. mol L - [H ] 0.5 mol L - CuS Cu S - 设 CuS 在 ph0.5 的饱和 H S 溶液中的溶解度为 [ ] δ [ H S] ( ) δ [ H S] 0.δ S S S δs ( ) mol L- 5. 计算 BSO 在 0.0 mol L - BCl 0.070mol L - HCl 中的溶解度 解 : 由题意知 : 此题要同时考虑酸效应 盐效应和同离子效应 查表 BSO 的. H SO 的.0 ( ) 0. I 由 P 85 附表查得 B - 的 å 值为 500SO 的 å 值为 00 活度系数分别为 : γ B γ SO [ H ] SO (H) 0.0 设 BSO 在 0.0 mol L - BCl mol L - HCl 中的溶解度为 γ SO 则 0.0γ B 0.0γ SO (H) SO (H) 7 B γ SO 考虑 S - 的水解 计算下列硫化物在水中的溶解度.CuS b.ns S mol L - 解 :. 查表知 CuS 的 很小 故由 S - 水解引起溶解中 ph 值的变化可
11 忽略不计 以 [H ].0 7 mol L - 计算 : H S 的. 7 [ H ] β [ H ] S β (H) 7. 5 只考虑酸效应 (.0 ) CuS Cu S - 设 CuS 在水溶液中的溶解度为 [ Cu ][ S ] p S (H) mol L - p S (H) b. 查表知 ns 的.0 较大 故溶液中的 ph 值几乎由水解来决定 S - 水解主要产物是 HS - 第二步水解忽略不计 ns H O n OH - HS - 设 ns 在水溶液中的溶解度为 平衡常数 [n ][OH - ][HS - ] W [ n ][ S ][ OH ][ H ][ HS ] [ H ][ S ] mol L 将固体 gcl 和 gbr 加入到 50.0ml 纯水中 不断搅拌使其达到平衡 计算溶液中 g 浓度 解 : 查表知 gcl 的 (gcl).8 gbr 的 (gbr) 5.0 当溶解达到平衡时 根据电荷守恒 : (gcl) (gbr) g g [g ][Cl ][Br ] [ ] [ ] [ g ] mol L - (gcl) (gbr) 8. 计算 CC O 在下列溶液中的溶解度.pH.00 的 HCl 溶液中 ; b.ph.00 含有草酸总浓度为 0.0 mol L - 的溶液中 解 : 查表知 CC O 的.0 9 H C O 的 ( ).ph.00 时 : C O (H) mol L - ; C O (H) b. 在这种情况下 要同时考虑同离子效应和酸效应 : W
12 ( ) 当 ph.00 时 : C O (H) 设 CC O 在 ph.00 草酸总浓度为 0.0 mol L - 溶液中的溶解度为 CC O C - C O [C ][C O - ] C O (H) 9 C O (H) mol L 计算 CCO 在纯水中的溶解度和平衡时溶液的 ph 解 : 查表知 CCO 的 比较大 并且溶液中的 ph 取决于 CO 的水 解 第一步水解产物为 HCO - 第二步水解忽略 H CO 的 CCO H O C OH - HCO - 平衡常数 :[C ][OH - - ][HCO ] 设 CCO 在纯水中的溶解度为 [ C ][ CO ][ OH ][ H ][ HCO ] [ H ][ CO ] W mol L - ; 5.6 W 由 [OH - ] poh-lg(8.0 5 ). ph 为了防止 gcl 从含有 0.0 mol L - gno 和 0.0 mol L - NCl 的溶液中沉淀 应加入氨的总浓度为多少 ( 忽略溶液体积变化 )? 解 : 查表知 gcl 的.8 g(nh ) 的 lgβ 和 lgβ 分别为. 和 7.05 g(nh ) [ NH ] β [ NH ] β [ NH ] β [g ]0.0 mol L - [Cl ] 0.0 ) g(nh mol L - 只要 [g ][Cl ] 就没有 g 沉淀下来 0.0 即 [ ] g(nh ) 0.0 NH [NH 7.05 ] 0. mol L -.8
13 ] 总 故 [ NH mol L -. 求 gi 在 0.0 mol L - N S O 和 0.0 mol L - I 溶液中的溶解度 解 :gi 的 9. 7 g(s O - ) 的 lgβ ~lgβ 分别为 和.5 [ S O ] β [ S O ] β [ S O ] β g(s O ) 设 gi 在 0.0 mol L - N S O 和 0.0 mol L - I 溶液中的溶解度 gi g I [g ][I - ] g(s O ) g(s O ) mol L -. 今有 ph.0 并含有 0.0 mol L - EDT 和 0.0 mol L - HF 及 0.0 mol L - CCl 的溶液 问 :.EDT 对沉淀的络合效应是否可以忽略?b. 能否生成沉淀? 解 :.CF 的.7 lg CY.69pH.0 时的 lg Y(H) C(y) CY [Y] 由于 C(y).0 故 EDT 对沉淀的络合效应可以忽略 b.hf 的 6.6 F(H) β[h ] [C ][F ] >.7 所以有 CF 沉定生成.5. 于 0ml 含 0.00gB 的溶液中 加入 50ml0.0 mol L - H SO 溶液 问溶液中 还剩留多少克的 B? 如沉定用 0ml 纯水或 0ml0.0 mol L - 的 H SO 洗涤 假设洗 涤时达到了沉淀平衡 则各损失 BSO 多少毫克? 解 : 查得 H SO 的 SO B 7. gmol BSO. 9.0 n gmol BSO 的 mol 7. B B n mol 所以溶液中 B 过量 则生成 BSO 的质量 m n g SO BSO 溶液中还剩留 B 的质量 ( ) 7..mg 用 0ml 纯水洗涤时 : 溶于水中的 BSO 的浓度为
14 ..0 5 mol L - 故损失 BSO 的质量为 : mg; 用 0ml0.0 mol L - 的 H SO 溶液洗涤时 : [ SO ] 解得 [ ] ch δ ch SO SO SO. mol L - SO [ H ] 0.0 ( 0.0 [ SO ]) 故 BSO 在 0.0 mol L - 的 H SO 溶液中的溶解度为..7 8 mol L -. 所以 BSO 的损失为 : mg. 考虑络合效应 计算下列微溶化合物的溶解度.gBr 在.0 mol L - NH 溶液中 ; b.bso 在 ph8.0 的 0.0 mol L - EDT 溶液中 解 :. 查表知 g(nh ) 的 lgβ.lgβ 7.05 gbr 的 5.0 g(nh ) 故溶解度 [ NH ] β [ NH ] β g(nh ) 5.0 b. 查表知 BSO 的. lg BY 7.8 ph8.0 时 : 0.0 lg Y(H).7 β [ Y].7 mol L B(Y) BY.7 Y(H).5 B(Y).0 6. mol L - 5. 某溶液含有 B - SO 和 EDT 已知其分析浓度分别为 c 0. mol L - c Y 0. mol L - c.0 mol L - 欲利用 EDT 的酸效应阻止 BSO 沉淀生成 SO 则溶液的 ph 至少应大于多少? 已知 BSO 的 关数据如下 :.0 BY 7.8 ph 与 lg Y(H) 的有 ph lg Y(H) 解 : 只要 [B - ][SO ]< 就没有沉淀生成 查表知 H SO 的 B.0 较大 故 SO 的水解度是比较小 所以 SO 的副反应忽略不计 则 [SO ].0 mol L - 而 B 有 Y 的络合效应 并且 Y 又有酸效应 : 5
15 B (Y) Y(H) Y(H) β [ Y] [B ][SO - ] 0. B (Y) 即 Y(H) <6.9 lg Y(H) <0.8 故 ph> 在列情况下有无沉定生成? 0..0 Y(H).0 < mol L - C(NO ) 溶液与 0.00 mol L - NH HF 溶液等体积相混合 ; b.0. mol L - g(nh ) 的 mol L - NH 溶液与 mol L - Cl 溶液等体积相混合 ; c.0.0 mol L - gcl 溶液与 0. mol L - NH - mol L - NH Cl 溶液等体积相混合 解 :.CF 的.7 HF 的 6.6 在溶液中存在下列平衡 : NH HF NH F HF; HF H F - ; F - 存在酸效应 先求溶液中的 [H ]: ( [ H ])[ H ] [ H ] 解得 [H ]5. mol L - F(H) 5. [ H ] β ( ) [C ][F ] b. gcl 的.8 g(nh ) 的 lgβ 7.05 g NH g(nh ) [ ] [ g(nh) ] g β [ g(nh) ] β [ g ][ NH ] 7.05 [ NH ] [g ][Cl ] >.7 8 > 所以有测定生成.8 8 mol L - d. g(oh) 的.8 NH 的 b.8 5 溶液等体积混合后 溶液中 [OH - ] 浓度为 : [ ] 所以有沉淀生成 5 NH [OH - b ].8 8 mol L - NH 0. [ ] 50 [g ][OH ] (.8 5 ).6 < 所以没有测定生成 7. 计算 gcl 在 0. mol L - NH -0. mol L - NH Cl 缓冲溶液中的溶解度 (g 消耗 NH 的浓度忽略不计 ) 解 : 查表知 gcl 的.8 g(nh ) 的 lgβ.lgβ
16 g(nh ) [ NH ] β [ NH ] β 设 gcl 在 0. mol L - NH -0. mol L - NH Cl 缓冲溶液中的溶解度为 gcl g Cl - [g ][Cl - ] 0. p g(nh ) [ Cl ] 0. g(nh ) mol L - p 8. 计算 CdS 在 ph9.0nh NH 总浓度为 0. mol L - 的缓冲溶液中的溶解度 ( 忽略离子强度和 Cd 的氢氧基络合物的影响 ) 解 : 查表知 CdS 的 H S 的 NH 的 b.8 5 ;Cd 与 NH 络合物的 lgβ 分别为 : [ ] [ OH ] c 0.0 NH 0. mol L - 5 OH.8 [ ] 5 b Cd(NH ) β 5 [ NH ] β [ NH ] β [ NH ] β [ NH ] β [ NH ] β [ NH ] [ ] [ ] ( ). 5 ; β S (H) H β H 设 CdS 在 ph9.0nh NH 总浓度为 0. mol L - 缓冲溶液中溶解度为 7 5 pcd(nh ) S (H). 9 mol L - 9. 考虑生成氢氧基络合物的影响 计算 Zn(OH) 在 ph 的溶液中的溶解度 此时 溶液中 Zn 主要存在形式是什么? 解 : Zn(OH) 的 Zn(OH ) β. 7 Zn [ OH ] β [ OH ] β [ OH ] β [ OH ] 与 OH - 形成络合物的 lgβ 分别为 :. -. ( - ). ( - ) 5.5 ( - ).9 设 Zn(OH) 在 ph 的溶液中的溶解度 7
17 0.g p Zn(OH ). 7 [ OH ] ( ) mol L - 此时溶液中 Zn - 是以 Zn(OH) Zn(OH) 和两种主要存在形式存在 能与 Cl - - 生成 gcl 沉定和 gcl 水 gcl 络合物. 计算 [Cl ]0. mol L - 时 gcl 沉淀的溶解度 ; b.[cl ] 为多大时 gcl 沉淀的溶解度最小? 解 :. 查表知 gcl 的.8 g(cl - - ) 的 lgβ.0lgβ 5.0 设 gcl 沉淀的溶解度为 [ ] [ gcl ] [ gcl ] [g ](β [Cl - ]β [Cl - ] ) p (β [ Cl ] [Cl - ]β [Cl - ] ) g [g ]β [g ][Cl - ]β [g ][Cl - ] p β β [ ] [ Cl ] 当 [Cl ]0. mol L - 时 : Cl mol L - ; 0. d 0 β p 0 d Cl 即 Cl β [ Cl ] b. [ ] [ ] Cl β [ ] 计算下列换算因数. 根据 PbCrO 测定 Cr O ; b. 根据 g P O 7 测定 gso 7HO;.0 mol L - 最小 c. 根据 (NH ) PO 0O 测定 C (PO ) 和 P O 5 ; d. 根据 (C 9 H 6 NO) l 测定 l O (Cr O) 5.99 解 :. F 0. 5 (PbCrO ). ; (gso 7HO) 6.7 b. F.5; (g PO 7).55 [ C (PO) ].8 c. F 0.086; [(NH ) PO O] (PO 5).9 F ; (NH ) PO O 876. [ ] 5 0
18 (l O).96 d. F 0. (C H NO) l 59. [ ] 推导一元弱酸盐的微溶化合物 在下列溶液中溶解度的计算公式. 在强酸溶液中 ; b. 在酸性溶液中和过量沉淀剂 - 存在下 ; c. 在过量 存在下的酸性溶液中 ; d. 在过量络合剂 L 存在下 ( 只形成 L 络合物 ) 的酸性溶液中 解 : 设 的溶度积为 k 溶液酸度为 [H ] 弱酸 H 的离解常数为 k 络合物 L 的累积稳定常数为 β 的溶解度为 :. - [ ] [ ][ ] [ H ] p δ (H) [ H ] p b. - [ ] c c [ ][ ] [ H ] p ; [ H ] p c ; [ H ] δ c c. - [ ] c c c [ ][ ] p c [ H ] p [ H ] c c [ H ] δ (H) ; [ H ] 9
19 d. [ ] - [ ][ ] (L) [ H ] p βc L βc L(H) L [ H ] [ ] L(H) p βc L L(H) [ H ] δ 称取 CC O 和 gc O 纯混合试样 0.60g 在 500 下加热 定量转化为 CCO 和 gco 后为 0.80g. 计算试样中 CC O 和 gc O 的质量分数 ;b. 若在 900 下加热该混合物 定量转化为 CO 和 go 的质量为多少克? 解 :. 分子量 :CC O 8.gC O.gCO 8.CCO 0. CO56.08 go0.0; 设 CC O 和 gc O 的质量分别为 x 和 y: x y x y x 0.78g 解此方程组得 y 0.9g 0.78 CC O % 0% 76.09% 0.60 gc O % 76.09%.9%; b.0.78g 0.9g 0.079g0.0555g0.6g 8... 称取纯 Fe O 和 l O 混合物 0.56g 在加热状态下通氢气 将 Fe O 还原为 Fe 此时 l O 不改变 冷却后称量该混合物为 0.58g 计算试样中 Fe 和 l 的质量分数 解 : 分子量 :Fe O 59.7l O.0Fe55.85l6.98; 设混合物中 Fe O 和 l O 的质量分别为 x 和 y: x y x y x 0.6g 解此方程组得 y 0.6g Fe% %.06% l%.0 0% 0.% 称取含硫的纯有机化合物.0000g 首先用 N O 熔融 使其中的硫定量转化为 50
20 N SO 然后溶解于水 用 BCl 溶液处理 定量转化为 BSO.0890g 计算 :. 有机化 合物中硫的质量分数 ;b. 若有机化合物的摩尔质量为.g mol - 求该有机化合物中 硫原子个数 解 : 分子量 :BSO.9 S.07; % 0%.96%;.9 00 b. 设该有机化合物中含有 x 个硫原子 : x 解得 x 称取 gcl 和 gbr 纯混合物 0.7g 然后用氯气处理 使其中的 gbr 定量转 化为 gcl 若混合物中 gbr 的质量分数为 用氯气处理后 gcl 共多少克? 解 : 分子量 :gcl.gbr87.77;. 0.7 (-60%)0.7 60% g 某试样中约含有 50% 的 BO 用 BSO 重量法测定其准确含量时 其中的 Fe 将 产生共沉淀 若 Fe 共沉淀的量为溶液中 Fe 含量的 5% 那么要想 Fe 共沉淀引起的误差不大于 0.% 试样中 Fe 的含量应少于多少? 已知 BO 5. Fe 解 : 设 Fe 的含量为 x BO 试样的质量为.00g 则经转化处理后可得 BSO 的质 BSO.9 量为 : mbso.00 50%.00 50% 0.76g 5. BO 由于共沉淀的 Fe 经灼烧后转化为 Fe O 从而影响测定 因此应计算产生了多少 Fe O 而不仅仅是以 Fe 形式存在于 BSO 中的量 根据反应计量关系可知 : Fe O mfe O.00 5% x.00 5% x 0. x Fe 由于 Fe 共沉淀引起的相对误差为 : E 0.x 0.% x 0.5% 0.5% 0.76 r BSO Fe O mfe 0. O x 要想误差不大于 0.% 则 m 0.76 BSO 5
第一章 化学反应中的质量关系和能量关系
 第 章酸碱反应和沉淀反应习题参考答案 解 :(1)pHlg (H )1.00 ()0.050mol HOA 溶液中, HOA H OA 平 /(mol ) 0.050 (H ) (OA ) a 1.8 (HOA ) 0.050 (H ) 9.5 mol ph lg (H ).0. 解 :(1)pH 1.00 (H ) 0.mol ph.00 (H ) 0.0mol 等体积混合后 :(H ) (0.mol
第 章酸碱反应和沉淀反应习题参考答案 解 :(1)pHlg (H )1.00 ()0.050mol HOA 溶液中, HOA H OA 平 /(mol ) 0.050 (H ) (OA ) a 1.8 (HOA ) 0.050 (H ) 9.5 mol ph lg (H ).0. 解 :(1)pH 1.00 (H ) 0.mol ph.00 (H ) 0.0mol 等体积混合后 :(H ) (0.mol
<4D F736F F D20B5DACBC4D5C22EB3C1B5EDB5C4D0CEB3C9D3EBB3C1B5EDC6BDBAE2B2E2D1E9CCE2>
 一 选择题 第四章. 沉淀的形成与沉淀平衡测验题 1 AgCl 在 1mol L 1 氨水中比在纯水中的溶解度大 其原因是 ( ) A. 盐效应 ; B. 配位效应 ; C. 酸效应 ; D. 同离子效应 2 已知 AgCl 的 pk sp =9.80 若 0.010mol L 1 NaCl 溶液与 0.020mol L 1 AgNO 3 溶液等体积混 合, 则混合后溶液中 [Ag + ]( 单位
一 选择题 第四章. 沉淀的形成与沉淀平衡测验题 1 AgCl 在 1mol L 1 氨水中比在纯水中的溶解度大 其原因是 ( ) A. 盐效应 ; B. 配位效应 ; C. 酸效应 ; D. 同离子效应 2 已知 AgCl 的 pk sp =9.80 若 0.010mol L 1 NaCl 溶液与 0.020mol L 1 AgNO 3 溶液等体积混 合, 则混合后溶液中 [Ag + ]( 单位
<4D F736F F F696E74202D20B5DABEC5D5C220D6D8C1BFB7D6CEF6B7A82E707074>
 第 9 章重量分析法 Chapter 9 Gravimetric alysis 9. 重量分析法概述 9.. Classificatio of methods used i gravimetric aalysis I ay direct gravimetric aalysis, the costituet beig determied is separated from the other costituets
第 9 章重量分析法 Chapter 9 Gravimetric alysis 9. 重量分析法概述 9.. Classificatio of methods used i gravimetric aalysis I ay direct gravimetric aalysis, the costituet beig determied is separated from the other costituets
 3 3 4 4 3 3 3 1 6 ( n) 85 U 0 9 85 1 90 1 U + n + Kr + 3 n 9 36 0 =1 sp sp 3 sp 14. H + 1 O = H O( ) + 68 NH + 3 O = 3 1 N + 3H O( ) +18 N + 3 H = NH 3 CO( ) + 1 O ( ) = CO ( ) + 67. 6 (1) () (3) (4)
3 3 4 4 3 3 3 1 6 ( n) 85 U 0 9 85 1 90 1 U + n + Kr + 3 n 9 36 0 =1 sp sp 3 sp 14. H + 1 O = H O( ) + 68 NH + 3 O = 3 1 N + 3H O( ) +18 N + 3 H = NH 3 CO( ) + 1 O ( ) = CO ( ) + 67. 6 (1) () (3) (4)
 é SI 12g C = 6 12 = 1 H2( g) + O2( g) H2O( l) + 286kJ ( 1) 2 1 1 H 2( g) + O2( g) H2O( l) H = 286kJ mol ( 2) 2 1 N 2 ( g) + O2( g) NO 2 ( g) 34kJ 2 1 1 N 2 ( g) + O2( g) NO 2 ( g) H = + 34kJ mol 2 1 N
é SI 12g C = 6 12 = 1 H2( g) + O2( g) H2O( l) + 286kJ ( 1) 2 1 1 H 2( g) + O2( g) H2O( l) H = 286kJ mol ( 2) 2 1 N 2 ( g) + O2( g) NO 2 ( g) 34kJ 2 1 1 N 2 ( g) + O2( g) NO 2 ( g) H = + 34kJ mol 2 1 N
中华人民共和国国家标准
 1 1 1.1 1.2 1.3 2 2.1 2.2 3 4 4.1 4.2 5 5.1 5.2 5.3 5.4 6 6.1 6.2 6.3 2 7 7.1 7.2 7.3 7.4 8 9 10 11 3 1 1.1 30% 20% 20% 45-50% 30% 15% 10000 50 5000 2.5 3 100 100 m 2 600 4 5 3000 4 38% 10% 24% 10 0.82t/m
1 1 1.1 1.2 1.3 2 2.1 2.2 3 4 4.1 4.2 5 5.1 5.2 5.3 5.4 6 6.1 6.2 6.3 2 7 7.1 7.2 7.3 7.4 8 9 10 11 3 1 1.1 30% 20% 20% 45-50% 30% 15% 10000 50 5000 2.5 3 100 100 m 2 600 4 5 3000 4 38% 10% 24% 10 0.82t/m
zyk00217zw.PDF
 NH NO N 2H O 4 2 2 2 1 1 N2 + O2 === NO 2 2 /K 1000 1500 1811 2033 8.86 10 5 3.30 10 3 1.14 10 2 2.21 10 2 CaC2 N 2 CaCN 2C 1000 Na 2CO 34CN 2 2NaCN3CO /Pa NH / 1.01 5.05 1.01 3.03 6.06 10 6 10 6 10 7
NH NO N 2H O 4 2 2 2 1 1 N2 + O2 === NO 2 2 /K 1000 1500 1811 2033 8.86 10 5 3.30 10 3 1.14 10 2 2.21 10 2 CaC2 N 2 CaCN 2C 1000 Na 2CO 34CN 2 2NaCN3CO /Pa NH / 1.01 5.05 1.01 3.03 6.06 10 6 10 6 10 7
EXAMINATION RULES
 考 試 規 則 : 1. 競 賽 者 必 須 在 考 試 前 10 分 鐘 到 達 考 場 2. 競 賽 者 不 可 以 攜 帶 任 何 工 具, 但 是 個 人 所 需 要 的 醫 藥 用 品 及 器 具 不 在 此 限 3. 競 賽 者 必 須 坐 在 指 定 的 位 置 4. 在 考 試 開 始 前, 競 賽 者 必 須 檢 查 大 會 提 供 的 文 具 及 任 何 工 具 ( 筆 尺 計
考 試 規 則 : 1. 競 賽 者 必 須 在 考 試 前 10 分 鐘 到 達 考 場 2. 競 賽 者 不 可 以 攜 帶 任 何 工 具, 但 是 個 人 所 需 要 的 醫 藥 用 品 及 器 具 不 在 此 限 3. 競 賽 者 必 須 坐 在 指 定 的 位 置 4. 在 考 試 開 始 前, 競 賽 者 必 須 檢 查 大 會 提 供 的 文 具 及 任 何 工 具 ( 筆 尺 計
SPM-based Nanofabrication and Its Applications
 第五章 沉淀溶解平衡 一 溶度积原理 1 溶度积 Ksp 2 溶度积原理 3 Ksp 的计算 : 热力学方法 ; 电化学方法 ; 溶解度方法 二 沉淀的生成 溶解与转化沉淀的完全度 ; 同离子效应 ; 盐效应生产弱电解质 ; 发生氧还反应 ; 生产络合离子三 分步沉淀 溶解度 : 每 100 克水中溶解的物质的量 ( 克 /100 克水 ) 25 ºC, 100 克水中可溶解 ( 克 ) ZnCl
第五章 沉淀溶解平衡 一 溶度积原理 1 溶度积 Ksp 2 溶度积原理 3 Ksp 的计算 : 热力学方法 ; 电化学方法 ; 溶解度方法 二 沉淀的生成 溶解与转化沉淀的完全度 ; 同离子效应 ; 盐效应生产弱电解质 ; 发生氧还反应 ; 生产络合离子三 分步沉淀 溶解度 : 每 100 克水中溶解的物质的量 ( 克 /100 克水 ) 25 ºC, 100 克水中可溶解 ( 克 ) ZnCl
酸檸檬?鹼檸檬??食物的酸鹼性.doc
 篇 名 : 酸 檸 檬? 鹼 檸 檬? 食 物 的 酸 鹼 性 作 者 : 何 國 維 國 立 埔 里 高 工 化 工 科 二 年 乙 班 指 導 老 師 : 余 志 輝 老 師 壹 前 言 食 物, 是 人 類 每 天 的 能 量 的 來 源, 無 論 酸 甜 苦 辣, 各 式 各 樣 的 食 物 隨 處 可 見, 頗 具 豐 富 性 及 變 化 性, 令 人 食 指 大 動 但 是, 日 前 科
篇 名 : 酸 檸 檬? 鹼 檸 檬? 食 物 的 酸 鹼 性 作 者 : 何 國 維 國 立 埔 里 高 工 化 工 科 二 年 乙 班 指 導 老 師 : 余 志 輝 老 師 壹 前 言 食 物, 是 人 類 每 天 的 能 量 的 來 源, 無 論 酸 甜 苦 辣, 各 式 各 樣 的 食 物 隨 處 可 見, 頗 具 豐 富 性 及 變 化 性, 令 人 食 指 大 動 但 是, 日 前 科
 + 7 1 5, Cl Cl + 4 + 6 HSO4 S S S + 6 + 6 HSO4 S S S 0 + 6 + 4 + S S S S + 7 + KMnO 4 Mn Mn + + + [I ] 0 1M 0 I E Fe3+ / Fe+ ( 0771. ) E 1 /1 ( 0536. ) 3+ 3+ + 3+ Fe I I Fe + I = Fe + I [ Fe ] = [ I ]
+ 7 1 5, Cl Cl + 4 + 6 HSO4 S S S + 6 + 6 HSO4 S S S 0 + 6 + 4 + S S S S + 7 + KMnO 4 Mn Mn + + + [I ] 0 1M 0 I E Fe3+ / Fe+ ( 0771. ) E 1 /1 ( 0536. ) 3+ 3+ + 3+ Fe I I Fe + I = Fe + I [ Fe ] = [ I ]
cm CO Na CO HC NaO H CO SO
 cm CO Na CO HC NaO H CO SO C H Na CO CaCO Na CO CaCO ml mm mm cm cm b a b c d K CO A B C D E F G H F C A D B H G C F A KC O MnO MnO KC O MnO KClO MH NO H SO N H N O H SO NaO H Na O ml Na O O NaO
cm CO Na CO HC NaO H CO SO C H Na CO CaCO Na CO CaCO ml mm mm cm cm b a b c d K CO A B C D E F G H F C A D B H G C F A KC O MnO MnO KC O MnO KClO MH NO H SO N H N O H SO NaO H Na O ml Na O O NaO
<4D6963726F736F667420576F7264202D20B2C4A44BB3B92020B8ADADB1AC49AACEAD6EBBE22E646F63>
 第 八 章 葉 面 施 肥 要 領 植 物 葉 片 兩 面 有 很 多 氣 孔, 可 以 吸 收 噴 在 葉 片 上 溶 液 狀 態 的 肥 料, 也 可 直 接 透 過 葉 片 角 質 層 細 胞 壁 和 原 形 質 膜 而 進 入 細 胞 內 部, 這 就 是 葉 面 施 肥 葉 面 施 肥 為 土 壤 施 肥 以 外, 補 充 養 分 的 一 個 經 濟 有 效 的 辦 法 葉 面 肥 料 一
第 八 章 葉 面 施 肥 要 領 植 物 葉 片 兩 面 有 很 多 氣 孔, 可 以 吸 收 噴 在 葉 片 上 溶 液 狀 態 的 肥 料, 也 可 直 接 透 過 葉 片 角 質 層 細 胞 壁 和 原 形 質 膜 而 進 入 細 胞 內 部, 這 就 是 葉 面 施 肥 葉 面 施 肥 為 土 壤 施 肥 以 外, 補 充 養 分 的 一 個 經 濟 有 效 的 辦 法 葉 面 肥 料 一
的 浓 度 为 0.1125 mol/ L. 7. 痕 量 Au 3+ 的 溶 液 在 盐 酸 介 质 中 能 被 阴 离 子 交 换 树 脂 交 换 而 得 到 富 集, 这 时 Au 3+ 是 以 AuCl 4 - 形 式 被 交 换 到 树 脂 上 去 的 8. 将 Fe 3+ 和 Al 3+
 二 填 空 题 原 子 吸 收 1. 空 心 阴 极 灯 是 一 种 ( 锐 性 ) 光 源, 它 的 发 射 光 谱 具 有 ( 谱 线 窄 强 度 大 ) 特 点 当 灯 电 流 升 高 时, 由 于 ( 自 吸 变 宽 热 变 宽 ) 的 影 响, 导 致 谱 线 轮 廓 ( 变 宽 ), 测 量 灵 敏 度 ( 下 降 ), 工 作 曲 线 ( 线 性 关 系 变 差 ), 灯 寿 命 (
二 填 空 题 原 子 吸 收 1. 空 心 阴 极 灯 是 一 种 ( 锐 性 ) 光 源, 它 的 发 射 光 谱 具 有 ( 谱 线 窄 强 度 大 ) 特 点 当 灯 电 流 升 高 时, 由 于 ( 自 吸 变 宽 热 变 宽 ) 的 影 响, 导 致 谱 线 轮 廓 ( 变 宽 ), 测 量 灵 敏 度 ( 下 降 ), 工 作 曲 线 ( 线 性 关 系 变 差 ), 灯 寿 命 (
( ) 1. HCO - 3 ( OH - ) ( 1.3) 2. ( 1.4) -64-
 -63- (antagonism) Berger(1962) 21 11 3 9 ph 0.1% 0.1% 0.1mg/kg ( ) 1. HCO - 3 ( OH - ) ( 1.3) 2. ( 1.4) -64- ( 1.5) 3. CO 2 +K + Ca 2+ + N 4 1.3 H+ K + Ca 2+ NH 4+ +4 H 2 O CO 2 +HCO - 3 K + K + HCO -
-63- (antagonism) Berger(1962) 21 11 3 9 ph 0.1% 0.1% 0.1mg/kg ( ) 1. HCO - 3 ( OH - ) ( 1.3) 2. ( 1.4) -64- ( 1.5) 3. CO 2 +K + Ca 2+ + N 4 1.3 H+ K + Ca 2+ NH 4+ +4 H 2 O CO 2 +HCO - 3 K + K + HCO -
1 { ph
 !!!!!!!!!!!!!!!!!!!!!!!!!!! 1 1!!!!!!!!!!!!!!!!!!!!!! 1 2!!!!!!!!!!!!!!!!!!!!!!!!!! 7 3!!!!!!!!!!!!!!!!!!!!!!!!! 15 4!!!!!!!!!!!!!!!!!!!!!!!!!!! 21!!!!!!!!!!!!!!!!!!!!!!!!!!!! 30!!!!!!!!!!!!!!!!!!!!!!!
!!!!!!!!!!!!!!!!!!!!!!!!!!! 1 1!!!!!!!!!!!!!!!!!!!!!! 1 2!!!!!!!!!!!!!!!!!!!!!!!!!! 7 3!!!!!!!!!!!!!!!!!!!!!!!!! 15 4!!!!!!!!!!!!!!!!!!!!!!!!!!! 21!!!!!!!!!!!!!!!!!!!!!!!!!!!! 30!!!!!!!!!!!!!!!!!!!!!!!
á à
 á à + 2- NH 4 SO4 1 1 2 1 3 1 14 12 6 13 6 6 12 6 2 1 3 1 235 92 18 8 131 53 12 6 1 16 8 12 1 12 6 1 1 2 1 1 1 2 1 6 1 1 6 10 14 p d f 3 5 7 p d f 0 0 0 p d f NH + 4 A werner 1866 1919
á à + 2- NH 4 SO4 1 1 2 1 3 1 14 12 6 13 6 6 12 6 2 1 3 1 235 92 18 8 131 53 12 6 1 16 8 12 1 12 6 1 1 2 1 1 1 2 1 6 1 1 6 10 14 p d f 3 5 7 p d f 0 0 0 p d f NH + 4 A werner 1866 1919
FeS 2 在 晶 體 中 為 Fe 2+ S 22ˉ 故 選 (A) 4. 下 圖 代 表 某 反 應 座 標 圖, 下 列 敘 述 何 者 錯 誤? (A) B - A 為 活 化 能 (B) A - C 為 反 應 熱 (C) B 代 表 活 化 錯 合 物 的 相 對 能 量 (D) B -
 1. 在 含 有 0.050 M MgCl 2 及 1.0 M 氨 的 1.00 升 水 溶 液 中, 頇 加 入 多 少 克 的 氯 化 銨, 才 能 使 鎂 的 鹽 類 不 沉 澱? Mg(OH) 2 的 K sp 為 1.5 10-11,NH 3 的 K b 為 1.8 10-5 (A) 50 g (B) 56 g (C) 5.0 g (D) 4.3 g 答 案 :(B) [Mg 2+ ] =
1. 在 含 有 0.050 M MgCl 2 及 1.0 M 氨 的 1.00 升 水 溶 液 中, 頇 加 入 多 少 克 的 氯 化 銨, 才 能 使 鎂 的 鹽 類 不 沉 澱? Mg(OH) 2 的 K sp 為 1.5 10-11,NH 3 的 K b 為 1.8 10-5 (A) 50 g (B) 56 g (C) 5.0 g (D) 4.3 g 答 案 :(B) [Mg 2+ ] =
 ö ❾ 1 F2 H 2O 2HF O2 2 ❹ Å Å Å Å Å Å Å y 1.3470x 0.3547 y mg/ L 1 2 mmol C V + C E E S V V V 0 0 0 = f E 0 lg + j + 0 ä
ö ❾ 1 F2 H 2O 2HF O2 2 ❹ Å Å Å Å Å Å Å y 1.3470x 0.3547 y mg/ L 1 2 mmol C V + C E E S V V V 0 0 0 = f E 0 lg + j + 0 ä
 ö ❾ 1 F2 H 2O 2HF O2 2 ❹ Å Å Å Å Å Å Å y 1.3470x 0.3547 y mg/ L 1 2 mmol C V + C E E S V V V 0 0 0 = f E 0 lg + j + 0 ä
ö ❾ 1 F2 H 2O 2HF O2 2 ❹ Å Å Å Å Å Å Å y 1.3470x 0.3547 y mg/ L 1 2 mmol C V + C E E S V V V 0 0 0 = f E 0 lg + j + 0 ä
校园之星
 CO Na HCO AL SO Na SO Al O H SiO C H O CO H O CH CH Cl KClO KCl O P O P O MgCO MgCO AgI Fe O H gs PbS PbCO Pb O H H S PbS CO H O PbS H O PbSO H O CuS Cu S CuCO Ca O H CoCl H O CoCl H O born to
CO Na HCO AL SO Na SO Al O H SiO C H O CO H O CH CH Cl KClO KCl O P O P O MgCO MgCO AgI Fe O H gs PbS PbCO Pb O H H S PbS CO H O PbS H O PbSO H O CuS Cu S CuCO Ca O H CoCl H O CoCl H O born to
第九章 元素概论
 1. 2. 5 1. 2. 3. 4. p393:467p394:915p395: 16 12.1 VA ns 2 np 3 1. NH 4 ClNaNO 2 NH 4 NO 2 NaCl NH 4 NO 2 N22H 2 O 2. N 2 COP 351 1. N 2 3H 2 2NH ( ) 3 2NH 4 ClCa(OH) 2 CaCl22NH 3 2H 2 O 2NH 3 NH 4 NH 2
1. 2. 5 1. 2. 3. 4. p393:467p394:915p395: 16 12.1 VA ns 2 np 3 1. NH 4 ClNaNO 2 NH 4 NO 2 NaCl NH 4 NO 2 N22H 2 O 2. N 2 COP 351 1. N 2 3H 2 2NH ( ) 3 2NH 4 ClCa(OH) 2 CaCl22NH 3 2H 2 O 2NH 3 NH 4 NH 2
untitled
 [] [] [] 15.1 1 2 Cu 2+ 2e=Cu Zn 2+ 2e=Zn 2H + 2eH 2 Cu2e=Cu 2+ Ni2e=Ni 2+ 2OH 2e=H 2 O 1/2O 2 2Cl 2e=Cl 2 1 1. 2. 15.2 z+ ze l H 3 O + e 2 1 H 2 O 2a H 2 O e 2 1 OH 2b O 2 2H 2 O 4e4OH 3 z+ ze 4 z+ (zh)e
[] [] [] 15.1 1 2 Cu 2+ 2e=Cu Zn 2+ 2e=Zn 2H + 2eH 2 Cu2e=Cu 2+ Ni2e=Ni 2+ 2OH 2e=H 2 O 1/2O 2 2Cl 2e=Cl 2 1 1. 2. 15.2 z+ ze l H 3 O + e 2 1 H 2 O 2a H 2 O e 2 1 OH 2b O 2 2H 2 O 4e4OH 3 z+ ze 4 z+ (zh)e
<4D6963726F736F667420576F7264202D203130332D322DA57CA7DEA447B14D2DBDC3A5CDBB50C540B27AC3FEB14DA440B8D5C344>
 103- 衛 生 與 護 理 類 專 業 科 目 ( 一 ) 1. 有 關 原 始 生 物 起 源 的 演 化 大 方 向 中, 下 列 何 者 正 確? (A) 由 好 氧 厭 氧 (B) 由 構 造 複 雜 構 造 簡 單 (C) 由 異 營 自 營 (D) 由 多 細 胞 單 細 胞. 植 物 的 莖 頂 及 根 尖 細 胞 利 用 能 量 進 行 細 胞 分 裂, 與 下 列 何 種 生 命
103- 衛 生 與 護 理 類 專 業 科 目 ( 一 ) 1. 有 關 原 始 生 物 起 源 的 演 化 大 方 向 中, 下 列 何 者 正 確? (A) 由 好 氧 厭 氧 (B) 由 構 造 複 雜 構 造 簡 單 (C) 由 異 營 自 營 (D) 由 多 細 胞 單 細 胞. 植 物 的 莖 頂 及 根 尖 細 胞 利 用 能 量 進 行 細 胞 分 裂, 與 下 列 何 種 生 命
蔬菜有機栽培
 1 2 (1) (2) (3) (4) (ph ) ph 5.5~7.0 (ph 6.0 ) (ph 7.5 ) 8.0 a. ( ) b. ( ) c. 3 (
1 2 (1) (2) (3) (4) (ph ) ph 5.5~7.0 (ph 6.0 ) (ph 7.5 ) 8.0 a. ( ) b. ( ) c. 3 (
物質科學_化學篇
 物 質 科 學 化 學 篇 ( 上 ) 講 義 編 者 : 陳 義 忠 55 物 質 科 學 _ 化 學 篇 ( 上 ) 第 四 章 溶 液 4-1 溶 液 的 性 質 : 1. 溶 液 : (1) 由 兩 種 或 兩 種 以 上 的 純 物 質 混 合 而 成 的 均 勻 混 合 物, 稱 為 溶 液 包 含 固 態 液 態 及 氣 態 () 溶 液 由 溶 質 和 溶 劑 所 組 成 在 形 成
物 質 科 學 化 學 篇 ( 上 ) 講 義 編 者 : 陳 義 忠 55 物 質 科 學 _ 化 學 篇 ( 上 ) 第 四 章 溶 液 4-1 溶 液 的 性 質 : 1. 溶 液 : (1) 由 兩 種 或 兩 種 以 上 的 純 物 質 混 合 而 成 的 均 勻 混 合 物, 稱 為 溶 液 包 含 固 態 液 態 及 氣 態 () 溶 液 由 溶 質 和 溶 劑 所 組 成 在 形 成
Microsoft Word - 24.doc
 閱 讀 (1) 楊 桃 毒 素 過 去 有 許 多 糖 尿 病 或 高 血 壓 患 者 吃 過 新 鮮 楊 桃 或 楊 桃 汁 後, 出 現 嘔 吐 頭 暈 意 識 不 清 等 症 狀, 研 判 因 為 他 們 腎 功 能 不 佳, 無 法 排 出 楊 桃 中 不 明 的 中 毒 成 分 楊 桃 中 的 不 明 成 分 可 能 導 致 部 分 特 殊 體 質 的 尿 毒 症 病 患, 出 現 神 經
閱 讀 (1) 楊 桃 毒 素 過 去 有 許 多 糖 尿 病 或 高 血 壓 患 者 吃 過 新 鮮 楊 桃 或 楊 桃 汁 後, 出 現 嘔 吐 頭 暈 意 識 不 清 等 症 狀, 研 判 因 為 他 們 腎 功 能 不 佳, 無 法 排 出 楊 桃 中 不 明 的 中 毒 成 分 楊 桃 中 的 不 明 成 分 可 能 導 致 部 分 特 殊 體 質 的 尿 毒 症 病 患, 出 現 神 經
<4D6963726F736F667420576F7264202D20B5DAC1F9D5C22020BBD2B7D6BCB0BCB8D6D6D6D8D2AABFF3CEEFD4AACBD8BAACC1BFB5C4B2E2B6A8A3A8B8C4B9FDA3A92E646F63>
 第 六 章 灰 分 及 几 种 重 要 矿 物 元 素 含 量 的 测 定 第 一 节 灰 分 的 测 定 一 概 述 食 品 的 组 成 十 分 复 杂, 除 含 有 大 量 有 机 物 质 外, 还 含 有 丰 富 的 无 机 成 分, 这 些 无 机 成 分 包 括 人 体 必 须 的 无 机 盐 ( 或 称 矿 物 质 ), 其 中 含 量 较 多 的 有 Ca Mg K Na S P C1
第 六 章 灰 分 及 几 种 重 要 矿 物 元 素 含 量 的 测 定 第 一 节 灰 分 的 测 定 一 概 述 食 品 的 组 成 十 分 复 杂, 除 含 有 大 量 有 机 物 质 外, 还 含 有 丰 富 的 无 机 成 分, 这 些 无 机 成 分 包 括 人 体 必 须 的 无 机 盐 ( 或 称 矿 物 质 ), 其 中 含 量 较 多 的 有 Ca Mg K Na S P C1
基 礎 化 學 ( 一 ) 講 義 目 次 第 1 章 物 質 的 組 成 1 1 物 質 的 分 類 1 1 2 原 子 與 分 子 16 1 3 原 子 量 與 分 子 量 31 1 4 溶 液 48 實 驗 二 硝 酸 鉀 的 溶 解 與 結 晶 74 國 戰 大 考 試 題 78 實 驗 相
 內 容 由 蔡 明 倫 老 師 和 李 雅 婷 老 師 編 纂 基 礎 化 學 ( 一 ) 講 義 第 1 章 物 質 的 組 成 班 級 : 拉 瓦 節 和 其 使 用 的 實 驗 儀 器 座 號 : 姓 名 : 基 礎 化 學 ( 一 ) 講 義 目 次 第 1 章 物 質 的 組 成 1 1 物 質 的 分 類 1 1 2 原 子 與 分 子 16 1 3 原 子 量 與 分 子 量 31 1
內 容 由 蔡 明 倫 老 師 和 李 雅 婷 老 師 編 纂 基 礎 化 學 ( 一 ) 講 義 第 1 章 物 質 的 組 成 班 級 : 拉 瓦 節 和 其 使 用 的 實 驗 儀 器 座 號 : 姓 名 : 基 礎 化 學 ( 一 ) 講 義 目 次 第 1 章 物 質 的 組 成 1 1 物 質 的 分 類 1 1 2 原 子 與 分 子 16 1 3 原 子 量 與 分 子 量 31 1
 - 2-2- HCO HPO SO 3 4 4 P P R P QR Q R Q + - - H HCO3 - HCO 3 - - Cl HCO 3 HCO - 3 - HCO - 3 - HCO 3 - = 100 2- SO 4 - H 2 PO 4 HPO 4 - HPO 4 2- Na
- 2-2- HCO HPO SO 3 4 4 P P R P QR Q R Q + - - H HCO3 - HCO 3 - - Cl HCO 3 HCO - 3 - HCO - 3 - HCO 3 - = 100 2- SO 4 - H 2 PO 4 HPO 4 - HPO 4 2- Na
试卷
 玉 溪 一 中 高 2015 届 高 三 上 学 期 期 中 考 化 学 试 题 相 对 原 子 质 量 : N-14,Na-23,Cl-35.5, Cu-64 说 明 : 测 试 时 间 120 分 钟, 满 分 100 分 第 I 卷 ( 选 择 题 共 46 分 ) 一 选 择 题 ( 本 题 包 括 23 小 题, 每 小 题 2 分, 共 46 分 每 小 题 只 有 一 个... 选 项
玉 溪 一 中 高 2015 届 高 三 上 学 期 期 中 考 化 学 试 题 相 对 原 子 质 量 : N-14,Na-23,Cl-35.5, Cu-64 说 明 : 测 试 时 间 120 分 钟, 满 分 100 分 第 I 卷 ( 选 择 题 共 46 分 ) 一 选 择 题 ( 本 题 包 括 23 小 题, 每 小 题 2 分, 共 46 分 每 小 题 只 有 一 个... 选 项
 70 1999 4 f x = Msinω x + ϕ ω 0 [a b] f a = -M f b = M g x = Mcos ω x + ϕ [a b] [ ] A B C M D - M ωα + ϕ = kπ π ωb + ϕ = kπ + π k Z ωx + ϕ [ kπ π kπ]( k Z) g π (x) ωx + ϕ [ kπ kπ + ]( k Z) g x ωx +
70 1999 4 f x = Msinω x + ϕ ω 0 [a b] f a = -M f b = M g x = Mcos ω x + ϕ [a b] [ ] A B C M D - M ωα + ϕ = kπ π ωb + ϕ = kπ + π k Z ωx + ϕ [ kπ π kπ]( k Z) g π (x) ωx + ϕ [ kπ kπ + ]( k Z) g x ωx +
Ps22Pdf
 1 9 9 9 ( ) 063,, :,,,,,,,,,, ( CIP ) /. - :, 1999. 2 ISBN7 113 03209 5.... N 0 CIP ( 98) 198 : : : ( 100054, 8 ) : : : : 787 1092 1/ 16 : 11. 25 : 280 : 1999 3 1 1999 3 1 : 1 5000 : ISBN 7 113 03209 5/
1 9 9 9 ( ) 063,, :,,,,,,,,,, ( CIP ) /. - :, 1999. 2 ISBN7 113 03209 5.... N 0 CIP ( 98) 198 : : : ( 100054, 8 ) : : : : 787 1092 1/ 16 : 11. 25 : 280 : 1999 3 1 1999 3 1 : 1 5000 : ISBN 7 113 03209 5/
( ) 63 ( ) 68 ( ) 72 ( ) 77 ( ) 85 ( ) 91 ( ) ( ) 98 ( ) 103 ( ) 107 ( ) 111 ( ) 114 ( ) 117 ( ) 121 ( ) 125 ( ) 127 ( ) ( ) 133 ( ) 139
 1 ( ) 1 ( ) 2 ( ) 7 ( ) 9 ( ) 10 16 ( ) 16 ( ) 17 ( ) 19 ( ) 23 ( ) 25 ( ) 26 30 ( ) 30 ( ) 46 50 ( ) 50 ( ) 52 1 ( ) 63 ( ) 68 ( ) 72 ( ) 77 ( ) 85 ( ) 91 ( ) 94 98 ( ) 98 ( ) 103 ( ) 107 ( ) 111 ( )
1 ( ) 1 ( ) 2 ( ) 7 ( ) 9 ( ) 10 16 ( ) 16 ( ) 17 ( ) 19 ( ) 23 ( ) 25 ( ) 26 30 ( ) 30 ( ) 46 50 ( ) 50 ( ) 52 1 ( ) 63 ( ) 68 ( ) 72 ( ) 77 ( ) 85 ( ) 91 ( ) 94 98 ( ) 98 ( ) 103 ( ) 107 ( ) 111 ( )
zyk00124zw.PDF
 A B=AB( ) AB=AB( ) 4P 50 2 === 2P 2 O 5 2KClO 3 2KCl 3O 2 NH 3 H 2 O CO 2 =NH 4 HCO 3 2KMnO 4 K 2 MnO 4 MnO 2 O 2 CO CO 2 ( ) 1.250 / 1.977 / 1 1 1 0.02 2CO O2 2CO 2 CO CuO Cu CO 2 CO 2 C 2CO Ca(OH) 2
A B=AB( ) AB=AB( ) 4P 50 2 === 2P 2 O 5 2KClO 3 2KCl 3O 2 NH 3 H 2 O CO 2 =NH 4 HCO 3 2KMnO 4 K 2 MnO 4 MnO 2 O 2 CO CO 2 ( ) 1.250 / 1.977 / 1 1 1 0.02 2CO O2 2CO 2 CO CuO Cu CO 2 CO 2 C 2CO Ca(OH) 2
煤 炭 学 报 仪器与药品 黏土矿物的提纯 黏土样品的制备 红外光谱 分析 射线衍射 分析 射线光电子能谱 分析
 张明青 刘炯天 单爱琴 刘汉湖 为了深刻认识煤泥水中 同黏土矿物颗粒之间的相互作用 笔者用 溶液在不同 值条件下分别同高岭土和蒙脱土作用 测定黏土作用前后的 射线衍射 红外光谱和 射线光电子能谱 实验证实了在 溶液中 在黏土表面以静电形式吸附 在 溶液中 以 沉淀和静电形式吸附 此外 在 以上的溶液中还可能存在一 羟基络合吸附形式 提出了 沉淀吸附和一羟基络合吸附的吸附过程模式 黏土颗粒表面的 沉淀使颗粒间形成的非选择性
张明青 刘炯天 单爱琴 刘汉湖 为了深刻认识煤泥水中 同黏土矿物颗粒之间的相互作用 笔者用 溶液在不同 值条件下分别同高岭土和蒙脱土作用 测定黏土作用前后的 射线衍射 红外光谱和 射线光电子能谱 实验证实了在 溶液中 在黏土表面以静电形式吸附 在 溶液中 以 沉淀和静电形式吸附 此外 在 以上的溶液中还可能存在一 羟基络合吸附形式 提出了 沉淀吸附和一羟基络合吸附的吸附过程模式 黏土颗粒表面的 沉淀使颗粒间形成的非选择性
分 的 理 解 和 把 握, 对 基 础 知 识 多 回 顾 多 记 忆 北 京 新 东 方 学 校 优 能 中 学 高 中 理 综 项 目 3. 流 式 细 胞 仪 可 根 据 细 胞 中 DNA 含 量 的 不 同 对 细 胞 分 别 计 数 研 究 者 用 某 抗 癌 药 物 处 理 体 外
 北 京 市 2015 年 高 考 理 综 试 题 逐 题 解 析 北 京 新 东 方 优 能 中 学 高 中 理 综 项 目 1. 乙 肝 疫 苗 的 有 效 成 分 是 乙 肝 病 毒 的 一 种 抗 原, 接 种 该 疫 苗 后, 人 体 会 产 生 相 应 抗 体 该 抗 体 A. 由 T 淋 巴 细 胞 产 生 B. 可 与 多 种 抗 原 结 合 C. 可 裂 解 乙 肝 病 毒 D. 可
北 京 市 2015 年 高 考 理 综 试 题 逐 题 解 析 北 京 新 东 方 优 能 中 学 高 中 理 综 项 目 1. 乙 肝 疫 苗 的 有 效 成 分 是 乙 肝 病 毒 的 一 种 抗 原, 接 种 该 疫 苗 后, 人 体 会 产 生 相 应 抗 体 该 抗 体 A. 由 T 淋 巴 细 胞 产 生 B. 可 与 多 种 抗 原 结 合 C. 可 裂 解 乙 肝 病 毒 D. 可
YYHX.mps
 第 七 章 配 位 化 合 物 和 生 物 元 素 自 然 界 有 一 类 组 成 较 为 复 杂, 在 理 论 上 和 应 用 上 都 十 分 重 要 的 化 合 物, 这 类 化 合 物 的 核 心 部 分 是 以 配 位 键 相 连, 故 称 为 配 位 化 合 物, 简 称 配 合 物 近 几 十 年 来, 随 着 科 学 的 发 展 近 代 物 理 仪 器 的 涌 现 和 实 验 技 术
第 七 章 配 位 化 合 物 和 生 物 元 素 自 然 界 有 一 类 组 成 较 为 复 杂, 在 理 论 上 和 应 用 上 都 十 分 重 要 的 化 合 物, 这 类 化 合 物 的 核 心 部 分 是 以 配 位 键 相 连, 故 称 为 配 位 化 合 物, 简 称 配 合 物 近 几 十 年 来, 随 着 科 学 的 发 展 近 代 物 理 仪 器 的 涌 现 和 实 验 技 术
Microsoft Word - Z8I11A0-102.doc
 自 然 考 科 學 測 試 題 關 鍵 解 析 前 言 物 理 科 今 年 自 然 科 考 題 共 68 題, 其 中 物 理 科 占 了 17 題, 今 年 的 題 目 難 度 屬 中 偏 易, 考 題 分 配 十 分 平 均 由 於 是 新 課 綱 第 一 次 學 測, 所 以 新 的 內 容 大 致 上 均 入 題, 大 都 為 物 理 科 普 知 識 就 算 是 第 二 部 分 的 考 題,
自 然 考 科 學 測 試 題 關 鍵 解 析 前 言 物 理 科 今 年 自 然 科 考 題 共 68 題, 其 中 物 理 科 占 了 17 題, 今 年 的 題 目 難 度 屬 中 偏 易, 考 題 分 配 十 分 平 均 由 於 是 新 課 綱 第 一 次 學 測, 所 以 新 的 內 容 大 致 上 均 入 題, 大 都 為 物 理 科 普 知 識 就 算 是 第 二 部 分 的 考 題,
雅思写作应试教程(终稿).doc
 CIP ) /. :,2001.8 ( : 2) ISBN 7-5308 - 3032-3...- TV - 092 CIP ( 2001) 11633 : : : : 189 3 000 20 ( 0 22 ) 2730 631 4 * 787 10 92 1/ 16 2 4. 75 10 392 0 00 2 001 8 1 200 1 8 1 : 11 00 0 : 88. 00 1 8 8
CIP ) /. :,2001.8 ( : 2) ISBN 7-5308 - 3032-3...- TV - 092 CIP ( 2001) 11633 : : : : 189 3 000 20 ( 0 22 ) 2730 631 4 * 787 10 92 1/ 16 2 4. 75 10 392 0 00 2 001 8 1 200 1 8 1 : 11 00 0 : 88. 00 1 8 8
 Fe O + 3CO = 2Fe + 3CO 2 3 2 160 256 1500 x 160 1500 = 2 56 x 2 = 56 1500 x 160 = 1050 x x 100 12 38 12 100 38 316 = = =. x x 1000 37 2 137 2 37 2 1000 137 2 271 = = =.... 36 100 40 100 40 36
Fe O + 3CO = 2Fe + 3CO 2 3 2 160 256 1500 x 160 1500 = 2 56 x 2 = 56 1500 x 160 = 1050 x x 100 12 38 12 100 38 316 = = =. x x 1000 37 2 137 2 37 2 1000 137 2 271 = = =.... 36 100 40 100 40 36
PowerPoint 演示文稿
 基础化学实验 基础化学实验中心 山东省省级实验教学示范中心 无机化学实验 电离平衡和沉淀反应 一 实验目的 1 掌握同离子效应对离解平衡的影响 2 了解盐类的水解和影响盐类水解的因素 3 学习缓冲溶液的配制并了解其缓冲作用 4 了解沉淀生成和溶解的条件及分步沉淀和沉淀的转化 二 实验原理 1. 同离子效应 弱酸或弱碱溶液达到解离平衡时, 若加入与弱酸或弱碱具有相同离子的易溶强电解质时, 解离平衡发生秱动,
基础化学实验 基础化学实验中心 山东省省级实验教学示范中心 无机化学实验 电离平衡和沉淀反应 一 实验目的 1 掌握同离子效应对离解平衡的影响 2 了解盐类的水解和影响盐类水解的因素 3 学习缓冲溶液的配制并了解其缓冲作用 4 了解沉淀生成和溶解的条件及分步沉淀和沉淀的转化 二 实验原理 1. 同离子效应 弱酸或弱碱溶液达到解离平衡时, 若加入与弱酸或弱碱具有相同离子的易溶强电解质时, 解离平衡发生秱动,
Microsoft PowerPoint - 预习07络合之一.pptx
 第 4 章络合滴定法 4.1 概述 4.2 络合平衡 43 4.3 络合滴定基本原理 44 4.4 混合离子的选择性滴定 45 4.5 络合滴定的方式和应用 1 41 4.1 概述 H 3 N NH 3 常见的无机络合剂 : NH,Cl -,CN -,F -,OH - 3 H 3 N Cu 2+ NH 3 2+ 2+ 3 3 1 2+ 2+ 3 2+ 3 3 2 2 3 2 3 3 3 3 2+ 2+
第 4 章络合滴定法 4.1 概述 4.2 络合平衡 43 4.3 络合滴定基本原理 44 4.4 混合离子的选择性滴定 45 4.5 络合滴定的方式和应用 1 41 4.1 概述 H 3 N NH 3 常见的无机络合剂 : NH,Cl -,CN -,F -,OH - 3 H 3 N Cu 2+ NH 3 2+ 2+ 3 3 1 2+ 2+ 3 2+ 3 3 2 2 3 2 3 3 3 3 2+ 2+
 MnO - 4 MnO 2-2+ MnO Mn - MnO MnO 4 4 2 CH2 = CH2 + Br2 BrH2C CH2Br CaS + 2H O = Ca( OH) + H S 2 2 2 Ca P + 6H O = 3Ca( OH) + 2PH 3 2 2 2 3 Ca As + 6H O = 3Ca( OH) + 2AsH 3 2 2 2 3 k Cr O + 4H SO + 3H
MnO - 4 MnO 2-2+ MnO Mn - MnO MnO 4 4 2 CH2 = CH2 + Br2 BrH2C CH2Br CaS + 2H O = Ca( OH) + H S 2 2 2 Ca P + 6H O = 3Ca( OH) + 2PH 3 2 2 2 3 Ca As + 6H O = 3Ca( OH) + 2AsH 3 2 2 2 3 k Cr O + 4H SO + 3H
厨 房 垃 圾 D. 其 他 垃 圾 9.( 1 分 )(2015 西 城 区 一 模 )PM2.5 是 造 成 雾 霾 天 气 的 元 凶 之 一, 下 列 做 法 不 会 增 加 空 气 中 的 PM2.5 的 是 ( ) A. 焚 烧 秸 杆 B. 植 树 造 林 C. 燃 放 鞭 炮 D.
 2015 年 北 京 市 西 城 区 中 考 化 学 一 模 试 卷 一 第 一 部 分 选 择 题 ( 每 题 1 分, 每 小 题 只 有 一 个 选 项 符 合 题 意 ) 1.( 1 分 )(2015 西 城 区 一 模 ) 下 列 变 化 属 于 物 理 变 化 的 是 ( ) A. 冰 雪 融 化 B. 木 柴 燃 烧 C. 白 磷 自 燃 D. 食 物 变 质 2.( 1 分 )(2015
2015 年 北 京 市 西 城 区 中 考 化 学 一 模 试 卷 一 第 一 部 分 选 择 题 ( 每 题 1 分, 每 小 题 只 有 一 个 选 项 符 合 题 意 ) 1.( 1 分 )(2015 西 城 区 一 模 ) 下 列 变 化 属 于 物 理 变 化 的 是 ( ) A. 冰 雪 融 化 B. 木 柴 燃 烧 C. 白 磷 自 燃 D. 食 物 变 质 2.( 1 分 )(2015
试卷
 严 州 中 学 015 届 高 三 4 月 阶 段 测 试 理 科 综 合 试 卷 本 试 卷 分 第 Ⅰ 卷 ( 选 择 题 ) 和 第 Ⅱ 卷 ( 综 合 题 ) 两 部 分 满 分 300 分 考 试 时 间 150 分 钟 可 能 用 到 的 相 对 原 子 质 量 :H-1 C-1 N-14 O-16 Al-7 S-3 Cl-35.5 K-39 Fe-56 Cu-64 Ba-137 第 Ι
严 州 中 学 015 届 高 三 4 月 阶 段 测 试 理 科 综 合 试 卷 本 试 卷 分 第 Ⅰ 卷 ( 选 择 题 ) 和 第 Ⅱ 卷 ( 综 合 题 ) 两 部 分 满 分 300 分 考 试 时 间 150 分 钟 可 能 用 到 的 相 对 原 子 质 量 :H-1 C-1 N-14 O-16 Al-7 S-3 Cl-35.5 K-39 Fe-56 Cu-64 Ba-137 第 Ι
1 Cu S CuFeS Cu O Cu (OH ) CO 3 Ag S AgCl Cu (I) FeS,CuCO 3.Cu(OH),Cu (I) S ( ) ( ) 76.3% 6
 1 Cu S CuFeS Cu O Cu (OH ) CO 3 Ag S AgCl Cu (I) FeS,CuCO 3.Cu(OH),Cu (I) S ( ) ( ) 76.3% 6 1 1 Cu Au (n-1)d 10 ns 1 1 3 1 1 3 IA IIA IB IIB s 1 IB IA ds 18 IA IIA 8 3 Cu Au 4 1 ZnS ZnCO 3 ( )HgS 3 4 1
1 Cu S CuFeS Cu O Cu (OH ) CO 3 Ag S AgCl Cu (I) FeS,CuCO 3.Cu(OH),Cu (I) S ( ) ( ) 76.3% 6 1 1 Cu Au (n-1)d 10 ns 1 1 3 1 1 3 IA IIA IB IIB s 1 IB IA ds 18 IA IIA 8 3 Cu Au 4 1 ZnS ZnCO 3 ( )HgS 3 4 1
tbjxD219zw.PDF
 nm 1nm=10-9m CO 2 CO 2 1 1 A+B=AB 2H + O 2H O 2 2 2 AB=A+B A+BC=AC+B MnO 2 2KClO3 2KCl3O2 Zn+2HCl==ZnCl +H AB+CD=AD+CB NaOH+HC==NaCl+H O 1-2 S + O2 SO2 CuO + H Cu + H O 2 2 2 3 2Fe + 3CO 2 Fe O +
nm 1nm=10-9m CO 2 CO 2 1 1 A+B=AB 2H + O 2H O 2 2 2 AB=A+B A+BC=AC+B MnO 2 2KClO3 2KCl3O2 Zn+2HCl==ZnCl +H AB+CD=AD+CB NaOH+HC==NaCl+H O 1-2 S + O2 SO2 CuO + H Cu + H O 2 2 2 3 2Fe + 3CO 2 Fe O +
 1 cal = 4.18 J N 0 = 6.02 10 : 1.00 : 12.0 : 14.0 : 16.0 : 32.0 23 1 40 2 1. (A) (B) (C) (D) (E) (C) (A) ( ) (B) ( ) (D) (NaI KIO 3 ) (E) ( Ca 2+ Mg 2+ Fe 2+ ) (C) 1 2 3 75 6 (Ga 29.8 2403 ) 310 K 1.3
1 cal = 4.18 J N 0 = 6.02 10 : 1.00 : 12.0 : 14.0 : 16.0 : 32.0 23 1 40 2 1. (A) (B) (C) (D) (E) (C) (A) ( ) (B) ( ) (D) (NaI KIO 3 ) (E) ( Ca 2+ Mg 2+ Fe 2+ ) (C) 1 2 3 75 6 (Ga 29.8 2403 ) 310 K 1.3
2007
 77 266071 http / /www. qdpub. com 13335059110 0532 85814750 85814611-8664 2006 9 7 2006 9 7 16 787mm 1092mm 7. 5 190 ISBN 7-5436 - 2241-6 7. 50 0532 85814926 0532 85814611-8628 2007 1!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!
77 266071 http / /www. qdpub. com 13335059110 0532 85814750 85814611-8664 2006 9 7 2006 9 7 16 787mm 1092mm 7. 5 190 ISBN 7-5436 - 2241-6 7. 50 0532 85814926 0532 85814611-8628 2007 1!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!
 用 矿 物 质 丰 富 的 盐 炼 成 的 竹 盐 是 科 学 Contents 可 以 解 决 矿 物 质 缺 乏 的 生 命 之 盐 - 竹 盐 2 什 么 是 矿 物 质? 3 盐 不 是 单 纯 的 氯 化 钠 4 难 道 盐 是 高 血 压 的 元 凶 吗? 5 推 荐 用 盐 补 充 体 内 缺 乏 矿 物 质 8 什 么 是 竹 盐? 10 盐 与 竹 盐 的 成 分 分 析 11 竹
用 矿 物 质 丰 富 的 盐 炼 成 的 竹 盐 是 科 学 Contents 可 以 解 决 矿 物 质 缺 乏 的 生 命 之 盐 - 竹 盐 2 什 么 是 矿 物 质? 3 盐 不 是 单 纯 的 氯 化 钠 4 难 道 盐 是 高 血 压 的 元 凶 吗? 5 推 荐 用 盐 补 充 体 内 缺 乏 矿 物 质 8 什 么 是 竹 盐? 10 盐 与 竹 盐 的 成 分 分 析 11 竹
第四章 自然环境及社会经济概况
 证 书 编 号 : 国 环 评 证 乙 字 第 2904 号 崇 左 红 狮 水 泥 窑 协 同 处 置 10 万 吨 / 年 工 业 废 物 项 目 环 境 影 响 报 告 书 ( 公 示 稿 ) 建 设 单 位 : 崇 左 红 狮 环 保 科 技 有 限 公 司 编 制 单 位 : 广 西 宇 宏 环 保 咨 询 有 限 公 司 编 制 时 间 : 二 〇 一 五 年 十 一 月 前 言 项
证 书 编 号 : 国 环 评 证 乙 字 第 2904 号 崇 左 红 狮 水 泥 窑 协 同 处 置 10 万 吨 / 年 工 业 废 物 项 目 环 境 影 响 报 告 书 ( 公 示 稿 ) 建 设 单 位 : 崇 左 红 狮 环 保 科 技 有 限 公 司 编 制 单 位 : 广 西 宇 宏 环 保 咨 询 有 限 公 司 编 制 时 间 : 二 〇 一 五 年 十 一 月 前 言 项
沪教版初三化学(上)
 2010 中 考 化 学 试 题 汇 编 之 7 酸 碱 盐 一 选 择 1.(2010 肇 庆 ) 下 列 化 学 方 程 式 所 表 示 的 化 学 反 应 能 发 生 的 是 ( ) A.Cu+H 2 SO 4 CuSO 4 +H 2 B.Fe+ Zn( NO 3 ) 2 Fe(NO 3 ) 2 +Zn C.CuCl 2 +2NaOH Cu(OH) 2 +2NaCl D.Na 2 CO 3 +2KNO
2010 中 考 化 学 试 题 汇 编 之 7 酸 碱 盐 一 选 择 1.(2010 肇 庆 ) 下 列 化 学 方 程 式 所 表 示 的 化 学 反 应 能 发 生 的 是 ( ) A.Cu+H 2 SO 4 CuSO 4 +H 2 B.Fe+ Zn( NO 3 ) 2 Fe(NO 3 ) 2 +Zn C.CuCl 2 +2NaOH Cu(OH) 2 +2NaCl D.Na 2 CO 3 +2KNO
分析化学
 作业 第 4 章 :9,11-13 预习 第 4 章至篇 319 答疑时间 : 本周四 (19 日 ) 10:00-12:00 答疑地点 : 化学楼 S406 1 第 4 章络合滴定法 演讲安排 习题 4.8 拟定分析方案, 指出滴定剂 酸度 指示剂及所需其他试剂, 并说明滴定的方式 : (2)Zn 2+ Mg 2+ 混合液中两者的测定 ( 举出 3 种方案 )(5.8) (4)Ca 2+ 与 EDTA
作业 第 4 章 :9,11-13 预习 第 4 章至篇 319 答疑时间 : 本周四 (19 日 ) 10:00-12:00 答疑地点 : 化学楼 S406 1 第 4 章络合滴定法 演讲安排 习题 4.8 拟定分析方案, 指出滴定剂 酸度 指示剂及所需其他试剂, 并说明滴定的方式 : (2)Zn 2+ Mg 2+ 混合液中两者的测定 ( 举出 3 种方案 )(5.8) (4)Ca 2+ 与 EDTA
1 ( CIP) /,. :, ISBN X753 CIP ( 2005 ) : : : : /
 ( 50474050) ( 20040533011) 1 ( CIP) /,. :, 2005. 12 ISBN 7-81105-260-1............. X753 CIP ( 2005 ) 151885 : : 410083 : 0731-8876770 : 0731-8710482 880 1230 1 /32 11. 25 277 2006 3 1 2006 3 1 ISBN 7-81105-260-1
( 50474050) ( 20040533011) 1 ( CIP) /,. :, 2005. 12 ISBN 7-81105-260-1............. X753 CIP ( 2005 ) 151885 : : 410083 : 0731-8876770 : 0731-8710482 880 1230 1 /32 11. 25 277 2006 3 1 2006 3 1 ISBN 7-81105-260-1
GeologicalScienceandTechnologyInformation Vol.37 No.5 Sep doi: /j.cnki.dzkq ,,,. [J].,2018,37(5): a,b a,b a,
![GeologicalScienceandTechnologyInformation Vol.37 No.5 Sep doi: /j.cnki.dzkq ,,,. [J].,2018,37(5): a,b a,b a, GeologicalScienceandTechnologyInformation Vol.37 No.5 Sep doi: /j.cnki.dzkq ,,,. [J].,2018,37(5): a,b a,b a,](/thumbs/97/134206629.jpg) 37 5 2018 9 GeologicalScienceandTechnologyInformation Vol.37 No.5 Sep. 2018 doi:10.19509/j.cnki.dzkq.2018.0528. [J]. 201837(5):206-21. ab ab ab ab ( )a. ;b. 3007) : : ph Ec SO 2- HCO 3 - As / / : ; ; ;
37 5 2018 9 GeologicalScienceandTechnologyInformation Vol.37 No.5 Sep. 2018 doi:10.19509/j.cnki.dzkq.2018.0528. [J]. 201837(5):206-21. ab ab ab ab ( )a. ;b. 3007) : : ph Ec SO 2- HCO 3 - As / / : ; ; ;
试卷
 江 西 省 三 校 2016 届 高 三 联 考 化 学 试 题 可 能 用 到 的 相 对 原 子 质 量 :H=1 O=16 C=12 N=14 S=32 Na=23 Fe=56 Cu=64 一 选 择 题 ( 每 小 题 只 有 一 个 正 确 答 案, 每 小 题 3 分, 共 计 48 分 ) 1. 下 列 有 关 化 学 用 语 表 示 正 确 的 是 ( ) A. 水 分 子 的 球
江 西 省 三 校 2016 届 高 三 联 考 化 学 试 题 可 能 用 到 的 相 对 原 子 质 量 :H=1 O=16 C=12 N=14 S=32 Na=23 Fe=56 Cu=64 一 选 择 题 ( 每 小 题 只 有 一 个 正 确 答 案, 每 小 题 3 分, 共 计 48 分 ) 1. 下 列 有 关 化 学 用 语 表 示 正 确 的 是 ( ) A. 水 分 子 的 球
 t H θ m [] Q Q q [] 9. 69kJ g q 32.0 620kJmol - 1 0. 500g mol C(s) 1 2 O (g) = CO(g) 2 SI n mol H 2H+H22H2+O2 [N2H41+O2g N2g+2H2O1] 1.2.3 qp qv [4] 1 C( ) O 2 (g) = CO(g), ( 2), 2 CO(g) CO (g),co(g) +
t H θ m [] Q Q q [] 9. 69kJ g q 32.0 620kJmol - 1 0. 500g mol C(s) 1 2 O (g) = CO(g) 2 SI n mol H 2H+H22H2+O2 [N2H41+O2g N2g+2H2O1] 1.2.3 qp qv [4] 1 C( ) O 2 (g) = CO(g), ( 2), 2 CO(g) CO (g),co(g) +
1 S P Cl Pro 2 K Na Ca Mg K Na Ca Mg % 1 6%-9% 2 1%-3% 3 70%-80% 4 P Ca Fe Cu Co Zn Se Mn Mo Ni Cr P Ca 5 VB V B1 Vpp V B2 B3 VE
 1 2 1 V Pro 2 3 1 Pro 2 Fe2+ Fe3+ 3 Vc 4 Vc 5 1-12% 45-64% 4 1 S P Cl Pro 2 K Na Ca Mg K Na Ca Mg 3 1-2 11-14% 1 6%-9% 2 1%-3% 3 70%-80% 4 P Ca Fe Cu Co Zn Se Mn Mo Ni Cr P Ca 5 VB V B1 Vpp V B2 B3 VE
1 2 1 V Pro 2 3 1 Pro 2 Fe2+ Fe3+ 3 Vc 4 Vc 5 1-12% 45-64% 4 1 S P Cl Pro 2 K Na Ca Mg K Na Ca Mg 3 1-2 11-14% 1 6%-9% 2 1%-3% 3 70%-80% 4 P Ca Fe Cu Co Zn Se Mn Mo Ni Cr P Ca 5 VB V B1 Vpp V B2 B3 VE
PowerPoint 演示文稿
 复习 1 溶液是由溶质和溶剂两部分组成 2 溶质的质量分数表达式可表示为 w(b)= m(b) m( 溶液 ) 100% 引言 : 前面我们分析了物质的质量与体积问题, 在化 学实验中还用到大量的溶液, 而对溶液来说除了溶液的质 量 体积之外, 很多情况下用浓度表示溶液的组成 问题 : 初中我们是怎样表示溶液组成的?( 溶质的质量分数 ) 在引入物质的量这个概念后, 溶质还可以用物质的量去衡量, 这就给我们一个启示
复习 1 溶液是由溶质和溶剂两部分组成 2 溶质的质量分数表达式可表示为 w(b)= m(b) m( 溶液 ) 100% 引言 : 前面我们分析了物质的质量与体积问题, 在化 学实验中还用到大量的溶液, 而对溶液来说除了溶液的质 量 体积之外, 很多情况下用浓度表示溶液的组成 问题 : 初中我们是怎样表示溶液组成的?( 溶质的质量分数 ) 在引入物质的量这个概念后, 溶质还可以用物质的量去衡量, 这就给我们一个启示
学 而 思 老 师 们 の 嘱 托 集 数 学 詹 昊 凯 老 师 の 嘱 托 丨 从 近 年 高 考 命 题 看 解 析 几 何 复 习 方 向...2 问 老 师 の 嘱 托 丨 一 点 高 等 数 学 知 识 就 能 够 秒 杀 函 数 导 数 题?!...5 杨 老 师 の 嘱 托 丨 1
 咨 询 电 话 1010899 2016 高 考 命 题 方 向 预 测 大 型 讲 座 在 考 后 填 报 志 愿 的 今 天, 每 1 分 都 变 得 更 加 珍 贵 知 己 知 彼 方 能 百 战 不 殆, 对 高 考 的 熟 悉 程 度 将 在 一 定 程 度 上 影 响 你 的 实 力 发 挥, 而 近 年 高 考 和 一 模 二 模 都 会 潜 移 默 化 的 影 响 着 今 年 高 考,
咨 询 电 话 1010899 2016 高 考 命 题 方 向 预 测 大 型 讲 座 在 考 后 填 报 志 愿 的 今 天, 每 1 分 都 变 得 更 加 珍 贵 知 己 知 彼 方 能 百 战 不 殆, 对 高 考 的 熟 悉 程 度 将 在 一 定 程 度 上 影 响 你 的 实 力 发 挥, 而 近 年 高 考 和 一 模 二 模 都 会 潜 移 默 化 的 影 响 着 今 年 高 考,
(CIP) : / :,, :,2000.5 ISBN 7-04 - 008822-3 - - N - 42 CIP (2000)60397 55 100009 010-64054588 010-64014048 / 8501168 1/ 32 7.875
 ( ) (CIP) : / :,, :,2000.5 ISBN 7-04 - 008822-3 - - N - 42 CIP (2000)60397 55 100009 010-64054588 010-64014048 http:/ / www.hep.edu.cn 8501168 1/ 32 7.875 190 000 8.40, ( ) 1 16 16 16 18 21 22 24 24 24
( ) (CIP) : / :,, :,2000.5 ISBN 7-04 - 008822-3 - - N - 42 CIP (2000)60397 55 100009 010-64054588 010-64014048 http:/ / www.hep.edu.cn 8501168 1/ 32 7.875 190 000 8.40, ( ) 1 16 16 16 18 21 22 24 24 24
教师招聘中学化学1-11.FIT)
 教 师 招 聘 考 试 中 学 化 学 历 年 真 题 汇 编 试 卷 渊 一 冤 渊 时 间 院 员 圆 园 分 钟 满 分 院 员 缘 园 分 冤 一 尧 单 项 选 择 题 渊 每 小 题 圆 分 袁 共 缘 园 分 冤 员 援 石 墨 烯 是 由 碳 原 子 构 成 的 单 层 片 状 结 构 的 新 材 料 渊 结 构 示 意 图 如 图 所 示 冤 袁 可 由 石 墨 剥 离 而 成 袁
教 师 招 聘 考 试 中 学 化 学 历 年 真 题 汇 编 试 卷 渊 一 冤 渊 时 间 院 员 圆 园 分 钟 满 分 院 员 缘 园 分 冤 一 尧 单 项 选 择 题 渊 每 小 题 圆 分 袁 共 缘 园 分 冤 员 援 石 墨 烯 是 由 碳 原 子 构 成 的 单 层 片 状 结 构 的 新 材 料 渊 结 构 示 意 图 如 图 所 示 冤 袁 可 由 石 墨 剥 离 而 成 袁
电 化 电 化 学 学 第 2 讲 原 电 池 一 教 学 目 标 理 解 原 电 池 的 工 作 原 理 并 正 确 书 写 电 极 反 应 和 总 反 应 方 程 式 知 识 导 航 构 造 条 件 构 造 及 工 作 原 理 工 作 原 理 燃 料 电 池 原 电 池 电 极 反 应 及 现
 www.xdf.cn 1 电 化 电 化 学 学 第 2 讲 原 电 池 一 教 学 目 标 理 解 原 电 池 的 工 作 原 理 并 正 确 书 写 电 极 反 应 和 总 反 应 方 程 式 知 识 导 航 构 造 条 件 构 造 及 工 作 原 理 工 作 原 理 燃 料 电 池 原 电 池 电 极 反 应 及 现 象 常 规 电 池 新 型 电 池 综 合 训 练 二 教 学 重 点 和
www.xdf.cn 1 电 化 电 化 学 学 第 2 讲 原 电 池 一 教 学 目 标 理 解 原 电 池 的 工 作 原 理 并 正 确 书 写 电 极 反 应 和 总 反 应 方 程 式 知 识 导 航 构 造 条 件 构 造 及 工 作 原 理 工 作 原 理 燃 料 电 池 原 电 池 电 极 反 应 及 现 象 常 规 电 池 新 型 电 池 综 合 训 练 二 教 学 重 点 和
第二十章 含氧盐矿物大类(二)
 第 二 十 章 含 氧 盐 矿 物 大 类 ( 二 ) SALT WITH OXYGEN (2) 本 大 类 ( 二 ) 简 称 杂 盐, 以 碳 酸 盐 硫 酸 盐 为 最 重 要, 其 次 为 磷 酸 盐 钨 酸 盐 硼 酸 盐 及 硝 酸 盐 其 他 含 氧 盐 矿 物 还 有 砷 酸 盐 钒 酸 盐 钼 酸 盐 和 铬 酸 盐 第 一 节 碳 酸 盐 矿 物 类 金 属 阳 离 子 与 碳
第 二 十 章 含 氧 盐 矿 物 大 类 ( 二 ) SALT WITH OXYGEN (2) 本 大 类 ( 二 ) 简 称 杂 盐, 以 碳 酸 盐 硫 酸 盐 为 最 重 要, 其 次 为 磷 酸 盐 钨 酸 盐 硼 酸 盐 及 硝 酸 盐 其 他 含 氧 盐 矿 物 还 有 砷 酸 盐 钒 酸 盐 钼 酸 盐 和 铬 酸 盐 第 一 节 碳 酸 盐 矿 物 类 金 属 阳 离 子 与 碳
 [Co(NH 3 ) 6 ] 3 [PtCl 4 ] 2 [SiF 6 ] 2 [Cu(H 2 O) 6 ] 2 [Cu(NH 3 ) 4 ] 2 [Co(NH 3 ) 6 ]Cl 3 K 4 [Fe(CN) 6 ][Cu(NH 3 ) 4 ]SO 4 F Cl Br I O OH S 2 CN H 2 O NH 3 KCl MgCl 2 KMgCl 3 (KClMgCl 2 ) 2 KCl PtCl
[Co(NH 3 ) 6 ] 3 [PtCl 4 ] 2 [SiF 6 ] 2 [Cu(H 2 O) 6 ] 2 [Cu(NH 3 ) 4 ] 2 [Co(NH 3 ) 6 ]Cl 3 K 4 [Fe(CN) 6 ][Cu(NH 3 ) 4 ]SO 4 F Cl Br I O OH S 2 CN H 2 O NH 3 KCl MgCl 2 KMgCl 3 (KClMgCl 2 ) 2 KCl PtCl
【中文名称】盐酸;氢氯酸
 1 ... 1... 9... 9... 10... 11... 11... 12... 13... 13... 14... 14... 15 1357-1357-3.3.1.1.3.7 HMTA... 16... 16... 17... 17... 18... 19... 19... 20... 20 33-4--13H-... 21 33-4--13H-... 21... 22 EDTA...
1 ... 1... 9... 9... 10... 11... 11... 12... 13... 13... 14... 14... 15 1357-1357-3.3.1.1.3.7 HMTA... 16... 16... 17... 17... 18... 19... 19... 20... 20 33-4--13H-... 21 33-4--13H-... 21... 22 EDTA...
第 13 章 氢和稀有气体
 第 11 章 氢 和 稀 有 气 体 教 学 要 求 1 掌 握 氢 原 子 的 性 质 成 键 特 征 氢 化 物 2 了 解 稀 有 气 体 的 原 子 结 构 性 质 和 用 途 教 学 重 点 氢 的 物 理 性 质 与 化 学 性 质 教 学 难 点 稀 有 气 体 化 合 物 的 性 质 教 学 时 数 4 学 时 教 学 内 容 11-1 氢 11-2 稀 有 气 体 教 学 方 法
第 11 章 氢 和 稀 有 气 体 教 学 要 求 1 掌 握 氢 原 子 的 性 质 成 键 特 征 氢 化 物 2 了 解 稀 有 气 体 的 原 子 结 构 性 质 和 用 途 教 学 重 点 氢 的 物 理 性 质 与 化 学 性 质 教 学 难 点 稀 有 气 体 化 合 物 的 性 质 教 学 时 数 4 学 时 教 学 内 容 11-1 氢 11-2 稀 有 气 体 教 学 方 法
( ) 039 (CIP) /. :, ISBN TS CIP ( 2005) : : : : * ( ) : ( 010 ) / www. cip. com. cn
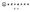 ( ) 039 (CIP) /. :, 2005. 3 ISBN 7-5025-6678-3... -. TS211. 4 CIP ( 2005) 012222 : : : : * ( 3 100029 ) : ( 010 ) 64982530 http:/ / www. cip. com. cn * 850mm 1168mm 1/ 32 7 196 2005 4 1 2005 4 1 ISBN 7-5025-6678-3/
( ) 039 (CIP) /. :, 2005. 3 ISBN 7-5025-6678-3... -. TS211. 4 CIP ( 2005) 012222 : : : : * ( 3 100029 ) : ( 010 ) 64982530 http:/ / www. cip. com. cn * 850mm 1168mm 1/ 32 7 196 2005 4 1 2005 4 1 ISBN 7-5025-6678-3/
 福 建 省 建 设 项 目 环 境 影 响 报 告 表 ( 适 用 于 生 态 型 建 设 项 目 ) 项 目 名 称 宁 宝 公 园 配 套 工 程 建 设 单 位 厦 门 市 集 美 区 建 设 局 ( 盖 章 ) 法 人 代 表 邹 荣 生 ( 盖 章 或 签 字 ) 联 系 人 邓 工 联 系 电 话 0592-6106390 邮 政 编 码 361021 环 保 部 门 填 写 收 到 报
福 建 省 建 设 项 目 环 境 影 响 报 告 表 ( 适 用 于 生 态 型 建 设 项 目 ) 项 目 名 称 宁 宝 公 园 配 套 工 程 建 设 单 位 厦 门 市 集 美 区 建 设 局 ( 盖 章 ) 法 人 代 表 邹 荣 生 ( 盖 章 或 签 字 ) 联 系 人 邓 工 联 系 电 话 0592-6106390 邮 政 编 码 361021 环 保 部 门 填 写 收 到 报
<4D6963726F736F667420576F7264202D20BBB7C6C0B1A8B8E6CAE9D7CAD6CA312E646F63>
 天 锰 新 材 料 生 产 项 目 环 境 影 响 报 告 书 编 制 人 员 名 单 表 主 持 编 制 机 构 : 重 庆 市 环 境 保 护 工 程 设 计 研 究 院 有 限 公 司 编 制 主 持 人 职 ( 执 ) 业 资 登 记 ( 注 册 证 ) 姓 名 专 业 类 别 格 证 书 编 号 编 号 肖 骏 0008882 B31060080400 化 工 石 化 医 药 类 本 人
天 锰 新 材 料 生 产 项 目 环 境 影 响 报 告 书 编 制 人 员 名 单 表 主 持 编 制 机 构 : 重 庆 市 环 境 保 护 工 程 设 计 研 究 院 有 限 公 司 编 制 主 持 人 职 ( 执 ) 业 资 登 记 ( 注 册 证 ) 姓 名 专 业 类 别 格 证 书 编 号 编 号 肖 骏 0008882 B31060080400 化 工 石 化 医 药 类 本 人
Ps22Pdf
 CO SO N H H O N H SO N H SO SO H O N H H SO CO ppm CO ppm NO NO ppm NO ppm NO NO N O ppm NO m I O SO T PMCO N OO I O I O g m a lppm PPm PPm PPm nl l a a l ll lmg ph p H p H ph p H mv ph p H p H p H p
CO SO N H H O N H SO N H SO SO H O N H H SO CO ppm CO ppm NO NO ppm NO ppm NO NO N O ppm NO m I O SO T PMCO N OO I O I O g m a lppm PPm PPm PPm nl l a a l ll lmg ph p H p H ph p H mv ph p H p H p H p
4. 下 列 有 关 系 保 内 物 质 含 量 比 值 的 关 系, 正 确 的 是 A. 细 胞 内 结 合 水 / 自 由 水 的 比 值, 种 子 萌 发 时 比 休 眠 时 高 B. 人 体 细 胞 内 O /CO 的 比 值, 线 粒 体 内 比 细 胞 质 基 质 高 C. 神 经 纤
 绝 密 启 用 前 015 年 普 通 高 等 学 校 招 生 全 国 统 一 考 试 ( 山 东 卷 ) 理 科 综 合 注 意 事 项 : 1. 本 试 卷 分 第 I 卷 和 第 II 卷 两 部 分, 共 1 页 满 分 300 分 考 试 用 时 150 分 钟 答 题 前, 考 生 务 必 用 0.5 毫 米 黑 色 签 字 笔 将 自 己 的 姓 名 座 号 考 生 号 县 区 和 科
绝 密 启 用 前 015 年 普 通 高 等 学 校 招 生 全 国 统 一 考 试 ( 山 东 卷 ) 理 科 综 合 注 意 事 项 : 1. 本 试 卷 分 第 I 卷 和 第 II 卷 两 部 分, 共 1 页 满 分 300 分 考 试 用 时 150 分 钟 答 题 前, 考 生 务 必 用 0.5 毫 米 黑 色 签 字 笔 将 自 己 的 姓 名 座 号 考 生 号 县 区 和 科
99600936zw.PDF
 附 录 相对原子质量表 按照元素符号的字母次序排列 ( ) ( ) ( ) [ 1 1] ( 1 1) ( ) [ 1 2] ( ) [ 1 3] ( 1 3) [ 1 4] ( ) 4 1 2 3 4 [ ] 1 2 (1) (2) (3) (4) (5) (6) 3 0 1535 232 ( ) 101.325 101.325 100 357 2750 / 3 / 3 7.8 / 3 2.7
附 录 相对原子质量表 按照元素符号的字母次序排列 ( ) ( ) ( ) [ 1 1] ( 1 1) ( ) [ 1 2] ( ) [ 1 3] ( 1 3) [ 1 4] ( ) 4 1 2 3 4 [ ] 1 2 (1) (2) (3) (4) (5) (6) 3 0 1535 232 ( ) 101.325 101.325 100 357 2750 / 3 / 3 7.8 / 3 2.7
35 C 58 B 1 :
 1 2 1. 0625522. 050061 120 120 46 60 40 20 2012 2011 2012 1 2 3 4 5 6 8 9 11 12 14 28 30 36 7 13 29 31 35 144 35 C 58 B 1 : 3 4 5 40 84 9 11 2 6 27 9 29 13 28 31 31 35 35 36 7 3 12 27 6 7 29 30 31 29 30
1 2 1. 0625522. 050061 120 120 46 60 40 20 2012 2011 2012 1 2 3 4 5 6 8 9 11 12 14 28 30 36 7 13 29 31 35 144 35 C 58 B 1 : 3 4 5 40 84 9 11 2 6 27 9 29 13 28 31 31 35 35 36 7 3 12 27 6 7 29 30 31 29 30
 ο ο ο ο 100 A 1000 A 20A 100 A 20A ο ο 20 A 327 ] [Al OH SO ] 3 m n 2 m 4 m n 3 2 ([Fe ( OH) ( SO ) ] [Fe OH Cl ] 2 m 4 m 3-2 n 2 m 6-m n D
ο ο ο ο 100 A 1000 A 20A 100 A 20A ο ο 20 A 327 ] [Al OH SO ] 3 m n 2 m 4 m n 3 2 ([Fe ( OH) ( SO ) ] [Fe OH Cl ] 2 m 4 m 3-2 n 2 m 6-m n D
 3 3 3 1.01 105 74 100 100 = 10 100 90 = 11.1 50 98 x 245 20 100 100 1 1 = = -12 1/ 12 = = 12 1/ 12-26 2.65710 = 11.6610-27 -12 6 6 2N 100% = 2 14 100% CO( NH ) 60 2 2
3 3 3 1.01 105 74 100 100 = 10 100 90 = 11.1 50 98 x 245 20 100 100 1 1 = = -12 1/ 12 = = 12 1/ 12-26 2.65710 = 11.6610-27 -12 6 6 2N 100% = 2 14 100% CO( NH ) 60 2 2
CuNH c Cu x NH β mol L CuNH c Cu x 7.0 NH β mol L 7.0 溶液中以 Cu(NH ),Cu(NH ) 为主. 乙酰丙酮 (L) 与 Fe + 络合物的 lgβ ~lgβ 分别为.,.,6.7 请指出在下面不同 p
 . 已知铜氨络合物各级不稳定常数为 不稳 =7.8 0 - 不稳 =. 0 - 不稳 =. 0 - 不稳 =7. 0-5 () 计算各级稳定常数 ~ 和各级累积常数 β ~β ; () 若铜氨络合物水溶液中 Cu(NH ) + 的浓度为 Cu(NH ) + 的 0 倍, 问溶液中 [NH ] 是多少? () 若铜氨络合物溶液中 c(nh )=.0 0 - mol L -,c(cu + )=.0 0
. 已知铜氨络合物各级不稳定常数为 不稳 =7.8 0 - 不稳 =. 0 - 不稳 =. 0 - 不稳 =7. 0-5 () 计算各级稳定常数 ~ 和各级累积常数 β ~β ; () 若铜氨络合物水溶液中 Cu(NH ) + 的浓度为 Cu(NH ) + 的 0 倍, 问溶液中 [NH ] 是多少? () 若铜氨络合物溶液中 c(nh )=.0 0 - mol L -,c(cu + )=.0 0
40,,, (CIP) /.:, ISBN P641.5 CIP ( 2004) KUANGQUANSHU I WENQUANSHUI DE KANCHAPINGJIA YU KAIFA LIYONG : : : : 31, 100
 40,,, (CIP) /.:,2004. 4 ISBN 7-116 - 04049-8.... P641.5 CIP ( 2004) 015147 KUANGQUANSHU I WENQUANSHUI DE KANCHAPINGJIA YU KAIFA LIYONG : : : : 31, 100083 : ( 010 ) 82324508 ( ) : http:/ / www.gph. com.
40,,, (CIP) /.:,2004. 4 ISBN 7-116 - 04049-8.... P641.5 CIP ( 2004) 015147 KUANGQUANSHU I WENQUANSHUI DE KANCHAPINGJIA YU KAIFA LIYONG : : : : 31, 100083 : ( 010 ) 82324508 ( ) : http:/ / www.gph. com.
三言两拍.PDF
 003 015 021 026 033 040 050 056 064 072 079 087 097 105 111 117 127 137 148 159 168 177 186 194 202 210 217 225 235 ( ) , ( )
003 015 021 026 033 040 050 056 064 072 079 087 097 105 111 117 127 137 148 159 168 177 186 194 202 210 217 225 235 ( ) , ( )
99710b45zw.PDF
 1 2 1 4 C && Zn H H H H H Cl H O H N H H H CH C H C H 3 2 5 3 7 H H H H CH 3 C2H 5 H H H O H H O K K O NO 2 H O NO 2 NO O 2 C2H5 H O C2H5 C H O C2H3 2 5 H H H O H H O 1826 O
1 2 1 4 C && Zn H H H H H Cl H O H N H H H CH C H C H 3 2 5 3 7 H H H H CH 3 C2H 5 H H H O H H O K K O NO 2 H O NO 2 NO O 2 C2H5 H O C2H5 C H O C2H3 2 5 H H H O H H O 1826 O
投影片 1
 化 學 性 危 害 及 毒 性 化 學 物 質 基 本 概 念 內 容 壹 危 險 物 有 害 物 及 化 學 危 害 貳 化 學 危 害 的 認 知 參 化 學 危 害 的 預 防 與 控 制 肆 化 學 危 害 之 案 例 壹 危 險 物 有 害 物 及 化 學 危 害 3 何 謂 化 學 性 危 害 化 學 危 害 可 以 定 義 為 化 學 物 質 與 人 體 接 觸, 因 其 化 學 性
化 學 性 危 害 及 毒 性 化 學 物 質 基 本 概 念 內 容 壹 危 險 物 有 害 物 及 化 學 危 害 貳 化 學 危 害 的 認 知 參 化 學 危 害 的 預 防 與 控 制 肆 化 學 危 害 之 案 例 壹 危 險 物 有 害 物 及 化 學 危 害 3 何 謂 化 學 性 危 害 化 學 危 害 可 以 定 義 為 化 學 物 質 與 人 體 接 觸, 因 其 化 學 性
高雄市立五福國民中學95學年度第2學期第3次段考二年級自然與生活科技學習領域試題卷
 五 福 二 自 p1 高 雄 市 立 五 福 國 民 中 學 96 學 年 度 第 2 學 期 第 2 次 段 考 二 年 級 自 然 與 生 活 科 技 學 習 領 域 試 題 卷 一 選 擇 題 :( 每 題 2 分, 共 50 分 ) 1. 下 列 敘 述 何 者 錯 誤? (A) 銅 可 導 電, 但 銅 為 非 電 解 質 (B) 水 溶 液 能 導 電 的 物 質, 一 定 是 電 解
五 福 二 自 p1 高 雄 市 立 五 福 國 民 中 學 96 學 年 度 第 2 學 期 第 2 次 段 考 二 年 級 自 然 與 生 活 科 技 學 習 領 域 試 題 卷 一 選 擇 題 :( 每 題 2 分, 共 50 分 ) 1. 下 列 敘 述 何 者 錯 誤? (A) 銅 可 導 電, 但 銅 為 非 電 解 質 (B) 水 溶 液 能 導 電 的 物 質, 一 定 是 電 解
侧 为 两 个 半 电 池 习 惯 上 把 正 极 写 在 右 边, 负 极 写 在 左 边 1.1.1.2 电 位 分 析 法 的 分 类 和 特 点 电 位 分 析 法 是 将 一 支 电 极 电 位 与 被 测 物 质 的 活 ( 浓 ) 度 1 有 关 的 电 极 ( 称 指 示 电 极 )
 1 电 位 分 析 法 1.1 基 本 原 理 1.2 直 接 电 位 法 1.3 电 位 滴 定 法 1.4 实 验 1.1 基 本 原 理 1.1.1 概 述 1.1.2 电 位 分 析 法 的 理 论 依 据 1.1.3 参 比 电 极 1.1.4 指 示 电 极 1.1.1 概 述 电 位 分 析 法 是 电 化 学 分 析 法 的 一 个 重 要 组 成 部 分 电 化 学 分 析 是 利
1 电 位 分 析 法 1.1 基 本 原 理 1.2 直 接 电 位 法 1.3 电 位 滴 定 法 1.4 实 验 1.1 基 本 原 理 1.1.1 概 述 1.1.2 电 位 分 析 法 的 理 论 依 据 1.1.3 参 比 电 极 1.1.4 指 示 电 极 1.1.1 概 述 电 位 分 析 法 是 电 化 学 分 析 法 的 一 个 重 要 组 成 部 分 电 化 学 分 析 是 利
法 去 对 待 : 溴 水 碘 水 氯 化 氢 水 溴 化 氢 水 碘 化 氢 水 氨 水 二 氧 化 硫 水 硫 化 氢 水 二 氧 化 碳 水 -------- 的 组 成 与 溶 解 过 程 从 氯 水 参 与 的 化 学 反 应 的 本 质 与 类 型 去 学 会 分 析 : 金 属 钠 过
 枝 乱 我 不 乱 高 考 化 学 总 复 习 的 策 略 与 思 路 措 施 与 方 法 从 容 看 万 条 一. 刍 议 河 北 省 用 高 考 试 题 抓 基 础 抓 主 干 抓 核 心 ; 重 能 力 重 理 解 重 应 用 ; 变 宽 度 降 难 度 改 深 度 ; 稳 求 变 稳 求 新 稳 求 进 试 题 导 向 健 康 难 度 控 制 得 当, 主 干 知 识 突 出, 区 分 度
枝 乱 我 不 乱 高 考 化 学 总 复 习 的 策 略 与 思 路 措 施 与 方 法 从 容 看 万 条 一. 刍 议 河 北 省 用 高 考 试 题 抓 基 础 抓 主 干 抓 核 心 ; 重 能 力 重 理 解 重 应 用 ; 变 宽 度 降 难 度 改 深 度 ; 稳 求 变 稳 求 新 稳 求 进 试 题 导 向 健 康 难 度 控 制 得 当, 主 干 知 识 突 出, 区 分 度
实验室安全手册.doc
 序 言 欢 迎 您 进 入 实 验 室 进 行 科 学 的 探 索 和 创 新 的 尝 试 为 了 保 证 您 在 实 验 室 学 习 顺 利, 确 保 保 证 在 实 验 过 程 中 的 安 全, 请 您 务 必 仔 细 阅 读 实 验 室 安 全 手 册 本 手 册 基 于 以 人 为 本 的 原 则, 从 使 用 者 的 角 度 提 出 做 好 自 身 防 护 的 措 施, 指 明 安 全 的
序 言 欢 迎 您 进 入 实 验 室 进 行 科 学 的 探 索 和 创 新 的 尝 试 为 了 保 证 您 在 实 验 室 学 习 顺 利, 确 保 保 证 在 实 验 过 程 中 的 安 全, 请 您 务 必 仔 细 阅 读 实 验 室 安 全 手 册 本 手 册 基 于 以 人 为 本 的 原 则, 从 使 用 者 的 角 度 提 出 做 好 自 身 防 护 的 措 施, 指 明 安 全 的
实验室安全基础
 实 验 室 安 全 知 识 讲 座 ( 教 案 ) 第 1 章 绪 论 1.1 实 验 室 安 全 知 识 讲 座 课 程 概 况 1.1.1 教 学 目 的 通 过 学 习 必 要 的 安 全 知 识 和 安 全 管 理 制 度, 提 高 学 生 安 全 意 识 和 安 全 素 质, 减 少 和 消 除 实 验 室 安 全 事 故, 掌 握 必 要 的 灭 火 方 法 和 逃 生 自 救 常 识,
实 验 室 安 全 知 识 讲 座 ( 教 案 ) 第 1 章 绪 论 1.1 实 验 室 安 全 知 识 讲 座 课 程 概 况 1.1.1 教 学 目 的 通 过 学 习 必 要 的 安 全 知 识 和 安 全 管 理 制 度, 提 高 学 生 安 全 意 识 和 安 全 素 质, 减 少 和 消 除 实 验 室 安 全 事 故, 掌 握 必 要 的 灭 火 方 法 和 逃 生 自 救 常 识,
" "!!##$!##%!##%! "
 "!! " "!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!! " #$$%!& #$$%! " #! " " "!!##$!##%!##%! " " #$ %& # # () &$ %&#! *) #! +),) -$ %& () *) +),)./!$ %&! 0 ($ 12 - *$ 12 +$ *$,$ /+3 +$ 4$ %&#-,$ ($ ) %##% *$ () *)!
"!! " "!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!!! " #$$%!& #$$%! " #! " " "!!##$!##%!##%! " " #$ %& # # () &$ %&#! *) #! +),) -$ %& () *) +),)./!$ %&! 0 ($ 12 - *$ 12 +$ *$,$ /+3 +$ 4$ %&#-,$ ($ ) %##% *$ () *)!
) 1 : (1) ZR4-6 (2) 1 000ml 6 6 1 000mL :,, (3) : Al2 ( SO4 ) 3103050607080mg/ L (4) ZR4-6 ( ),, (5),, 2 (6) 500r/ min 30s, 150r/ min 5 min, 80r/ min
 (1), (2),,,,, :,, ; ;, : 4 1000mL, 2 ; 1000mL, 100mL, 10mL, 2mL,,,,, ph, : Al2 ( SO4 )3 ; FeCl3 6 ; 2 ; 2 ; 1 ; 1 ; 1 ; 1 ; 1 ; 1 ) 1 : (1) ZR4-6 (2) 1 000ml 6 6 1 000mL :,, (3) : Al2 ( SO4 ) 3103050607080mg/
(1), (2),,,,, :,, ; ;, : 4 1000mL, 2 ; 1000mL, 100mL, 10mL, 2mL,,,,, ph, : Al2 ( SO4 )3 ; FeCl3 6 ; 2 ; 2 ; 1 ; 1 ; 1 ; 1 ; 1 ; 1 ) 1 : (1) ZR4-6 (2) 1 000ml 6 6 1 000mL :,, (3) : Al2 ( SO4 ) 3103050607080mg/
应用化学《有机化学实验》讲义
 2 3 4 5 6 - K = m 0 m 1 / V 1 m 1 / V 0 m K = m V 0 / 1 0 V 0 / K + V 1 / V 0 / + / n K = m V m 0 n 0 K V 1 n 7 8 9 10 11 8. = 100% 12 13 14 15 16 17 CH 3 CH 3 CH 3 C H + HCl CH 3 C Cl + H 2 CH 3 CH 3
2 3 4 5 6 - K = m 0 m 1 / V 1 m 1 / V 0 m K = m V 0 / 1 0 V 0 / K + V 1 / V 0 / + / n K = m V m 0 n 0 K V 1 n 7 8 9 10 11 8. = 100% 12 13 14 15 16 17 CH 3 CH 3 CH 3 C H + HCl CH 3 C Cl + H 2 CH 3 CH 3
臺 灣 地 區 今 天 傍 晚 5 點 32 分 發 生 強 烈 地 震, 震 央 在 南 投 名 間 南 方 10 公 里 的 地 方, 震 源 深 度 19 公 里, 屬 於 淺 層 地 震, 名 間 鄉 的 震 度 達 到 7 級, 雲 林 古 坑 6 級, 隨 後 在 5 點 38 分, 南
 國 立 臺 東 高 級 中 學 103 學 年 度 第 一 學 期 期 末 考 高 一 環 境 科 學 概 論 卷 別 : 綜 高 班 作 答 方 式 : 答 案 卡 適 用 班 級 : 1-1 1-2 1-3 1-4 命 題 範 圍 : 第 5-7 章 ; 施 測 時 間 :70 分 鐘 104.01.16 一 題 組 題 (1~42 題, 每 題 2 分, 共 84 分 ) 題 組 右 圖 為
國 立 臺 東 高 級 中 學 103 學 年 度 第 一 學 期 期 末 考 高 一 環 境 科 學 概 論 卷 別 : 綜 高 班 作 答 方 式 : 答 案 卡 適 用 班 級 : 1-1 1-2 1-3 1-4 命 題 範 圍 : 第 5-7 章 ; 施 測 時 間 :70 分 鐘 104.01.16 一 題 組 題 (1~42 題, 每 題 2 分, 共 84 分 ) 題 組 右 圖 為
untitled
 天津一中网校 同步教学 年级 高三 天津市立思辰网络教育有限公司 版权所有 科目 生物 教师 刘媛 2004-2005 年第二学期第一周 第 1 页 2 ATP 3 1 V D V A RNA V C V B1 V B2 2 ph 35 0 40 0 C 4050 0 C 3 CO 2 NH 3 CO 2 NH 3 4 R R 4 5 ATP 1ATP 1ATP ATP AP~P~P A T 3 P
天津一中网校 同步教学 年级 高三 天津市立思辰网络教育有限公司 版权所有 科目 生物 教师 刘媛 2004-2005 年第二学期第一周 第 1 页 2 ATP 3 1 V D V A RNA V C V B1 V B2 2 ph 35 0 40 0 C 4050 0 C 3 CO 2 NH 3 CO 2 NH 3 4 R R 4 5 ATP 1ATP 1ATP ATP AP~P~P A T 3 P
à
 à ó à 50000 8000 6000 4000 3000 2000 1700 1400 1000 500 300 400 100 200 200 400 700 13 1000 ( ) 1250 1450 1596 1892 1661 1669 1703 1735 1741 1746 1728 1799 1731 1810 1753 1754 1771 1772 1774
à ó à 50000 8000 6000 4000 3000 2000 1700 1400 1000 500 300 400 100 200 200 400 700 13 1000 ( ) 1250 1450 1596 1892 1661 1669 1703 1735 1741 1746 1728 1799 1731 1810 1753 1754 1771 1772 1774
(Microsoft Word - 103\300\347\267~\266\265\245\330\245N\275X)
 A 大 農 林 漁 牧 業 一 分 說 明 1. 獸 醫 業 非 屬 公 司 法 商 業 登 記 法 所 管 轄, 不 納 入 本 大 2. 各 依 性 質 包 括 其 從 事 業 務 產 品 之 批 發 零 售 二 分 示 意 圖 大 中 小 A A1 農 業 A101 農 藝 及 園 藝 A101011 種 苗 業 業 A101020 農 作 物 栽 培 業 A101030 特 用 作 物 栽
A 大 農 林 漁 牧 業 一 分 說 明 1. 獸 醫 業 非 屬 公 司 法 商 業 登 記 法 所 管 轄, 不 納 入 本 大 2. 各 依 性 質 包 括 其 從 事 業 務 產 品 之 批 發 零 售 二 分 示 意 圖 大 中 小 A A1 農 業 A101 農 藝 及 園 藝 A101011 種 苗 業 業 A101020 農 作 物 栽 培 業 A101030 特 用 作 物 栽
試料分解と目的元素精製法_2010日本分析化学会
 H2007T(10:3011:00) ICPAES,ICPMS 22416 http://www.caa.go.jp/safety/pdf/100419kouhyou_1.pdf http://www.caa.go.jp/safety/pdf/100419kouhyou_1.pdf 2010-07-28 Cd0.4 ppm232 * CODEX STAN 193-1995, Rev.3-2007 Web
H2007T(10:3011:00) ICPAES,ICPMS 22416 http://www.caa.go.jp/safety/pdf/100419kouhyou_1.pdf http://www.caa.go.jp/safety/pdf/100419kouhyou_1.pdf 2010-07-28 Cd0.4 ppm232 * CODEX STAN 193-1995, Rev.3-2007 Web
第一章 绪 论
 环 境 监 测 主 编 : 王 怀 宇 姚 运 先 高 等 教 育 出 版 社 内 容 提 要 本 书 将 环 境 监 测 的 对 象 进 行 了 明 确 的 分 类, 详 细 讲 述 了 各 种 监 测 技 术 的 基 础 理 论 和 手 段 内 容 包 括 环 境 监 测 绪 论 环 境 监 测 质 量 控 制 水 体 监 测 大 气 监 测 噪 声 监 测 土 壤 与 固 体 废 物 监 测
环 境 监 测 主 编 : 王 怀 宇 姚 运 先 高 等 教 育 出 版 社 内 容 提 要 本 书 将 环 境 监 测 的 对 象 进 行 了 明 确 的 分 类, 详 细 讲 述 了 各 种 监 测 技 术 的 基 础 理 论 和 手 段 内 容 包 括 环 境 监 测 绪 论 环 境 监 测 质 量 控 制 水 体 监 测 大 气 监 测 噪 声 监 测 土 壤 与 固 体 废 物 监 测
njj00004zw.PDF
 100m 2 000m 4 150m 2 000m 50m 1700 1 C H O N P S Ca ATP 20 8 DNA RNA DNA RNA ATP 2 3 4 5 6 DNA 7 1 1970 Winniwarter 47 46 23 X Winniwarter 1921 Painter Y 48 46 XX 46 XY 20 50 1954 Hansen-Melander 46 48
100m 2 000m 4 150m 2 000m 50m 1700 1 C H O N P S Ca ATP 20 8 DNA RNA DNA RNA ATP 2 3 4 5 6 DNA 7 1 1970 Winniwarter 47 46 23 X Winniwarter 1921 Painter Y 48 46 XX 46 XY 20 50 1954 Hansen-Melander 46 48
壹、
 1 1 20ml. 10 35% 10 3 2 2 250ml. 10 2 (30c.c) 1 75ml 2 4 3 2 1 1 2 1. 2. 1c 3 4 5 1. 2. 3. 4. 5. 1. 2 6 2. 1 3. 7 1. 2. 3. 1. 2. 1 3. 8 1. 9 2. 50 3. 4. 10 5. 10 6. 25c.c. 4 7. 8. 50c.c. 9. 10. 11 12 25.63
1 1 20ml. 10 35% 10 3 2 2 250ml. 10 2 (30c.c) 1 75ml 2 4 3 2 1 1 2 1. 2. 1c 3 4 5 1. 2. 3. 4. 5. 1. 2 6 2. 1 3. 7 1. 2. 3. 1. 2. 1 3. 8 1. 9 2. 50 3. 4. 10 5. 10 6. 25c.c. 4 7. 8. 50c.c. 9. 10. 11 12 25.63
<4D6963726F736F667420576F7264202D20A6DBB54DACECBEC7BEFAA67EB8D5C344>
 自 然 科 學 歷 年 試 題 1. ( 2 ) 電 線 間 的 絕 緣 破 壞, 裸 線 彼 此 直 接 接 觸 時, 發 生 爆 炸 性 火 花 稱 為 下 列 何 者?(1) 漏 電 (2) 短 路 (3) 尖 端 放 電 (4) 一 般 放 電 2. ( 3 ) 電 器 安 全 中, 下 列 何 者 不 是 短 路 事 故 原 因?(1) 電 纜 電 線 絕 緣 物 自 然 劣 化 (2)
自 然 科 學 歷 年 試 題 1. ( 2 ) 電 線 間 的 絕 緣 破 壞, 裸 線 彼 此 直 接 接 觸 時, 發 生 爆 炸 性 火 花 稱 為 下 列 何 者?(1) 漏 電 (2) 短 路 (3) 尖 端 放 電 (4) 一 般 放 電 2. ( 3 ) 電 器 安 全 中, 下 列 何 者 不 是 短 路 事 故 原 因?(1) 電 纜 電 線 絕 緣 物 自 然 劣 化 (2)

 H2SO4 NaOH HCN NH3 1 CH CH OH Na CH CH ONa H 2 3 2 3 2 2 1 Cu O 2
H2SO4 NaOH HCN NH3 1 CH CH OH Na CH CH ONa H 2 3 2 3 2 2 1 Cu O 2