2898
|
|
|
- 袁 柳
- 4 years ago
- Views:
Transcription
1 2898 物理化学学报 (Wuli Huaxue Xuebao) Acta Phys. -Chim. Sin. 2016, 32 (12), December [Article] doi: /PKU.WHXB Criegee 中间体 CH 3 CHOO 与 H 2 O 反应机理及酸催化效应 * 高志芳周丽婷王渭娜刘峰毅王文亮 ( 陕西省大分子科学重点实验室, 陕西师范大学化学化工学院, 西安 ) 摘要 : 采用 CCSD(T)//B3LYP/6-311+G(d,p) 方法研究了 H 2O 及甲酸等 6 种有机酸对 CH 3CHOO 与 H 2O 加成反应的催化作用 结果表明, 非催化反应存在双质子迁移和加成反应 2 条通道, 其中加成反应为优势通道 其加成机理为 H 2O 中 OH 加到 CH 3CHOO 的 α-c 上, 同时 H 2O 中另一个 H 迁移到 CH 3CHOO 的端 O 上 催化剂 H 2O 及有机酸以氢键复合物的形式参与反应促进了 H 质子转移, 可降低基元反应能垒和表观活化能, 且催化效应与有机酸的强度成正比 例如, 当分别用 H 2O (pk a = 15.7) 甲酸(pK a = 3.75) 和草酸 (pk a = 1.23) 催化时, 生成 syn-hahp 的基元反应能垒由非催化的 kj mol -1 分别降至 和 kj mol -1 非催化反应具有正的表观活化能, 而所有催化反应则均具有负的表观活化能 关键词 :Criegee 中间体 ;CH 3CHOO; 酸催化 ; 加成反应 中图分类号 :O643.1 Reaction Mechanism of Criegee Intermediate CH 3 CHOO with H 2 O and the Acid Catalytic Effect GAO Zhi-Fang ZHOU Li-Ting WANG Wei-Na LIU Feng-Yi WANG Wen-Liang * (School of Chemistry and Chemical Engineering, Shaanxi Normal University, Key Laboratory for Macromolecular Science of Shaanxi Province, Xi'an , P. R. China) Abstract: The catalytic effect of H 2O and six kinds of organic acids (e.g., formic acid) on the reaction of CH 3CHOO with H 2O is studied at the CCSD(T)//B3LYP/6-311+G(d,p) level. The results reveal that two possible channels exist as the double proton transfer and addition, of which the latter dominates for the non-catalytic reactions. For the additions, the OH of water is added to the α-c of CH 3CHOO, and the H atoms migrate to the end oxygen atoms. Catalysts such as H 2O and organic acid can form a hydrogen- bonded complex with CH 3CHOO, which promotes the H transfer and thus significantly reduces the elementary reaction energy barrier and apparent activation energy when compared with that of the non-catalytic reaction. The catalytic effect is proportional to the strength of the organic acids. For example, for the formation of syn-hahp catalyzed by H 2O (pk a = 15.7), formic acid (pk a = 3.75) and oxalic acid (pk a = 1.23), the energy barrier is reduced from to 40.78, and kj mol -1, respectively. In addition, the non-catalytic reaction has a positive activation energy, whereas the catalytic reactions have an negative apparent activation energy. Key Words: Criegee intermediate; CH 3CHOO; Acid catalysis; Addition reaction Received: July 18, 2016; Revised: September 13, 2016; Published online: September 14, * Corresponding author. wlwang@snnu.edu.cn; Tel: The project was supported by the National Natural Science Foundation of China ( , ), Fundamental Research Funds for Shaanxi Innovative Team of Key Science and Technology, China (2013KCT-17), and Fundamental Research Funds for the Central Universities, China (JK ). 国家自然科学基金 ( , ), 陕西省重点科技创新团队基金 (2013KCT-17) 和中央高校基本科研业务费专项资金 (JK ) 资助项目 Editorial office of Acta Physico-Chimica Sinica
2 No.12 高志芳等 :Criegee 中间体 CH 3CHOO 与 H 2O 反应机理及酸催化效应 引言 烯烃的臭氧化反应生成 Criegee 中间体反应机 理如示意图 1 上部框图所示,O 3 两端的氧首先协同 加到烯烃双键碳上, 形成初级臭氧化物 (POZ), 接 着发生 C=C 键断裂分解形成羰基化合物和 Criegee 中间体 CIs 1 CIs 是高反应活性物种, 可与大气中 的 HCHO CO NO NO 2 SO 2 H 2O OH 等发 2-4 生反应 由于水是大气中分布最广 浓度最高 的气体组分之一, 因此 CIs 与水的反应是大气中最 为重要的反应之一, 可引发羟基烷基取代的氢过 氧化物 有机酸 羰基化合物和 H 2O 等生成 ( 示 意图 1 下部框图所示 ), 这些物种对酸雨及气溶胶 形成等大气环境问题具有重要影响 因此,Criegee 中间体与水的反应格外受到关注 日常生活和 工业排放产生的短链烯烃 ( 4 个 C) 是大气的主要 污染物之一 8, 与 O 3 反应生成活性较高的 Criegee 中 间体 R 2COO( 如 CH 3CHOO) CH 3CHOO 与 H 2O 反 应的机理为 H 2O 中的 OH 加成到 α-c 上, 同时 H 2O 的另一个 H 迁移到 CH 3CHOO 的端氧上, 生成一个 羟基取代的氢过氧化物 CH 3CH(OH)(OOH) (α-hydroxyalkyl hydroperoxide, HAHP) 9,10 Monod 等 从实验上观察到酸雨中羟基取代的氢过氧化物浓 度较高, 并推测其主要是来源于 CIs 与 H 2O 的反 11 应 这类羟基取代的氢过氧化物在大气条件下不 稳定, 既可以参与二次有机气溶胶的形成, 也可 以分解生成甲酸 醛 酮 羟基和过氧化氢 文献报道 H 2O 及甲酸等能够有效地降低一些水 解反应体系反应能垒, 促使二次有机气溶胶的形 成, 且甲酸的催化效果比 H 2O 催化更为显著 遗憾 的是关于有机酸对 Criegee 中间体 CH 3CHOO 与 H 2O 反应是否有催化作用 酸性强弱与催化效应间的 关系 有机酸的参与方式等问题目前还未见文献 详细报道 因此本文采用 CCSD(T)//B3LYP/ G(d,p) 方法对标题反应的机理及酸催化效应等问题 进行了详细研究, 以期回答上述问题 2 计算方法 最新文献报道, syn-ch 3CHOO 与 anti- CH 3CHOO 构象的基态电子结构主要为闭壳层单重 22,23 态特征, 本文计算中所涉及的其它物种也均为 单重态, 波函数的自旋污染问题可以忽略 另 外, 我们前文选用 B3LYP/6-311+G(d,p) 方法优化获 得了合理的几何构型 3 因此本文仍选用 B3LYP/6-311+G(d,p) 方法对反应通道上的各个驻点 ( 反应 物 中间体 过渡态和产物 ) 的几何构型进行了全 参数优化, 并进行内禀反应坐标 (IRC) 分析, 以证 Scheme 1 示意图 1 烯烃臭氧分解形成羰基化合物及其后续与 H 2O 反应机理示意图 Diagram of reaction mechanism for ozonolysis of alkenes forming carbonyl compound and the subsequent reaction with H 2O
3 2900 Acta Phys. -Chim. Sin Vol.32 实反应物 中间体 过渡态 产物的相关性, 通 过振动频率分析确认各驻点构型为势能面上的极 值点 为了更加合理地预测反应路径能量信息, 采用 CCSD(T)/6-311+G(d,p) 方法对所有驻点进行了 单点能计算, 得到各反应通道中物种的能量信息 24 与反应能垒 所有计算基于 Gaussian 09 程序完 成 3 结果与讨论 3.1 Criegee 中间体 CH 3CHOO 与 H 2O 反应机理 虽然 CH 3CHOO 与 H 2O 的反应机理以及单个水 17,25 分子对主通道的催化作用已有文献报道, 但为 了与本文所研究的 6 种有机酸催化效应比较, 图 1 仍然绘出了 CH 3CHOO + H 2O 所有反应通道 ( 加成和 双质子迁移反应 ) 的势能面, 详细的能量信息 T 1 检验值及有机酸的 pk a 值等列在表 S1 (Supporting Information) 中 表 S1 中 T 1 检验值均远小于 0.044, 在此表明本文选用 CCSD(T)//B3LYP/6-311+G(d,p) 26,27 方法是合理的 从图 1 看出,CH 3CHOO 与 H 2O 发生加成反应生成 syn-hahp( 图 1 右 ) 及 anti-hahp ( 图 1 左 ) 为优势通道 形成中间体 RC1-s 和 RC2-a 放出约 30 kj mol - 1 的能量, 经过渡态 (TS2-s 和 TS2-a) 生成产物对应基元反应能垒分别为 和 kj mol , 与文献采用 CCSD(T)//6-311+G (2d,2p) 计算形成中间体放出 和 kj mol -1 的能量以及基元反应能垒分别为 和 kj mol -1 的结论基本一致 从反应中间体 RC1-s 和 RC1-a 出发, 分别经过 渡态 TS1-s 和 TS1-a, 分别生成了产物 CH 2CHO + OH + H 2O 和 CH 3CO + OH + H 2O 这是一个双质子 迁移过程, 即 RC1-s 中 β-c 上的 H9 迁移到 H 2O 中 O4 上的同时,H 2O 上的 H5 也迁移到端 O3 上 从 能量数据看出, 双质子迁移过程的能垒高于加成 反应通道, 且放出的能量也少于加成反应通道, 并不是优势反应通道, 因此本文只讨论有机酸对 加成反应通道的催化作用 3.2 H 2O 催化加成生成 HAHP 机理 在催化加成通道中, 包括催化剂在内是三分 子反应 事实上三分子同时碰撞直接反应的几率 很小, 目前多数文献按先形成双分子复合物再与 第三个分子进行反应的方式处理 反应物与催 化剂形成反应复合物有两种结合方式 : 一是反应 物之一 H 2O 与催化剂 CA 先形成复合物 H 2O CA, 然后再与 CH 3CHOO 形成三分子复合物 CH 3CHOO H 2O CA; 二是先形成 CH 3CHOO H 2O 再与 CA 形成 CH 3CHOO H 2O CA 图 2 示 出 H 2O 对 CH 3CHOO + H 2O 主通道催化反应势能面 及相应驻点物种的几何构型 从结构图看出, 反 应物 H 2O 中 OH 上的 O 端加到 Criegee 中间体的 α-c 上, 另一个 H 迁移到催化剂 H 2O 中的 O 上, 同时催 化剂 H 2O 上的 H 迁移到 Criegee 中间体端位 O 上, 释放出约 70 kj mol -1 的能量 显然催化剂 H 2O 以氢 Fig.1 图 1 CCSD(T)//B3LYP/6-311+G(d,p) 水平上 CH 3CHOO + H 2O 反应势能剖面 Potential energy surface of CH 3CHOO + H 2O reaction at the CCSD(T)//B3LYP/6-311+G(d,p) level energy in kj mol -1 ; anti-: anti-ch3choo, syn-: syn-ch3choo
4 No.12 高志芳等 :Criegee 中间体 CH 3CHOO 与 H 2O 反应机理及酸催化效应 2901 图 2 Fig.2 CCSD(T)//B3LYP/6-311+G(d,p) 水平上水催化 CH 3CHOO + H 2O 加成反应势能剖面 Potential energy surface of the addition reaction for CH 3CHOO + H 2O assisted by water at the CCSD(T)//B3LYP/6-311+G(d,p) level energy in kj mol -1, bond distance in nm, angle in degree 键复合物的形式参与反应, 起到传递质子的作 用, 降低了基元反应能垒和表观活化能 水催化 下 syn- 和 anti- 与 H 2O 反应的基元反应能垒分别是 和 kj mol -1 17, 与文献采用 CCSD(T)//6-311+G(2d,2p) 方法计算所得 和 kj mol -1 的报道值吻合 与裸反应相比, 水分子可使 syn- 和 anti- 加成反应的基元反应能垒分别降低了 和 kj mol 这与文献报道 H 2O 能有效降低 一些水解反应能垒的结论一致 因此, 大气中 H 2O 的存在会加速 Criegee 中间体 CH 3CHOO 生成羟基 取代的氢过氧化物 CH 3CH(OH)(OOH) (HAHP), 进 而促使二次有机气溶胶形成 3.3 甲酸催化加成生成 HAHP 机理 甲酸 HCOOH 催化 CH 3CHOO+H 2O 反应机理仍 然是反应物 H 2O 中的 OH 加成到 α-c 上,H 迁移到 HCOOH 的羰基 C=O 氧原子上, 同时 HCOOH 的 OH 上的 H 迁移到 Criegee 中间体的端位氧原子上, 生成 CH 3C(OH)(OOH)H (HAHP) 催化剂 HCOOH 作为桥梁传递质子, 促进了 H 迁移 从图 3 看出, HCOOH 催化时, 复合物的形成有 3 种方式 : 一是 先形成复合物 H 2O HCOOH 再与 CH 3CHOO 反 应, 二是先形成复合物 CH 3CHOO H 2O 再与 HCOOH 反应, 三是先形成复合物 CH 3CHOO HCOOH 再与 H 2O 反应 但不论复合物形成次序如何, 最终均形成十元环结构的 H 2O HCOOH CH 3CHOO(syn-/anti-) 三分子复合物 RC4-s 和 RC4- a, 分别释放 和 kj mol -1 的能量, 远远 大于 H 2O 水催化体系, 说明甲酸 HCOOH 催化体系 中氢键作用更强, 复合物更稳定 复合物 RC4-s 与 RC4-a 经过过渡态 TS4-s 与 TS4-a, 分别越过 与 kj mol - 1 的能垒生成产物 HAHP 和 HCOOH 与 H 2O 催化相比,HCOOH 催化反应能 垒更低 这是因为 HCOOH 催化形成复合物和过渡 态中的氢键 O H 及 C1 O4 相互作用强于 H 2O 催 化体系 从图 4 所示的有关过渡态结构中也可看 出, 在 H 2O 催化 syn- + H 2O 过渡态 TS3-s 中, CH 3CHOO 与 H 2O 之间将要形成的 C1 O4 及 O3 H8 键长分别为 和 nm 而 HCOOH 催化 syn- + H 2O 过渡态 TS4-s 中,C1 O4 及 O3 H10 键长相对较短, 分别为 和 nm 显然 TS4-s 中氢键更强, 能量较低 另一方面从七元环 的 TS3-s 到十元环的 TS4-s, 张力减小 从图 3 和图 4 看出,HCOOH 催化 anti- + H 2O 反应也存在类似 的情况 3.4 六种不同酸催化效果差异分析 H 2O 及 HCOOH 等对 CH 3CHOO + H 2O 的加成 反应有不同的催化效果, 主要是与形成氢键的个 数 强度及环结构的大小有关 比较图 4 所列过渡 态结构可知, 非催化裸反应过渡态 TS2-s 及 TS2-a 中只存在 1 个氢键, 而在 H 2O 催化加成反应 TS3-s 及 TS3-a,HCOOH 催化加成反应 TS4-s 及 TS4-a 中 均形成 2 个氢键, 不同之处是 H 2O 催化过渡态是七
5 2902 Acta Phys. -Chim. Sin Vol.32 图 3 CCSD(T)//B3LYP/6-311+G(d,p) 水平上甲酸催化 CH 3CHOO + H 2O 加成反应势能剖面 Fig.3 Potential energy surface of the addition reaction for CH 3CHOO + H 2O assisted by formic acid at the CCSD(T)//B3LYP/6-311+G(d,p) level energy in kj mol -1, bond distance in nm, angle in degree 元环构型, 而 HCOOH 催化过渡态是十元环构型 另外, 一般情况下, 当氢键 (X H Y) 的给体 (Y) 与受体 (X) 越接近 成直线, 越有利于电子从 21,22 Y 传递到 X, 反应越容易进行 从图 4 所示结构 看出, 裸反应过渡态 TS2-s 及 TS2-a 中仅有的氢键 O H O 键角为 146.6,H 2O 催化体系中的 2 个 O H O 键角分别为 和 164.8,HCOOH 催 化体系中 2 个 O H O 键角分别为 和 175.3, 逐步趋向于更合理构型, 更有利于形成强氢键 对于本文研究的催化体系, 将更有利于氢键 X H Y 中 X H 的断裂与 H Y 的形成, 即更有利于 H 的转移, 促进加成反应的进行 另外, 本文还考察了乙酸 (pk a = 3.75) 丙酸 (pk a = 4.87) 氟乙酸 (pk a = 2.59) 氯乙酸 (pk a = 2.86) 草酸(pK a = 1.23) 等不同强度酸的催化效应, 详细能量信息列在表 S1, 基元反应能垒与表观活 Fig.4 图 4 B3LYP/6-311+G(d,p) 水平上优化过渡态几何构型 Structures of transition state obtained at B3LYP/6-311+G(d,p) level bond distance in nm, angle in degree
6 No.12 高志芳等 :Criegee 中间体 CH 3CHOO 与 H 2O 反应机理及酸催化效应 2903 表 1 在 CCSD(T)//B3LYP/6-311+G(d,p) 水平上非催化和催化反应的基元反应能垒 (E bar) 和表观活化能 (E app) Table 1 Elementary reaction energy barrier (E bar) and apparent activation energy (E app) of the naked reaction and catalytic reaction at the CCSD(T)//B3LYP/6-311+G(d,p) level Catalytic non-catalytic H2O CH3CH2COOH CH3COOH HCOOH CH2ClCOOH CH2FCOOH (COOH)2 pka Ebar/(kJ mol -1 ) Eapp/(kJ mol -1 ) syn- anti- syn- anti 化能列在表 1 中, 并示于图 5 从表 1 和图 5 看出, 随 pk a 值的减小, 即酸强度增大, 基元反应能垒与 表观活化能逐渐降低 草酸 (COOH) 2 的 pk a 值最 小, 反应能垒降低最明显, 基元反应能垒从非催 化反应的 (syn-) 和 (anti-) kj mol -1 大幅 度降为 (syn-) 和 4.52 kj mol -1 (anti-) 有机酸 催化活性显著差异的原因是因为解离出质子能力 差异所致 当酸强度越大, 越易于解离出质子, 也就是越有利于氢键 X H Y 中 X H 的断裂与 H Y 的形成, 即 H 迁移到 CH 3CHOO 端位氧的能垒就越小 因此水及有机酸可显著加速大气中 Criegee 中间体水解反应, 生成羟基取代氢过氧化物 这类羟基取代的氢过氧化物在大气条件下不稳定, 可分解生成甲酸 醛 酮 羟基和过氧化氢, 过氧化氢可引发二次有机气溶胶的形成, 甲酸等可催化加速引发二次有机气溶胶的形成 同 29,31 时, 甲酸等也可促使无机气溶胶的形成 4 结论在 CCSD(T)//B3LYP/6-311+G(d,p) 水平上计算研究了 H 2O 及 HCOOH 等六种有机酸催化 CH 3CHOO + H 2O 加成反应机理和动力学, 结果表明 : (1) CH 3CHOO + H 2O 非催化反应存在双质子迁移和加成反应 2 条通道, 其中加成反应虽然能垒较高, 但仍为优势通道 其加成机理为 H 2O 中 OH 加到 CH 3CHOO 的 α-c 上,H 2O 中另一个 H 迁移到 CH 3CHOO 的端 O 上 (2) 有机酸能够显著影响降低加成反应能垒和表观活化能, 且催化效应与有机酸的强度成正比, 即 pk a 值越小, 反应势垒降低越明显 其原因可能是有机酸的强度强度越大, 越有利于复合物氢键 X H Y 中 X H 的断裂与 H Y 的形成, 即越有利于 H 质子转移 所有催化反应均表现出负的表观活化能 Supporting Information: Electric density of transfer H, relative energies, relative enthalpies, relative Gibbs free energies (kj mol - 1 ), and T 1 for the title reaction system have been included. This information is available free of charge via the internet at References (1) Johnson, D.; Marston, G. Chem. Soc. Rev. 2008, 37 (27), 699. doi: /b704260b (2) Kroll, J. H.; Sahay, S. R.; Anderson, J. G. J. Phys. Chem. A 2001, 105 (18), doi: /acs.jpca.5b07295 (3) Gao, Z. F.; Wang, W. N.; Ma, Q.; Liu, F. Y.; Wang, W. L. Chem. J. Chin. Univ. 2016, 37 (3), 513. [ 高志芳, 王渭娜, 马倩, 刘峰毅, 王文亮. 高等学校化学学报, 2016, 37 (3), 513.] doi: /cjcu (4) Qi, B.; Chao, Y. T. Acta Chim. Sin. 2007, 65 (19), [ 齐 图 5 不同催化剂对 CH 3CHOO + H 2O 加成反应能垒的影响 Fig.5 Potential energy profiles of CH 3CHOO + H 2O in the presence of catalysts color online 斌, 晁余涛. 化学学报, 2007, 65 (19), 2117.] (5) Ga b, S.; Hellpointner, E.; Turner, W. V.; Korte, F. Nature 1985, 316, 535. doi: /318080a0 (6) Neeb, P.; Sauer, F.; Horie, O.; Moortgat, G. K. Atmos. Environ.
7 2904 Acta Phys. -Chim. Sin Vol , 31, doi: /S (96) (7) Wolff, S.; Boddenberg, A.; Thamm, J.; Turner, W.; Ga b, V. S. Atmos. Environ. 1997, 31, doi: /S (97) (8) Paulson, S. E.; Chung, M. Y.; Hasson, A. S. J. Phys. Chem. A 1999, 103 (41), doi: /jp991995e (9) Anglada, J. M.; Aplincourt, P.; Boll, J. M.; Cremer, D. ChemPhysChem 2002, 3, 215. doi: / ( )3:2<215::AID-CPHC215>3.0.CO:2-3 (10) Zhu, C. Q.; Manoj, K.; Zhong, J.; Li, L.; Joseph, S. F.; Zeng, X. C. J. Am. Chem. Soc. 2016, doi: /jacs.6b04338 (11) Monod, A.; Chebbi, A.; Durand-Jolibois, R.; Carlier, P. Atmos. Environ. 2000, 34 (29), doi: /S (00) (12) Rieche, A.; Meister, R. Berichte Der Deutschen Chemischen Gesellschaft 1935, 68 (8), doi: /cber (13) Neeb, P.; Sauer, F.; Horie, O. Atmos. Environ. 1997, 31 (10), doi: /S (96) (14) Sauer, F.; Schafer, C.; Neeb, P.; Horie, O.; Horie, G. K. Atmos. Environ. 1999, 33 (2), 229. doi: /S (98) (15) Hewitt, C. N.; Kok, G. L. J. Atmos. Chem. 1991, 12 (12), 181. doi: /BF (16) Hazra, K.; Sinha, A. J. Am. Chem. Soc. 2011, 133 (43), doi: /ja207393v (17) Ryzhkov, A. B.; Ariya, P. A. Phys. Chem. Chem. Phys. 2004, 6 (21), doi: /B408414D (18) Hazra, M. K.; Francisco, J. S.; Sinha, A. J. Phys. Chem. A 2013, 117 (46), doi: /jp (19) Louie, M. K.; Francisco, J. S.; Verdicchio, M.; Klippenstein, S. J.; Sinha, A. J. Phys. Chem. A 2015, 119 (19), doi: /jp (20) Rypkema, H. A.; Sinha, A.; Francisco, J. S. J. Phys. Chem. A 2015, 119 (19), doi: /jp510704j (21) Liu, J. J.; Fang, S.; Bing, Q. M.; Tao, F. M.; Liu, J. Y. Comput. Theor. Chem. 2015, 1076, 11. doi: /j.comptc (22) Li, H. W.; Fang, Y.; Kidwell, N. M.; Beames, J. M.; Lester, M. I. J. Phys. Chem. A 2015, 119 (30), doi: /acs. jpca.5b05352 (23) Kettner, M.; Karton, A.; McKinley, A. J.; Wild, D. A. Chem. Phys. Lett. 2015, 621, 193. doi: /j.cplett (24) Frisch, M. J.; Trucks, G. W.; Schlegel, H. B.; et al. Gaussian 09, Revision C.01; Gaussian Inc.: Wallingford, CT, (25) Sheps, L.; Scully, A. M.; Au, K. Phys. Chem. Chem. Phys. 2014, 16, doi: /c4cp04408h (26) Lee, T. J.; Taylor, P. R. Int. J. Quantum Chem. 2009, 36 (S23), 199. doi: /qua (27) Rienstra-Kiracofe, J. C.; Allen, W. D.; Schaefer, H. F., III. J. Phys. Chem. A 2000, 104 (44), doi: /jp001041k (28) Robert, J. B.; John, R. B.; Joseph, S. F. J. Phys. Chem. A 2012, 116, doi: /jp (29) Hazra, M. K.; Sinha, A. J. Am. Chem. Soc. 2011, 133, doi: /ja207393v (30) Javier, G.; Josep, M. A.; Robert, J. B.; Joseph, S. F. J. Am. Chem. Soc. 2011, 133, doi: /ja100976b (31) Herb, J.; Nadykto, A. B.; Yu, F. Chem. Phys. Lett. 2011, 518, 7. doi: /j.cplett
8 Supporting Information for Acta Phys. -Chim. Sin. 2016, 32 (12), doi: /PKU.WHXB Criegee 中间体 CH 3 CHOO 与 H 2 O 反应机理及酸催化效应 高志芳周丽婷王渭娜刘峰毅王文亮 * ( 陕西省大分子科学重点实验室, 陕西师范大学化学化工学院, 西安 ) Reaction Mechanism of Criegee Intermediate CH 3 CHOO with H 2 O and the Acid Catalytic Effect GAO Zhi-Fang ZHOU Li-Ting WANG Wei-Na LIU Feng-Yi WANG Wen-Liang* (School of Chemistry and Chemical Engineering, Shaanxi Normal University, Key Laboratory for Macromolecular Science of Shaanxi Province, Xi'an , P. R. China) Corresponding author. wlwang@snnu.edu.cn; Tel: S1
9 表 S1 CCSD(T)//B3LYP/6-311+G(d,p) 水平上标题反应的相对能量 相对焓 相对吉普斯 自由能 (kj mol -1 ) 和 T 1 检验值 Table S1 Relative energies, relative enthalpies, relative Gibbs free energies (kj mol -1 ), and T 1 for the title reaction system at the CCSD(T)//B3LYP/6-311+G(d,p) level pk a stationary point CH 3 CHOO E H G T 1 non-catalytic - RC syn anti TS syn anti PC syn anti H 2 O 15.7 RC syn anti TS syn anti PC syn anti CH 3 CH 2 COOH 4.87 RC syn anti TS syn anti PC syn anti CH 3 COOH 4.75 RC syn anti TS syn anti PC syn anti HCOOH 3.75 RC syn anti TS syn anti PC syn anti CH 2 ClCOOH 2.86 RC syn anti TS syn anti S2
10 PC syn anti CH 2 FCOOH 2.59 RC syn anti TS syn anti PC syn anti (COOH) RC syn anti TS syn anti PC syn anti 表 S2 B3LYP/6-311+G(d,p) 水平上 CH 3 CHOO+H 2 O 反应中转移 H 的电荷密度 Table S2 Electric density of transfer H in CH 3 CHOO+H 2 O reaction at the B3LYP/6-311+G(d,p) level Mulliken NBO H OH H OH RC1-s RC2-a non-catalytic TS2-s TS2-a syn-hahp anti-hahp RC3-s RC3-a H 2 O-catalytic TS3-s TS3-a PC3-s PC3-a S3
11 RC4-s RC4-a HCOOH-catalytic TS4-s TS4-a PC4-s PC4-a S4
在 培 养 职 前 卓 越 化 学 教 师 的 院 校, 会 编 一 本 过 去 称 作 化 学 教 学 论 实 验, 现 在 拟 为 卓 越 化 学 教 师 教 育 实 验 教 学 研 究 的 教 材 各 院 校 对 这 门 课 程 所 给 的 学 时 不 太 一 样, 但 都 是 围 绕 实 验
 doi: 10.3866/pku.DXHX201607011 卓 越 化 学 教 师 教 育 实 验 教 学 研 究 课 程 探 微 * 杨 承 印 汪 蒙 蒙 赵 洋 ( 陕 西 师 范 大 学 化 学 化 工 学 院, 西 安 710119) 摘 要 : 在 对 实 验 操 作 进 行 编 码 的 基 础 上 对 高 中 化 学 课 程 标 准 中 有 关 实 验 进 行 统 计 分 析, 以
doi: 10.3866/pku.DXHX201607011 卓 越 化 学 教 师 教 育 实 验 教 学 研 究 课 程 探 微 * 杨 承 印 汪 蒙 蒙 赵 洋 ( 陕 西 师 范 大 学 化 学 化 工 学 院, 西 安 710119) 摘 要 : 在 对 实 验 操 作 进 行 编 码 的 基 础 上 对 高 中 化 学 课 程 标 准 中 有 关 实 验 进 行 统 计 分 析, 以
Microsoft Word - 793-797 tb20150504赵宏宇s-高校教改纵横.doc
 微 生 物 学 通 报 Microbiology China tongbao@im.ac.cn Apr. 20, 2016, 43(4): 793 797 http://journals.im.ac.cn/wswxtbcn DOI: 10.13344/j.microbiol.china.150504 高 校 教 改 纵 横 生 物 工 程 专 业 发 酵 课 程 群 建 设 探 索 * 赵 宏 宇
微 生 物 学 通 报 Microbiology China tongbao@im.ac.cn Apr. 20, 2016, 43(4): 793 797 http://journals.im.ac.cn/wswxtbcn DOI: 10.13344/j.microbiol.china.150504 高 校 教 改 纵 横 生 物 工 程 专 业 发 酵 课 程 群 建 设 探 索 * 赵 宏 宇
220 20, Vol. 32, No. 6 食 品 科 学 分 析 检 测 荡 体 系 被 用 来 检 测 和 鉴 别 组 成 极 其 复 杂 的 中 药 2007 年 [7-20] 张 泰 铭 等 提 出 了 中 药 非 线 性 化 学 指 纹 图 谱 的 概 念, 并 对 其 形 成 的 原
![220 20, Vol. 32, No. 6 食 品 科 学 分 析 检 测 荡 体 系 被 用 来 检 测 和 鉴 别 组 成 极 其 复 杂 的 中 药 2007 年 [7-20] 张 泰 铭 等 提 出 了 中 药 非 线 性 化 学 指 纹 图 谱 的 概 念, 并 对 其 形 成 的 原 220 20, Vol. 32, No. 6 食 品 科 学 分 析 检 测 荡 体 系 被 用 来 检 测 和 鉴 别 组 成 极 其 复 杂 的 中 药 2007 年 [7-20] 张 泰 铭 等 提 出 了 中 药 非 线 性 化 学 指 纹 图 谱 的 概 念, 并 对 其 形 成 的 原](/thumbs/42/22870184.jpg) 29 赵 哲, 张 泰 铭, *, 方 宣 启 2, 向 凤 琴, 乔 君 喜, 朱 蓉 (. 中 南 大 学 化 学 化 工 学 院, 湖 南 长 沙 40083;2. 湖 南 省 食 品 质 量 监 督 检 验 所, 湖 南 长 沙 40002) 通 过 向 稳 态 体 系 溴 酸 钠 - 硫 酸 锰 - 硫 酸 - 丙 酮 中 加 入 不 同 的 茶 饮 料, 获 得 来 自 不 同 产 家
29 赵 哲, 张 泰 铭, *, 方 宣 启 2, 向 凤 琴, 乔 君 喜, 朱 蓉 (. 中 南 大 学 化 学 化 工 学 院, 湖 南 长 沙 40083;2. 湖 南 省 食 品 质 量 监 督 检 验 所, 湖 南 长 沙 40002) 通 过 向 稳 态 体 系 溴 酸 钠 - 硫 酸 锰 - 硫 酸 - 丙 酮 中 加 入 不 同 的 茶 饮 料, 获 得 来 自 不 同 产 家
 August 大 学 化 学 (Daxue Huaxue) Univ. Chem. 2016, 31 (8), 71-75 71 化 学 实 验 doi: 10.3866/PKU.DXHX201510028 www.dxhx.pku.edu.cn 高 校 化 学 实 验 教 学 中 产 生 的 化 学 废 物 的 回 收 及 处 理 * 兰 景 凤 俞 娥 ( 兰 州 大 学 化 学 化 工 学 院,
August 大 学 化 学 (Daxue Huaxue) Univ. Chem. 2016, 31 (8), 71-75 71 化 学 实 验 doi: 10.3866/PKU.DXHX201510028 www.dxhx.pku.edu.cn 高 校 化 学 实 验 教 学 中 产 生 的 化 学 废 物 的 回 收 及 处 理 * 兰 景 凤 俞 娥 ( 兰 州 大 学 化 学 化 工 学 院,
果葡糖浆中5-HMF生成影响因素及其去除方法
 Journal of Advances in Physical Chemistry 物 理 化 学 进 展, 2013, 2, 27-32 http://dx.doi.org/10.12677/japc.2013.23005 Published Online August 2013 (http://www.hanspub.org/journal/japc.html) Influencing Factors
Journal of Advances in Physical Chemistry 物 理 化 学 进 展, 2013, 2, 27-32 http://dx.doi.org/10.12677/japc.2013.23005 Published Online August 2013 (http://www.hanspub.org/journal/japc.html) Influencing Factors
Supporting information Combination of N-Arylstilbazolium Organic Nonlinear Optical Chromophores with Iodoargentates: Structural Diversities and Optica
 Supporting information Combination of N-Arylstilbazolium Organic Nonlinear Optical Chromophores with Iodoargentates: Structural Diversities and Optical Properties Yu-Kang Wang, Li-Ming Zhao, Yu-Qing Fu,
Supporting information Combination of N-Arylstilbazolium Organic Nonlinear Optical Chromophores with Iodoargentates: Structural Diversities and Optical Properties Yu-Kang Wang, Li-Ming Zhao, Yu-Qing Fu,
物理学报 Acta Phys. Sin. Vol. 62, No. 14 (2013) 147802 叠 [4]. PET 设备最重要的部件就是探测器环, 探测 备重建图像具有减少数据插值的优势. 器环的性能直接影响 PET 的成像能力. 探头与探头 之间得到的符合直线叫做投影线. 所有的投影线在
![物理学报 Acta Phys. Sin. Vol. 62, No. 14 (2013) 147802 叠 [4]. PET 设备最重要的部件就是探测器环, 探测 备重建图像具有减少数据插值的优势. 器环的性能直接影响 PET 的成像能力. 探头与探头 之间得到的符合直线叫做投影线. 所有的投影线在 物理学报 Acta Phys. Sin. Vol. 62, No. 14 (2013) 147802 叠 [4]. PET 设备最重要的部件就是探测器环, 探测 备重建图像具有减少数据插值的优势. 器环的性能直接影响 PET 的成像能力. 探头与探头 之间得到的符合直线叫做投影线. 所有的投影线在](/thumbs/41/22573722.jpg) 数 据 插 值 对 正 电 子 发 射 断 层 成 像 设 备 的 图 像 重 建 影 响 的 研 究 * 杨 昆 刘 新 新 李 晓 苇 ( 河 北 大 学 物 理 学 院, 保 定 071000 ) ( 2013 年 1 月 30 日 收 到 ; 2013 年 4 月 9 日 收 到 修 改 稿 ) 正 电 子 发 射 断 层 扫 描 (positron emission computed tomography,
数 据 插 值 对 正 电 子 发 射 断 层 成 像 设 备 的 图 像 重 建 影 响 的 研 究 * 杨 昆 刘 新 新 李 晓 苇 ( 河 北 大 学 物 理 学 院, 保 定 071000 ) ( 2013 年 1 月 30 日 收 到 ; 2013 年 4 月 9 日 收 到 修 改 稿 ) 正 电 子 发 射 断 层 扫 描 (positron emission computed tomography,
, Vol.34, No.21 nm nm nm nm μm μm μm a b c d e
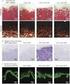 2013, Vol.34, No.21 359 Abstract Key words TS201.2 A 360 2013, Vol.34, No.21 nm nm nm nm μm μm μm a b c d e 2013, Vol.34, No.21 361 362 2013, Vol.34, No.21 ph ph 2013, Vol.34, No.21 363 () (1) (2) (SiO
2013, Vol.34, No.21 359 Abstract Key words TS201.2 A 360 2013, Vol.34, No.21 nm nm nm nm μm μm μm a b c d e 2013, Vol.34, No.21 361 362 2013, Vol.34, No.21 ph ph 2013, Vol.34, No.21 363 () (1) (2) (SiO
Molecules 2017, 22, 236; doi: /molecules S1 of S21 Supplementary Materials: Bioactive Stilbenes from Cortex Mori Radicis, and Their Neur
 S1 of S21 Supplementary Materials: Bioactive Stilbenes from Cortex Mori Radicis, and Their Neuroprotective and Analgesic Activities Mediated by mglur1 Ya-Nan Wang, Mao-Feng Liu, Wei-Zhen Hou, Rui-Ming
S1 of S21 Supplementary Materials: Bioactive Stilbenes from Cortex Mori Radicis, and Their Neuroprotective and Analgesic Activities Mediated by mglur1 Ya-Nan Wang, Mao-Feng Liu, Wei-Zhen Hou, Rui-Ming
1 GIS 95 Y = F y + (1 F) (1) 0 0 Y0 kg/hm 2 /day F y 0 y c kg/hm 2 /day [12] y m 20 kg/hm 2 /hour Y = cl cn ch G [ F( y ) T m yo + (2) (1 F)(
![1 GIS 95 Y = F y + (1 F) (1) 0 0 Y0 kg/hm 2 /day F y 0 y c kg/hm 2 /day [12] y m 20 kg/hm 2 /hour Y = cl cn ch G [ F( y ) T m yo + (2) (1 F)( 1 GIS 95 Y = F y + (1 F) (1) 0 0 Y0 kg/hm 2 /day F y 0 y c kg/hm 2 /day [12] y m 20 kg/hm 2 /hour Y = cl cn ch G [ F( y ) T m yo + (2) (1 F)(](/thumbs/91/104997423.jpg) 24 1 Vol.24 No.1 94 2008 1 Transactions of the CSAE Jan. 2008 2008 1 100094 2 100035 3 100081 4 100081 5 100101 GIS ( ) 65.12 16.82 13.74 15.27 11.07 t/(hm 2 a) 10.93% 41.43% 46.93% 65.4%. Bi Jiye, Zhu
24 1 Vol.24 No.1 94 2008 1 Transactions of the CSAE Jan. 2008 2008 1 100094 2 100035 3 100081 4 100081 5 100101 GIS ( ) 65.12 16.82 13.74 15.27 11.07 t/(hm 2 a) 10.93% 41.43% 46.93% 65.4%. Bi Jiye, Zhu
untitled
 20 1 2010 10 Vol.20 Special 1 The Chinese Journal of Nonferrous Metals Oct. 2010 1004-0609(2010)S1-s0127-05 Ti-6Al-4V 1 2 2 (1. 710016 2., 710049) 500~1 000 20 Ti-6Al-4V(TC4) TC4 800 TC4 800 TC4 TC4 800
20 1 2010 10 Vol.20 Special 1 The Chinese Journal of Nonferrous Metals Oct. 2010 1004-0609(2010)S1-s0127-05 Ti-6Al-4V 1 2 2 (1. 710016 2., 710049) 500~1 000 20 Ti-6Al-4V(TC4) TC4 800 TC4 800 TC4 TC4 800
128 中 南 大 学 学 报 ( 社 会 科 学 版 ) 2012 年 第 18 卷 第 5 期 毫 无 价 值, 而 且 还 会 遗 患 无 穷 随 着 社 会 生 活 节 奏 的 加 快 和 生 活 方 式 的 改 变, 食 品 供 应 将 日 益 社 会 化, 更 多 的 人 依 赖 食 品
 第 18 卷 第 5 期 中 南 大 学 学 报 ( 社 会 科 学 版 ) Vol.18 No.5 2012 年 10 月 J. CENT. SOUTH UNIV. (SOCIAL SCIENCE) Oct. 2012 论 食 品 安 全 伦 理 的 基 本 价 值 诉 求 喻 文 德 ( 吉 首 大 学 马 克 思 主 义 学 院, 湖 南 吉 首,416000) 摘 要 : 食 品 安 全 亟
第 18 卷 第 5 期 中 南 大 学 学 报 ( 社 会 科 学 版 ) Vol.18 No.5 2012 年 10 月 J. CENT. SOUTH UNIV. (SOCIAL SCIENCE) Oct. 2012 论 食 品 安 全 伦 理 的 基 本 价 值 诉 求 喻 文 德 ( 吉 首 大 学 马 克 思 主 义 学 院, 湖 南 吉 首,416000) 摘 要 : 食 品 安 全 亟
<4D6963726F736F667420576F7264202D203631372D3632312032303133303430333030312DBACEC0F25FD0A3B6D4B8E55F2DB6FED0A32D2D2DC8A5B5F4CDBCD6D0B5C4BBD8B3B5B7FBBAC52E646F63>
 第 4 卷 第 2 期 食 品 安 全 质 量 检 测 学 报 Vol. 4 No. 2 2013 年 4 月 Journal of Food Safety and Quality Apr., 2013 何 莉 *, 姜 笑 寒 ( 广 东 省 食 品 药 品 职 业 技 术 学 校, 广 州 510663) 摘 要 : 本 文 通 过 科 学 地 运 用 html5+jsp+sql 技 术, 建
第 4 卷 第 2 期 食 品 安 全 质 量 检 测 学 报 Vol. 4 No. 2 2013 年 4 月 Journal of Food Safety and Quality Apr., 2013 何 莉 *, 姜 笑 寒 ( 广 东 省 食 品 药 品 职 业 技 术 学 校, 广 州 510663) 摘 要 : 本 文 通 过 科 学 地 运 用 html5+jsp+sql 技 术, 建
<4D F736F F D20B8BDBCFEA3BAB9ABCABEC4DAC8DD2DB9FDB6C9BDF0CAF4D1F5BBAFCEEFC4C9C3D7BDE1B9B9D0C2D3B1B5C4CDE2B3A1D7F7D3C3CFECD3A6CCD8D0D4BCB0BBFAC0EDD1D0BEBF2E646F6378>
 / 20 SCI 1210 817 8 SCI 854 548 384 219 2018 1 NO 2 Adv MaterChem Soc RevJ Am Chem SocEnergy & Environmental ScienceAdv Funct MaterNano LettElectrochemistry Communications 8 854 384 2018 2 8 Adv MaterChem
/ 20 SCI 1210 817 8 SCI 854 548 384 219 2018 1 NO 2 Adv MaterChem Soc RevJ Am Chem SocEnergy & Environmental ScienceAdv Funct MaterNano LettElectrochemistry Communications 8 854 384 2018 2 8 Adv MaterChem
Microsoft Word - 050771.doc
 2005 年 第 25 卷 有 机 化 学 Vol. 25, 2005 第 7 期, 771~779 Chinese Journal of Organic Chemistry No. 7, 771~779 综 述 与 进 展 紫 草 素 的 全 合 成 研 究 进 展 徐 德 锋 管 鹏 健 毛 志 强 李 绍 顺 * ( 上 海 交 通 大 学 药 学 院 上 海 200030) 摘 要 综 述
2005 年 第 25 卷 有 机 化 学 Vol. 25, 2005 第 7 期, 771~779 Chinese Journal of Organic Chemistry No. 7, 771~779 综 述 与 进 展 紫 草 素 的 全 合 成 研 究 进 展 徐 德 锋 管 鹏 健 毛 志 强 李 绍 顺 * ( 上 海 交 通 大 学 药 学 院 上 海 200030) 摘 要 综 述
Hyperascyrones A–H, Polyprenylated Spirocyclic Acylphloroglucinol Derivatives from Hypericum ascyron Linn
 Electronic Supplementary Material (ESI) for rganic & Biomolecular Chemistry. This journal is The Royal Society of Chemistry 2018 Supplementary Material Anti-inflammatory fusicoccane-type diterpenoids from
Electronic Supplementary Material (ESI) for rganic & Biomolecular Chemistry. This journal is The Royal Society of Chemistry 2018 Supplementary Material Anti-inflammatory fusicoccane-type diterpenoids from
197 2 相 关 背 景 多 巴 胺 D 2 类 受 体 包 括 D 2 D 3 和 D 4 受 体 1975 年,Randrup 首 先 提 出, 多 巴 胺 可 能 参 与 抑 郁 症 的 发 病 后 来 Maj 等 通 过 一 系 列 的 实 验 证 明, 几 乎 所 有 的 长 期 抗 抑
 196 未 来 药 物 新 型 多 巴 胺 D 2 类 受 体 部 分 激 动 剂 brexpiprazole 刘 长 鹰 1, 于 鹏 2, 李 祎 亮 1 1. 天 津 药 物 研 究 院 天 津 市 新 药 设 计 与 发 现 重 点 实 验 室, 天 津 300193 2. 天 津 药 物 研 究 院 医 药 信 息 中 心, 天 津 300193 摘 要 : 在 多 巴 胺 D 2 类 受
196 未 来 药 物 新 型 多 巴 胺 D 2 类 受 体 部 分 激 动 剂 brexpiprazole 刘 长 鹰 1, 于 鹏 2, 李 祎 亮 1 1. 天 津 药 物 研 究 院 天 津 市 新 药 设 计 与 发 现 重 点 实 验 室, 天 津 300193 2. 天 津 药 物 研 究 院 医 药 信 息 中 心, 天 津 300193 摘 要 : 在 多 巴 胺 D 2 类 受
01-0982.doc
 第 32 卷 第 7 期 岩 土 工 程 学 报 Vol.32 No.7 2010 年 7 月 Chinese Journal of Geotechnical Engineering July 2010 沿 海 碎 石 回 填 地 基 上 高 能 级 强 夯 系 列 试 验 对 比 研 究 年 廷 凯 1,2, 水 伟 厚 3, 李 鸿 江 4, 杨 庆 1,2, 王 玉 立 (1. 大 连 理 工
第 32 卷 第 7 期 岩 土 工 程 学 报 Vol.32 No.7 2010 年 7 月 Chinese Journal of Geotechnical Engineering July 2010 沿 海 碎 石 回 填 地 基 上 高 能 级 强 夯 系 列 试 验 对 比 研 究 年 廷 凯 1,2, 水 伟 厚 3, 李 鸿 江 4, 杨 庆 1,2, 王 玉 立 (1. 大 连 理 工
BISQ理论模型与声波测井响应研究
 * BISQ, 133 BISQ BISQ BISQ BISQ BISQ : PACC: 43, 665, 913 1. [1], * (:4743). 119 133 431-8449917 431-898966 431-8941554 Email cuizwjlu@sina.com; kexiew@public.cc.jl.cn [] [3 4] Dvorkin Nur [5 6] - BISQ
* BISQ, 133 BISQ BISQ BISQ BISQ BISQ : PACC: 43, 665, 913 1. [1], * (:4743). 119 133 431-8449917 431-898966 431-8941554 Email cuizwjlu@sina.com; kexiew@public.cc.jl.cn [] [3 4] Dvorkin Nur [5 6] - BISQ
第 猿 猿 卷 第 愿 期 20 员 猿 年 愿 月 张 媛 媛 等 院 肥 胖 与 雌 激 素 的 相 互 关 系 及 其 对 子 宫 的 作 用 研 究 原 员 远 员 原 素 等 多 种 原 因 有 关 袁 对 于 女 性 而 言 绝 经 后 雌 激 素 水 平 下 降 是 更 年 期 肥 胖
 原 员 远 原 南 京 医 科 大 学 学 报 渊 自 然 科 学 版 冤 ACTA UNIVERSITATIS MEDICINALIS NANJING 渊 Natural Science 冤 第 猿 猿 卷 第 愿 期 20 员 猿 年 愿 月 肥 胖 与 雌 激 素 的 相 互 关 系 及 其 对 子 宫 的 作 用 研 究 张 媛 媛 袁 张 日 华 袁 薛 一 袁 刘 梦 兰 袁 黄 琼 袁
原 员 远 原 南 京 医 科 大 学 学 报 渊 自 然 科 学 版 冤 ACTA UNIVERSITATIS MEDICINALIS NANJING 渊 Natural Science 冤 第 猿 猿 卷 第 愿 期 20 员 猿 年 愿 月 肥 胖 与 雌 激 素 的 相 互 关 系 及 其 对 子 宫 的 作 用 研 究 张 媛 媛 袁 张 日 华 袁 薛 一 袁 刘 梦 兰 袁 黄 琼 袁
1.0 % 0.25 % 85μm % U416 Sulfate expansion deformation law and mechanism of cement stabilized macadam base of saline areas in Xinjiang Song
 1.0 % 0.25 % 85μm 0.97 0.136 % U416 Sulfate expansion deformation law and mechanism of cement stabilized macadam base of saline areas in Xinjiang Song Liang 1,2 Wang Xuan-cang 1 1 School of Highway, Chang
1.0 % 0.25 % 85μm 0.97 0.136 % U416 Sulfate expansion deformation law and mechanism of cement stabilized macadam base of saline areas in Xinjiang Song Liang 1,2 Wang Xuan-cang 1 1 School of Highway, Chang
Microsoft Word - 19王建华.doc
 2012 年 12 月 图 学 学 报 December 2012 第 33 卷 第 6 期 JOURNAL OF GRAPHICS Vol.33 No.6 工 程 图 学 计 算 机 辅 助 教 学 实 践 与 思 考 王 建 华, 郝 育 新, 刘 令 涛 ( 北 京 信 息 科 技 大 学 机 电 学 院, 北 京 100192) 摘 要 : 随 着 计 算 机 技 术 的 迅 猛 发 展 和
2012 年 12 月 图 学 学 报 December 2012 第 33 卷 第 6 期 JOURNAL OF GRAPHICS Vol.33 No.6 工 程 图 学 计 算 机 辅 助 教 学 实 践 与 思 考 王 建 华, 郝 育 新, 刘 令 涛 ( 北 京 信 息 科 技 大 学 机 电 学 院, 北 京 100192) 摘 要 : 随 着 计 算 机 技 术 的 迅 猛 发 展 和
Microsoft Word - 11--方刚_new_.doc
 第 44 卷 第 3 期 煤 田 地 质 与 勘 探 Vol. 44 No.3 2016 年 6 月 COAL GEOLOGY & EXPLORATION Jun. 2016 文 章 编 号 : 1001-1986(2016)03-0057-08 铜 川 玉 华 煤 矿 顶 板 离 层 水 突 水 机 理 与 防 治 方 刚 1,2,3, 靳 德 武 (1. 中 煤 科 工 集 团 西 安 研 究
第 44 卷 第 3 期 煤 田 地 质 与 勘 探 Vol. 44 No.3 2016 年 6 月 COAL GEOLOGY & EXPLORATION Jun. 2016 文 章 编 号 : 1001-1986(2016)03-0057-08 铜 川 玉 华 煤 矿 顶 板 离 层 水 突 水 机 理 与 防 治 方 刚 1,2,3, 靳 德 武 (1. 中 煤 科 工 集 团 西 安 研 究
JOURNAL OF EARTHQUAKE ENGINEERING AND ENGINEERING VIBRATION Vol. 31 No. 5 Oct /35 TU3521 P315.
 31 5 2011 10 JOURNAL OF EARTHQUAKE ENGINEERING AND ENGINEERING VIBRATION Vol. 31 No. 5 Oct. 2011 1000-1301 2011 05-0075 - 09 510405 1 /35 TU3521 P315. 8 A Earthquake simulation shaking table test and analysis
31 5 2011 10 JOURNAL OF EARTHQUAKE ENGINEERING AND ENGINEERING VIBRATION Vol. 31 No. 5 Oct. 2011 1000-1301 2011 05-0075 - 09 510405 1 /35 TU3521 P315. 8 A Earthquake simulation shaking table test and analysis
ph ph ph Langmuir mg /g Al 2 O 3 ph 7. 0 ~ 9. 0 ph HCO - 3 CO 2-3 PO mg /L 5 p
 1 2 1 2 3 1 2 1. 100054 2. 100054 3. 100036 ph ph ph Langmuir 166. 67 mg /g Al 2 O 3 ph 7. 0 ~ 9. 0 ph HCO - 4 5. 00 mg /L 5 ph doi 10. 13928 /j. cnki. wrahe. 2017. 03. 017 TV213. 4 + TU991. 26 + 6 A 1000-0860
1 2 1 2 3 1 2 1. 100054 2. 100054 3. 100036 ph ph ph Langmuir 166. 67 mg /g Al 2 O 3 ph 7. 0 ~ 9. 0 ph HCO - 4 5. 00 mg /L 5 ph doi 10. 13928 /j. cnki. wrahe. 2017. 03. 017 TV213. 4 + TU991. 26 + 6 A 1000-0860
/MPa / kg m - 3 /MPa /MPa 2. 1E ~ 56 ANSYS 6 Hz (a) 一阶垂向弯曲 (b) 一阶侧向弯曲 (c) 一阶扭转 (d) 二阶侧向弯曲 (e) 二阶垂向弯曲 (f) 弯扭组合 2 6 Hz
 31 3 Vol. 31 No. 3 218 9 Journal of Shijiazhuang Tiedao University Natural Science Edition Sep. 218 1 1 2 1 2 1 1. 543 2. 543 U462. 3 217-2 - 16 A 295-373 218 3-63 - 6 1-4 5-7 8-11 1 11 11 398 mm 86 mm
31 3 Vol. 31 No. 3 218 9 Journal of Shijiazhuang Tiedao University Natural Science Edition Sep. 218 1 1 2 1 2 1 1. 543 2. 543 U462. 3 217-2 - 16 A 295-373 218 3-63 - 6 1-4 5-7 8-11 1 11 11 398 mm 86 mm
* CUSUM EWMA PCA TS79 A DOI /j. issn X Incipient Fault Detection in Papermaking Wa
 2 *. 20037 2. 50640 CUSUM EWMA PCA TS79 A DOI 0. 980 /j. issn. 0254-508X. 207. 08. 004 Incipient Fault Detection in Papermaking Wastewater Treatment Processes WANG Ling-song MA Pu-fan YE Feng-ying XIONG
2 *. 20037 2. 50640 CUSUM EWMA PCA TS79 A DOI 0. 980 /j. issn. 0254-508X. 207. 08. 004 Incipient Fault Detection in Papermaking Wastewater Treatment Processes WANG Ling-song MA Pu-fan YE Feng-ying XIONG
TOPIC 专 题 45 1 加 快 农 业 大 数 据 发 展 的 现 实 意 义 农 业 大 数 据 运 用 大 数 据 的 理 论 技 术 和 方 法, 解 决 农 业 领 域 数 据 的 采 集 存 储 计 算 和 应 用 等 一 系 列 问 题, 大 数 据 技 术 是 保 障 国 家 粮
 44 山 东 省 农 业 大 数 据 发 展 刍 议 山 东 省 农 业 信 息 中 心, 山 东 济 南 250013 摘 要 关 键 词 doi: 10.11959/j.issn.2096-0271.2016005 Study on the agricultural big data development of Shandong province ZHENG Yong, MENG Lei, LI
44 山 东 省 农 业 大 数 据 发 展 刍 议 山 东 省 农 业 信 息 中 心, 山 东 济 南 250013 摘 要 关 键 词 doi: 10.11959/j.issn.2096-0271.2016005 Study on the agricultural big data development of Shandong province ZHENG Yong, MENG Lei, LI
相 关 报 道 近 年 来 临 床 上 运 用 多 种 针 灸 疗 法 治 疗 肥 胖 及 其 引 起 的 并 发 症, 如 高 脂 血 症 糖 尿 病 高 血 压 及 痛 经 等, 均 获 得 满 意 疗 效. caused by sedentary lifestyle and genetic f
 在 线 投 稿 : http://www.baishideng.com/wcjd/ch/index.aspx 帮 助 平 台 : http://www.wjgnet.com/esps/helpdesk.aspx DOI: 10.11569/wcjd.v24.i5.815 世 界 华 人 消 化 杂 志 2016 年 2 月 18 日 ; 24(5): 815-820 ISSN 1009-3079 (print)
在 线 投 稿 : http://www.baishideng.com/wcjd/ch/index.aspx 帮 助 平 台 : http://www.wjgnet.com/esps/helpdesk.aspx DOI: 10.11569/wcjd.v24.i5.815 世 界 华 人 消 化 杂 志 2016 年 2 月 18 日 ; 24(5): 815-820 ISSN 1009-3079 (print)
10.11648.j.sd.20160403.18
 Science Discovery 2016; 4(3): 202-206 http://www.sciencepublishinggroup.com/j/sd doi: 10.11648/j.sd.20160403.18 ISSN: 2331-0642 (Print); ISSN: 2331-0650 (Online) Construction for the Engineering Application-Oriented
Science Discovery 2016; 4(3): 202-206 http://www.sciencepublishinggroup.com/j/sd doi: 10.11648/j.sd.20160403.18 ISSN: 2331-0642 (Print); ISSN: 2331-0650 (Online) Construction for the Engineering Application-Oriented
s 15 contact s W Si 3 N μm N / m 4 AFM 95% AFM WPOJ UPOJ WPOJ UPOJ 260 ~ 280 nm WPOJ-DS UPOJ-DS 1 cm 1 cm DEAE-ce
 32 1 2013 2 Journal of Chinese Electron Microscopy Society Vol. 32 No. 1 2013-02 1000-6281 2013 01-0054-08 1 1* 2 1 1 1. 2. 710062 AFM SEM WPOJ-DS UPOJ-DS WPOJ-DS β- UPOJ-DS AFM WPOJ-DS UPOJ-DS SEM UPOJ-DS
32 1 2013 2 Journal of Chinese Electron Microscopy Society Vol. 32 No. 1 2013-02 1000-6281 2013 01-0054-08 1 1* 2 1 1 1. 2. 710062 AFM SEM WPOJ-DS UPOJ-DS WPOJ-DS β- UPOJ-DS AFM WPOJ-DS UPOJ-DS SEM UPOJ-DS
% GIS / / Fig. 1 Characteristics of flood disaster variation in suburbs of Shang
 20 6 2011 12 JOURNAL OF NATURAL DISASTERS Vol. 20 No. 6 Dec. 2011 1004-4574 2011 06-0094 - 05 200062 1949-1990 1949 1977 0. 8 0. 03345 0. 01243 30 100 P426. 616 A Risk analysis of flood disaster in Shanghai
20 6 2011 12 JOURNAL OF NATURAL DISASTERS Vol. 20 No. 6 Dec. 2011 1004-4574 2011 06-0094 - 05 200062 1949-1990 1949 1977 0. 8 0. 03345 0. 01243 30 100 P426. 616 A Risk analysis of flood disaster in Shanghai
708 北 京 工 业 大 学 学 报 2011 年 以 往 的 试 验 结 果 进 行 对 比, 选 取 15D 20D 作 为 对 比 参 数, 试 件 参 数 见 表 1. Fig. 1 图 1 试 件 尺 寸 及 配 筋 图 ( mm) Geometry and reinforcement
 第 37 卷 第 5 期 2011 年 5 月 北 京 工 业 大 学 学 报 JOURNAL OF BEIJING UNIVERSITY OF TECHNOLOGY Vol. 37 No. 5 May 2011 植 筋 钢 筋 混 凝 土 锚 固 构 件 抗 震 性 能 试 验 研 究 邓 宗 才 1, 钟 林 杭 1, 张 永 方 1, 曾 洪 超 1 2, 范 世 平 ( 1. 北 京 工 业
第 37 卷 第 5 期 2011 年 5 月 北 京 工 业 大 学 学 报 JOURNAL OF BEIJING UNIVERSITY OF TECHNOLOGY Vol. 37 No. 5 May 2011 植 筋 钢 筋 混 凝 土 锚 固 构 件 抗 震 性 能 试 验 研 究 邓 宗 才 1, 钟 林 杭 1, 张 永 方 1, 曾 洪 超 1 2, 范 世 平 ( 1. 北 京 工 业
180 中 南 大 学 学 报 ( 社 会 科 学 版 ) 2013 年 第 19 卷 第 1 期 乐 府 诗 集 相 和 歌 辞 相 和 曲 下 陌 上 桑 : 蚕 饥 妾 复 思, 拭 泪 且 提 筐 值 得 注 意 的 是, 农 书 齐 民 要 术 中 拭 的 使 用 范 围 很 广, 不 但
 第 19 卷 第 1 期 中 南 大 学 学 报 ( 社 会 科 学 版 ) Vol.19 No.1 2013 年 2 月 J. CENT. SOUTH UNIV. (SOCIAL SCIENCE) Feb. 2013 拭 揩 抹 擦 搌 的 历 史 演 变 与 方 言 分 布 王 娟 ( 太 原 师 范 学 院 文 学 院, 山 西 太 原,030012; 华 东 师 范 大 学 中 文 系, 上
第 19 卷 第 1 期 中 南 大 学 学 报 ( 社 会 科 学 版 ) Vol.19 No.1 2013 年 2 月 J. CENT. SOUTH UNIV. (SOCIAL SCIENCE) Feb. 2013 拭 揩 抹 擦 搌 的 历 史 演 变 与 方 言 分 布 王 娟 ( 太 原 师 范 学 院 文 学 院, 山 西 太 原,030012; 华 东 师 范 大 学 中 文 系, 上
标题
 DOI:10. 15942 / j. jcsu. 2016. 03. 001 成 都 体 育 学 院 学 报 2016 年 ( 第 42 卷 ) 第 3 期 Journal of Chengdu Sport University Vol. 42 No. 3. 2016 成 都 体 育 学 院 建 设 体 育 特 色 鲜 明 多 学 科 协 调 发 展 的 高 水 平 应 用 研 究 型 大 学 冶
DOI:10. 15942 / j. jcsu. 2016. 03. 001 成 都 体 育 学 院 学 报 2016 年 ( 第 42 卷 ) 第 3 期 Journal of Chengdu Sport University Vol. 42 No. 3. 2016 成 都 体 育 学 院 建 设 体 育 特 色 鲜 明 多 学 科 协 调 发 展 的 高 水 平 应 用 研 究 型 大 学 冶
1 引言
 P P 第 40 卷 Vol.40 第 7 期 No.7 计 算 机 工 程 Computer Engineering 014 年 7 月 July 014 开 发 研 究 与 工 程 应 用 文 章 编 号 :1000-348(014)07-081-05 文 献 标 识 码 :A 中 图 分 类 号 :TP391.41 摘 基 于 图 像 识 别 的 震 象 云 地 震 预 测 方 法 谢 庭,
P P 第 40 卷 Vol.40 第 7 期 No.7 计 算 机 工 程 Computer Engineering 014 年 7 月 July 014 开 发 研 究 与 工 程 应 用 文 章 编 号 :1000-348(014)07-081-05 文 献 标 识 码 :A 中 图 分 类 号 :TP391.41 摘 基 于 图 像 识 别 的 震 象 云 地 震 预 测 方 法 谢 庭,
标题
 第 26 卷 第 5 期 2013 年 9 月 北 京 航 空 航 天 大 学 学 报 ( 社 会 科 学 版 ) Journal of Beijing University of Aeronautics and Astronautics( Social Sciences Edition) Vol. 26 摇 No. 5 September, 2013 中 国 国 防 科 技 研 发 投 入 特 点
第 26 卷 第 5 期 2013 年 9 月 北 京 航 空 航 天 大 学 学 报 ( 社 会 科 学 版 ) Journal of Beijing University of Aeronautics and Astronautics( Social Sciences Edition) Vol. 26 摇 No. 5 September, 2013 中 国 国 防 科 技 研 发 投 入 特 点
10 ( ) ( ) [5] 1978 : [1] (P13) [6] [1] (P217) [7] [1] (P19) : : [1] [4] (P1347) (P18) 1985 : [1] (P343) 1300 : [1] (P12) 1984 :
![10 ( ) ( ) [5] 1978 : [1] (P13) [6] [1] (P217) [7] [1] (P19) : : [1] [4] (P1347) (P18) 1985 : [1] (P343) 1300 : [1] (P12) 1984 : 10 ( ) ( ) [5] 1978 : [1] (P13) [6] [1] (P217) [7] [1] (P19) : : [1] [4] (P1347) (P18) 1985 : [1] (P343) 1300 : [1] (P12) 1984 :](/thumbs/91/106610658.jpg) 27 3 ( ) Vol.27 No.3 2010 5 Journal of Shenzhen University (Humanities & Social Sciences) May 2010 ( 518060) : ; : ; : ; ; ; ; : F 127.9 :A :1000-260X(2010)03-0009-13 30 [2] : [2] (P381) 1979 : : [3] :1978
27 3 ( ) Vol.27 No.3 2010 5 Journal of Shenzhen University (Humanities & Social Sciences) May 2010 ( 518060) : ; : ; : ; ; ; ; : F 127.9 :A :1000-260X(2010)03-0009-13 30 [2] : [2] (P381) 1979 : : [3] :1978
Microsoft Word - 3782.doc
 民 国 时 期 乡 村 治 理 方 式 的 变 革 : 以 河 北 定 县 为 例 李 德 芳 ( 李 德 芳 海 南 大 学 公 共 管 理 学 院 海 口 570228) 摘 要 : 本 文 以 河 北 定 县 为 例, 论 述 了 民 国 时 期 乡 村 治 理 方 式 的 变 革 这 对 目 前 中 国 的 乡 村 治 理 改 革 具 有 一 定 的 借 鉴 意 义 关 键 词 : 治 理
民 国 时 期 乡 村 治 理 方 式 的 变 革 : 以 河 北 定 县 为 例 李 德 芳 ( 李 德 芳 海 南 大 学 公 共 管 理 学 院 海 口 570228) 摘 要 : 本 文 以 河 北 定 县 为 例, 论 述 了 民 国 时 期 乡 村 治 理 方 式 的 变 革 这 对 目 前 中 国 的 乡 村 治 理 改 革 具 有 一 定 的 借 鉴 意 义 关 键 词 : 治 理
课程13-7.FIT)
 母 亲 给 出 的 答 案 有 个 孩 子 对 一 个 问 题 一 直 想 不 通 : 为 什 么 他 的 同 桌 想 考 第 一 一 下 子 就 考 了 第 一, 而 自 己 想 考 第 一 却 只 考 了 全 班 第 二 十 一 名? 回 家 后 他 问 道 : 妈 妈 我 是 不 是 比 别 人 笨? 我 觉 得 我 和 他 一 样 听 老 师 的 话, 一 样 认 真 地 做 作 业, 可
母 亲 给 出 的 答 案 有 个 孩 子 对 一 个 问 题 一 直 想 不 通 : 为 什 么 他 的 同 桌 想 考 第 一 一 下 子 就 考 了 第 一, 而 自 己 想 考 第 一 却 只 考 了 全 班 第 二 十 一 名? 回 家 后 他 问 道 : 妈 妈 我 是 不 是 比 别 人 笨? 我 觉 得 我 和 他 一 样 听 老 师 的 话, 一 样 认 真 地 做 作 业, 可
Microsoft Word 張嘉玲-_76-83_
 64 4 Journal of Taiwan Agricultural Engineering 107 12 Vol. 64, No. 4, December 2018 DOI: 10.29974/JTAE.201812_64(4).0005 WASP - Applying the WASP Model to Evaluate the Effect of Wastewater Sewer Takeover
64 4 Journal of Taiwan Agricultural Engineering 107 12 Vol. 64, No. 4, December 2018 DOI: 10.29974/JTAE.201812_64(4).0005 WASP - Applying the WASP Model to Evaluate the Effect of Wastewater Sewer Takeover
4 115,,. : p { ( x ( t), y ( t) ) x R m, y R n, t = 1,2,, p} (1),, x ( t), y ( t),,: F : R m R n.,m, n, u.,, Sigmoid. :,f Sigmoid,f ( x) = ^y k ( t) =
 2007 4 4 :100026788 (2007) 0420114206, (, 430074) :,,,,,,GIS.,,. : ; ; ; ; : TP391 ;P338 : A Development of Combinatorial Intelligentized Decision2Making Support System and Its Utilization in Runoff Forecasting
2007 4 4 :100026788 (2007) 0420114206, (, 430074) :,,,,,,GIS.,,. : ; ; ; ; : TP391 ;P338 : A Development of Combinatorial Intelligentized Decision2Making Support System and Its Utilization in Runoff Forecasting
《红楼梦》中茗烟与李贵的对比分析
 第 13 卷 第 2 期 中 南 大 学 学 报 ( 社 会 科 学 版 ) Vol.13 No.2 2007 年 4 月 J. CENT. SOUTH UNIV. (SOCIAL SCIENCE) Apr. 2007 红 楼 梦 茗 烟 与 李 贵 形 象 比 较 研 究 李 鸿 渊, 奉 旨 亨 ( 湖 南 科 技 大 学 人 文 学 院, 湖 南 湘 潭,411201) 摘 要 : 茗 烟 与
第 13 卷 第 2 期 中 南 大 学 学 报 ( 社 会 科 学 版 ) Vol.13 No.2 2007 年 4 月 J. CENT. SOUTH UNIV. (SOCIAL SCIENCE) Apr. 2007 红 楼 梦 茗 烟 与 李 贵 形 象 比 较 研 究 李 鸿 渊, 奉 旨 亨 ( 湖 南 科 技 大 学 人 文 学 院, 湖 南 湘 潭,411201) 摘 要 : 茗 烟 与
Microsoft Word - 14--李海波_new_.doc
 46 5 Vol.46, No.5 2015 9 OCEANOLOGIA ET LIMNOLOGIA SINICA Sep., 2015 (Trichiurus lepturus) * 1 1 李 桂 芬 21 2 2 (1. 316021; 2. 316022), (Trichiurus lepturus),, (),, : 6.8%, 7.4%, 1..5, ; ; ; TS254 doi: 10.11693/hyhz20150600173,,,
46 5 Vol.46, No.5 2015 9 OCEANOLOGIA ET LIMNOLOGIA SINICA Sep., 2015 (Trichiurus lepturus) * 1 1 李 桂 芬 21 2 2 (1. 316021; 2. 316022), (Trichiurus lepturus),, (),, : 6.8%, 7.4%, 1..5, ; ; ; TS254 doi: 10.11693/hyhz20150600173,,,
Microsoft Word - 20120619-188_editing
 固 定 时 间 - 离 子 选 择 性 电 极 浓 度 直 读 法 快 速 测 定 腐 竹 中 的 硼 砂 魏 姜 勉 1 高 向 阳 1 * 张 娜 (1 河 南 农 业 大 学 食 品 科 学 技 术 学 院, 郑 州, 450002, 中 国 ; 2 郑 州 科 技 学 院, 郑 州,450064, 中 国 ) 2 摘 要 : 为 建 立 一 种 快 速 测 定 食 品 中 硼 砂 的 新 方
固 定 时 间 - 离 子 选 择 性 电 极 浓 度 直 读 法 快 速 测 定 腐 竹 中 的 硼 砂 魏 姜 勉 1 高 向 阳 1 * 张 娜 (1 河 南 农 业 大 学 食 品 科 学 技 术 学 院, 郑 州, 450002, 中 国 ; 2 郑 州 科 技 学 院, 郑 州,450064, 中 国 ) 2 摘 要 : 为 建 立 一 种 快 速 测 定 食 品 中 硼 砂 的 新 方
 90 2011 7 1 90 90 90 * 30 1984 1989 4 * 2011 6 1993 1997 1992 1998 2003 5 2004 2007 2008 2010 2008 6 2011 6 * 33% 21% 19% 18% 3% 8 5% * 7 - - - 8 2011 6 * 1921 2011 90 90 90 90 90 1921 1949 1949 16 12
90 2011 7 1 90 90 90 * 30 1984 1989 4 * 2011 6 1993 1997 1992 1998 2003 5 2004 2007 2008 2010 2008 6 2011 6 * 33% 21% 19% 18% 3% 8 5% * 7 - - - 8 2011 6 * 1921 2011 90 90 90 90 90 1921 1949 1949 16 12
酸檸檬?鹼檸檬??食物的酸鹼性.doc
 篇 名 : 酸 檸 檬? 鹼 檸 檬? 食 物 的 酸 鹼 性 作 者 : 何 國 維 國 立 埔 里 高 工 化 工 科 二 年 乙 班 指 導 老 師 : 余 志 輝 老 師 壹 前 言 食 物, 是 人 類 每 天 的 能 量 的 來 源, 無 論 酸 甜 苦 辣, 各 式 各 樣 的 食 物 隨 處 可 見, 頗 具 豐 富 性 及 變 化 性, 令 人 食 指 大 動 但 是, 日 前 科
篇 名 : 酸 檸 檬? 鹼 檸 檬? 食 物 的 酸 鹼 性 作 者 : 何 國 維 國 立 埔 里 高 工 化 工 科 二 年 乙 班 指 導 老 師 : 余 志 輝 老 師 壹 前 言 食 物, 是 人 類 每 天 的 能 量 的 來 源, 無 論 酸 甜 苦 辣, 各 式 各 樣 的 食 物 隨 處 可 見, 頗 具 豐 富 性 及 變 化 性, 令 人 食 指 大 動 但 是, 日 前 科
Microsoft Word - 11-秦华伟.doc
 热 带 海 洋 学 报 JOURNAL OF TROPICAL OCEANOGRAPHY 海 洋 调 查 与 观 测 仪 器 doi:10.3969/j.issn.1009-5470.2013.01.011 2013 年 第 32 卷 第 1 期 : 76 80 http://www.jto.ac.cn * 应 用 于 龟 山 岛 热 液 喷 口 探 寻 的 散 射 光 式 水 下 浊 度 仪 研
热 带 海 洋 学 报 JOURNAL OF TROPICAL OCEANOGRAPHY 海 洋 调 查 与 观 测 仪 器 doi:10.3969/j.issn.1009-5470.2013.01.011 2013 年 第 32 卷 第 1 期 : 76 80 http://www.jto.ac.cn * 应 用 于 龟 山 岛 热 液 喷 口 探 寻 的 散 射 光 式 水 下 浊 度 仪 研
p 3 p 4 p 5 p 6 p 7 p 8 p 9 p 10 p 11 θ 1 θ 2 θ 3 θ 4 θ 5 θ 6 θ 7 θ 8 θ 9 θ d 1 = 0 X c 0 p 1 p 2 X c 0 d pi p j p i p j 0 δ 90
 22 4 2017 8 Vol. 22 No. 4 JOURNAL OF HARBIN UNIVERSITY OF SCIENCE AND TECHNOLOGY Aug. 2017 1 1 1 1 2 2 2 1. 150080 2. 150080,,,, ; ; ; DOI: 10. 15938 /j. jhust. 2017. 04. 001 TP273 A 1007-2683 2017 04-0001-
22 4 2017 8 Vol. 22 No. 4 JOURNAL OF HARBIN UNIVERSITY OF SCIENCE AND TECHNOLOGY Aug. 2017 1 1 1 1 2 2 2 1. 150080 2. 150080,,,, ; ; ; DOI: 10. 15938 /j. jhust. 2017. 04. 001 TP273 A 1007-2683 2017 04-0001-
TGF-β AngⅡ B SD ~ 220g SPF. SCXK No SYXK ~ 25 40% ~ 70% OR37G-C
 2017 7 43 4 Journal of Southwest Minzu University Natural Science Edition Jul. 2017 Vol. 43 No. 4 doi10. 11920 /xnmdzk. 2017. 04. 008 1 1 1 2 1 1 3 1. 610212 2. 6100413. 610031 AngⅡ TGF-β. SD 60 180 ~
2017 7 43 4 Journal of Southwest Minzu University Natural Science Edition Jul. 2017 Vol. 43 No. 4 doi10. 11920 /xnmdzk. 2017. 04. 008 1 1 1 2 1 1 3 1. 610212 2. 6100413. 610031 AngⅡ TGF-β. SD 60 180 ~
931-33FR-E 1,2,3,4- BTCA DP60 931-33 FR-E BTCA DP60 143.0 177.4 173.7 137.4 141.6 140.3 144.0 119.3 X- DP60 Ea 90.988kJ/mol 99.793kJ/mol lna 20.898 22
 2005 Research of Crease-Resistant Finishing on Natural Bamboo Fabric 2005 5 931-33FR-E 1,2,3,4- BTCA DP60 931-33 FR-E BTCA DP60 143.0 177.4 173.7 137.4 141.6 140.3 144.0 119.3 X- DP60 Ea 90.988kJ/mol 99.793kJ/mol
2005 Research of Crease-Resistant Finishing on Natural Bamboo Fabric 2005 5 931-33FR-E 1,2,3,4- BTCA DP60 931-33 FR-E BTCA DP60 143.0 177.4 173.7 137.4 141.6 140.3 144.0 119.3 X- DP60 Ea 90.988kJ/mol 99.793kJ/mol
Electronic Supplementary Material (ESI) for Materials Chemistry Frontiers. This journal is the Partner Organisations 2018 Supporting Information Well-
 Electronic Supplementary Material (ESI) for Materials Chemistry Frontiers. This journal is the Partner Organisations 2018 Supporting Information Well-aligned metal-organic framework array-derived CoS 2
Electronic Supplementary Material (ESI) for Materials Chemistry Frontiers. This journal is the Partner Organisations 2018 Supporting Information Well-aligned metal-organic framework array-derived CoS 2
标题
 摇 1524 艾 滋 病 合 并 肺 部 感 染 中 医 证 型 研 究 进 展 综 述 扶 伟 摇 徐 立 然 摇 马 秀 霞 摇 孟 鹏 飞 摇 宋 夕 元 摇 李 亮 平 摇 李 正 摇 丁 雪 摇 邱 荃 摇 杨 超 华 揖 摘 要 铱 摇 艾 滋 病 合 并 肺 部 感 染 的 治 疗 过 程 中 因 其 病 因 复 杂, 临 床 症 状 多 样, 辨 证 分 型 及 临 床 疗 效 评
摇 1524 艾 滋 病 合 并 肺 部 感 染 中 医 证 型 研 究 进 展 综 述 扶 伟 摇 徐 立 然 摇 马 秀 霞 摇 孟 鹏 飞 摇 宋 夕 元 摇 李 亮 平 摇 李 正 摇 丁 雪 摇 邱 荃 摇 杨 超 华 揖 摘 要 铱 摇 艾 滋 病 合 并 肺 部 感 染 的 治 疗 过 程 中 因 其 病 因 复 杂, 临 床 症 状 多 样, 辨 证 分 型 及 临 床 疗 效 评
5 551 [3-].. [5]. [6]. [7].. API API. 1 [8-9]. [1]. W = W 1) y). x [11-12] D 2 2πR = 2z E + 2R arcsin D δ R z E = πr 1 + πr ) 2 arcsin
![5 551 [3-].. [5]. [6]. [7].. API API. 1 [8-9]. [1]. W = W 1) y). x [11-12] D 2 2πR = 2z E + 2R arcsin D δ R z E = πr 1 + πr ) 2 arcsin 5 551 [3-].. [5]. [6]. [7].. API API. 1 [8-9]. [1]. W = W 1) y). x [11-12] D 2 2πR = 2z E + 2R arcsin D δ R z E = πr 1 + πr ) 2 arcsin](/thumbs/91/107147441.jpg) 38 5 216 1 1),2) 163318) 163318). API. TE256 A doi 1.652/1-879-15-298 MODE OF CASING EXTERNA EXTRUSION BASED ON THE PRINCIPE OF VIRTUA WORK 1) ZHAO Wanchun,2) ZENG Jia WANG Tingting FENG Xiaohan School
38 5 216 1 1),2) 163318) 163318). API. TE256 A doi 1.652/1-879-15-298 MODE OF CASING EXTERNA EXTRUSION BASED ON THE PRINCIPE OF VIRTUA WORK 1) ZHAO Wanchun,2) ZENG Jia WANG Tingting FENG Xiaohan School
Supplementary Information LC-MS-guided isolation of anti-inflammatory 2-(2-phenylethyl)chromone dimers from Chinese agarwood (Aquilaria sinensis) Hui-
 Supplementary Information LC-MS-guided isolation of anti-inflammatory 2-(2-phenylethyl)chromone dimers from Chinese agarwood (Aquilaria sinensis) Hui-Xia Huo #, Yu-Fan Gu #, Zhi-Xiang Zhu, Yun-Feng Zhang,
Supplementary Information LC-MS-guided isolation of anti-inflammatory 2-(2-phenylethyl)chromone dimers from Chinese agarwood (Aquilaria sinensis) Hui-Xia Huo #, Yu-Fan Gu #, Zhi-Xiang Zhu, Yun-Feng Zhang,
Microsoft Word 聂雪梅.doc
 4 4 Vol. 4 No. 4 2013 8 Journal of Food Safety and Quality Aug., 2013 聂雪梅 *, 李立, 孙利, 高飞 (, 100123) 摘要 : 2011 12,, 2007~2011,,,, 关键词 : ; ; ; ; Trade and notification situation on food import and export
4 4 Vol. 4 No. 4 2013 8 Journal of Food Safety and Quality Aug., 2013 聂雪梅 *, 李立, 孙利, 高飞 (, 100123) 摘要 : 2011 12,, 2007~2011,,,, 关键词 : ; ; ; ; Trade and notification situation on food import and export
Fig. 1 Frame calculation model 1 mm Table 1 Joints displacement mm
 33 2 2011 4 ol. 33 No. 2 Apr. 2011 1002-8412 2011 02-0104-08 1 1 1 2 361003 3. 361009 3 1. 361005 2. GB50023-2009 TU746. 3 A Study on Single-span RC Frame Reinforced with Steel Truss System Yuan Xing-ren
33 2 2011 4 ol. 33 No. 2 Apr. 2011 1002-8412 2011 02-0104-08 1 1 1 2 361003 3. 361009 3 1. 361005 2. GB50023-2009 TU746. 3 A Study on Single-span RC Frame Reinforced with Steel Truss System Yuan Xing-ren
LaDefense Arch Petronas Towers 2009 CCTV MOMA Newmark Hahn Liu 8 Heredia - Zavoni Barranco 9 Heredia - Zavoni Leyva
 39 6 2011 12 Journal of Fuzhou University Natural Science Edition Vol 39 No 6 Dec 2011 DOI CNKI 35-1117 /N 20111220 0901 002 1000-2243 2011 06-0923 - 07 350108 105 m 14 69% TU311 3 A Seismic analysis of
39 6 2011 12 Journal of Fuzhou University Natural Science Edition Vol 39 No 6 Dec 2011 DOI CNKI 35-1117 /N 20111220 0901 002 1000-2243 2011 06-0923 - 07 350108 105 m 14 69% TU311 3 A Seismic analysis of
附件1
 附 件 1 教 学 成 果 报 告 成 果 名 称 建 设 国 家 精 品 课 程, 培 养 化 学 创 新 人 才 成 果 完 成 人 巢 晖 陈 六 平 乔 正 平 石 建 新 陈 小 明 龚 孟 濂 毛 宗 万 童 叶 翔 汪 波 成 果 完 成 单 位 中 山 大 学 1 中 山 大 学 提 出 了 大 学 是 学 术 共 同 体 教 授 就 是 大 学 善 待 学 生 和 人 心 向 学
附 件 1 教 学 成 果 报 告 成 果 名 称 建 设 国 家 精 品 课 程, 培 养 化 学 创 新 人 才 成 果 完 成 人 巢 晖 陈 六 平 乔 正 平 石 建 新 陈 小 明 龚 孟 濂 毛 宗 万 童 叶 翔 汪 波 成 果 完 成 单 位 中 山 大 学 1 中 山 大 学 提 出 了 大 学 是 学 术 共 同 体 教 授 就 是 大 学 善 待 学 生 和 人 心 向 学
(2) (3) 1.3 (1) (2) (3) (4) (5) (6)
 (GB/T -1987) 771 (GB/T 1.1 2000---- ) GB/T 7714-2005 ( ) 1 (1) (2) (3) (4) (5) (6) abstract (7) 1.2 (1) 1 (2) (3) 1.3 (1) (2) (3) (4) (5) (6) 2.1 1. 25 1 2. 15 2 3. 4. 300 4 8 2 3 5. abstract 6. : 5 2.2
(GB/T -1987) 771 (GB/T 1.1 2000---- ) GB/T 7714-2005 ( ) 1 (1) (2) (3) (4) (5) (6) abstract (7) 1.2 (1) 1 (2) (3) 1.3 (1) (2) (3) (4) (5) (6) 2.1 1. 25 1 2. 15 2 3. 4. 300 4 8 2 3 5. abstract 6. : 5 2.2
Microsoft Word - 465.doc
 第 13 卷 第 4 期 中 南 大 学 学 报 ( 社 会 科 学 版 ) Vol.13 No4 2007 年 8 月 J. CENT. SOUTH UNIV. (SOCIAL SCIENCE) Aug 2007 幽 人 空 山, 过 雨 采 蘋 唐 代 诗 歌 蘋 意 象 探 微 张 俊 峰 ( 南 京 师 范 大 学 文 学 院, 江 苏 南 京,210097) 摘 要 : 蘋 意 象 源 自
第 13 卷 第 4 期 中 南 大 学 学 报 ( 社 会 科 学 版 ) Vol.13 No4 2007 年 8 月 J. CENT. SOUTH UNIV. (SOCIAL SCIENCE) Aug 2007 幽 人 空 山, 过 雨 采 蘋 唐 代 诗 歌 蘋 意 象 探 微 张 俊 峰 ( 南 京 师 范 大 学 文 学 院, 江 苏 南 京,210097) 摘 要 : 蘋 意 象 源 自
13-4-Cover-1
 106 13 4 301-323 302 2009 2007 2009 2007 Dewey 1960 1970 1964 1967 303 1994 2008 2007 2008 2001 2003 2006 2007 2007 7 2013 2007 2009 2009 2007 2009 2012 Kendall 1990 Jacoby 1996 Sigmon 1996 1 2 3 20062000
106 13 4 301-323 302 2009 2007 2009 2007 Dewey 1960 1970 1964 1967 303 1994 2008 2007 2008 2001 2003 2006 2007 2007 7 2013 2007 2009 2009 2007 2009 2012 Kendall 1990 Jacoby 1996 Sigmon 1996 1 2 3 20062000
Microsoft Word - 201506定版
 56 Chinese Journal of Library and Information Science for Traditional Chinese Medicine Dec. 2015 Vol. 39 No. 6 综 述 中 医 药 学 语 言 系 统 研 究 综 述 于 彤, 贾 李 蓉, 刘 静, 杨 硕 *, 董 燕, 朱 玲 中 国 中 医 科 学 院 中 医 药 信 息 研 究 所,
56 Chinese Journal of Library and Information Science for Traditional Chinese Medicine Dec. 2015 Vol. 39 No. 6 综 述 中 医 药 学 语 言 系 统 研 究 综 述 于 彤, 贾 李 蓉, 刘 静, 杨 硕 *, 董 燕, 朱 玲 中 国 中 医 科 学 院 中 医 药 信 息 研 究 所,
382 25,,, 4.2 g 96% m.p.139~140 ( [21] :138~139 ), (4- )-2,2 6,2 - (L), [17], 2.5 mmol 1-(2- )-, 2.5 mmol 1-(2- )-(4- ) -1-2,2 6,2 (25.0 mmol),
![382 25,,, 4.2 g 96% m.p.139~140 ( [21] :138~139 ), (4- )-2,2 6,2 - (L), [17], 2.5 mmol 1-(2- )-, 2.5 mmol 1-(2- )-(4- ) -1-2,2 6,2 (25.0 mmol), 382 25,,, 4.2 g 96% m.p.139~140 ( [21] :138~139 ), (4- )-2,2 6,2 - (L), [17], 2.5 mmol 1-(2- )-, 2.5 mmol 1-(2- )-(4- ) -1-2,2 6,2 (25.0 mmol),](/thumbs/91/105235115.jpg) 25 3 2009 3 CHINESE JOURNAL OF INORGANIC CHEMISTRY Vol.25 No.3 381~385 4-1 *,1 1 1,2 ( 1, 361005) ( 2, 361005) : -2,2 6,2 -,4 - -2,2 6,2 - (L), L (ZnL),, ZnL 1 1 2 1 2 1,ZnL : ; 4 - -2,2 6,2 - ; ; : O614.24
25 3 2009 3 CHINESE JOURNAL OF INORGANIC CHEMISTRY Vol.25 No.3 381~385 4-1 *,1 1 1,2 ( 1, 361005) ( 2, 361005) : -2,2 6,2 -,4 - -2,2 6,2 - (L), L (ZnL),, ZnL 1 1 2 1 2 1,ZnL : ; 4 - -2,2 6,2 - ; ; : O614.24
标题
 第 40 卷 第 3 期 物 探 与 化 探 Vol.40,No.3 2016 年 6 月 GEOPHYSICAL & GEOCHEMICAL EXPLORATION Jun.,2016 doi: 10.11720 / wtyht.2016.3.27 林 希 仲. 井 地 直 流 电 法 在 岩 溶 地 基 探 测 中 的 应 用 [J]. 物 探 与 化 探,2016,40(3):619-623.http:
第 40 卷 第 3 期 物 探 与 化 探 Vol.40,No.3 2016 年 6 月 GEOPHYSICAL & GEOCHEMICAL EXPLORATION Jun.,2016 doi: 10.11720 / wtyht.2016.3.27 林 希 仲. 井 地 直 流 电 法 在 岩 溶 地 基 探 测 中 的 应 用 [J]. 物 探 与 化 探,2016,40(3):619-623.http:
km km mm km m /s hpa 500 hpa E N 41 N 37 N 121
 32 2 2014 4 Journal of Arid Meteorology Vol. 32 No. 2 Apr 2014. 08. 03 J. 2014 32 2256-262 LU Guirong WANG Wen YU Huaizhenget al. The Influence of Damrey Typhoon on 08. 03 Rainstorm Process in Rizhao of
32 2 2014 4 Journal of Arid Meteorology Vol. 32 No. 2 Apr 2014. 08. 03 J. 2014 32 2256-262 LU Guirong WANG Wen YU Huaizhenget al. The Influence of Damrey Typhoon on 08. 03 Rainstorm Process in Rizhao of
[1-3] (Smile) [4] 808 nm (CW) W 1 50% 1 W 1 W Fig.1 Thermal design of semiconductor laser vertical stack ; Ansys 20 bar ; bar 2 25 Fig
![[1-3] (Smile) [4] 808 nm (CW) W 1 50% 1 W 1 W Fig.1 Thermal design of semiconductor laser vertical stack ; Ansys 20 bar ; bar 2 25 Fig [1-3] (Smile) [4] 808 nm (CW) W 1 50% 1 W 1 W Fig.1 Thermal design of semiconductor laser vertical stack ; Ansys 20 bar ; bar 2 25 Fig](/thumbs/91/106435555.jpg) 40 6 2011 6 Vol.40 No.6 Infrared and Laser Engineering Jun. 2011 808 nm 2000 W 1 1 1 1 2 2 2 2 2 12 (1. 710119 2. 710119) : bar 808 nm bar 100 W 808 nm 20 bar 2 000 W bar LIV bar 808 nm : : TN248.4 TN365
40 6 2011 6 Vol.40 No.6 Infrared and Laser Engineering Jun. 2011 808 nm 2000 W 1 1 1 1 2 2 2 2 2 12 (1. 710119 2. 710119) : bar 808 nm bar 100 W 808 nm 20 bar 2 000 W bar LIV bar 808 nm : : TN248.4 TN365
Microsoft Word - 05張政偉121-144
 靜 宜 中 文 學 報 第 一 期 2012 年 6 月 頁 121 144 靜 宜 大 學 中 國 文 學 系 以 經 為 法 : 廖 燕 文 學 觀 的 另 一 個 面 向 * 張 政 偉 摘 要 學 界 對 清 初 文 人 廖 燕 的 文 學 創 作 與 理 論 的 研 究 逐 漸 展 開, 並 且 獲 致 一 定 的 成 果 然 而 目 前 似 乎 將 廖 燕 的 文 學 觀 點 歸 類 為
靜 宜 中 文 學 報 第 一 期 2012 年 6 月 頁 121 144 靜 宜 大 學 中 國 文 學 系 以 經 為 法 : 廖 燕 文 學 觀 的 另 一 個 面 向 * 張 政 偉 摘 要 學 界 對 清 初 文 人 廖 燕 的 文 學 創 作 與 理 論 的 研 究 逐 漸 展 開, 並 且 獲 致 一 定 的 成 果 然 而 目 前 似 乎 將 廖 燕 的 文 學 觀 點 歸 類 為
普通高等学校本科专业设置管理规定
 普 通 高 等 学 校 本 科 专 业 设 置 申 请 表 ( 备 案 专 业 适 用 ) 学 校 名 称 ( 盖 章 ): 复 旦 大 学 学 校 主 管 部 门 : 教 育 部 专 业 名 称 : 能 源 化 学 专 业 代 码 : 0703XX 所 属 学 科 门 类 及 专 业 类 : 理 学 / 化 学 学 位 授 予 门 类 : 理 学 学 士 修 业 年 限 : 四 年 申 请 时 间
普 通 高 等 学 校 本 科 专 业 设 置 申 请 表 ( 备 案 专 业 适 用 ) 学 校 名 称 ( 盖 章 ): 复 旦 大 学 学 校 主 管 部 门 : 教 育 部 专 业 名 称 : 能 源 化 学 专 业 代 码 : 0703XX 所 属 学 科 门 类 及 专 业 类 : 理 学 / 化 学 学 位 授 予 门 类 : 理 学 学 士 修 业 年 限 : 四 年 申 请 时 间
1
 1 2 EI ( 2005) 3 EI ( 2005) 4 2006 3 1 2 3 EI ( 2005) http://www.ei.org.cn/twice/coverage.jsp ISSN 0567-7718 Acta Mechanica Sinica/Lixue Xuebao 1006-7191 Acta Metallurgica Sinica (English Letters) 0253-4827
1 2 EI ( 2005) 3 EI ( 2005) 4 2006 3 1 2 3 EI ( 2005) http://www.ei.org.cn/twice/coverage.jsp ISSN 0567-7718 Acta Mechanica Sinica/Lixue Xuebao 1006-7191 Acta Metallurgica Sinica (English Letters) 0253-4827
380 研 究 论 文 发 酵 天 数 双 乙 酰 测 定 : 参 照 GB4927-4928-2001 标 准 发 酵 液 中 的 化 学 成 分 的 测 定 : 采 用 GC-8A 型 气 相 色 谱 测 定 1.5 离 子 注 入 方 法 [6] 把 待 处 理 的 菌 株 细 胞 均 匀 涂
![380 研 究 论 文 发 酵 天 数 双 乙 酰 测 定 : 参 照 GB4927-4928-2001 标 准 发 酵 液 中 的 化 学 成 分 的 测 定 : 采 用 GC-8A 型 气 相 色 谱 测 定 1.5 离 子 注 入 方 法 [6] 把 待 处 理 的 菌 株 细 胞 均 匀 涂 380 研 究 论 文 发 酵 天 数 双 乙 酰 测 定 : 参 照 GB4927-4928-2001 标 准 发 酵 液 中 的 化 学 成 分 的 测 定 : 采 用 GC-8A 型 气 相 色 谱 测 定 1.5 离 子 注 入 方 法 [6] 把 待 处 理 的 菌 株 细 胞 均 匀 涂](/thumbs/43/23114460.jpg) 中 国 细 胞 生 物 学 学 报 Chinese Journal of Cell Biology 2011, 33(4): 379-384 http://www.cjcb.org 全 小 麦 啤 酒 酵 母 菌 株 的 诱 变 育 种 及 应 用 研 究 袁 仲 1* 张 百 胜 1 张 慎 举 1 马 绮 云 2 陈 柯 羽 2 ( 1 商 丘 职 业 技 术 学 院 园 林 食 品 加 工 系,
中 国 细 胞 生 物 学 学 报 Chinese Journal of Cell Biology 2011, 33(4): 379-384 http://www.cjcb.org 全 小 麦 啤 酒 酵 母 菌 株 的 诱 变 育 种 及 应 用 研 究 袁 仲 1* 张 百 胜 1 张 慎 举 1 马 绮 云 2 陈 柯 羽 2 ( 1 商 丘 职 业 技 术 学 院 园 林 食 品 加 工 系,
4 10% 90%
 2016 7 33 4 Journal of Shanghai University Social Sciences Jul. 2016 Vol. 33 No. 4 doi 10. 3969 /j. issn 1007-6522. 2016. 04. 008 201701 D035 A 1007-6522 2016 04-0098-14 1 2016-03-09 GH16049 GH16047 1968-98
2016 7 33 4 Journal of Shanghai University Social Sciences Jul. 2016 Vol. 33 No. 4 doi 10. 3969 /j. issn 1007-6522. 2016. 04. 008 201701 D035 A 1007-6522 2016 04-0098-14 1 2016-03-09 GH16049 GH16047 1968-98
Microsoft Word - 2.Invitee list_PAC 2011_CN_ _Website.docx
 The China Sustainable Energy Program 2011 11 18 The Energy Foundation San Francisco Office: 301 Battery Street San Francisco, CA 94111, U.S.A. Tel: (415) 561-6700 Fax: (415) 561-6709 Email: china@ef.org
The China Sustainable Energy Program 2011 11 18 The Energy Foundation San Francisco Office: 301 Battery Street San Francisco, CA 94111, U.S.A. Tel: (415) 561-6700 Fax: (415) 561-6709 Email: china@ef.org
254 22 [11] Bennetts (1988) [12] and Locatelli (1994) [13] e 1999 6 23 08 24 08 2 1 1 23 12 3033 N 900 hpa 23 14 950 hpa23 16 23 18 23 20 23 22 3033 N
![254 22 [11] Bennetts (1988) [12] and Locatelli (1994) [13] e 1999 6 23 08 24 08 2 1 1 23 12 3033 N 900 hpa 23 14 950 hpa23 16 23 18 23 20 23 22 3033 N 254 22 [11] Bennetts (1988) [12] and Locatelli (1994) [13] e 1999 6 23 08 24 08 2 1 1 23 12 3033 N 900 hpa 23 14 950 hpa23 16 23 18 23 20 23 22 3033 N](/thumbs/40/20608965.jpg) 22 3 Vol.22, No.3 2006 06 JOURNAL OF TROPICAL METEOROLOGY Jun., 2006 1004-4965200603-0253-06 ( 211101) 1999 6 P433 A 1 [13] Xu [4] [5] Emanuel [6] Jascourt [7] Xu [8] upscale development Xu downscale development
22 3 Vol.22, No.3 2006 06 JOURNAL OF TROPICAL METEOROLOGY Jun., 2006 1004-4965200603-0253-06 ( 211101) 1999 6 P433 A 1 [13] Xu [4] [5] Emanuel [6] Jascourt [7] Xu [8] upscale development Xu downscale development
N
 2016 9 38 5 Modern Law Science Sep. 2016 Vol. 38 No. 5 1001-2397 2016 05-0104 - 11 200042 DF 623 A DOI 10. 3969/j. issn. 1001-2397. 2016. 05. 09 2014 12 1 2015 12 3 1913 1912 2 1 10. 5 1883 2014 3 3 5
2016 9 38 5 Modern Law Science Sep. 2016 Vol. 38 No. 5 1001-2397 2016 05-0104 - 11 200042 DF 623 A DOI 10. 3969/j. issn. 1001-2397. 2016. 05. 09 2014 12 1 2015 12 3 1913 1912 2 1 10. 5 1883 2014 3 3 5
14审稿专家
 第 69 卷 第 9 期 2014 年 9 月 ACTA GEOGRAPHICA SINICA Vol.69, No.9 September, 2014 审 稿 专 家 名 单 ( 按 单 位 行 政 区 域 和 审 稿 专 家 姓 氏 拼 音 为 序 ) 在 创 刊 80 周 年 之 际, 编 辑 部 谨 向 所 有 为 审 稿 的 专 家 表 示 衷 心 的 感 谢! 以 下 是 2000 年
第 69 卷 第 9 期 2014 年 9 月 ACTA GEOGRAPHICA SINICA Vol.69, No.9 September, 2014 审 稿 专 家 名 单 ( 按 单 位 行 政 区 域 和 审 稿 专 家 姓 氏 拼 音 为 序 ) 在 创 刊 80 周 年 之 际, 编 辑 部 谨 向 所 有 为 审 稿 的 专 家 表 示 衷 心 的 感 谢! 以 下 是 2000 年
instillation therapy combined with Western medicine can reduce the levels of ALT, TBA, ALP, TBIL, DBIL and GGT, and improve the anti-cmv-igm negative
 在 线 投 稿 : http://www.baishideng.com/wcjd/ch/index.aspx 帮 助 平 台 : http://www.wjgnet.com/esps/helpdesk.aspx DOI: 10.11569/wcjd.v23.i28.4568 世 界 华 人 消 化 杂 志 2015 年 10 月 8 日 ; 23(28): 4568-4573 ISSN 1009-3079
在 线 投 稿 : http://www.baishideng.com/wcjd/ch/index.aspx 帮 助 平 台 : http://www.wjgnet.com/esps/helpdesk.aspx DOI: 10.11569/wcjd.v23.i28.4568 世 界 华 人 消 化 杂 志 2015 年 10 月 8 日 ; 23(28): 4568-4573 ISSN 1009-3079
<4D6963726F736F667420576F7264202D20B9DCC0EDD6C6B6C8BBE3B1E0B5DAB6FEB8E5>
 土 木 工 程 防 灾 国 家 重 点 实 验 室 ( 同 济 大 学 ) STATE KEY LABORATORY OF DISASTER REDUCTION IN CIVIL ENGINEERING, TONGJI UNIVERSITY 管 理 制 度 汇 编 土 木 工 程 防 灾 国 家 重 点 实 验 室 ( 同 济 大 学 ) 目 录 国 家 重 点 实 验 室 建 设 与 运 行 管
土 木 工 程 防 灾 国 家 重 点 实 验 室 ( 同 济 大 学 ) STATE KEY LABORATORY OF DISASTER REDUCTION IN CIVIL ENGINEERING, TONGJI UNIVERSITY 管 理 制 度 汇 编 土 木 工 程 防 灾 国 家 重 点 实 验 室 ( 同 济 大 学 ) 目 录 国 家 重 点 实 验 室 建 设 与 运 行 管
Microsoft Word - 10-06-0186-D10-0627孙竹森.doc
 第 34 卷 第 6 期 电 网 技 术 Vol. 34 No. 6 2010 年 6 月 Power System Technology Jun. 2010 文 章 编 号 :1000-3673(2010)06-0186-07 中 图 分 类 号 :TM 754 文 献 标 志 码 :A 学 科 代 码 :470 4051 输 电 线 路 钢 管 塔 的 推 广 与 应 用 孙 竹 森 1, 程
第 34 卷 第 6 期 电 网 技 术 Vol. 34 No. 6 2010 年 6 月 Power System Technology Jun. 2010 文 章 编 号 :1000-3673(2010)06-0186-07 中 图 分 类 号 :TM 754 文 献 标 志 码 :A 学 科 代 码 :470 4051 输 电 线 路 钢 管 塔 的 推 广 与 应 用 孙 竹 森 1, 程
11 : 1345,,. Feuillebois [6]. Richard Mochel [7]. Tabakova [8],.,..,. Hindmarsh [9],,,,,. Wang [10],, (80 µm),.,. Isao [11]. Ismail Salinas [12],. Kaw
![11 : 1345,,. Feuillebois [6]. Richard Mochel [7]. Tabakova [8],.,..,. Hindmarsh [9],,,,,. Wang [10],, (80 µm),.,. Isao [11]. Ismail Salinas [12],. Kaw 11 : 1345,,. Feuillebois [6]. Richard Mochel [7]. Tabakova [8],.,..,. Hindmarsh [9],,,,,. Wang [10],, (80 µm),.,. Isao [11]. Ismail Salinas [12],. Kaw](/thumbs/93/114003806.jpg) 1344 E 2006, 36(11): 1344~1354 * ** (, 100022).,.,.,.,....,,,,,,,.,.,.,,,.,. Hayashi [1] :., [2] [3~5],,.,,.,. : 2006-03-22; : 2006-06-17 * ( : 50376001) ( : G2005CB724201) **, E-mail: liuzhl@bjut.edu.cn
1344 E 2006, 36(11): 1344~1354 * ** (, 100022).,.,.,.,....,,,,,,,.,.,.,,,.,. Hayashi [1] :., [2] [3~5],,.,,.,. : 2006-03-22; : 2006-06-17 * ( : 50376001) ( : G2005CB724201) **, E-mail: liuzhl@bjut.edu.cn
4 51 1 Scoones 1998 20 60 70 2002 2001 20 90 World Bank DFID Sussex IDS 2012 2 2. 1 UNDP CARE DFID DFID DFID 1997 IDS 2009 1 5
 38 4 2014 7 Vol. 38 No. 4 July 2014 50 Population Research * 30 4 100872 Livelihood and Development Capacity of Families Obeying the Family Planning Policy in Rural China A Sustainable Livelihood Analytical
38 4 2014 7 Vol. 38 No. 4 July 2014 50 Population Research * 30 4 100872 Livelihood and Development Capacity of Families Obeying the Family Planning Policy in Rural China A Sustainable Livelihood Analytical
,,.,, : 1),,,,, 2),,,,, 3),,,,,,,,,, [6].,,, ( ),, [9], : 1), 2),,,,, 3),,, 2.,, [10].,,,,,,,,, [11]. 2.1,, [12],, ;, ; Fig. 1 1 Granular hier
![,,.,, : 1),,,,, 2),,,,, 3),,,,,,,,,, [6].,,, ( ),, [9], : 1), 2),,,,, 3),,, 2.,, [10].,,,,,,,,, [11]. 2.1,, [12],, ;, ; Fig. 1 1 Granular hier ,,.,, : 1),,,,, 2),,,,, 3),,,,,,,,,, [6].,,, ( ),, [9], : 1), 2),,,,, 3),,, 2.,, [10].,,,,,,,,, [11]. 2.1,, [12],, ;, ; Fig. 1 1 Granular hier](/thumbs/48/24888380.jpg) 36 7 Vol. 36, No. 7 2010 7 ACTA AUTOMATICA SINICA July, 2010 1, 2 1, 2, 3 1, 2,,,,,,, DOI,,, 10.3724/SP.J.1004.2010.00923 Distributed Simulation System Hierarchical Design Model Based on Quotient Space
36 7 Vol. 36, No. 7 2010 7 ACTA AUTOMATICA SINICA July, 2010 1, 2 1, 2, 3 1, 2,,,,,,, DOI,,, 10.3724/SP.J.1004.2010.00923 Distributed Simulation System Hierarchical Design Model Based on Quotient Space
标题
 第 38 卷 第 3 期 教 学 研 究 Vol 38 No 3 2015 年 5 月 Research in Teaching May 2015 普 通 高 校 军 事 技 能 训 练 评 估 指 标 体 系 的 构 建 研 究 基 于 对 陕 西 省 高 校 的 考 察 刘 玉 青 ( 西 安 交 通 大 学 军 事 教 研 室, 陕 西 西 安 710049) [ 摘 要 ] 普 通 高 校
第 38 卷 第 3 期 教 学 研 究 Vol 38 No 3 2015 年 5 月 Research in Teaching May 2015 普 通 高 校 军 事 技 能 训 练 评 估 指 标 体 系 的 构 建 研 究 基 于 对 陕 西 省 高 校 的 考 察 刘 玉 青 ( 西 安 交 通 大 学 军 事 教 研 室, 陕 西 西 安 710049) [ 摘 要 ] 普 通 高 校
10.11648.j.si.20160402.18
 Science Innovation 2016; 4(2): 65-71 http://www.sciencepublishinggroup.com/j/si doi: 10.11648/j.si.20160402.18 ISSN: 2328-7861 (Print); ISSN: 2328-787X (Online) Case Study on Career Plan of College's Students
Science Innovation 2016; 4(2): 65-71 http://www.sciencepublishinggroup.com/j/si doi: 10.11648/j.si.20160402.18 ISSN: 2328-7861 (Print); ISSN: 2328-787X (Online) Case Study on Career Plan of College's Students
WATER PURIFICATION TECHNOLOGY April 5th, 0.4 TiO TiO UV-0PC UNICO [0] TiO TiO TiO HNO 00 W TiO TiO TiO >40 nm TiO 0 ml 0 mg / L -. TiO 6 ml 40 ml 60 m
![WATER PURIFICATION TECHNOLOGY April 5th, 0.4 TiO TiO UV-0PC UNICO [0] TiO TiO TiO HNO 00 W TiO TiO TiO >40 nm TiO 0 ml 0 mg / L -. TiO 6 ml 40 ml 60 m WATER PURIFICATION TECHNOLOGY April 5th, 0.4 TiO TiO UV-0PC UNICO [0] TiO TiO TiO HNO 00 W TiO TiO TiO >40 nm TiO 0 ml 0 mg / L -. TiO 6 ml 40 ml 60 m](/thumbs/49/25216804.jpg) 0 0 50-54 Water Vol. Purification 0, No. Technology, 0,,. 50090. 0040 TiO TiO TiO + [] + + TiO TiO TiO TiO TiO TiO TiO TiO TU99 B 009-077 0 0-0050-05 Degradation of Methyl Orange with Metal Ion Modified
0 0 50-54 Water Vol. Purification 0, No. Technology, 0,,. 50090. 0040 TiO TiO TiO + [] + + TiO TiO TiO TiO TiO TiO TiO TiO TU99 B 009-077 0 0-0050-05 Degradation of Methyl Orange with Metal Ion Modified
亚临界大容量电站锅炉过热器系统阻力
 能 源 研 究 与 信 息 第 28 卷 第 1 期 Energy Research and Information Vol. 28 No. 1 2012 文 章 编 号 : 1008-8857(2012)01-0001-06 我 国 地 源 热 泵 相 关 技 术 专 利 综 合 分 析 焦 文 静, 戴 传 山 ( 天 津 大 学 机 械 学 院, 天 津 300072) 摘 要 : 地 源 热
能 源 研 究 与 信 息 第 28 卷 第 1 期 Energy Research and Information Vol. 28 No. 1 2012 文 章 编 号 : 1008-8857(2012)01-0001-06 我 国 地 源 热 泵 相 关 技 术 专 利 综 合 分 析 焦 文 静, 戴 传 山 ( 天 津 大 学 机 械 学 院, 天 津 300072) 摘 要 : 地 源 热
2 ( 自 然 科 学 版 ) 第 20 卷 波 ). 这 种 压 缩 波 空 气 必 然 有 一 部 分 要 绕 流 到 车 身 两 端 的 环 状 空 间 中, 形 成 与 列 车 运 行 方 向 相 反 的 空 气 流 动. 在 列 车 尾 部, 会 产 生 低 于 大 气 压 的 空 气 流
 第 20 卷 第 3 期 2014 年 6 月 ( 自 然 科 学 版 ) JOURNAL OF SHANGHAI UNIVERSITY (NATURAL SCIENCE) Vol. 20 No. 3 June 2014 DOI: 10.3969/j.issn.1007-2861.2013.07.031 基 于 FLUENT 测 轨 道 交 通 隧 道 中 电 波 折 射 率 结 构 常 数 张 永
第 20 卷 第 3 期 2014 年 6 月 ( 自 然 科 学 版 ) JOURNAL OF SHANGHAI UNIVERSITY (NATURAL SCIENCE) Vol. 20 No. 3 June 2014 DOI: 10.3969/j.issn.1007-2861.2013.07.031 基 于 FLUENT 测 轨 道 交 通 隧 道 中 电 波 折 射 率 结 构 常 数 张 永
Technical Acoustics Vol.27, No.4 Aug., 2008,,, (, ) :,,,,,, : ; ; : TB535;U : A : (2008) Noise and vibr
 8 8 Technical Acoustics Vol., No. Aug., 8,,, (, 8) :,,,,,, : ; ; : TB;U.+ 9 : A : -(8)--- Noise and vibration tests for fuel cell vehicel and noise sources identification SHEN Xiu-min, ZUO Shu-guang, CAI
8 8 Technical Acoustics Vol., No. Aug., 8,,, (, 8) :,,,,,, : ; ; : TB;U.+ 9 : A : -(8)--- Noise and vibration tests for fuel cell vehicel and noise sources identification SHEN Xiu-min, ZUO Shu-guang, CAI
第16卷 第2期 邯郸学院学报 2006年6月
 第 18 卷 第 4 期 邯 郸 学 院 学 报 2008 年 12 月 Vol.18 No.4 Journal of Handan College Dec. 2008 赵 文 化 研 究 论 赵 都 邯 郸 与 赵 国 都 城 研 究 问 题 朱 士 光 ( 陕 西 师 范 大 学 历 史 地 理 研 究 所, 陕 西 西 安 710062) 摘 要 : 战 国 七 雄 之 一 的 赵 国 都 城
第 18 卷 第 4 期 邯 郸 学 院 学 报 2008 年 12 月 Vol.18 No.4 Journal of Handan College Dec. 2008 赵 文 化 研 究 论 赵 都 邯 郸 与 赵 国 都 城 研 究 问 题 朱 士 光 ( 陕 西 师 范 大 学 历 史 地 理 研 究 所, 陕 西 西 安 710062) 摘 要 : 战 国 七 雄 之 一 的 赵 国 都 城
12-1b T Q235B ML15 Ca OH Table 1 Chemical composition of specimens % C Si Mn S P Cr Ni Fe
 * - - 100084 Q235B ML15 Ca OH 2 DOI 10. 13204 /j. gyjz201508023 STUDY OF GALVANIC CORROSION SENSITIVITY BETWEEN ANY COUPLE OF STUD WELDMENT OR BEAM Lu Xinying Li Yang Li Yuanjin Department of Civil Engineering
* - - 100084 Q235B ML15 Ca OH 2 DOI 10. 13204 /j. gyjz201508023 STUDY OF GALVANIC CORROSION SENSITIVITY BETWEEN ANY COUPLE OF STUD WELDMENT OR BEAM Lu Xinying Li Yang Li Yuanjin Department of Civil Engineering
208 中 南 大 学 学 报 ( 社 会 科 学 版 ) 2013 年 第 19 卷 第 6 期 节 目 录 上 卷 一 所 载 篇 名, 乃 总 目 录 中 篇 名 之 误, 正 文 卷 一 收 录 篇 名 为 月 支 使 者 玄 觉 杜 凝 妻 灌 国 婴 女 独 狐 及 吕 卿 均 五 篇
 第 19 卷 第 6 期 中 南 大 学 学 报 ( 社 会 科 学 版 ) Vol.19 No.6 2013 年 12 月 J. CENT. SOUTH UNIV. (SOCIAL SCIENCE) Dec. 2013 篇 目 考 辨 三 则 以 韩 藏 详 节 为 校 勘 依 据 盛 莉 ( 江 汉 大 学 人 文 学 院, 湖 北 武 汉,430056) 摘 要 : 详 节 为 朝 鲜 时 期
第 19 卷 第 6 期 中 南 大 学 学 报 ( 社 会 科 学 版 ) Vol.19 No.6 2013 年 12 月 J. CENT. SOUTH UNIV. (SOCIAL SCIENCE) Dec. 2013 篇 目 考 辨 三 则 以 韩 藏 详 节 为 校 勘 依 据 盛 莉 ( 江 汉 大 学 人 文 学 院, 湖 北 武 汉,430056) 摘 要 : 详 节 为 朝 鲜 时 期
中国科技论文在线中文稿件模板
 5 10 15 20 25 30 35 本 土 品 牌 刻 板 印 象 的 成 因 及 对 策 研 究 # 基 于 刻 板 思 维 与 符 号 认 知 的 文 本 分 析 * 刘 进 平, 张 燚, 张 锐 ( 重 庆 文 理 学 院 品 牌 科 学 研 究 所,402160) 摘 要 : 由 于 中 国 社 会 普 遍 存 在 本 土 品 牌 刻 板 印 象, 导 致 了 对 洋 品 牌 的 崇
5 10 15 20 25 30 35 本 土 品 牌 刻 板 印 象 的 成 因 及 对 策 研 究 # 基 于 刻 板 思 维 与 符 号 认 知 的 文 本 分 析 * 刘 进 平, 张 燚, 张 锐 ( 重 庆 文 理 学 院 品 牌 科 学 研 究 所,402160) 摘 要 : 由 于 中 国 社 会 普 遍 存 在 本 土 品 牌 刻 板 印 象, 导 致 了 对 洋 品 牌 的 崇
CONTENTS 目 录 大 事 要 闻 2 两 学 一 做 5 科 研 动 态 8 交 流 合 作 14 队 伍 建 设 17 人 才 培 养 19 运 行 管 理 21
 2016 ISSUE 01 1-5 月 SKLEC BULLETIN 河 口 海 岸 学 国 家 重 点 实 验 室 ( 华 东 师 范 大 学 ) State Key Laboratory of Estuarine and Coastal Research (East China Normal University) CONTENTS 目 录 大 事 要 闻 2 两 学 一 做 5 科 研 动 态
2016 ISSUE 01 1-5 月 SKLEC BULLETIN 河 口 海 岸 学 国 家 重 点 实 验 室 ( 华 东 师 范 大 学 ) State Key Laboratory of Estuarine and Coastal Research (East China Normal University) CONTENTS 目 录 大 事 要 闻 2 两 学 一 做 5 科 研 动 态
Microsoft Word - 6微调 _1_
 国 际 中 医 中 药 杂 志 2016 年 6 月 第 38 卷 第 6 期 Int J Trad Chin Med, June 2016, Vol. 38, No.6 481 国 外 传 统 医 学 管 理 模 式 探 讨 一 带 一 路 胡 艳 敏 李 宗 友 徐 俊 李 彦 文 王 俊 文 姜 威 赵 阳 摘 要 传 统 医 学 以 其 在 疾 病 治 疗 及 预 防 保 健 中 的 确 切
国 际 中 医 中 药 杂 志 2016 年 6 月 第 38 卷 第 6 期 Int J Trad Chin Med, June 2016, Vol. 38, No.6 481 国 外 传 统 医 学 管 理 模 式 探 讨 一 带 一 路 胡 艳 敏 李 宗 友 徐 俊 李 彦 文 王 俊 文 姜 威 赵 阳 摘 要 传 统 医 学 以 其 在 疾 病 治 疗 及 预 防 保 健 中 的 确 切
标题
 2016 年 5 月 西 南 民 族 大 学 学 报 ( 自 然 科 学 版 ) 第 423 卷 期 第 3 期 Journal 谢 of 琪 Southwest ꎬ 等 :C++ University 程 序 设 计 for 实 Nationalities( 验 教 学 微 课 Natural 的 设 计 Science 与 实 现 Edition) May 2016 Vol 42 No 3 doi:10
2016 年 5 月 西 南 民 族 大 学 学 报 ( 自 然 科 学 版 ) 第 423 卷 期 第 3 期 Journal 谢 of 琪 Southwest ꎬ 等 :C++ University 程 序 设 计 for 实 Nationalities( 验 教 学 微 课 Natural 的 设 计 Science 与 实 现 Edition) May 2016 Vol 42 No 3 doi:10
<4D6963726F736F667420576F7264202D20B2CCA3BA4542B2A1B6BE52746120496747BFB9CCE5D3EBB1C7D1CAB0A9B7D6C6DAB5C4B9D8CFB52E646F63>
 EB 病 毒 Rta/IgG 抗 体 与 鼻 咽 癌 分 期 的 关 系 蔡 永 林, 郑 裕 明, 成 积 儒, 李 军, 莫 永 坤, 钟 青 燕 ( 广 西 梧 州 市 红 十 字 会 医 院, 梧 州 市 肿 瘤 防 治 研 究 所, 广 西 梧 州 543002) 摘 要 : 目 的 探 讨 EB 病 毒 Rta/IgG 抗 体 与 鼻 咽 癌 临 床 分 期 的 关 系 方 法 用 酶
EB 病 毒 Rta/IgG 抗 体 与 鼻 咽 癌 分 期 的 关 系 蔡 永 林, 郑 裕 明, 成 积 儒, 李 军, 莫 永 坤, 钟 青 燕 ( 广 西 梧 州 市 红 十 字 会 医 院, 梧 州 市 肿 瘤 防 治 研 究 所, 广 西 梧 州 543002) 摘 要 : 目 的 探 讨 EB 病 毒 Rta/IgG 抗 体 与 鼻 咽 癌 临 床 分 期 的 关 系 方 法 用 酶
R&D % % 92.27% 1.33% 3.54% % 7.47%
 2012 7 13 4 F279.2 The Journal of Shanghai Administration Institute :A :1009-3176(2012)04-085-(13) Jul., 2012 Vol. 13, No4 * 200050,,, : ; ; ; * 2011 :2012-4-27 : 1975-1976- 85 4 2012 1. R&D 2009 2.87%
2012 7 13 4 F279.2 The Journal of Shanghai Administration Institute :A :1009-3176(2012)04-085-(13) Jul., 2012 Vol. 13, No4 * 200050,,, : ; ; ; * 2011 :2012-4-27 : 1975-1976- 85 4 2012 1. R&D 2009 2.87%
PCA+LDA 14 1 PEN mL mL mL 16 DJX-AB DJ X AB DJ2 -YS % PEN
 21 11 2011 11 COMPUTER TECHNOLOGY AND DEVELOPMENT Vol. 21 No. 11 Nov. 2011 510006 PEN3 5 PCA + PCA+LDA 5 5 100% TP301 A 1673-629X 2011 11-0177-05 Application of Electronic Nose in Discrimination of Different
21 11 2011 11 COMPUTER TECHNOLOGY AND DEVELOPMENT Vol. 21 No. 11 Nov. 2011 510006 PEN3 5 PCA + PCA+LDA 5 5 100% TP301 A 1673-629X 2011 11-0177-05 Application of Electronic Nose in Discrimination of Different
Microsoft Word - 695-699 tb20120355谢涛.doc
 微 生 物 学 通 报 Microbiology China tongbao@im.ac.cn Apr. 20, 2013, 40(4): 695 699 2013 by Institute of Microbiology, CAS 高 校 教 改 纵 横 湖 南 工 程 学 院 生 物 工 程 专 业 实 践 教 学 模 式 创 新 与 实 践 * 谢 涛 张 儒 ( 湖 南 工 程 学 院 化
微 生 物 学 通 报 Microbiology China tongbao@im.ac.cn Apr. 20, 2013, 40(4): 695 699 2013 by Institute of Microbiology, CAS 高 校 教 改 纵 横 湖 南 工 程 学 院 生 物 工 程 专 业 实 践 教 学 模 式 创 新 与 实 践 * 谢 涛 张 儒 ( 湖 南 工 程 学 院 化
11 25 stable state. These conclusions were basically consistent with the analysis results of the multi - stage landslide in loess area with the Monte
 211 11 11 158 JOURNAL OF RAILWAY ENGINEERING SOCIETY Nov 211 NO. 11 Ser. 158 16-216 211 11-24 - 6 1 2 3 3 3 1. 126 2. 92181 74 3. 181 1 2 3 4 1. 27 1. 3 1. 56 1. 73 4 1 2 3 4. 96 1. 15 1. 48 1. 6 f s =
211 11 11 158 JOURNAL OF RAILWAY ENGINEERING SOCIETY Nov 211 NO. 11 Ser. 158 16-216 211 11-24 - 6 1 2 3 3 3 1. 126 2. 92181 74 3. 181 1 2 3 4 1. 27 1. 3 1. 56 1. 73 4 1 2 3 4. 96 1. 15 1. 48 1. 6 f s =
